磺胺嘧啶钠在淮南麻鸭体内药物动力学试验
2020-09-29刘锦妮王向茹吴海港姬万民
刘锦妮,王向茹,吴海港,姬万民
[1.信阳农林学院 信阳市兽药新制剂研发与创制工程技术研究中心,河南 信阳 464000;2.瑞普(天津)生物技术股份有限公司,天津 空港 300308]
淮南麻鸭因原产于信阳市淮河以南、大别山以北的广大地区而得名,属麻鸭类,中等体型,蛋肉兼用,具有适应性强、抗逆性强、耐粗饲、早熟、繁殖力强、生长快等特点,1986年经河南省地方优良畜禽品种编委会正式命名为淮南麻鸭,列入《河南省地方优良畜禽品种志》,是河南省重点保护的优良地方品种之一[1]。磺胺嘧啶钠是兽医临床中广泛使用的一种磺胺类抗菌药物[2],其具有在血液中有效药物浓度高,与血清蛋白结合率低,易通过血脑屏障等优点,在兽医临床上主要用于治疗由革兰阳性及阴性菌等敏感细菌引起的脑膜炎、肺炎、子宫内膜炎以及禽巴氏杆菌病、雏鸡白痢等[3]。目前,国内外对磺胺嘧啶钠在多种动物体内的药动学进行了研究,主要包括磺胺嘧啶钠在猪、羊、牛、家禽、兔子、鸵鸟、欧洲鳗鲡等动物体内的药动学、血浆蛋白结合率及生物利用度等内容[4-10]。然而由于磺胺类药物在不同种属动物体内的代谢情况存在明显差异性,即使同一种磺胺药物在不同种类动物体内代谢过程也有显著的差异,目前磺胺嘧啶钠在淮南麻鸭体内药物动力学的研究还未见报道。因此本试验通过分析磺胺嘧啶钠在淮南麻鸭体内的药物动力学特征,为兽医临床中的磺胺嘧啶钠科学合理使用提供理论参考依据。
1 材料与方法
1.1 药品与试剂 磺胺嘧啶钠(含量≥90%,批号:170814),由河南自然康生物技术有限公司馈赠;磺胺嘧啶钠标准品(98%,批号:2089190),购自上海晶抗生物工程有限公司;10%磺胺嘧啶钠注射液(10%,批号:220381634),购自四川恒通动物药业有限公司;三氯醋酸、亚硝酸钠、氢氧化钠(均为分析纯),均购自上海国药集团化学试剂有限公司;氨基磺酸铵(分析纯),购自上海易恩化学技术有限公司;麝香草酚(分析纯),购自成都市科龙化工试剂厂。
1.2 仪器 紫外可见分光光度计:北京普析分析仪器有限公司;JY2002型电子天平:上海精密科学仪器有限公司。
1.3 动物分组、给药与采样
1.3.1 试验动物 16只健康成年淮南麻鸭,100日龄左右,体重1.5~2.3 kg,雌雄各半,试验前按常规饲养1周,饲喂不含抗菌药物的全价日粮,自由饮水。
1.3.2 给药 16只健康成年淮南麻鸭,随机分成2组,每组8只,雌雄各半,其中一组于翼下静脉缓慢注射单剂量100 mg/(kg·bw)磺胺嘧啶钠注射液,另一组按100 mg/(kg·bw)进行口服给药磺胺嘧啶钠溶液。
1.3.3 血浆样品采集 给药后,剥离出翅下静脉血管,分别于0.08、0.25、0.5、0.75、1、1.5、2、3、4、5、6、8、12 h和24 h采血1 mL左右,置于已加入肝素钠的离心管中,以3 000 r/min离心5 min,取上清液于-20 ℃保存待测。
1.4 血浆样品的处理 取待测血样0.6 mL加入到含有20%三氯乙酸2 mL的离心管中,充分摇匀,3 000 r/min 离心5 min;取上清液加入0.5%亚硝酸钠0.5 mL,充分摇匀;再加入0.5%麝香草酚1 mL摇匀。于530 nm波长处进行检测分析。
1.5 标准工作曲线 向6支10 mL具塞离心管中各加入0.6 mL空白血浆,添加适量磺胺嘧啶钠标准工作液,使得的药物浓度依次为5、10、20、50、100 μg/mL和200 μg/mL血浆样品。按照血浆样品处理方法处理后进行分析。以磺胺嘧啶钠吸光度(A)为横坐标,磺胺嘧啶钠在样品中的浓度(C)为纵坐标,建立标准曲线,求出回归方程以及相关系数(r)。
1.6 方法学验证 取空白血浆,添加适量磺胺嘧啶钠标准液,配制成含磺胺嘧啶钠浓度分别为100、20 μg/mL和5 μg/mL 的血浆样品,按照血浆的处理方法处理分析,每个浓度设置3个样品以测定日内变异系数,连续重复3 d以测定日间变异系数。
1.7 统计分析 药物动力学模型采用3P97药动学软件进行拟合;药时曲线图和消除动态图采用Excel软件绘制;方法学验证考察数据采用SPSS 18.0软件分析处理。
2 结果
2.1 标准曲线及线性范围 本试验所建立的血浆标准工作曲线相关性好,线性范围5~200 μg/mL,回归方程C=180.8A-15.97,相关系数为0.990以上。
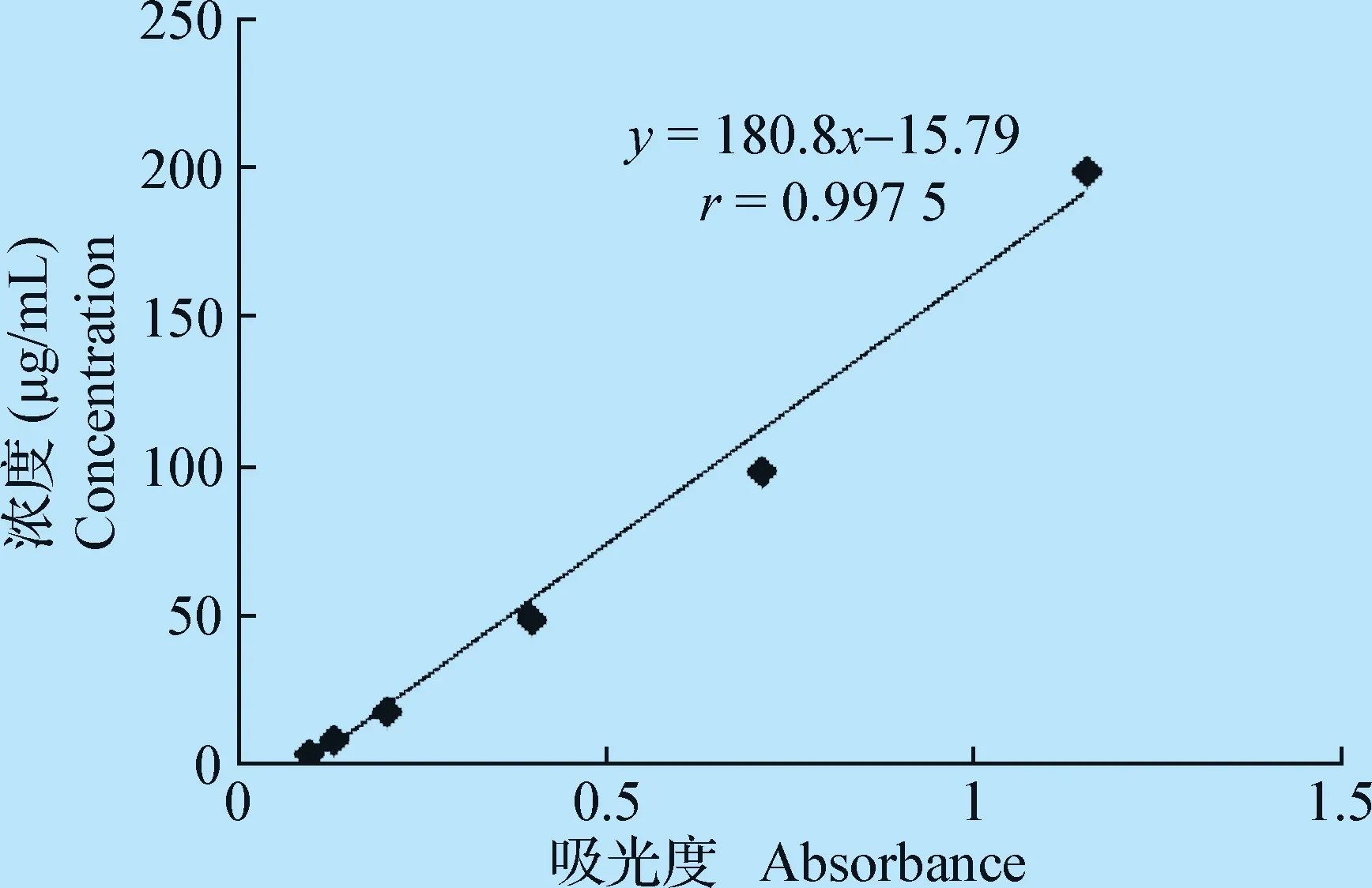
图1 磺胺嘧啶钠在血浆中标准曲线Fig.1 Calibration curve of SD-Na in plasma
2.2 方法学结果 参照1.5所描述的方法,在淮南麻鸭血浆中添加药物,所测回收率及精密度数据见表1。采用本方法,磺胺嘧啶钠血浆中的回收率为77.64%~90.03%,日内变异系数均小于5%,日间变异系数均小于10%,方法具有较好的精密度。
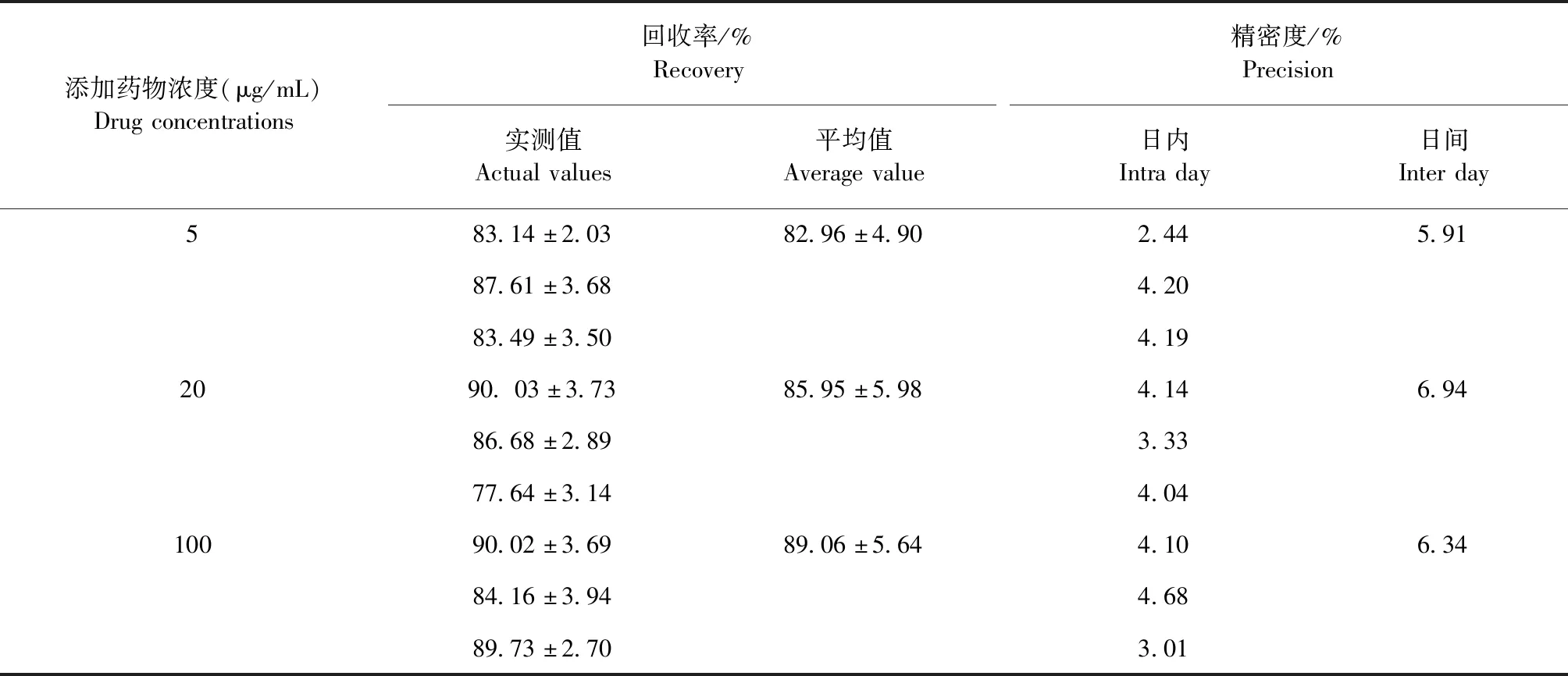
表1 淮南麻鸭空白血浆中添加磺胺嘧啶钠的方法学考察结果Table 1 The result of method validation of SD-Na in Huainan patridge duck plasma (n=3)
2.3 药物动力学数据分析 分别给淮南麻鸭以100 mg/(kg·bw)的剂量单次口灌和静脉注射磺胺嘧啶钠以后,血药浓度的数据见表2,药物在血浆中的药-时曲线见图2。经3P97药动学软件房室模型的模拟,其中有吸收二室模型的赤池信息量准则(AIC)和加权平方和(WSS)最小。所得的药物动力学参数见表3,静脉注射给药后,其血药浓度-时间数据均符合无吸收二室开放模型。其理论方程为C=52.91e-1.12t+72.86e-0.22t。该药物经静脉注射后分布很快,分布半衰期(t1/2α)为(0.62±0.08)h;消除半衰期(t1/2β)为(3.21±0.98)h;药时曲线下面积(AUC)为(385.14±13.52) (μg/mL)·h;口服磺胺嘧啶钠后其血药浓度-时间数据均符合吸收二室开放模型,其理论方程为C=80.66e-0.15t+34.70e-0.10t-115.36e-0.48t。该药物经口服后吸收迅速、分布快,分布半衰期(t1/2α)为(4.61±0.94)h;消除半衰期(t1/2β)为(6.66±0.74)h;药时曲线下面积(AUC)为(395.06±24.03)(μg/mL)·h;达峰时间(Tp)为(3.71±0.84)h;峰浓度(Cmax)为(49.97±5.66)μg/mL。
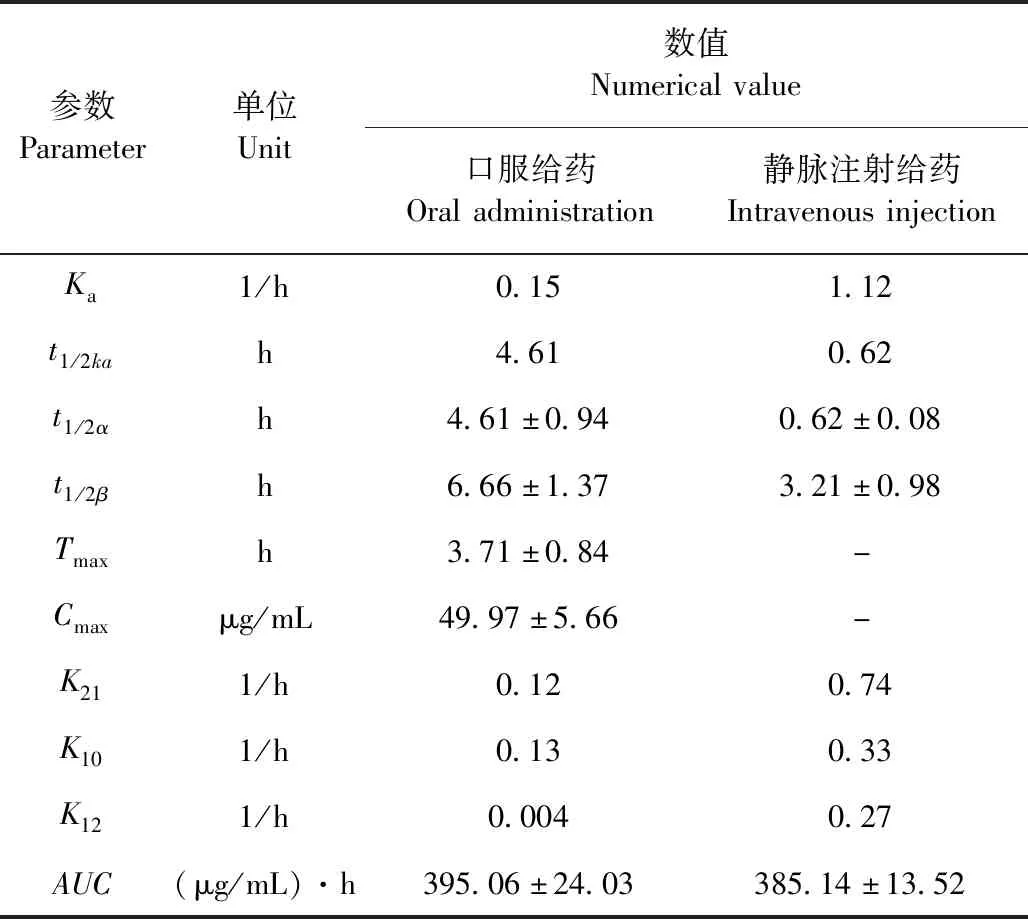
表3 磺胺嘧啶钠在淮南麻鸭体内的药物动力学参数Table 3 Pharmacokinetic parameters of sulfadiazine sodium in Huainan patridge duck

表2 磺胺嘧啶钠在淮南麻鸭体内的血药浓度Table 2 SD concentrations in plasma following oral administration and intravenous injection in Huainan patridge duck plasma (n=8)
3 讨论
目前针对磺胺嘧啶等磺胺类药物分析方法主要有微生物法、免疫分析方法、分光光度法、酶联免疫分析法及色谱法等,其中色谱法应用最为广泛,而分光光度法则是一种较为成熟、快捷、高效的方法[11-13]。本试验利用磺胺嘧啶钠在酸性条件下能够发生重氮化反应的特点,建立了分光光度法测定淮南麻鸭血浆中磺胺嘧啶钠的含量,该方法测定方法简便,重现性好,所建立的标准曲线相关性好,相关系数达0.990以上,平均回收率在75%以上;日内变异系数小于5%,日间变异系数小于10%,能够满足样品检测及分析的要求。
种属不同等因素影响磺胺嘧啶的药物动力学参数,文献报道磺胺嘧啶钠在不同动物体内的半衰期不同,其中在猪体内半衰期为0.5~0.8 h、绵羊体内的半衰期为4.03 h,狗为9.9 h,家禽类中的鹅为5.68 h、鸡为4.5 h、鸭为5.88 h。而在欧洲鳗鲡体内的半衰期为104.27 h[14]。本试验中静脉注射和口服消除半衰期(t1/2β)分别为3.21 h和 6.66 h,和上述文献报道存在一定差异,其原因可能是由物种间的差异、动物年龄、性别或营养状况不同造成的。此外给药途径、制剂工艺等条件同样会影响磺胺嘧啶钠的药物动力学参数,张晓晓等报道,单次口服复方磺胺嘧啶混悬液在肉鸡体内的半衰期为3.82 h,参比制剂的半衰期为3.09 h[15]。而本试验中不同给药途径,其药物动力学参数也不相同,这可能和血浆蛋白结合率及肾小管重吸收有关。此外文献中报道磺胺类药动学研究多为一室开放模型[16]。本试验中磺胺嘧啶钠在淮南麻鸭体内血药浓度-时间数据符合二室开放模型,其中静脉给药为无吸收二室开放模型,口服给药为有吸收二室开放模型,这同样表明磺胺嘧啶钠的动力学模型对动物有种属差异和分布差异。
