成人自身免疫性肝炎二线药物治疗选择的Meta分析
2020-09-28钱乐,应力
钱 乐,应 力
1 辽健集团本钢总医院 内窥镜科,辽宁 本溪 117000;2大连医科大学附属第二医院 消化内科,辽宁 大连116000
自身免疫性肝炎(AIH)是由免疫介导的慢性进展性肝脏炎症性疾病,以女性患者多见[1],其主要特征表现为自身抗体呈阳性、血清IgG/γ-球蛋白升高、肝脏组织学提示界面性肝炎[2],临床表现多种多样化[3]。糖皮质激素或联用硫唑嘌呤是目前推荐的AIH一线治疗方案[4]。但仍有多达10%~20%的患者对该标准治疗表现为无应答或药物不耐受[5]。目前对于这类患者采用的替代药物选择缺乏较全面的有效性及安全性评估。因此,通过对相关临床研究资料进行归纳分析,为AIH二线药物的合理选择提供循证学依据。
1 资料与方法
1.1 文献检索 计算机检索2019年12月31日前PubMed、EMBASE、Cochrane Library、Web of Science、中国知网(CNKI)、中国生物医学文献数据库(CBM)、万方数据库及维普数据库等公开发表的关于AIH二线药物治疗的相关英文和中文文献,检索词包括“Hepatitis, Autoimmune”“Prednisone”“Azathioprine”“Tacrolimus”“Mycophenolatemofetil”“Cyclophosphamide”“Cyclosporine”“Budesonide”“Methotrexate”“肝炎,自身免疫性”“泼尼松”“硫唑嘌呤”“他克莫司结合蛋白质类”“吗替麦考酚酯”“环磷酰胺”“亲环素类”“布地奈德”“甲氨蝶呤”等,未限制研究类型、语言及研究对象等。为了保证其相关性,由2位专家分别独立评估任何可能符合纳入标准的研究文献,如遇分歧,引入第3位专家分析投票仲裁。
1.2 文献纳入及排除标准
1.2.1 纳入标准 (1)符合AIH诊断标准的成人(>16岁)患者;(2)将泼尼松(龙)单药或者联合硫唑嘌呤作为初始治疗方案;(3)研究对象包括但不仅限于初次治疗失败的患者;(4)有明确的终点结局指标(随访终点的应答率、严重不良反应类型及发生频率等);(5)可以获取全文,并有明确数据。
1.2.2 排除标准 (1)对结局指标的描述不完整或不明确;(2)无法获取全文;(3)重复发表;(4)研究对象非人类;(5)非中英文文献;(6)综述、会议文摘、学位论文等;(7)将二线药物作为初始治疗药物进行研究。
1.3 纳入文献质量评估 确认纳入文献的研究类型。考虑纳入文献多为回顾性研究,故对纽卡斯尔-渥太华量表(NOS)进行修改[6],除去“可比性”的评价内容,通过评估如下指标,(1)选择:暴露人群的代表性(能够很真实地代表社区人群的平均水平或基本代表社区人群的平均水平可获得1颗★)、暴露的确定(通过可靠的记录或结构化调查获得的数据可获得1颗★)、研究开始前没有研究对象发生结局事件(是,获得1颗★);(2)结局:结局事件的评估(通过独立的、盲法的评估或鉴定,例如可靠的原始数据或联动数据则可获得1颗★)、为观察到结局发生随访是否充分(有充分的随访时间来观察结局发生可获得1颗★)、队列随访的完整性(所有参与者都完成了随访或少数失访但不大可能引入偏倚或对失访进行了描述则可获得1颗★)。每项研究最多可获得6颗★,4颗★以上为较高质量研究。在数据描述不明的情况下,联系研究作者进行确认。
1.4 数据提取 相关信息由2位人员分别从所有纳入的研究中独立提取,使用自定义表格进行数据的收集及整理。在纳入文献中提取的数据内容包括:(1)第一作者姓名;(2)文献发表年份;(3)研究类型;(4)二线治疗药物类型;(5)病例总数;(6)平均年龄;(7)平均随访时间;(8)应答的定义;(9)应答病例数;(10)药物剂量;(11)不良反应类型及比例。
1.5 统计学方法 采用Meta-Analyst统计软件进行Meta分析。主要结局指标为随访终点的应答率,次要结局指标是关于二线药物不良反应的类型及发生率。最终数据使用DerSimonian-Laird随机效应模型进行分析,汇总的结局指标采用汇总效应值和95%可信区间(95%CI)来表示,如果数据可用,进一步将患者按照对一线治疗不应答和不耐受进行分组,两组的应答率比较结果用相对危险度(RR)及95%CI表示。如果存在零应答率,则将其统计值替换为0.5作为校正因子。同时总结归纳随访时间及不良反应类型。使用Q检验评估统计异质性,结果用I2进行量化,0≤I2<25%提示无异质性,25%≤I2<50%提示轻度异质性,50%≤I2<75%提示中度异质性,I2≥75%提示重度异质性。如果数据可提供,则通过比较年龄、性别、种族、是否存在肝硬化以及AIH类型等基本资料进行亚组分析各研究的异质性。P<0.05为差异有统计学意义。
2 结果
2.1 文献检索结果 检索到相关文献4625篇,去除重复文献1172篇,通过阅读题目及摘要,严格按照纳入及排除标准,排除不符合要求文献(综述、会议文献、学位论文等),剩余91篇,继续详细阅读全文,排除不符合纳入标准的文献,包括数据重复、试验数据不明确等,最后共纳入文献22篇[7-28],包含研究对象636例。纳入文献中有12篇研究[10,13-15,17-19,21-22,24,26-27]报道了吗替麦考酚酯(MMF),5篇研究[12,15,22,25,28]报道了他克莫司(TAC),3篇研究[8,11,28]报道了环孢素(CsA),5篇研究[7,9,16,20,23]报道了布地奈德(BUD)。文献筛选流程详见图1。每项研究的基本信息详见表1。所有研究改为二线治疗的原因包括对一线治疗无应答、治疗失败或药物不耐受。
2.2 文献质量评估 18篇文献[7-12,14,17-20,22-24,25-28]获得6颗★;4篇文献[13,15-16,21]获得5颗★,其中1项研究[21]纳入患者无明确诊断标准,3项研究[13,15-16]纳入患者例数≤5例,队列的代表性不充分。研究的偏倚风险中等,均为较高质量文献。
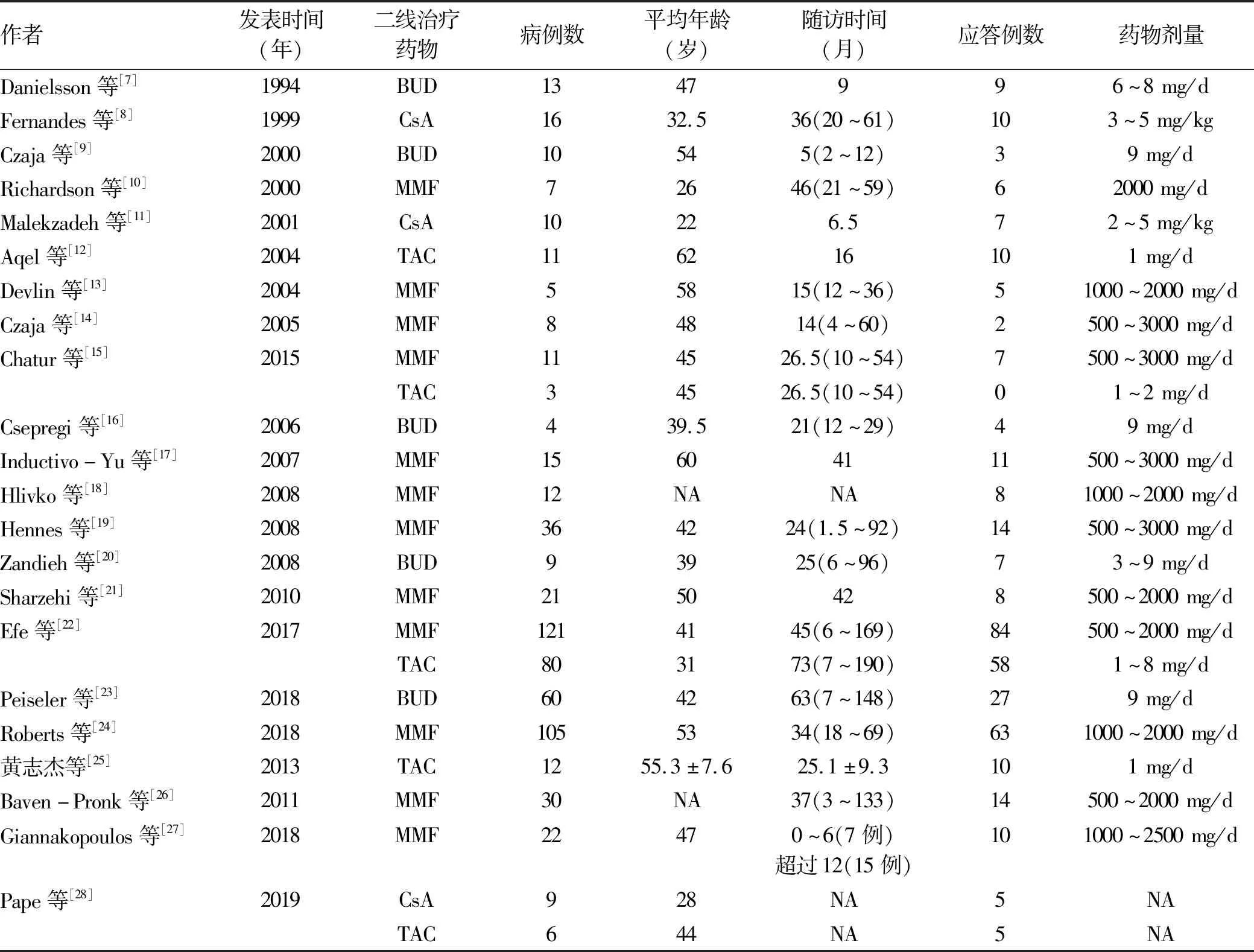
表1 纳入研究的基本信息
2.3 Meta分析结果
2.3.1 应答率 12篇文献[10,13-15,17-19,21-22,24,26-27](n=393)报道了MMF作为二线治疗的应答率,其中2项研究[18-19]将应答定义为转氨酶水平低于2倍正常值上限,其余研究定义为转氨酶水平的正常化,一项研究[10]提供了随访期间的转氨酶情况,虽然未明确定义应答,但根据随访期间的转氨酶监测情况将应答视为转氨酶的正常化来进行结果统计。分析结果显示,MMF的汇总应答率为56.1%(95%CI:46.5%~65.3%);异质性检验:I2=0.369,P=0.154(图2)。
5篇文献[12,15,22,25,28](n=112)报道了TAC作为二线治疗药物的应答率,其中4项研究[15,22,25,28]均将应答定义为转氨酶水平的正常化,另1项研究[12]未明确定义,根据提供的随访过程中转氨酶数值,将应答定义为转氨酶的正常化来进行结果统计。分析结果显示,TAC的汇总应答率为76.0%(95%CI:60.3%~86.8%);异质性检验:I2=0.193,P=0.003(图3)。
3篇文献[8,11,28](n=35)报道了CsA作为二线治疗药物的应答率,其中2篇[8,11]均未对应答进行明确定义,利用提供的转氨酶数据,将应答定义为随访终点转氨酶的正常化来进行结果统计。分析结果显示,CsA的汇总应答率为62.7%(95%CI:45.7%~77.0%);异质性检验:I2=0,P=0.118(图4)。
5篇文献[7,9,16,20,23](n=96)报道了BUD作为二线治疗药物的应答率,其中2篇[7,9]将应答定义为AST/ALT低于2倍正常值上限,其余研究均将应答定义为转氨酶的正常化。分析结果显示,BUD的汇总应答率为57.3%(95%CI:37.2%~75.1%);异质性检验:I2=0.347,P=0.237(图5)。
2.3.2 不良反应 药物不良反应类型及病例数详见表2。共10篇文献[10,15,17-19,21-22,24,26-27]报道了MMF的不良反应,主要包括白细胞减少以及恶心呕吐、腹痛腹泻等胃肠道症状,同时还有肌痛、牙齿松动、皮肤病、肿瘤及感染等少见不良反应。MMF汇总不良反应发生率为22.5%(95%CI:15.8%~30.8%);异质性检验:I2=0.373,P<0.001。
4篇文献[12,15,22,25]均报道了TAC不良反应,以头痛最多见,另外还包括了肾功能不全、周身水肿、高血压、胃肠道症状以及震颤、脱发等少见不良反应。TAC汇总不良反应发生率为47.4%(95%CI:14.4%~82.8%);异质性检验:I2=0.466,P=0.284。

表2 不良反应类型及病例数
2篇文献[8,11]报道了CsA不良反应,以感觉异常(神经损伤)、多毛症及齿龈增生最为常见,其他不良反应包括肾小球滤过率下降、震颤、高血压等,还有1例出现了少见的出血性腹泻。CsA汇总不良反应发生率为48.4%(95%CI:29.4%~67.8%);异质性检验:I2=0.230,P=0.283。
3篇文献[10-12]报道了BUD不良反应,包括外观改变(满月脸、粉刺、紫纹、脱发)、体质量增加、2型糖尿病等。BUD汇总不良反应发生率为33.0%(95%CI:24.0%~43.4%);异质性检验:I2=0,P<0.001。
2.3.3 分组分析 对应用MMF治疗的7项研究[10,19,21-22,24,26-27]按照一线治疗不耐受和一线治疗无应答进行分组分析,统计的RR值为1.965,95%CI:1.181~3.269,P=0.014,差异有统计学意义,而异质性检验I2=0.665,提示各研究数据之间异质性较大,但因为数据有限,难以进行亚组分析(图6)。
3 讨论
本研究采用Meta分析方法系统回顾了关于成人AIH二线用药的有效性及安全性。在随访终点,TAC的应答率最高(76.0%),其次为CsA(62.7%)、BUD(57.3%)、MMF(56.1%),且四者的I2值均<50%。对于安全性的分析,结果显示MMF不良反应发生率最低(22.5%),BUD(33.0%)稍高,TAC(47.4%)及CsA(48.4%)均较高。2项研究[22,29]表明无论对儿童或成人AIH患者,MMF及TAC在一线药物不耐受的患者中有效率相近,而TAC在一线治疗无应答的患者中显示出更高的应答率。作为二线治疗药物,汇总的应答率提示TAC优于MMF,且目前证据表明对一线治疗无应答的患者TAC应答率更高,尽管TAC较MMF的不良反应发生率高,但目前综合考虑TAC在4种免疫抑制剂中可能是最优的选择。对MMF治疗[10,19,21-22,24,26-27]按照一线治疗不耐受及治疗无应答进行分组,发现MMF用于一线治疗不耐受患者比一线治疗无应答者更为有效。对一线治疗无应答的患者,其对药物的治疗反应不佳,即使改为另一种免疫抑制剂,效果也较微弱;而对一线治疗不耐受的患者,主要不能耐受一线治疗药物的副作用,不代表对一线治疗无效,因此对二线治疗的药物会有更高的应答率。但由于纳入研究样本较小,没有进行敏感性分析。两组之间应答率的结果存在显著异质性,提示研究之间存在关键差异,包括:(1)研究人群的异质性,诊断标准是否一致,是否包括重叠综合征等,诊断时是否存在肝硬化可能是一个较好的亚分组标准;(2)对应答的定义缺乏统一性;(3)随访终点的时间差异。
BUD是第2代糖皮质激素,药物代谢和作用与泼尼松相似,而抗炎作用相当于泼尼松的5倍。一项关于BUD与泼尼松分别联合硫唑嘌呤治疗AIH疗效及安全性的Meta分析[5]结果显示,BUD联合硫唑嘌呤的疗效优于泼尼松联合硫唑嘌呤,且治疗后不良反应发生率低。本研究将BUD作为二线药物治疗,结果发现其不良反应发生率低于TAC和CsA,略高于MMF,而其汇总有效率高于MMF,但低于TAC及CsA。这可能由于BUD与泼尼松都作用于激素受体,对于泼尼松治疗无应答的AIH患者,使用BUD治疗时也可能面临失败。肝硬化患者因侧支循环开放可导致药物直接进入体循环而失去首过效应的优势,BUD可作为某些AIH患者(非肝硬化且无合并其他免疫性疾病)的一线替代治疗药物也许值得在临床中推广[5]。CsA作为二线治疗药物,虽然有较高的应答率,但不良反应发生率亦高于其他药物。在未能达到获益高于风险(高血压、肾毒性、感染、胰腺炎、神经毒性和恶性肿瘤)的前提,结合其高昂的费用,且应用时需要频繁进行药物水平监测以避免肾毒性和神经毒性,因此限制了CsA的使用。
由于尚缺乏大样本、多中心随机对照试验,本研究纳入的文献数较少,Meta分析结果在一定程度上会受到影响。如:(1)在统计不良反应发生率的过程中,将所有不良反应纳入讨论范围,而免疫抑制剂的应用过程中,大部分的不良反应是可以通过减量而改善的,而且不同人群对不良反应的耐受性不同,最终导致停药多数是因为一些少见但严重的不良反应;(2)本研究纳入文献均为回顾性观察,其结果往往存在更多异质性,难以对不同治疗方法进行比较,因为需要假设患者在不同的研究间有足够相似性才可进行直接比较;(3)对AIH的病情评估需长期随访,而本研究所纳入的部分文献中患者的随访时间较短,故可能存在AIH复发但在随访期间内未观察到,这也导致了因随访时间的不同带来的异质性。
虽然本研究结果均来源于不同时期的回顾性病例分析,但通过严格的系统回顾,尽可能地规范纳入及排除标准以降低潜在的选择偏倚。希望通过汇总的效应值分析,在成人AIH患者的二线药物选择方面为临床医生提供较全面的依据,同时对未来的多中心、前瞻性研究设计有一定的启发作用。
