肺保护性通气策略对QT间期延长综合征胸交感神经切断单肺通气术后早期炎症反应的影响*
2020-09-26张卉颖卢光奎何绮月
张卉颖, 卢光奎, 何绮月
南京医科大学附属明基医院麻醉科(江苏南京 210019)
经胸腔镜胸交感神经切断术(endoscopic thoracic sympathectomy,ETS)是治疗QT间期延长综合征(LQTs)的新型手术方式[1]。LQTs临床发病率0.05%~8.5%,Costello等[2]在LQTs诊治的专家共识里提出,ETS可缩短药物作用不佳或合并严重心律失常的LQTs患者的QT间期,从而降低恶性心律失常及猝倒等发生率。LQTs患者术前心功能多受影响,易在围术期诱发交感神经易感状态导致尖端扭转型室性心动过速甚至室颤,尤其属心跳骤停依赖型的患者一旦发生尖端扭转型室速可致命[1-3]。我院ETS术使用微创视频辅助胸腔镜手术(video-assisted thoracic surgery,VATS)技术,手术创伤小、恢复快、疗效显著,术中行双腔气管插管复合间断单肺通气(one lung ventilation,OLV)。近年来加速康复外科(enhanced recovery after surgery,ERAS)概念兴起,ETS术中需双肺通气、OLV切换,术时长、创伤大,常规通气方法易造成肺泡容积伤、生物伤,增加围术期肺部并发症发生率,有悖ERAS的基本诉求。我们总结发现肺保护性通气策略(lung protective ventilation strategy,LPVS)在ETS患者的实施似乎可更加贴合ERAS的要求,但在VATS通气管理实施中对于具体潮气量的设定、合适呼气末正压通气(PEEP)的选择及最佳肺复张时间、要达到的氧合指标等,至今仍未见统一的具体标准,本研究拟通过2017年10月至2018年9月间在本院行ETS术的LQTs患者80例,观察应用LPVS对其术后早期炎症反应的影响,探索适合VATS患者LPVS的具体措施制定,以供临床参考。
1 资料与方法
1.1 一般资料 本研究经本院医学伦理委员会审查批准,所有患者及其家属均签署知情同意书。选择2017年10月至2018年9月间在南京医科大学附属明基医院择期行ETS的患者80例。所有患者采用随机数字法分为常规通气组(CV组)和肺保护性通气策略通气组(PV组),每组40例。入组标准:美国麻醉医师协会评分(American Society of Anesthesiologists,ASA)为Ⅰ~Ⅱ级,18岁<患者年龄<65岁、体质指数<30 kg/m2、手术时间1~2 h。排除标准:患者术前三大常规、心电图、胸部正侧位片、肺功能等相关检验检查均未见明显异常,术前无呼吸道及肺部感染,无严重心肺、肝肾功能不全及双腔气管插管绝对禁忌证。80例手术均操作顺利,两组患者一般资料差异无统计学意义(P>0.05),见表1。
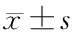
表1 两组患者一般资料比较
1.2 麻醉及通气管理方法
1.2.1 麻醉诱导及维持 所有入选患者均于术前30 min使用戊乙奎醚1 mg缓慢静脉注射。患者入手术室后,建立静脉通路,连接含脑电双频谱指数(bispectral index,BIS)监测模块(型号DE11012450,美国Conviden公司)的监护仪(Philips MP50),行上肢无创血压(BP)、心率(HR)、心电图(ECG)、脉搏氧饱和度(SpO2)的监测。依次静脉注射咪达唑仑0.05 mg/kg、芬太尼4 μg/kg、丙泊酚1 mg/kg、顺式阿曲库铵0.3 mg/kg。3 min后行气管内双腔气管插管(生产批号:lot201610078x,Mallinckrodt),呼吸机[Datex-Ohmeda麻醉机(Avance)]IPPV模式控制呼吸,以听诊法和纤维支气管镜(LF-DP,olympus)核查双腔管位置。术中持续静脉泵注丙泊酚1~4 mg/(kg·h)复合瑞芬太尼0.25~2.0 μg/(kg·min)维持BIS在40~60,另间断按需静脉注射顺式阿曲库铵2~4 mg,根据各生命体征个体化调整丙泊酚及瑞芬太尼用量。手术前及双侧交感神经切断即时需动态监测双手温度,以便指导术后研究、了解临床效果。术毕均予新斯的明1.0 mg与阿托品0.5 mg拮抗残余肌松,拔除气管导管后送麻醉恢复室(POR)观察。术后针对较明显的胸腔镜操作所致的疼痛不适,评估患者躁动情况等对个别病例行曲马多50 mg静脉注射处理。
1.2.2 通气管理 在术中根据手术进行步骤需要,于胸腔镜进胸及肺野周围电刀操作时行单肺通气,于术毕退镜时人工鼓肺行适当过度通气,以观察有无肺组织损伤及防止术后肺不张。
1.3 患者分组及干预措施 CMV参数设定:CV组患者双肺通气及单肺通气时均设VT10 mL/kg,I∶E=1∶1.5,FiO2100%,调节RR使PETCO2在35~45 mmHg;PV组患者双肺通气时参数设定同CV组,单肺通气时VT为5~6 mL/kg,I∶E=1∶1,并给予PEEP 3~5 cmH2O。
1.4 观察项目 取入室后(T0)、气管插管后(T1)、单肺通气60 min(T2)、术后24 h(T3)4个时间点。
1.4.1 血气分析 抽取动脉血,以床边血气分析仪(radiimeter ABL90 flex)行血气分析。
1.4.2 呼吸力学参数 以呼吸力学模块旁气流法监测:气道峰压(Ppeak)、气道阻力(Raw)、动态胸肺顺应性(Cdyn)。
1.4.3 炎症因子 采集静脉血3 mL加入EDTA抗凝管,以3 000 r/min离心10 min后取上清液放置于-70℃保存待测,用酶联免疫法(ELISA法)测定血中白细胞介素(IL)-6、IL-10、肿瘤坏死因子-α(TNF-α)的蛋白浓度。
1.4.4 计算指标 PAO2(mmHg)=713×FiO2-PaCO2(mmHg)/0.8;A-aDO2(mmHg)=PAO2-PaO2;氧合指数(oxygenation index,OI):OI=PaO2/FiO2;呼吸指数(spiro index,RI)=A-aDO2/PaO2。
1.4.5 术后肺部并发症 统计有无出现术后肺部并发症如低氧血症、肺不张。
1.4.6 ERAS相关参数 统计PACU内恢复时间、患者住院时间、入ICU患者数。
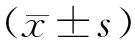
2 结果
2.1 两组手术时间和出血量情况 两组手术时间和出血量差异无统计学意义(P>0.05),见表2。
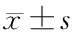
表2 两组手术时间和出血量情况
2.2 两组患者插管状态各时间点呼吸力学参数的比较 与CV组比较,PV组Ppeak、Raw、Cdyn在T1、T2时差异有统计学意义(P<0.05),见表3。
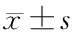
表3 两组患者插管状态各时间点呼吸力学参数的比较
2.3 两组患者各时间点炎症因子的比较 与CV组比较,PV组IL-6、IL-10、TNF-α在T1、T2、T3时差异有统计学意义(P<0.05),见表4。

表4 两组患者各时间点炎症因子的比较
2.4 两组患者各时间点动脉血气及相关计算指标比较 与CV组比较,PV组PAO2、A-aDO2、OI、RI在T1、T2、T3时差异有统计学意义(P<0.05),见表5。

表5 两组患者各时间点动脉血气及相关计算指标比较
2.5 两组患者术后24 h内肺部并发症的比较 与CV组比较,PV组低氧血症、肺不张、入ICU患者数差异有统计学意义(P<0.05),见表6。
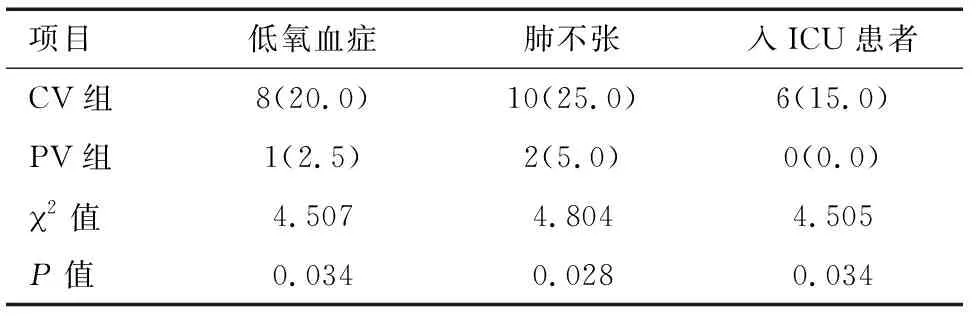
表6 两组患者术后24 h内肺部并发症的比较 例(%)
2.6 两组患者ERAS相关参数的比较 与CV组比较,PV组POR观察时间、住院时间差异有统计学意义(P<0.05),见表7。
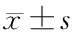
表7 两组患者ERAS相关参数的比较
3 讨论
Bell等[4]2014年在《ANZ journal of surgery》发表的一篇综述提到,胸交感神经的切断操作其本身可能在一定程度上影响肺通气,经过对612例ETS患者术后72 h随访观察发现,通气血流比值(V/Q)失调、肺不张、低氧血症、术后感染等一系列肺部并发症发生率增高,不利于患者术后快速康复,临床麻醉面临的难题是如何围绕肺保护加强ETS麻醉管理的探索。ERAS理念率先由丹麦学者Kehlet于1997年首次提出[5],各学科专家共同制定的《中国加速康复外科围术期管理专家共识(2016版)》[6]中特别提到麻醉学科应整合ERAS发挥综合评估、气道管理、应激控制、疼痛诊疗、优化预后等围术期管理方面的作用。因现有研究缺憾,关于我国胸外科围术期对ERAS理念的认知和应用现状研究较少。完善的术前评估与心理干预、适当的术前镇静用药、禁食禁饮时间的缩短、区域复合麻醉方式、液体管理与体温干预、多模式镇痛、精准麻醉、围术期并发症的防治等[7-10]组成了ERAS对于麻醉学科的基本要求。VATS较高的术后肺部并发症发生率经临床证实,可通过加强通气管理、控制过度应激等进一步降低[11-12],ETS的ERAS推行同样有其必要性,临床经验及文献证实,为加速患者外科康复,围术期的管理中ETS术中通气管理方式或许是可优化的方向之一。
机械通气时较大VT或较高气道压作用于肺泡表面牵张感受器,激活各种通路,介导炎性介质表达上调,可致急性肺损伤(acute lung injury,ALI)甚或急性呼吸系统窘迫综合征(acute respiratory distress syndrome,ARDS)[13]。OLV时相对大的VT必然伴随着过高的Ppeak及Pplat,使肺泡过度膨胀及萎陷,造成肺泡容积伤、生物伤,增加围术期肺部并发症发生率,有悖ERAS的基本诉求[14-15]。Uttman等[15]进行随机对照试验得出,较大潮气量(>12 mL/kg)可致气压伤[气道压>30 cmH2O(1 cmH2O=0.098 kPa)尤易]、容积伤和萎陷伤等。肺保护研究学界认为[16-19],气压伤主要导致 IL-6、IL-8、IL-10等炎症因子表达增强,而TNF-α在炎性过程中最早出现,可进一步激活肺泡上皮细胞等炎症效应细胞释放其他因子,如IL-1、IL-6、单核细胞趋化蛋白-1(MCP-1)等。活性氧自由基(ROS)主导NO参与炎症调节,其生成的关键限速酶一氧化氮合酶(NOS)激活iNOS通路,在IL-1、TNF-α炎症介质刺激下可高水平表达一氧化氮(NO),使Na+-K+-ATP酶活性升高,促使炎症发展[16-17]。这些促炎、抗炎因子的相互作用贯穿在机体整个炎症反应过程[18]。在本研究中,两组患者各时间点IL-6、IL-10、TNF-α炎症因子的比较,T1~T3时间点差异有统计学意义(P<0.05),表明PV组各炎症因子较CV组表达下调,有助于预防术后肺部并发症的发生。邱晓东等[19]认为双肺通气时的VT较OLV而言相对大,加之VATS多取侧卧位,导致气道压明显增高。因气管插管反应所致应激在研究起始时间点无特殊,而单肺通气时的LPVS模式为本研究观察重点,故本研究选取取入室后、气管插管后、单肺通气60 min、术后24 h 4个时间点记录观察通气参数。本研究结果表明,与T0时比较,PV组患者插管状态各时间点呼吸力学参数Ppeak、Raw、Cydn差异有统计学意义(P<0.05),两组患者各时间点PAO2、A-aDO2、OI、RI比较在T1~T3时间点差异有统计学意义(P<0.05),表明PV组可以减轻机械通气的气压伤影响,从而获得更平稳的呼吸力学状态。这与Bein等[20]改善通气模式以改善V/Q的研究相似,他们认为小潮气量通气(≈3 mL/kg)虽不增加肺不张的发生率,同时降低了Ppeak及Pplat,但有氧供不足及CO2蓄积之虞。以小潮气量、低气道压、适当呼气末正压通气(positive end expiratory pressure,PEEP)为综合指向的LPVS在ALI的的防治中取得了显著疗效[20-21]。部分学者提出“递增法”的调控方式[21-22],即患者在维持有效血容量、保证组织灌注条件下,PEEP宜从低水平(3~5 cmH2O)开始,逐渐增加至最佳PEEP。然而国内外多篇文献表明,“递增法”有“天花板效应”,且易忽视随之而来的容积伤,并不适合术时较长者,“滴定式”的个体化PEEP围术期动态调整方案或为VATS手术患者ERAS发展趋势[22]。本研究中两组患者术后24 h内肺部并发症(低氧血症、肺不张、入ICU患者数)的比较,差异有统计学意义(P<0.05),两组患者ERAS相关参数(POR观察时间、住院时间)的比较,差异有统计学意义(P<0.05),进一步证实应用LPVS可明显降低低氧血症、肺不张等的发生,降低入ICU患者数、缩短POR观察时间、缩短患者住院时间。由此可得,LPVS在ETS患者的实施似乎可更加贴合ERAS的要求。该研究结果表明,VATS患者全麻术中需双肺通气、OLV切换,术时长、创伤大,选择优化的保护性通气方式可加速ETS患者康复。
本研究吝于病例数和研究时间的限制,并未进行大样本、长周期的随机对照研究,其临床效果有待进一步观察。
回顾文献结合专家访谈,我们总结发现LPVS在ETS患者的实施似乎可更加贴合ERAS的要求,值得推广。该研究成果不仅在学术上有助于ETS患者ERAS路径的构建,也为ERAS可持续发展方案提供新的思路和治疗靶标。
