儿童异基因造血干细胞移植术后巨细胞病毒感染临床分析
2020-09-25朱成琳陈广华杨琪瑜胡绍燕
朱成琳 陈广华 翟 宗 杨琪瑜 吕 慧 李 捷 王 易 胡绍燕
1.苏州大学附属儿童医院血液肿瘤科(江苏苏州 215000);2.苏州大学附属第一医院江苏省血液研究所(江苏苏州 215000)
随着异基因造血干细胞移植技术(allogeneic hematopoietic stem cell transplantation,allo-HSCT)的进步和推广,越来越多的血液及非血液病患者可通过移植实现痊愈,而巨细胞病毒(cytomegalovirus,CMV)感染是allo-HSCT 后的常见严重并发症之一。HSCT患者由于免疫功能低下,不能有效清除CMV感染和产生免疫保护,易发生原发性CMV 感染或潜伏的CMV 再激活。在过去的几十年里,尽管采用更昔洛韦等抗病毒药物预防策略及结合CMV-DNA 检测的抢先治疗已显著降低CMV 病的发生率,但仍不能降低CMV病的病死率[1]。除引起局部器官损害以外,CMV 感染还可通过间接作用引起继发性细菌及侵袭性真菌感染、移植物抗宿主病及移植后骨髓衰竭、增加非复发相关死亡率等[2]。本文对allo-HSCT移植后CMV 感染危险因素进行分析并对CMV 感染情况进行描述,旨在为CMV 感染高危患儿的治疗和干预提供依据。
1 对象和方法
1.1 研究对象
回顾分析2016年1月至2018年12月在苏州大学附属儿童医院血液科进行allo-HSCT患儿的临床资料。研究对象入选标准:①年龄<18 岁;②具有HSCT 指征并进行HSCT治疗后存活30天及以上患儿;③排除回输造血干细胞之前或回输过程中死亡,输注造血干细胞移植后30天内因移植相关事件死亡,二次移植患儿,自体干细胞移植患儿。研究得到苏州大学附属儿童医院伦理委员会的批准。
入选研究对象依据是否感染CMV,分为CMV感染组与无CMV 感染组;根据对抗病毒治疗反应将CMV 感染组分为难治性CMV 感染(refractory cytomegalovirus infection,RCI)组及非RCI组。
1.2 方法
1.2.1 临床资料收集及随访 采用查询检验报告及电子病历的方式明确发生CMV 感染及RCI 患儿,通过查询电子病例进行随访,对于极少部分后期未再来院继续移植后检查患儿通过询问其负责医师了解其后续情况。
1.2.2 移植患者的CMV预防与治疗 ①CMV感染的预防:移植前9 天至前2 天所有受者予更昔洛韦,5 mg/kg,每12小时1次,静脉滴注1周,预防CMV感染;移植后改用阿昔洛韦,10 mg/kg,每12小时1次,静脉滴注至移植后1 个月;其后更改为口服预防,从中性粒细胞植入至移植后100天内,每周1、2次常规检测CMV 拷贝数,移植100 天后至移植后1 年内,每2~4 周定量检测CMV-DNA,直至停用免疫抑制剂;②CMV 感染的治疗:移植后第1 天开始定期监测CMV拷贝数状况,一旦连续两次检测到CMV-DNA拷贝数≥5×102copies/mL,立即静脉应用更昔洛韦或膦甲酸钠至CMV-DNA转阴(造血重建差者首选膦甲酸钠)或静脉用丙种球蛋白治疗,并在病情允许的情况下降低免疫抑制剂用量。CMV 肺炎者加用人CMV免疫球蛋白或人免疫球蛋白治疗。
1.2.3 CMV-DNA检测 采用人CMV核酸定量检测试剂盒(湖南圣湘生物科技有限公司)进行实时荧光定量PCR检测全血CMV-DNA拷贝数,该方法检测阈值为500 copies/mL,高于该值视为CMV-PCR阳性。
1.2.4 移植后CMV 感染及相关定义 CMV 感染:连续两次在外周血中检测到CMV-DNA≥500copies/mL[3]。复发性CMV感染:间隔28天以上CMV拷贝数转阴后,再次检测到CMV拷贝数上升,可为既往感染CMV 再激活或重新感染CMV。早期CMV 感染:移植后100天内发生CMV感染。晚期CMV感染:移植100天以后发生CMV感染[3]。RCI:经正规抗病毒治疗14天后,CMV-DNA拷贝数仍上升[4]。CMV病[4-7]:在相关液体和组织样本中发现CMV 感染的同时出现存在终末器官疾病的体征和症状(在相关器官的组织中存在临床症状和/或体征,并有相关的CMV检测)。CMV视网膜炎:经过专业眼科医师通过眼底检查确诊有相关视网膜改变。
1.2.5 急性移植物抗宿主病(acute graft-versus-host disease,aGVHD)与中性粒细胞植入 aGVHD 的诊断、分期和分度按照美国西雅图 FredHutchinson癌症研究中心关于aGVHD 的诊断分度及分类标准进行诊断[8]。中性粒细胞植入:连续3 天中性粒细胞计数(ANC)≥0.5×109/L的第1天[5]。
1.2.6 GVHD预防方案 亲缘全相合造血干细胞移植(Sib-HSCT)采用霉酚酸酯(MMF)联合环胞霉素A(CsA)或他克莫司(FK506)二联预防 GVHD;无关供者造血干细胞移植(URD-HSCT)及单倍体相合造血干细胞移植(Haplo-HSCT)采用CSA+MMF+短程甲氨蝶呤(MTX)三联预防GVHD。CsA于移植前9天起予3 mg/(kg·d),每12小时1次,静脉滴注,监测CsA浓度,调整至维持在150~250 ng/mL,后渐改为口服;FK506浓度维持8~15 ng/mL。MTX于移植后1天、3天、6天及11天给予,首次剂量15 mg/m2,其后为10 mg/m2。
1.3 统计学分析
采用SPSS 21.0统计软件进行数据分析。非正态分布计量资料以中位数(四分位数范围)表示。计数资料以百分比表示,组间比较采用χ2、校正χ2或Fisher精确概率法检验。采用二元logistic回归模型分析CMV感染及RCI发生的危险因素。采用Kaplan-Meier分析法分析CMV感染及RCI对总体生存率(OS)及无病生存率(DFS)的影响,并用Log-Rank检验比较组间差异。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况
共收集患儿269例,其中男167例、女102例;中位移植年龄65个月(33~115个月),最小7个月,最大206个月;中位随访时间16.2个月(11.7~25.0个月)。急性白血病148例(急性淋巴细胞白血病77例、急性髓系白血病71例),骨髓增生异常综合征(MDS)/骨髓增值性疾病(MPN) 18例,骨髓衰竭性疾病61例,免疫缺陷病26例,其他病种16例。采用脐带血造血干细胞移植(UCBT)81例,外周血造血干细胞移植(PBSCT)67例,PBSCT联合骨髓造血干细胞移植(BMT)113例,BMT者8 例。Sib-HSCT 33 例,Haplo-HSCT 116 例,URDHSCT120例。257例患儿采用改良 Bu/Cy 为主的预处理方案,12例伴髓外病变恶性血液病患儿采用含全身照射(TBI)预处理方案。见表1。
2.2 CMV感染情况
至随访终点,共165 例发生CMV 感染,CMV 感染率61.3%(165/269例),CMV感染发生时间为移植后23 d(15~34 d),感染持续时间38 d(25~66 d)。165例患儿中有12例患儿移植前检测出CMV-DNA。98.1%(162/165)为早期CMV感染,3例为晚期CMV感染,分别在移植后第103、115和148天,持续时间分别为24、43和20天。14.5%(39/269)患儿发生复发性CMV感染。见表2。
2.3 RCI情况
移植患儿中有17.8%(48/269例)发生RCI,RCI发生时间为移植后19.5d(13.0~27.3d),经治疗后RCI转阴的中位时间为61.5 d(41.0~100.5 d)。见表2。在发生RCI的患儿中有17例患儿发生复发性CMV感染,3例再次发生RCI。
RCI组初次检测到CMV感染时间为移植后19.5 d(13.0~27.3 d),非RCI组为24.0d(16.5~34.0 d),两组差异有统计学意义(Z=2.58,P=0.010)。
RCI组CMV感染拷贝数峰值为57 800 copies/mL(21 000~151 250 copies/mL),非RCI组为8 310copies/mL(2 845~23 150 copies/mL),两组差异有统计学意义(Z=6.82,P<0.001)。
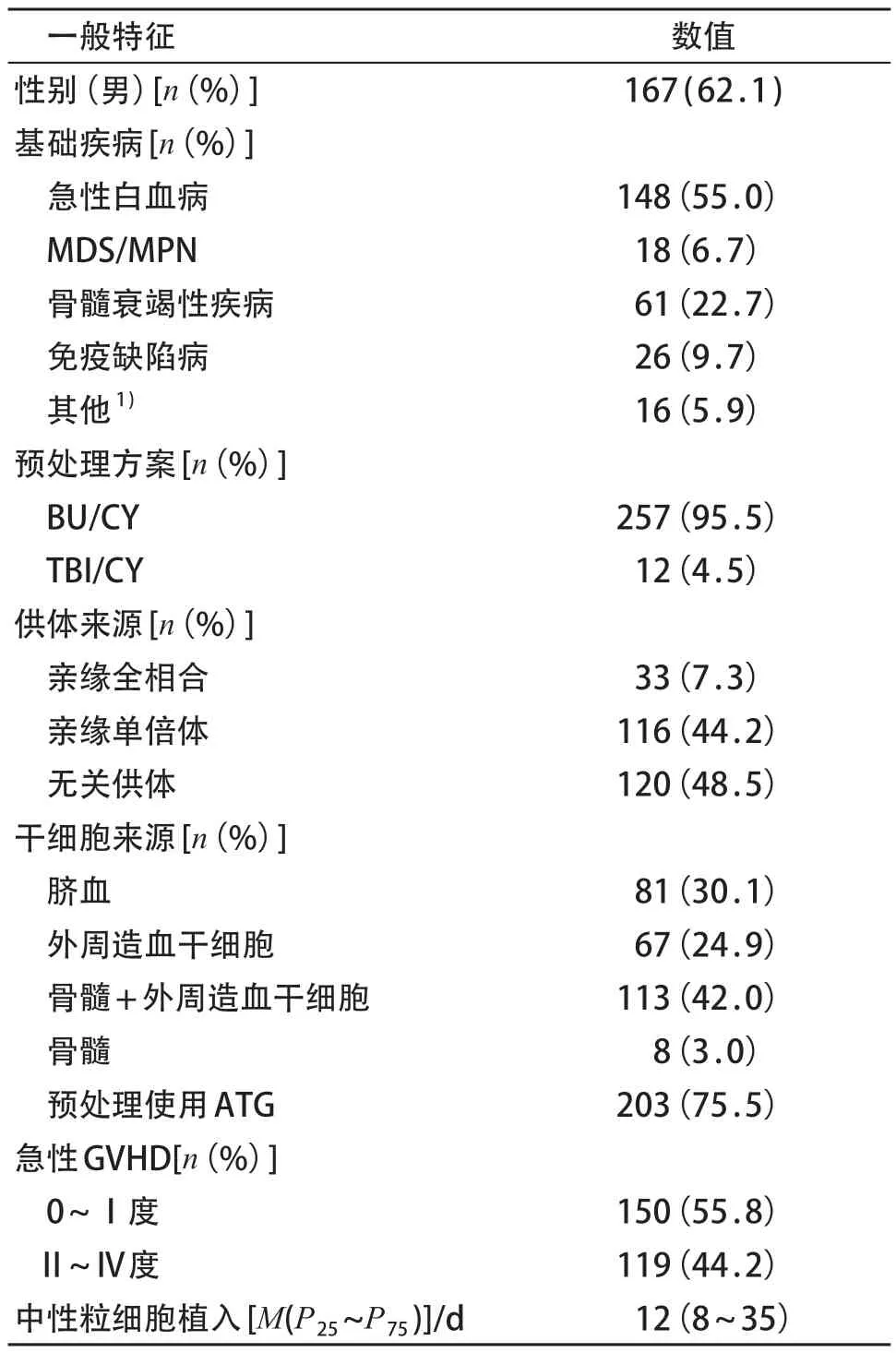
表1 造血干细胞移植患儿一般资料(n=269)
2.4 CMV病
3.3 %(9/269)的患儿发生CMV病,占发生RCI患儿的18.8%(9/48)。其中有3例患儿为CMV肺炎,CMV 肺炎患儿的支气管肺泡灌洗液均检测到CMVDNA;CMV肺炎患儿中有1例持续血便,并在粪便中检测到CMV-DNA 1.4×105copies/mL。6例患儿发生CMV 视网膜炎,其中5 例基础疾病均为湿疹、血小板减少伴免疫缺陷综合征,且均在移植前检测到CMVDNA;1例为急性淋巴细胞白血病(ALL)复发后移植。9 例患儿中2 例发生移植相关死亡。9 例CMV 病患儿中7例采用脐血移植,2例为单倍体移植。
2.5 CMV感染危险因素分析
与无CMV 感染组相比,CMV 感染组移植年龄>65 个月、恶性血液病、非亲缘全相合移植、发生Ⅱ~Ⅳ级aGVHD的发生比例较高,差异有统计学意义(P<0.05)。见表3。二元logistic回归分析发现患儿移植年龄>65个月、移植后发生Ⅱ~Ⅳ级aGVHD是发生CMV 感染的独立危险因素,亲缘全相合移植能降低CMV感染的发生风险(P<0.05)。见表4。

表2 CMV感染患儿分布情况 (n=269)
2.6 RCI危险因素分析
与非RCI 组相比,RCI 组脐血干细胞来源、发生Ⅱ~Ⅳ级aGVHD、输注CD34+细胞量≤1.009×106/kg、输注总有核细胞量≤2.17×108/kg的比例较高,差异有统计学意义(P<0.05)。见表3。二元logistic回归分析发现,发生Ⅱ~Ⅳ级aGVHD及使用脐血移植与发生RCI相关(P<0.05)。见表5。
2.7 CMV感染对预后的影响
至随访终点,入组的269例患儿中17例白血病复发,45例死亡(其中32例为移植相关死亡,13例为原发疾病复发相关死亡),中位随访时间16.2个月(11.7~25.0个月),累积总体生存率78.9%。
CMV 感染组和无CMV 感染组之间OS 及DFS 的差异无统计学意义(P>0.05)。RCI 组与非RCI 组OS及DFS的差异有统计学意义(P<0.05)。见图1、图2。
3 讨论
CMV 是一种普遍存于人群中疱疹病毒,在原发感染后会发生潜伏感染,在免疫抑制的情况下,可以发生再激活。CMV感染后有组织嗜性,在免疫低下的个体中,胃肠道及肺部最易被累积,严重者可造成全身性CMV播散[9]。目前治疗CMV感染用药包括更昔洛韦及膦甲酸钠,但存在骨髓抑制作用和肾毒性,进而限制其应用。故对移植后CMV 感染及RCI 高危患儿的早期诊治对改善移植预后仍有重要意义。
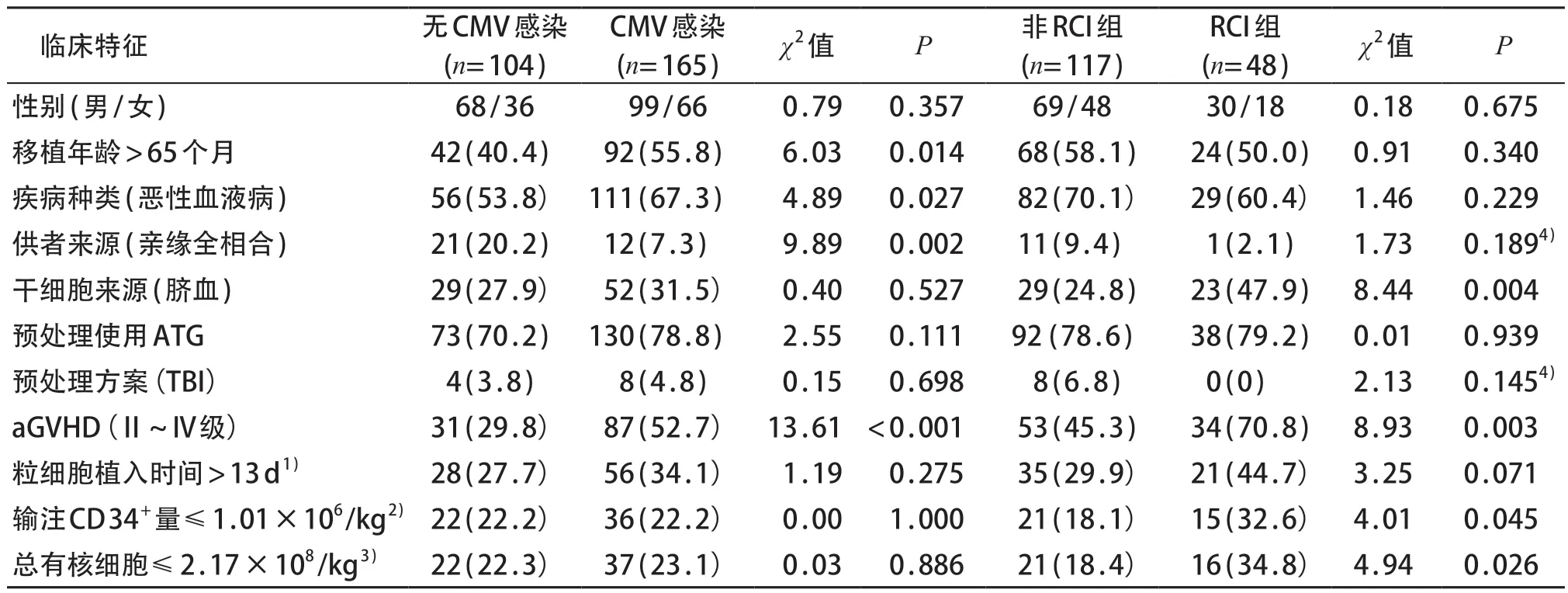
表3 CMV感染与无CMV感染组以及RCI组与非RCI组间比较[n(%)]
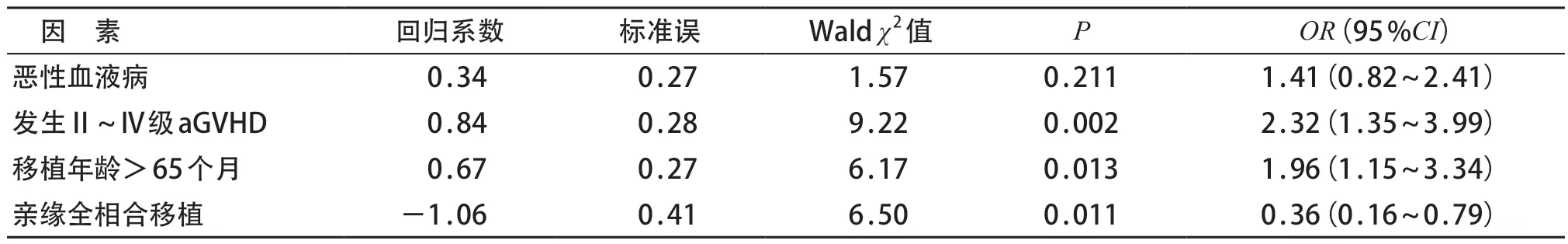
表4 Logistic回归分析CMV感染危险因素

表5 Logistic回归分析RCI危险因素
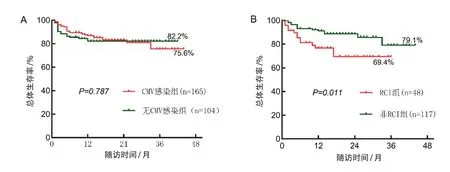
图1 不同组间生存曲线比较
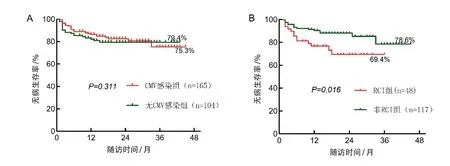
图2 不同组间无病生存率比较
本研究中儿童allo-HSCT 后CMV 感染总体发生率为61.3%,CMV感染发生时间为23 d(15~34 d),感染持续时间38 d(25~66 d),这与相关研究报道儿童CMV感染发生中位时间一致[10]。其中单倍体移植中发生CMV感染的概率为69%,无关供者中发CMV感染为60.8%,亲缘全相合移植发生CMV 感染率为36.4%。与相关研究中单倍体移植患儿CMV 感染的发生率60.6%接近[11]。单倍体移植发生CMV 感染率较亲缘全相合移植明显升高,这与相关研究结果一致[12]。本研究儿童造血干细胞移植后发生RCI 的概率为17.8%,较国内RCI的发生率(29.8%~50.6%)低[13],但目前针对RCI 的研究对象主要为成年人,儿童RCI的相关研究较少。
本研究发现,患儿移植年龄大、发生Ⅱ~Ⅳ级aGVHD 是发生CMV 感染的危险因素,而选择亲缘全相合移植可降低CMV 感染的发生率。相关研究也发现年龄偏大儿童移植后发生CMV 感染风险增加[10]。此外,发生aGVHD 后机体免疫状态遭到破坏及全身性糖皮质激素应用会抑制宿主的抗病毒免疫反应进而导致病毒清除困难和传播。治疗Ⅱ~Ⅳ级的aGVHD伴随着更高剂量和更长时间的全身激素使用[14],将会增加CMV 感染的风险。移植后免疫抑制种类及程度显著影响CMV 感染及RCI 的发生率[13],这也能解释在本研究中97%的CMV感染和RCI患儿发生在移植后的100天以内。既往多认为HLA不全相合的移植较全相合移植的CMV 再激活更明显。HLA 不全相合移植的患者中大多数发生了aGVHD,需要接受糖皮质激素治疗,从而导致CMV 特异性CD 4+和CD 8+T 细胞免疫恢复延迟。目前对HLA 不全相合位点对CMV感染的影响已有更进一步研究[15]。预处理方案中使用TBI 及移植中使用ATG 与CMV 感染相关,但在本研究中未见明显差异,可能与本研究中使用TBI 预处理的患儿数目偏少相关。
本研究中,移植干细胞选择脐血,发生Ⅱ~Ⅳ级aGVHD 是发生RCI 的危险因素。脐血移植患儿发生RCI 较其他干细胞来源发生RCI 的风险增加2.6 倍。由此可见脐血移植后一旦发生CMV感染会更难控制,这与相关研究结果相似[16]。在脐血移植中往往由于供者CMV血清阴性,无特异性病毒T淋巴细胞,受者体内血清阳性而更易发生CMV 活化,因此脐血移植后一旦发生CMV 感染会更难控制。本研究RCI 组首次检测到CMV 感染时间较非RCI 组早,CMV 感染峰值拷贝数高,这与相关研究结果一致[17]。
本研究发现,输注CD 34+细胞数目较少是发生RCI 的危险因素,与相关报道一致[18]。输注总有核细胞较少及中性粒细胞植入时间延长的患儿RCI发生比例较高,但并非为独立危险因素。本研究中发生RCI的部分患儿选用脐血移植,而脐血移植中CD34+细胞及总有核细胞数目有限。
儿童无论有无发生CMV感染,对于OS及DFS的影响未见明显差异,这与相关研究结果一致[18]。但与成人的相关研究结论存在差异[1,19]。在一项研究成人和儿童移植后感染预后的报道中,虽然儿童CMV 感染发生率不低于成人,但所导致的感染相关病死率较成人低[20]。且儿童移植后死亡事件和成人存在差异,感染不是儿童死亡首位因素。本研究中RCI 组与非RCI组之间OS及DFS均可见差异,与相关报道一致[13]。考虑CMV感染本身带来的影响,也可能是长期抗毒药物引起的毒副作用。目前对CMV 再激活能否降低白血病复发率现仍有争议。一项来自国际血液和骨髓移植研究登记处的研究(CIBMTR)认为,在AML及骨髓增殖性疾病中CMV 再激活能降低白血病复发率[19]。考虑本研究随访时间较短,未对CMV 再激活对恶性疾病的复发影响作进一步分析。
本研究表明,患儿移植年龄偏大,移植后发生Ⅱ~Ⅳ级aGVHD是发生CMV感染的危险因素,而选择亲缘全相合移植能降低CMV 感染的发生。选择脐血移植及发生Ⅱ~Ⅳ级aGVHD患儿发生CMV感染后更难控制,更易发生RCI。移植后检测到CMV 感染的时间越早、CMV 感染拷贝数峰值越高的患儿可能提示发生RCI 的可能性越大,应对这些CMV 感染的高危患儿采取更密切的CMV 监视和更合理积极的治疗方案。
