微小病变型肾病综合征合并急性肾损伤患者临床及病理特征分析
2020-09-22卿山林何敬东
卿山林,何敬东,任 波
原发性肾病综合征(primary nephrotic syndrome, PNS)主要表现为“三高一低”,即大量蛋白尿、水肿、高脂血症和低蛋白血症,是一种较为常见的肾内科疾病,临床上可见感染、血液高凝状态、血栓形成、急性肾损伤(acute kidney injury, AKI)、骨和钙代谢异常等并发症[1-4]。在PNS中,微小病变型(minimal change disease, MCD)为常见病理类型,发病率占小儿PNS的70.0%~90.0%,成人PNS的10.9%~38.5%,其中MCD肾病综合征合并AKI具有病情危重等特点[5]。MCD肾病综合征合并AKI是由于各种病因或者病理改变,引发原发性肾小球疾病而导致的综合征,预后较差[6-7]。但由于MCD肾病综合征合并AKI早期临床表现缺乏典型特征,故早期明确诊断存在一定难度。因此,探讨MCD肾病综合征合并AKI患者的临床及病理特征,有利于临床医生尽早诊断,采取最佳治疗方案,从而帮助患者尽快恢复肾功能[8-9]。本研究选取成都医学院第二附属医院收治的33例MCD肾病综合征的临床资料,其中15例合并AKI(45.45%),现对其临床和病理特征进行分析总结如下。
1 资料与方法
1.1一般资料 选取2012年1月—2019年4月成都医学院第二附属医院收治的符合纳入及排除标准的33例MCD肾病综合征作为研究对象,根据有无合并AKI分为观察组(合并AKI,占45.45%)和对照组(无AKI,占54.55%)两组。观察组15例,男12例,女3例;年龄20~79(38.73±19.32)岁;MCD肾病综合征病程2~60(7.43±6.88)d,AKI病程1~8(2.86±0.27)d;AKI 1期11例(73.33%),2和3期4例(26.67%),其中3例使用药物诱发AKI,4例由于感染诱发AKI,8例无明显诱因出现AKI。对照组18例,男9例,女9例;年龄16~76(38.76±19.21)岁;MCD肾病综合征病程3~180(15.41±11.65)d。两组性别、年龄及MCD肾病综合征病程比较差异无统计学意义(χ2=3.182,P=0.074;t=0.050,P=0.961;t=0.579,P=0.832)。本研究经医院医学伦理委员会批准同意执行。
1.2纳入及排除标准 纳入标准:①所有入选患者均符合MCD肾病综合征诊断标准[10],MCD病理表现为光镜下肾小球轻微病变,免疫荧光阴性或少量IgM、补体C3沉积,电镜下足突广泛融合但无电子致密物沉积。②观察组AKI诊断符合国际肾脏病委员会“KDIGO AKI临床实践指南”提出的AKI诊断标准[11]:血肌酐在2 d内增加26.5 μmol/L(0.3 mg/dl )或7 d内增加50%,或者尿量每小时<0.5 ml/kg,持续6 h,符合以上任一情况者,即可诊断为AKI。但由于本研究为回顾性研究很难统计48 h内血肌酐变化值,故本研究将AKI定义为血肌酐升高≥基线1.5倍,并且采用扩展定义,即住院期间血肌酐上升或下降50%,其中超过基线1.5倍为AKI 1期、2倍为2期、3倍为3期[12]。③所有入选患者均行肾脏活组织病理检查证实疾病诊断。
排除标准:①存在其他慢性肾脏病及继发性肾脏病等患者;②合并严重心脑血管疾病、肝功能不全及血液疾病等患者;③存在恶性肿瘤患者;④因外伤导致肾损伤患者;⑤临床及病理资料不完整或缺乏准确性患者。
1.3方法
1.3.1并发症监测:监测所有入选患者低血容量(血压<90/60 mmHg)、肾炎综合征、高血压(血压≥140/90 mmHg)、心力衰竭[脑利钠肽(BNP)≥2000 pg/ml]并肺水肿(有呼吸困难、心率加快、干湿啰音等临床表现,且X线和CT检查示肺门阴影、蝴蝶状表现等)及浆膜腔积液(通过X线和B超检查确定是否存在胸腔积液、心包积液和腹腔积液等)等并发症发生情况。
1.3.2实验室检查:收集所有入选患者24 h尿液采用生化分析仪(德国拜耳公司,1650 生化分析仪)检测尿蛋白。采集所有入选患者清晨空腹静脉血5 ml,离心,分离血清,采用全自动生化分析仪(美国雅培公司,AEROSEt 全自动生化分析仪)检测血肌酐和尿素。
1.3.3病理检查:所有入选患者均于彩色多普勒超声引导下,经皮穿刺右肾下极取活组织,行冷冻病理切片免疫荧光(包括IgG、IgA、IgM、C3、C4、C1q、FRA)和石蜡切片光镜(包括HE、PAS、PASM、MASSON染色)、电镜检查,综合判断肾脏病变病理类型。
1.4观察指标 比较两组并发症发性情况及实验室检查结果,分析MCD肾病综合征合并AKI患者病理特征及治疗、转归情况。
2 结果
2.1并发症发生情况比较 两组低血容量、肾炎综合征及高血压发生率比较差异均无统计学意义(P>0.05)。观察组心力衰竭并肺水肿及浆膜腔积液发生率明显高于对照组,差异有统计学意义(P<0.05)。见表1。
2.2实验室检查结果比较 观察组24 h尿量低于对照组,尿蛋白及血肌酐、尿素水平高于对照组,差异均有统计学意义(P<0.05或P<0.01),见表2。
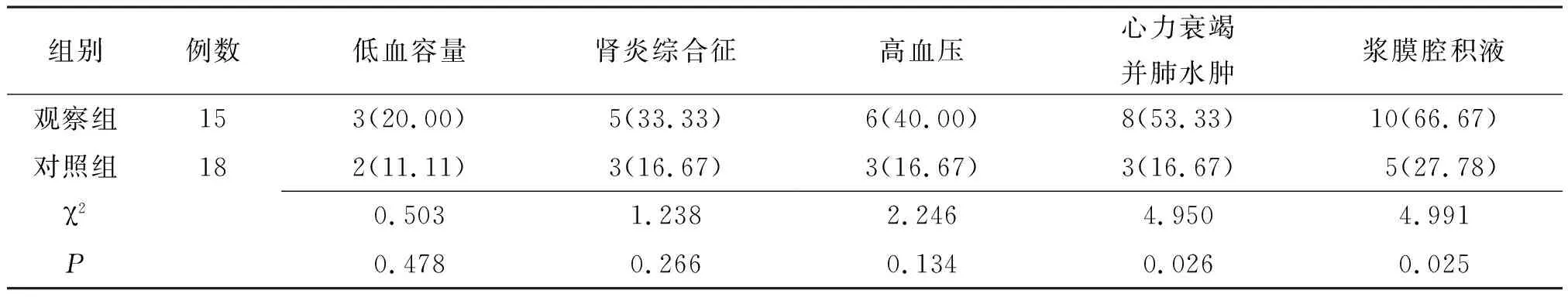
表1 有无合并急性肾损伤微小病变型肾病综合征两组并发症发生情况比较[例(%)]

表2 有无合并急性肾损伤微小病变型肾病综合征两组实验室检查结果比较
2.3MCD肾病综合征合并AKI患者病理特征 MCD肾病综合征合并AKI 15例中出现肾间质弥漫性水肿最多(10例,66.67%),其次为肾小管上皮细胞变性、坏死及脱落伴再生(4例,26.67%),出现肾小管管型最为少见(2例,13.33%)。
2.4MCD肾病综合征合并AKI治疗及转归情况 MCD肾病综合征合并AKI 15例住院期间均给予去除诱因、利尿、维持血容量等治疗,同时使用足量糖皮质激素(泼尼松,每日1.0 g/kg)口服治疗,必要时静脉给予白蛋白支持,水肿明显且白蛋白较低者静脉使用等效剂量甲泼尼龙治疗。AKI 3期2例行血液透析治疗。MCD肾病综合征合并AKI 15例均经相应治疗后尿蛋白呈现不同程度减少,尿量增加,全身水肿减轻或消退,达到完全缓解,且肾功能皆恢复正常。
3 讨论
MCD肾病综合征是临床PNS中常见病理类型,但该病并非独立发作的疾病,而是各种因素导致肾小球毛细血管滤过膜通透性增加,致出现大量蛋白尿造成[13-15]。MCD肾病综合征为肾病综合征中易合并 AKI的病理类型,主要是由于长期低蛋白血症使肾间质水肿,压迫肾小管,滤过率下降所导致;同时体液丢失、外科损伤、腹腔积液及抗高血压药物使用等造成血流动力学改变,可引起肾灌注减少、肾小球滤过率降低,造成AKI;另外,尿路梗阻及药物等因素亦可导致AKI的发生[16-18]。国内外研究结果显示MCD合并AKI的发病率并不一致,Jennette和Falk[19]研究显示MCD肾病综合征患者中AKI发病率为21.00%,尤小寒等[20]报道MCD肾病综合征中AKI发病率为8.50%,章友康等[21]研究显示MCD合并AKI的概率为25.00%。另外,杨琛等[22]对成人MCD肾病综合征403例进行研究,结果发现其中118例发生了AKI,发生率为29.3%。本研究结果显示,33例MCD肾病综合征中AKI发病率为45.45%,较既往研究明显高。考虑其原因可能与本研究所选取样本量较小有关,也可能与既往研究纳入标准与本研究不完全一致有关。此外,对以往相关研究进行分析发现均未对MCD肾病综合征合并AKI患者进行具体分期。本研究结果显示,MCD肾病综合征合并AKI 15例AKI 1期11例,占73.33%;2和3期4例,仅占26.67%。提示MCD肾病综合征合并AKI患者大部分为AKI 1期。本研究AKI 1期患者未发展成2和3期可能与早期诊断、及时正确治疗有关,故早期识别MCD肾病综合征合并AKI尤为重要。
本研究结果显示,观察组低血容量发生率高于对照组,但两组低血容量、肾炎综合征及高血压发生率比较差异无统计学意义。提示血流灌注不足在AKI发生过程中有可能起着一定临床作用[23]。本研究结果显示,观察组心力衰竭并肺水肿及浆膜腔积液发生率明显高于对照组,差异有统计学意义。提示MCD肾病综合征合并AKI患者临床表现较一般MCD肾病综合征患者更为严重,可存在大量蛋白尿或严重低蛋白,甚至出现全身高度水肿和极为严重的高脂血症,从而加大了肺水肿及浆膜腔积液发生的风险。本研究结果还显示,MCD肾病综合征合并AKI 15例中出现肾间质弥漫性水肿最多(10例,66.67%),其次为肾小管上皮细胞变性、坏死及脱落伴再生(4例,26.67%),出现肾小管管型最为少见(2例,13.33%)。表明MCD合并AKI患者病理表现主要为肾小管间质急性损伤。目前,临床上MCD肾病综合征合并AKI患者的治疗原则主要为积极去除诱因,维持稳定血流量,以及足量糖皮质激素使用。本研究MCD肾病综合征合并AKI 15例住院期间均给予去除诱因、利尿、维持血容量等治疗,同时使用足量糖皮质激素(泼尼松,每日1.0 g/kg)口服治疗,必要时静脉给予白蛋白支持,水肿明显且白蛋白较低者静脉使用等效剂量甲泼尼龙治疗。AKI 3期2例行血液透析治疗。MCD肾病综合征合并AKI 15例均经相应治疗后尿蛋白呈现不同程度减少,尿量增加,全身水肿减轻或消退,达到完全缓解,且肾功能皆恢复正常。本研究MCD肾病综合征合并AKI 15例的治疗及转归情况与既往研究报道基本一致[24]。现临床上对于MCD肾病综合征合并AKI的相关认知逐渐提高,从而可及时发现疾病并予以积极治疗,促使患者得到较好预后。但若未及时发现MCD肾病综合征合并AKI,未能及时予以对症治疗,会造成肾功能不全进一步加重,严重时会危及患者生命安全,导致患者死亡。由此可见,临床对MCD肾病综合征合并AKI患者应早期实施正确治疗方案,以减轻肾损害、改善预后。
综上所述,MCD肾病综合征合并AKI患者临床表现较严重、并发症较多,尿蛋白增多是其主要原因;肾小管间质急性损伤为其主要病理表现。临床上在对MCD肾病综合征合并AKI的治疗中,足量糖皮质激素的使用最为关键,而对于水肿明显、白蛋白较低者推荐静脉使用甲波尼龙治疗,对AKI 3期、少尿或无尿患者建议尽早行血液透析治疗。
