新绿原酸的大鼠体内代谢产物的UPLC-Q-TOF MS鉴定△
2020-09-14李洁刘子菡董凡王喻淇王少平代龙张加余卢建秋
李洁,刘子菡,董凡,王喻淇,王少平,代龙,张加余*,卢建秋
1.北京中医药大学 中药学院,北京 102488;2.滨州医学院 药学院,山东 烟台 264003;3.北京中医药大学 图书馆,北京 100029
绿原酸(chlorogenic acids,CGAs)是天然抗氧化剂,也是药食同源中药中最丰富的多酚之一[1]。绿原酸类化学成分是众所周知的抗菌消炎活性成分。此外,该类成分还具有保护DNA[2]、抗溃疡[3]、降低胆固醇、甘油三酯、低密度脂蛋白[4-5]等作用。其中,绿原酸(5-O-咖啡酰奎尼酸)是由咖啡酸与奎尼酸生成的缩酚酸[6],又名咖啡鞣酸和咖啡单宁酸。由于咖啡酰基与奎尼酸结合位点的不同,绿原酸还有新绿原酸(3-O-咖啡酰奎尼酸)和隐绿原酸(4-O-咖啡酰奎尼酸)等重要的同分异构体。
绿原酸类在金银花、菊花、茵陈、忍冬、杜仲等药用植物中含量较高,并凭借显著的抗炎效果成为《中华人民共和国药典》中对中药进行质量控制的指标。然而,绿原酸在高温、强光下不稳定,在中性及碱性条件下容易水解为新绿原酸、隐绿原酸[7]。因此,异构体之间的相互转化直接影响到药品质量,从而影响到临床疗效。药物进入人体后,吸收和代谢是药物体内代谢过程的重要步骤,与药理活性密切相关。目前绿原酸的体内代谢过程研究较为深入,但其位置异构体新绿原酸的研究尚未开展,体内代谢产物尚不明确。因此,新绿原酸的体内代谢过程亟需进一步研究。
超高效液相色谱结合四极杆飞行时间质谱(UPLC-Q-TOF MS)技术具有优秀的色谱重现性以及超高的灵敏度和选择性,可作为中药复杂体系的快速分析平台,并在代谢物鉴定中显示出优异的性能[8-10]。本文基于UPLC-Q-TOF MS筛选鉴定了新绿原酸的体内代谢产物,并阐明其主要的体内代谢通路,以期为绿原酸类成分的新药研发及药材、制剂的全面质量控制奠定基础。
1 材料
Exion LCTMAC液相色谱仪与X500R QTOF质谱,配有双喷雾Turbo V离子源,SCIEX OS 1.3工作站(AB SCIEX公司);R200D型电子分析天平(十万分之一,德国Sartorius公司);Millipore Synergy UV型超纯水机(美国Millipore公司);KQ-250 DE型数控超声波清洗器(昆山市超声仪器有限公司);Eppendorf Centrifuge 5424 R离心机(德国);SPE Cartridges C18固相萃取小柱[500 mg·(3 mL)-1]。
新绿原酸(批号:PRF8050442)、隐绿原酸(批号:PRF8010501)、咖啡酸(批号:PRF7102044)、奎尼酸(批号:PRF8060823)均购自成都普瑞法科技开发有限公司,绿原酸(批号:110753-200413)、阿魏酸(批号:110773-201313)购于中国食品药品检定研究院,异阿魏酸(批号:MUST-14110611)购自成都曼思特生物科技有限公司,所有对照品纯度均大于98%;乙腈和甲醇(质谱级,美国Thermo Fisher 公司);甲酸(色谱级,德国Merck公司)。
Sprague Dawley(SD)大鼠,雄性,体质量(200±10) g,购于北京维通利华实验动物技术有限公司,许可证号:SCXK(京)2016-0006。
2 方法
2.1 对照品溶液的配制
分别取上述7种对照品适量,精密称定,加入甲醇制成质量浓度约100 μg·mL-1的储备液,用时稀释成质量浓度适宜的对照品溶液。
2.2 生物样品的制备
2.2.1对照品给药液的配制 称取新绿原酸180 mg,加入8 mL 0.9%氯化钠溶液,超声至充分混悬,配制成给药溶液,于4 ℃储存。
将8只SD大鼠随机平均分为空白组和给药组。实验前,2组大鼠在动物房内进行适应性饲养1周(室温22~26 ℃,相对湿度40%~70%,12 h昼夜更替),给药前禁食12 h,全程不禁水。给药组按200 mg·kg-1的剂量给予0.9%氯化钠溶液混悬液,而空白组的每只大鼠灌胃等体积0.9%氯化钠溶液。各组均连续给药2 d。
2.2.2血浆样本的收集与储存 大鼠在最后一次给药后0.5、1、2、4 h,分别眼眶静脉取血0.5 mL。所采集的血样置于涂肝素钠的离心管中静置15 min,3500 r·min-1离心10 min(离心半径为5.5 cm),合并上述4个时间点的血液。分别吸取上清液,即得空白血浆和含药血浆,于-80 ℃冰箱冻存。
2.2.3尿样和粪样的收集与储存 灌胃给药后0~24 h内,每隔6 h收集1次尿液和粪便,分别合并。尿样3500 r·min-1离心10 min,后取上清液于-80 ℃冰箱冻存。粪样置于通风橱中晾干后碾碎,装于离心管中冻存。
2.3 大鼠生物样品的前处理
将2组冻存的血浆、尿液生物样本放到室温下解冻。取固相萃取柱,依次用3 mL甲醇和3 mL水对其进行活化,然后分别吸取生物样品2 mL上样,依次用3 mL水和3 mL甲醇洗脱,收集甲醇洗脱液。
取各组粪样适量,按照1∶5(W∶V)比例加入去离子水,超声处理60 min,3500 r·min-1离心10 min,取上清液。取各组处理好的上清液置于固相萃取小柱,用3 mL水冲洗杂质,最后用3 mL甲醇洗脱,收集甲醇洗脱液。
将上述所有甲醇洗脱液,在室温下用氮气吹干,残渣用100 μL的初始流动相复溶,涡旋振荡3 min后,14 000 r·min-1离心15 min(离心半径为5.5 cm)。取上清液进行分析。
2.4 液质联用分析条件
2.4.1色谱条件 色谱柱:Waters HSS T3 UPLC色谱柱(100 mm×2.1 mm,1.7 μm),流动相:0.1%甲酸水溶液(B)和乙腈(A),进样室温度:15 ℃,柱温:40 ℃,洗脱梯度(0~6 min,2%~10%A;6~10 min,10%~25%A;10~15 min,25%~35%A;15~16 min,35%~40%A;16~20 min,40%~80%A;20~21 min,80%~95%A;21~24 min,95%A),体积流量:0.3 mL·min-1,进样量:5 μL。
2.4.2质谱条件 HESI负离子模式,离子源温度:550 ℃,电离源电压:4.5 kV,鞘气和辅助气均为高纯氮气(纯度>99.99%),扫描模式:Full MS/dd-MS2;数据依赖性ddMS2采集,Full MS分辨率70 000,dd-MS2分辨率17 500,高分辨扫描范围m/z100~1000,碰撞能为30 eV。
2.5 高分辨质谱数据的预处理
药物的代谢产物通常具有相同或者相似的母核结构。基于此,可采用数据采集的质量亏损过滤(MDF)软件进行筛选追踪主要的代谢物,尤其是不可预知的代谢产物。基于母药新绿原酸的化学结构,设置了如下MDF模板:1)母药(m/z353.086 71)及其核心结构咖啡酸和奎宁酸(m/z179.035 02、m/z191.055 04);2)GSH结合产物(m/z660.171 51),糖基化产物(m/z515.140 43),葡萄糖醛酸结合产物(m/z529.119 90)和磺酸化产物(m/z433.043 53)等。另外,MDF窗口设置为±50 mDa。
所有数据采集和处理均在SCIEX OS 1.3.1工作站进行。根据精确分子质量,元素组成和可能发生的反应,对所有的母离子和碎片离子的分子式进行预测。相关参数设置为:C[0-30],H[0-50],O[0-30],S[0-2],N[0-3],环不饱和双键数(RDB equivalent value)[0-15],质量精度误差在1×10-5以内。
3 结果与讨论
3.1 新绿原酸的质谱裂解规律分析
对新绿原酸对照品在负离子模式下的碎片离子进行系统分析,总结得到相关的特征离子。在负离子模式下,新绿原酸的准分子离子峰为[M-H]-m/z353.087 40(1.83×10-6,C16H17O9),在质谱裂解过程中,其先丢掉1分子咖啡酰基,产生特征碎片离子m/z191.055 04(1.10×10-6,C7H11O6),该离子继续丢失1分子水产生m/z173.045 46(0.26×10-6,C9H7O4)。与此同时,还检测到特征碎片咖啡酸离子m/z179.035 02,另外此离子分别丢失1分子水和1分子CO2形成碎片离子m/z161.022 4和m/z135.045 22。可能的裂解规律见图1。
3.2 大鼠体内代谢产物的分析鉴定
通过对给药组生物样品与空白组样品的比较分析,结合在线MDF数据处理软件对新绿原酸代谢产物进行相对准确地筛查、鉴定,最终在大鼠的尿液、血浆和粪便样品中共筛选鉴定了43个代谢产物。其中在血、尿和粪中分别鉴定了20、30、11个,具体的质谱信息见表1。代谢产物的鉴定结果分析如下。
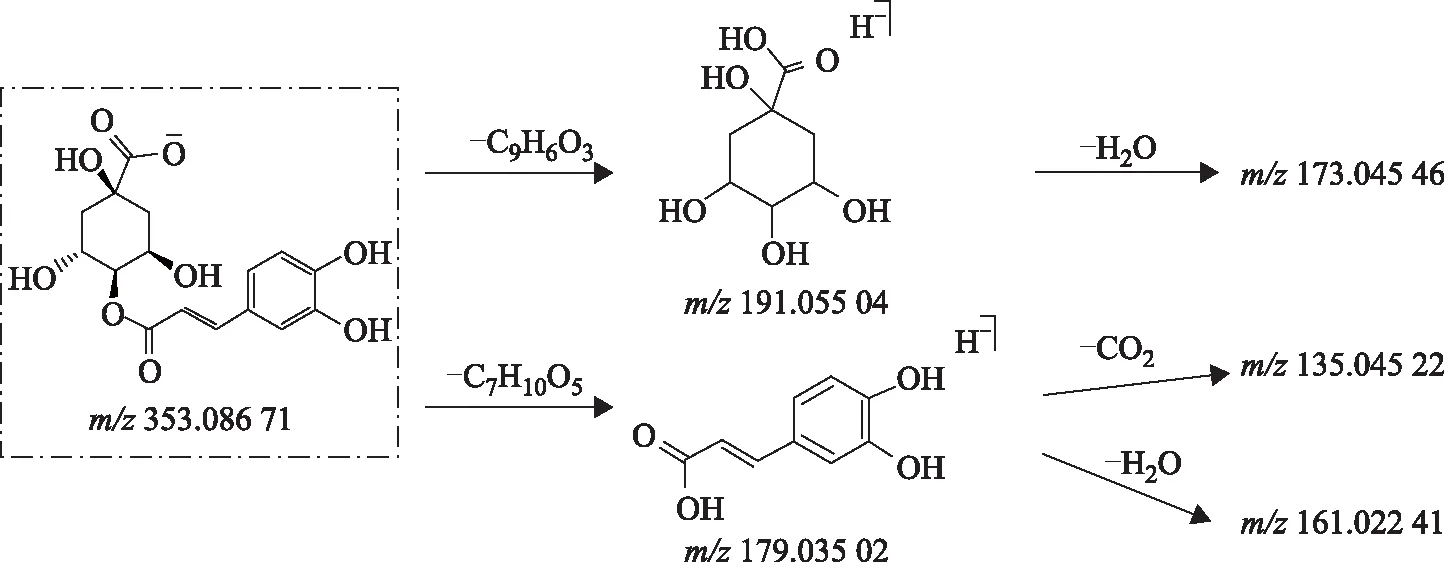
图1 负离子模式下新绿原酸对照品的质谱裂解图

表1 大鼠生物样品中新绿原酸代谢产物的质谱信息
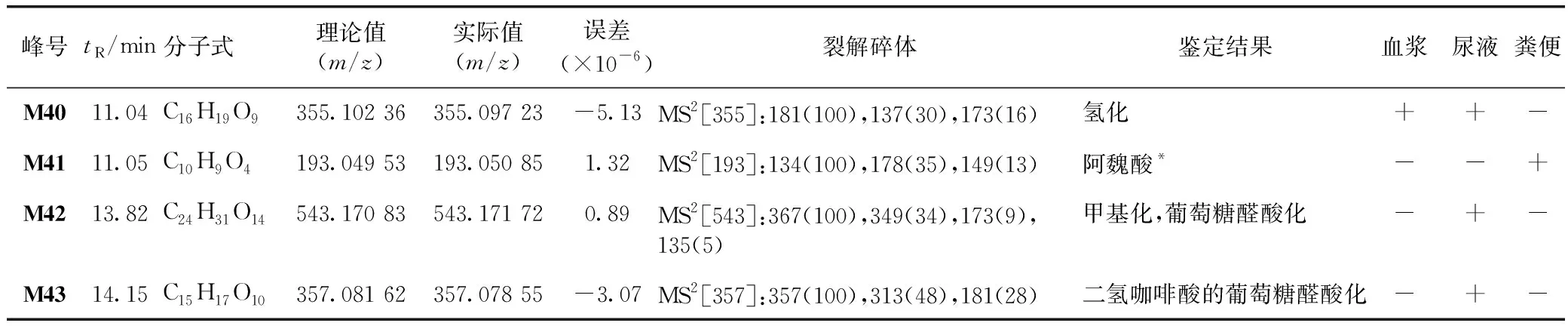
续表1
在负离子模式下,代谢物M10、M20、M17产生相同的准分子离子峰m/z353.086 71[M-H]-,推测其分子式为C16H17O9(误差≤±2.00×10-6)。在其ESI-MS2谱图中,它们均产生碎片离子m/z179.035 02(咖啡酸骨架离子)以及奎尼酸负离子碎片m/z191.055 04。其中,M10和M20的色谱保留时间与质谱裂解信息与新绿原酸、绿原酸相同,因此将两者分别准确鉴定为新绿原酸和绿原酸,并将M17推断为其同分异构体。
代谢物M39、M25、M26的相对保留时间分别为10.79、9.17、9.23 min。它们的准分子离子峰为m/z179.035 26[M-H]-,推断最可能的分子式为C9H7O4(误差≤±2.00×10-6)。在其ESI-MS2谱中,观察到碎片离子m/z135[M-H-CO2]-,表明它们的分子中存在羧基。另外,根据与咖啡酸对照品的保留时间以及质谱裂解行为比对,可将M25准确鉴定为咖啡酸,结合参考文献[11]报道将M39和M26推断为咖啡酸异构体。
代谢物M9、M16具有相同的准分子离子峰m/z181.049 53[M-H]-,比咖啡酸多2。根据精确相对分子质量推测其分子式为C9H9O4,相对误差均小于2×10-6。在ESI-MS2谱中,m/z181丢失1分子H2O(18 Da)产生了主要的碎片离子m/z163,并且可中性丢失1分子CO2(44 Da)形成碎片离子m/z137。结合参考文献[12]报道将两者鉴定为咖啡酸的氢化产物。
M6的准分子离子峰为m/z236.057 07[M-H]-,可知其分子式为C11H10NO5,误差为1.73×10-6。在其ESI-MS2谱图中,m/z236通过中性丢失C2H4NO2和C3H4NO3,生成碎片离子m/z162[M-H-NH2CH2COO]-和m/z134[M-H-C2H4NO2-CO]-,由此推测分子中有甘氨酸和羰基的存在。参照文献[13]报道,可将代谢产物M6鉴定为咖啡酸的甘氨酸结合产物。
代谢物M43在14.15 min被洗脱,其准分子离子峰为m/z357.078 55[M-H]-,推测其分子式为C15H17O10,误差<2×10-6。在ESI-MS2谱图中,m/z357通过中性丢失1分子CO2形成碎片离子m/z313。此外,还观察到碎片离子m/z181[M-H-glucuronide-H2O]-,推测葡萄糖醛酸结合反应发生。结合文献[14]报道,M43被鉴定为二氢咖啡酸的葡萄糖醛酸结合产物。
代谢物M4在准分子离子峰在m/z147.045 43[M-H]-,推测其相对分子式为C9H7O2(误差0.03×10-6)。在其ESI-MS2光谱中,m/z147通过中性丢失1分子CO2生成碎片离子m/z103[M-H-CO2]-。此外,它的相对分子质量比咖啡酸少32 Da。结合文献[15]报道以及相关的生物转化规律,将M4鉴定为肉桂酸。
M28的准分子离子峰为m/z163.040 30[M-H]-,根据精确相对分子质量推测其分子式为C9H7O3。M28的相对分子质量比咖啡酸少16 Da,并产生碎片离子m/z119[M-H-CO2]-,表明有羧酸基团的存在。因此,将M28鉴定为咖啡酸的脱羟基产物香豆酸。
M8、M14、M11、M15有相同的准分子离子峰m/z261.006 35[M-H]-,推测其分子式为C9H9O7S,所有质量误差均小于2×10-6。在ESI-MS2谱图中,由于中性损失1分子SO3和1分子CO2,分别产生碎片离子m/z181[M-H-SO3]-和m/z137[M-H-SO3-CO2]-,说明它们的分子结构中存在羧基和磺酸基。结合相关文献[14]报道,它们被鉴定为二氢咖啡酸磺酸化结合物。
代谢物M23的保留时间为9.08 min,准分子离子峰为m/z273.007 40[M-H]-,其分子式为C10H9O7S(质量误差0.20×10-6)。在ESI-MS2谱图中,由于中性丢失SO3、CO2和CH3,分别产生碎片离子m/z193[M-H-SO3]-、m/z149[M-H-SO3-CO2]-和m/z134[M-H-SO3-CO2-CH3]-,表明分子结构中存在羧酸基团、硫酸基团以及甲基。基于上述推论和相关的生物转化反应,M23被鉴定为甲基化咖啡酸的磺酸化产物。
M35的准分子离子峰为m/z135.044 06[M-H]-,保留时间为10.24 min。此外,分子式为C8H7O2(质量误差1.34×10-6)。在ESI-MS2图谱中,由于中性丢失1分子CH3,从而观察到二级碎片离子m/z120[M-H-CH3]-。根据相关的生物转化规律,将M35鉴定为咖啡酸脱羧产物。
代谢物M19、M30、M41的保留时间为8.64、9.41、11.05 min,准分子离子峰为m/z193.049 53[M-H]-。根据精确相对分子质量推测其分子式为C10H9O4(质量误差均在2.00×10-6以内)。在ESI-MS2图谱中,由于中性丢失1分子CO2和1分子CH3产生碎片离子m/z178[M-H-CH3]-、m/z149[M-H-CO2]-和m/z134[M-H-CO2-CH3]-,表明分子中存在羧基和甲基。通过与对照品的质谱碎片离子信息和色谱保留时间比较,M41被准确鉴定为阿魏酸,M30被准确鉴定为异阿魏酸,M19推断为其同分异构体。
M22、M38的色谱保留时间分别为9.01、10.72 min,准分子离子峰分别为m/z165.055 89和m/z165.055 85,根据精确相对分子量可知分子式组成为C9H9O4(误差分别为1.29×10-6和1.25×10-6)。在ESI-MS2图谱中,两者均通过丢失1分子CO2在m/z121[M-H-CO2]-处形成产物离子,这表明其分子中存在羰基。根据先前报道的文献[16],M22和M38被鉴定为对羟基苯丙酸或其异构体。
代谢物M1的准分子离子峰为m/z191.056 14[M-H]-,保留时间为0.93 min,分子式为C7H11O6(质量误差1.13×10-6)。在ESI-MS2图谱中,通过中性丢失1分子水和1分子CO2产生碎片离子m/z173[M-H-H2O]-和m/z147[M-H-CO2]-。此外,中性丢失2分子水和1分子CO2产生碎片离子m/z111[M-H-CO2-2H2O]-。据此推断分子中极有可能存在至少2个羟基和1个羧基。M1与奎尼酸对照品的色谱保留时间和质谱碎片相同,因此结合参考文献[17]将代谢物M1准确鉴定为为奎尼酸。
代谢物M2准分子离子峰为m/z173.045 72[M-H]-,基于精确分子质量可知其分子式为C7H9O5(误差≤±2.00×10-6)。其分子离子比奎尼酸少18 Da,推测它极有可能是奎尼酸的脱羟基产物。在ESI-MS2图谱中,通过中性丢失1分子CO2产生碎片离子m/z129[M-H-CO2]-,另外中性丢失1分子H2O产生碎片离子m/z155[M-H-H2O]-,这表明分子中存在羟基和羧基。结合相关的文献[11]报道,将代谢产物M2鉴定为莽草酸。
代谢物M27的准分子离子峰为m/z121.029 85[M-H]-,分子式为C7H5O2(误差为1.45×10-6)。此外,它通过丢失1分子CO产生碎片离子m/z93[M-H-CO]-,这表明该化合物中存在羰基。根据先前报道的文献[18],代谢产物M27被鉴定为苯甲酸。
代谢物M12准分子离子峰为m/z137.024 59[M-H]-。分子式为C7H5O3(误差为1.27×10-6),其分子离子比苯甲酸多16 Da,推测可能是苯甲酸的羟基化产物。在ESI-MS2图谱中,通过中性丢失1分子CO2和1分子H2O分别产生碎片离子m/z93[M-H-CO2]-和m/z109[M-H-H2O]-,表明该化合物中存在羟基和羰基。根据先前报道的文献[19],将代谢物M12鉴定为3-羟基苯甲酸。
代谢物M18准分子离子峰在m/z178.051 07[M-H]-,基于精确分子质量、同位素丰度比可知其分子式为C9H8NO3(误差1.21×10-6)。在ESI-MS2图谱中,通过中性丢失1分子CO2产生二级碎片离子m/z134[M-H-CO2]-,这表明分子中有羧酸基团的存在。因此,将其鉴定为马尿酸。
代谢物M13在7.77 min时洗脱,准分子离子峰为m/z194.046 43[M-H]-。其分子式为C8H8NO4(误差1.63×10-6)。另外,它的分子离子比马尿酸多16 Da。此外,通过中性丢失1分子CO2和1分子CH3生成碎片离子m/z135[M-H-CO2-CH3]-和m/z150[M-H-CO2]-,表明分子中存在羧基和甲基。因此,结合参考文献[19]将其鉴定为3-羟基马尿酸。
代谢物M3、M7色谱保留时间分别为4.7、6.15 min。它们的准分子离子峰为m/z197.044 45[M-H]-,分子式组成为C9H9O5(误差≤±2.00×10-6)。在ESI-MS2图谱中,通过丢失1分子OCH2、1分子H2O和1分子CO2生成碎片离子m/z167[M-H-OCH2]-,m/z149[M-OCH3-H2O]-和m/z121[M-OCH3-H2O-CO]-,表明分子中存在甲氧基、羰基以及羟基。结合相关的生物转化知识,代谢物M3、M7鉴定为丁香酸或其异构体。
代谢物M5色谱保留时间为5.33 min。在其ESI-MS谱图中,准分子离子峰m/z167.034 97[M-H]-(分子式为C8H7O4,误差1.09×10-6)。在其ESI-MS2谱图中,通过中性丢失1分子CO2(44 Da)和1分子H2O(18 Da)产生碎片离子m/z123[M-H-CO2]-和m/z149[M-H-H2O]-,这表明分子中存在羧基和羟基。结合相关的文献报道将其鉴定为香草酸。
在ESI-MS谱图中,代谢物M40的准分子离子峰为m/z355.097 23[M-H]-(C16H19O9,误差-5.13×10-6),色谱保留时间为11.04 min。其分子式比原型药物多2H,推测它是新绿原酸的氢化产物。除此之外,在其ESI-MS2谱图中,观察到二级碎片m/z173[奎尼酸-H2O-H]-和m/z181[二氢咖啡酸-H]-和m/z137[二氢咖啡酸-CO2-H]-。因此,代谢物M40鉴定为二氢新绿原酸。
在C17H19O9提取离子流图中,可以检测到4个准分子离子峰M21、M29、M34、M37(误差均 ≤± 2.00×10-6),色谱保留时间为8.92~10.42 min。它们分子式比原药新绿原酸多CH2。在其ESI-MS2谱图中,它们都具有相同的产物离子m/z134.045 22。此外,还存在碎片离子m/z191.055 04[奎尼酸-H]-和m/z173.045 72[奎宁酸-H2O-H]-。综上分析,它们具有与原药相同的特征离子并且比原药分子离子多14 Da,因此将其鉴定为新绿原酸的甲基化产物。
M24、M31、M32、M33、M36有相同的准分子离子峰为m/z369.118 01[M-H]-(C17H21O9,误差≤± 2.00×10-6)。它们分子式比原药的甲基化产物多2 H。在其ESI-MS2光谱中,它们具有与原药相同的特征离子m/z191[奎尼酸-H]-,m/z173[奎尼酸-H2O-H]-,据此推断它们是甲基化绿原酸的氢化产物。
代谢物M42保留时间为13.82 min,准分子离子峰为m/z543.170 83[M-H]-(C24H31O14)。在其ESI-MS2谱图中,通过丢失176 Da产生碎片离子m/z367[M-H-C7H12O5]-,这表明其分子中含有葡萄糖醛酸。且m/z367比原药分子式多CH2,结合二级碎片离子m/z173[奎宁酸-H2O-H]-和m/z135[咖啡酸-CO2-H]-。表明有奎尼酸骨架、咖啡酸骨架存在。因此,M42被鉴定为甲基新绿原酸的葡萄糖结合产物。
3.3 大鼠体内新绿原酸的代谢途径分析
新绿原酸进入大鼠体内后发生了广泛的代谢反应[20-22]。结合代谢产物分析新绿原酸在体内的代谢过程及转化,结果见图2,其在体内主要发生的反应有3种。1)异构化:在新绿原酸给药后的生物样品中发现了绿原酸和其异构体,说明新绿原酸在体内进行了位置异构等反应。2)分解反应:新绿原酸进入体内后可以水解为咖啡酸和奎尼酸2个核心代谢产物,并在此基础上发生进一步的二次代谢反应。奎尼酸经体内代谢转化为莽草酸,经2次脱羟基后生成羟基苯甲酸,再脱羟基变为苯甲酸,经过与甘氨酸结合后生成马尿酸,最后马尿酸羟基化反应生成3-羟基马尿酸;奎尼酸也可以直接转化为丁香酸,而后脱去甲氧基和羟基生成香草酸。而咖啡酸也发生多种反应。例如,甲基化生成阿魏酸或异阿魏酸;还原反应生成二氢咖啡,并在此基础上进行硫酸酯化生成二氢咖啡酸硫酸酯结合物或者二氢咖啡酸葡萄糖醛酸化生成二氢咖啡酸葡萄糖醛酸结合物;咖啡酸还发生了分解反应,比如脱羧反应,再者脱羟基后生成香豆酸而后继续脱羟基生成肉桂酸等。3)其他反应:首先新绿原酸容易还原生成二氢新绿原酸;其次甲基化反应,新绿原酸在咖啡酸侧链上发生甲基化反应;最后,新绿原酸能够在侧链上连接葡萄糖醛酸发生葡萄糖醛酸结合反应。
4 结论
本研究利用UPLC-Q-TOF MS高分辨液质联用技术分析鉴定了新绿原酸在大鼠的血浆、尿液和粪便样品中的代谢产物。通过分析这些代谢产物的精确相对分子质量、特征碎片离子以及色谱保留行为等,共筛选鉴定出包括新绿原酸原型在内的43个代谢产物。同时,本研究还推测了新绿原酸的体内代谢途径,初步阐释了其发挥药效的物质基础轮廓。新绿原酸的体内代谢产物主要有咖啡酸、阿魏酸、异阿魏酸、莽草酸、香草酸等,它们均具有很好的抗菌、抗氧化作用,这为阐明新绿原酸发挥抗菌、抗炎等药理活性提供了一定依据。上述研究结果也为含有绿原酸类物质的中药及食品的体内代谢研究提供了借鉴,尤其对药效物质基础的研究具有重要参考意义。

图2 新绿原酸在大鼠体内的代谢途径
