HPLC测定盐酸苯达莫司汀纯度和降解破坏
2020-09-10杜超,邵斐,唐云,李伟*
杜 超,邵 斐,唐 云,李 伟*
(1.宜春学院 化学与生物工程学院,江西 宜春 336000;2.深圳万乐药业有限公司,广东 深圳 518000)
盐酸苯达莫司汀,是目前医疗领域对抗肿瘤病症的主要药物之一。当前,其主要用于治疗非霍奇金淋巴瘤、乳腺癌以及骨髓瘤等多种疾病,并且使复发与死亡出现的机率显著降低[1-2]。盐酸苯达莫司汀最早是60年代在东德被合成出来,本意是想合成一种比其他烷化剂毒性更小,但性能相当的的氮芥化合物,当把氮芥群移到苯并咪唑环的5位上后,就形成了一种新的氮芥类化合物[3]。后来,因为其逐渐用于抗肿瘤领域,且疗效明显,最终被名为盐酸苯达莫司汀。同时,因为它独特的结构特征,使其同时具有烷基化和抗代谢作用。其构成部分主要是一个氮芥群,一个苯并咪唑环和一个丁酸侧链[4-5],结构式见图1。

图1 盐酸苯达莫司汀结构式
盐酸苯达莫司汀是一种双功能烷化剂,具有拮抗肿瘤,杀灭或抑制细胞发育的功能。其机制是利用药物的烷化功能,使DNA单、双链交叉结合,干扰DNA的功能与合成,进而使肿瘤的生长趋势减缓[6]。在体内药物动力学中,药物可以在人的红细胞中自由分布,不会抑制人肝微粒体酶,且无蓄积。从而表明,其安全性高,对肿瘤细胞具有针对性,因此具有良好的推广前景。
目前该药物在我国尚未得到大范围推广应用,国内对盐酸苯达莫司汀药品质量的检测标准还未成型,参阅相关资料文献[7-8],采用HPLC仪器,探索出一种测定盐酸苯达莫司汀纯度及降解破坏的方法。本研究就盐酸苯达莫司汀在各种破坏的情况下,了解降解产物的情况,从而为其后期的稳定性等试验提供一定的参考价值。
1 仪器与试药
1.1 仪器
Waters2695分离系统,2996检测器,Empower色谱管理系统;烘箱(太仓市华利达,ZDF-6021);电子天平(梅特勒-托利多,XP205);强光照射试验箱(重庆市永生,SHH-300GD-2);水浴锅(上海宜昌仪器,XMTD-6000)
1.2 试药
盐酸苯达莫司汀中试样品(深圳万乐药业有限公司提供,批号:191202);氮甲基吡咯烷酮(NMP)(上海跃进,色谱纯,19010738);盐酸(西陇科学,AR,190327);氢氧化钠(广东省化学试剂,AR,20171227);乙腈(默克,色谱纯,JB086630);三氟乙酸(TFA)(上海麦克林,色谱纯,C10672543);30%过氧化氢(西陇科学,AR,190327)
2 实验部分
2.1 HPLC检测条件
采用高效液相色谱法(HPLC),选择ZORBAX BONUS-RP(4.6 x150mm,5um) 色谱柱,流动相A:0.1%TFA水溶液,流动相B:0.1%TFA乙腈溶液,稀释剂:以NMP-0.1%TFA水溶液(1:1),流速:为1.0 mL/min,波长:254 nm,时长:45 min。同时按照表1序列进行梯度洗脱。
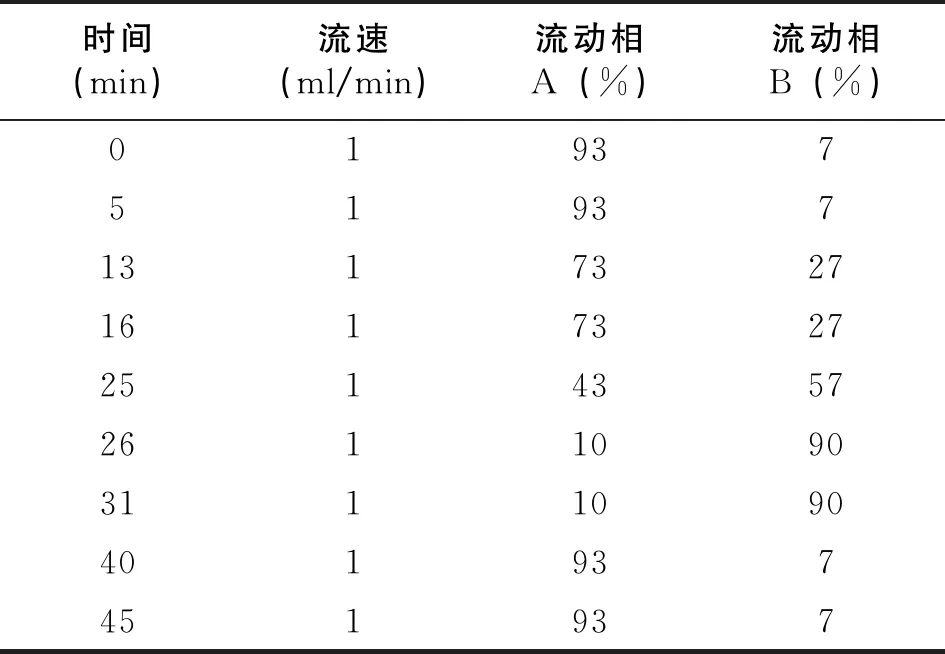
表1 流动相梯度洗脱表
2.2 盐酸苯达莫司汀样品纯度分析
称取本品适量,加稀释剂NMP-0.1%TFA水溶液溶解成每1 mL约含0.5mg的溶液。同法配制空白。取供试品溶液20μL,注入色谱仪,记录色谱图。

图2 盐酸苯达莫司汀纯度分析色谱图-空白
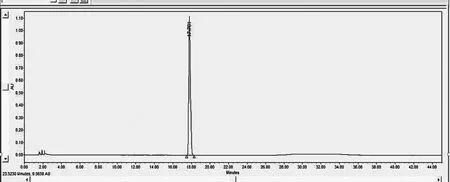
图3 盐酸苯达莫司汀纯度分析色谱图-样品
从图可以发现,盐酸苯达莫司汀样品在17分钟左右开始出峰,并且可以看出其峰面积非常大,峰形较好,基本没有杂质峰的出现。通过峰面积归一化法,我们可以看出盐酸苯达莫司汀样品的纯度分析非常高,含量高达99.8%。
2.3 破坏性实验分析
通过对盐酸苯达莫司汀的纯度分析,我们了解到其纯度非常高。但是,外界或内部的影响是否会对它在成影响,这还是需要进行下一步的研究。同时,文献查阅可知,对于发现未知的降解产物,了解降解途径,其方法思路都是通过强制破坏性实验进行的。并且了解分子内在的稳定性,认证所使用分析方法的有效性。所以,通过对盐酸苯达莫司汀进行破坏性的实验研究,从而为后期临床使用与存放提供参考[9-10]。
2.3.1 酸破坏实验
室温条件下,精密称取,盐酸苯达莫司汀样品约12.5 mg,置25mL容量瓶中。加盐酸溶液(1 mol/L)1mL,浸润润湿后,并按照同样的方法调配空白溶液。之后,将调配好的样品与空白溶液于60℃水浴放置1h。水浴过后,取出样品与空白溶液并冷却至室温。之后,滴加氢氧化钠溶液(1 mol/L)调节PH至中性,加稀释剂NMP-0.1%TFA水溶液定容至刻度,同法调配空白溶液的pH至中性(防止剧烈条件对仪器损坏)。量取酸破坏溶液及空白各20μL,注入色谱仪,记录盐酸苯达莫司汀样品变化的色谱图。

图4 盐酸苯达莫司汀酸破坏色谱图—空白

图5 盐酸苯达莫司汀酸破坏色谱图-样品
从图可以看出,盐酸苯达莫司汀样品经过1 mol/L的盐酸溶液破坏后,在HPLC色谱图上有A,B两个明显的降解峰,且这两个杂质峰在盐酸苯达莫司汀样品色谱图中并未出现,为新杂质峰。归一化法计算得到:A,B的杂质含量分别为5.22%,7.19%,明显超出ICH规定的单个杂质限度(单个杂质%<0.1),从而说明盐酸苯达莫司汀样品在酸性环境下会产生大量的降解杂质,所以盐酸苯达莫司汀产品在后期的保存中应避免处于酸性环境下。
2.3.2 碱破坏实验
室温条件下,精密称取,盐酸苯达莫司汀供试品约10.0 mg,置20 mL容量瓶中。同时,加氢氧化钠溶液(1 mol/L)1mL,浸润润湿后,并按照同样的方法调配空白溶液。然后,将调配好的样品与空白溶液室温暗处放置5h。5小过后,滴加盐酸溶液(1 mol/L)调节PH至中性,加稀释剂NMP-0.1%TFA水溶液稀释至刻度,同法调配空白溶液pH至中性。量取碱破坏溶液及空白各20μL,注入色谱仪,记录盐酸苯达莫司汀样品变化的色谱图。

图6 盐酸苯达莫司汀碱破坏色谱图-空白

图7 盐酸苯达莫司汀碱破坏色谱图-样品
从图可以看出,盐酸苯达莫司汀样品经过1mol/L的氢氧化钠溶液破坏后,在HPLC图谱上有六个明显降解杂质峰,其中C,D,E,F降解峰在以前的色谱图中均未出现,属于新型杂质峰;而杂质峰A,B在酸破坏的图谱中就已存在,但峰面积明显减小。归一化法计算得到:A,B,C,D,E,F的杂质含量分别为0.55%,1.43%,0.36%,0.61%,1.33%,0.89%。从而说明盐酸苯达莫司汀样品在碱性环境下会产生大量的降解杂质,所以盐酸苯达莫司汀产品在后期的保存中应避免处于碱性环境下。
2.3.3 氧化破坏实验
室温条件下,精密称取,盐酸苯达莫司汀样品约12.5 mg,置25 mL容量瓶中。然后,加入30%过氧化氢浓溶液(30%)1 mL,浸润润湿后,并按照同样的方法调配空白溶液。之后,将调配好的样品与空白溶液,室温暗处放置2.5 h。之后,加稀释剂NMP-0.1%TFA水溶液稀释至刻度。量取氧化破坏溶液及空白各20μL,注入色谱仪,记录盐酸苯达莫司汀样品变化的色谱图。
图8 盐酸苯达莫司汀氧化破坏色谱图-空白
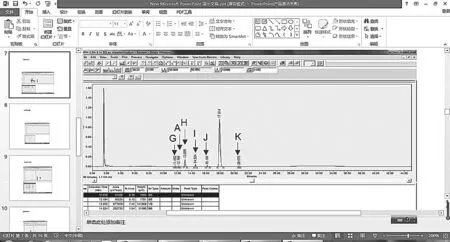
图9 盐酸苯达莫司汀氧化破坏色谱图-样品
从图可以看出,盐酸苯达莫司汀样品经过30%的过氧化氢溶液破坏后,在HPLC图谱上有六个明显降解杂质峰,其中G,H,I,G,K降解峰在以前的色谱图中均未出现,而且杂质峰H的峰面积最大,属于新型杂质峰;而杂质峰A在酸破坏的图谱中就已存在,但峰面积明显减小。归一化法计算得到:A,G,H,I,J,K的杂质含量分别为0.13%,0.10%,7,4 %,1.54 %,0.56%,0.2%。从而说明盐酸苯达莫司汀样品在在氧化条件下会产生大量的降解杂质,所以盐酸苯达莫司汀产品在后期的保存中应进行密闭保存,防止其被氧化。
2.3.4 高温破坏实验
(1)高温破坏实验(溶液样品):
室温条件下,精密称取,盐酸苯达莫司汀样品约12.5 mg,置25 mL容量瓶中。加稀释剂NMP-0.1%TFA水溶液溶解并定容至25 mL,于40℃水浴中20分钟,放冷至室温,即得高温破坏溶液。同法制备空白溶液。量取高温破坏溶液及空白各20 μL注入色谱仪,记录盐酸苯达莫司汀样品变化的色谱图。
图10 盐酸苯达莫司汀高温破坏实验-溶液空白色谱图

图11 盐酸苯达莫司汀高温破坏实验-溶液样品色谱图
从图可以看出,盐酸苯达莫司汀样品经过在40℃水浴放置20分钟破坏后,在HPLC色谱图上有六个明显的杂质峰,其中杂质峰H,K在以前的色谱图中就已出现,且杂质峰H的峰面积在经过高温破坏后,超越了先前氧化破坏的峰面积。而杂质峰L,M,N,O在以前的色谱中均未出现,属于新型杂质峰。归一化法计算得到,L,H,K,M,N,O的杂质含量分别为0.52%,11.64%,0.12 %,0.15 %,0.21%,0.14%。从而说明,盐酸苯达莫司汀溶液样品在高温环境下非常不稳定,并产生大量的降解杂质。因此,盐酸苯达莫司汀溶液样品应放置阴凉处存放。
(2)高温破坏实验(固体样品):
室温条件下,取本品适量,在130℃烘箱放置8h后。冷却至室温,称取盐酸苯达莫司汀样品约12.5 mg,置25 mL容量瓶中。加稀释剂NMP-0.1%TFA水溶液溶解,定容至刻度,即得高温破坏溶液。量取高温破坏溶液及空白各20 μL,注入色谱仪,记录盐酸苯达莫司汀样品变化的色谱图。
图12 盐酸苯达莫司汀高温破坏实验-固体空白色谱图
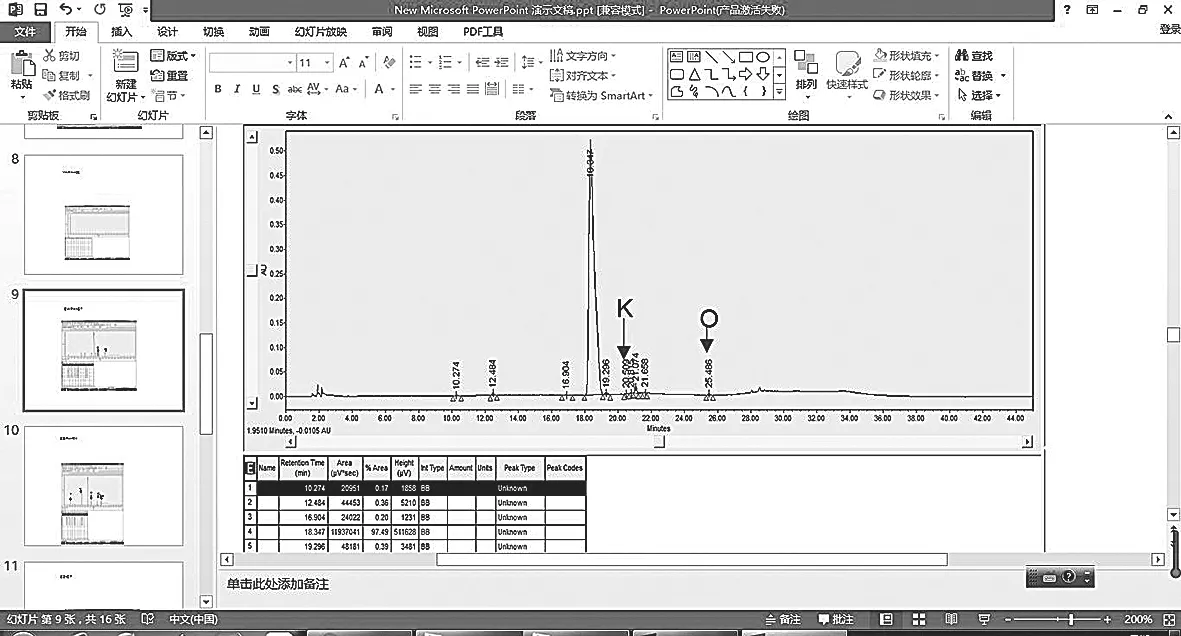
图13 盐酸苯达莫司汀高温破坏实验-固体样品色谱图
从图看出,盐酸苯达莫司汀样品经过在130℃烘箱放置8小时破坏后,色谱图中出现较多的杂质峰,除了杂质O和杂质K在之前的色谱图出现过,其他的均为新型杂质峰。根据峰面积归一化法计算得到,图谱中的杂质含量总和约为2.51%,主峰峰面积则为97.49%。从而说明,盐酸苯达莫司汀固体样品长期处于高温环境下,会影响后期的稳定性。所以,盐酸苯达莫司汀样品应避免长期处于高温环境。
2.3.5 光照破坏实验
(1)光照破坏实验(固体样品):室温条件下,取适当样品,在日光灯10000lx下放置5天,90 uW/cm2,1天。两个循环以后,取本品12.5 mg,加稀释剂NMP-0.1%TFA水溶液溶解并稀释至25 mL即得光照破坏溶液。量取高温破坏溶液及空白各20 μL,注入色谱仪,记录盐酸苯达莫司汀样品变化的色谱图。

图14 盐酸苯达莫司汀光照破坏-固体空白色谱图
图15 盐酸苯达莫司汀光照破坏-固体样品色谱图
从图看出,盐酸苯达莫司汀固体样品经过在日光灯10000lx下放置5天,90 uW/cm2,1天,两个循环以后。色谱图中并未出现降解杂质,从而说明光照对盐酸苯达莫司汀固体样品的影响不大。
(2)光照破坏试验(溶液样品):精密称取本品12.5 mg,加稀释剂NMP-0.1%TFA水溶液溶解并稀释至25 mL,在日光灯10000lx下放置5天,90 uW/cm2,1天,即得光照破坏溶液。并按照同样的方法调配空白溶液。量取高温破坏溶液及空白各20 μL,注入色谱仪,记录盐酸苯达莫司汀样品变化的色谱图。
图16 盐酸苯达莫司汀光照破坏-溶液空白色谱图
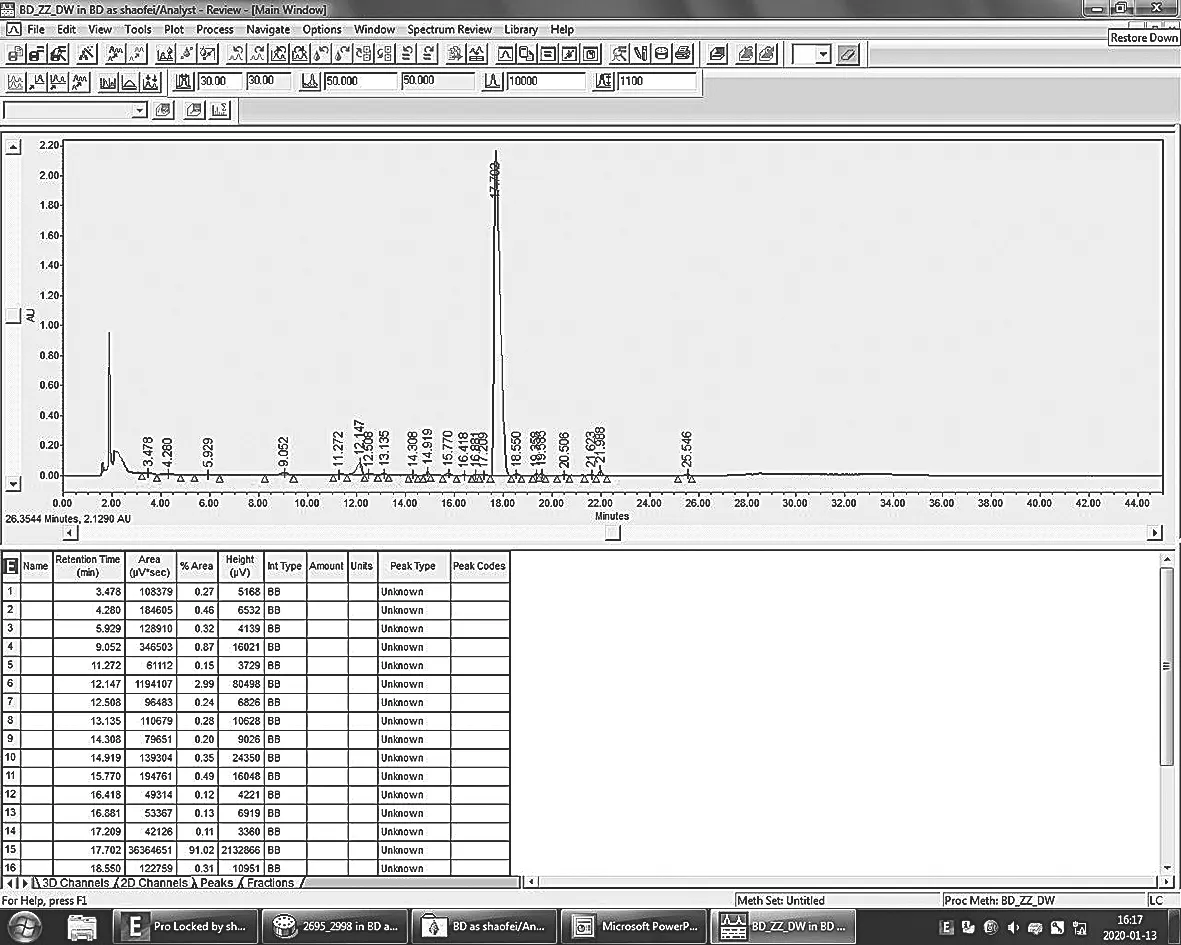
图17 盐酸苯达莫司汀光照破坏-溶液样品色谱图
从图可看出,盐酸苯达莫司汀样品经过在日光灯10000lx下放置5天,90 uW/cm2,1天,两个循环处理以后。图谱出现了大量杂质,且种类和数量明显增加。根据峰面积归一化法计算得到,主峰峰面积仅有91.02%,其他杂质总和为8.98%。从而说明,盐酸苯达莫司汀溶液样品在强光环境下,会产生大量的杂质。因此,盐酸苯达莫司汀溶液样品应在凉暗处存放和使用。
3 总结与讨论
盐酸苯达莫司汀试样与其所含的杂质可以通过HPLC法进行分离检测,最终能够采用峰面积归一化法得到盐酸苯达莫司汀的纯度含量;
盐酸苯达莫司汀的破坏性试验结果如下:
(1)酸破坏实验:其表明,酸对于盐酸苯达莫司汀样品的纯度影响较大,产生两个杂质峰,且含量较大。因此,盐酸苯达莫司汀样品应避免处于这种环境中。
(2)碱破坏实验:其表明,碱对于盐酸苯达莫司汀样品的纯度影响比较大,产生六个杂质,相比酸破坏,其种类和数量明显增加。所以,盐酸苯达莫司汀样品应避免处于这种环境中。
(3)氧化破坏实验:其表明,过氧化氢对于盐酸苯达莫司汀样品的破坏性更大,种类和数量较于酸碱破坏,都明显增加。故盐酸苯达莫司汀样品应密闭存放,防止氧化。
(4)高温破坏实验:其表明,盐酸苯达莫司汀固体样品长期处于高温状态下,会产生降解。同时,高温对盐酸苯达莫司汀溶液样品的纯度影响则更明显,杂质数量也明显增多。因此盐酸苯达莫司汀样品应避免长期处于高温状态下。
(5)光照破坏实验:其实表明,盐酸苯达莫司汀固体样品不受光照破坏的影响,但是盐酸苯达莫司汀溶液样品则受光照影响较大。故盐酸苯达莫司汀样品的使用和存放应尽量避免强光照射。
结论:酸度破坏,碱度破坏,氧化破坏以及高温对盐酸苯达莫司汀样品的纯度影响十分明显,并且产生了大量的降解物杂质,降解物杂质种类和数量繁多。光照破坏对于盐酸苯达莫司汀固体样品几乎没有影响,但对于溶液样品影响巨大。所以,盐酸苯达莫司汀应当避免置于此类环境之中。对于造成其不稳定的原因,经过初步分析是由于结构的特殊性导致的。如结构中的氮芥群和丁酸侧链,虽然它们赋予了盐酸苯达莫司汀完整的烷基化作用,但也使得其更易受外界环境的影响。
同时,通过HPLC谱图分析可知,盐酸苯达莫司汀样品出峰时间,出峰高度,降解产物以及其他杂质峰之间存在和较大的区别,二者能够进行分离检出,从而进一步验证了该法的可行性。
