反应温度对Raney-Ni催化剂1,4-丁炔二醇加氢性能的影响及其结构变化
2020-09-09郜宪龙莫文龙马凤云陈隽陈莉
郜宪龙,莫文龙,马凤云,陈隽,陈莉
(1.新疆大学 化学化工学院 新疆维吾尔自治区重点实验室煤炭洁净转化与化工过程,新疆 乌鲁木齐 830046;2.新疆美克化工股份有限公司,新疆 库尔勒 841000)
1,4-丁烯二醇是重要的化工原料之一,广泛用于农药、药物、化工、电池、造纸等领域[1-3]。雷尼镍(Raney-Ni)具有制备简单、活性高及稳定性强等优越性,广泛应用于加氢、脱氢、脱卤等反应[4-9]。侯凯军等[10]发现,反应温度升高,乙烯收率增加,在620 ℃达到最大值。孙卫中等[11]研究显示,反应温度为850 ℃所制备的试样,具有较高的CH4产率,为90%。闫飞飞等[12]发现,反应温度升高,液体产率先增加后减少,于380 ℃差率最大,94.40%。综上所述,反应温度对催化剂性能的影响较为显著。本文主要考察了不同反应温度对Raney-Ni催化剂的结构和1,4-丁炔二醇加氢性能的影响。
1 实验部分
1.1 试剂与仪器
镍铝合金粉(ZL-N401,Ni 48%~50%,Al余量),工业级;无水乙醇、氢氧化钠、1,4-丁炔二醇均为分析纯;氢气(99.9%)。
78-1磁力搅拌器;CJF-605反应釜;GC-2014C气相色谱仪;Rigaku D/max2500型X射线衍射仪;Autosorb-2型物理吸附仪;H-600型透射电子显微镜;ICP-OES 730电感耦合等离子发射光谱仪;CJF-605型反应釜。
1.2 催化剂制备
采用10%(质量分数)NaOH溶液,浸取工业级Ni-Al合金粉(80~100目),恒温(80 ℃)水浴中搅拌90 min,无水乙醇洗涤数次,直至中性,所制备的Raney-Ni样品最终保存在无水乙醇中,记为RN。
1.3 催化剂表征
采用X射线衍射仪进行试样的X-射线衍射分析,Cu靶Kα射线(λ=1.540 56 nm),Ni滤波,扫描速度8(°)/min。使用物理吸附仪在液氮温度-196 ℃下进行材料的孔结构参数测定。采用透射电子显微镜观察试样的表面形貌。采用电感耦合等离子发射光谱仪测试催化剂的元素含量:准确称取0.100 0 g试样于50 mL聚四氟乙烯消解管,加入适量无机酸(5 mL浓硝酸或1 mL氢氟酸)后将消解管放入不锈钢反应釜,于190 ℃烘箱中恒温加热10 h后,将溶液转移至25 mL塑料容量瓶,并用去离子水定容。通过ICP谱图确定各样品元素含量。
1.4 催化剂试样性能评价
1.4.1 评价实验 在50 mL反应釜中进行催化剂的性能评价(见图1)。评价条件:P=4.0 MPa,T=110~160 ℃,t=3 h,r=500 r/min。原料为30 mL 35%(质量分数)BYD溶液,催化剂加入量为BYD溶液质量的1%。反应后的催化剂试样分别对应命名为RN110、RN120、RN130、RN140、RN150、RN160。加氢液相产物经气相色谱仪分析。

图1 1,4-丁炔二醇反应评价装置示意图
1.4.2 产物计算方法 本实验采用气相色谱仪,选择SH-Rtx-Wax型毛细管柱,分离BYD加氢反应的主要产物。以BYD转化率(X)、BED选择性(S)和收率(Y)评价加氢反应催化剂的性能。
主反应方程:

BYD(1) BED(2)
副反应方程:

BED BDO(3)
HO-CH2-CH2-CH=CH-OH→
BED
HO-CH2-CH2-CH2-COH
HBD(4)
BYD转化率(X):
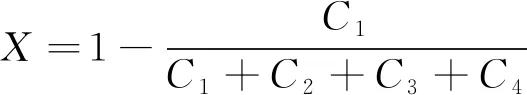
(1)
BED选择性(S):
(2)
BED收率(Y):
Y=S×X×100%
(3)
其中,Ci表示组分i的摩尔百分含量。其中,i=1,2,3,4分别代表组分BYD、BED、BDO和HBD。
2 结果与讨论
2.1 催化剂性能评价
温度对催化剂试样BYD加氢性能影响见图2。

图2 催化剂BYD的转换率、BED的选择性和收率
由图2可知,温度升高,BED的收率增加,于150 ℃达到最大,为48.25%。
由图2还可知,各试样BYD转化率在20%~51%之间,说明反应温度对所制备的Raney-Ni催化剂应用于1,4-丁炔二醇加氢反应体系性能差异较大。反应温度增加至160 ℃,BYD转化率未发生明显变化,为50.49%,说明≥160 ℃的反应温度已不利于该反应的进行。

2.2 加氢反应后催化剂的表征
2.2.1 试样元素含量的变化 对不同温度加氢反应后的催化剂试样进行了ICP元素定量分析,结果见图3。

图3 不同温度催化剂的元素含量
由图3可知,对于加氢反应后的试样,当温度为140 ℃时,Ni/Al摩尔比值最大,为3.98,继续升高温度,反而略有所降低。另外,当温度为140 ℃时,试样RN140活性组分Ni含量较大,为87.73%。Raney-Ni催化剂除了含有大量Ni元素外,通常还含有少量的Al元素,若Al被完全浸取,则催化剂的骨架结构会严重坍塌,产生颗粒团聚现象,降低催化剂的活性,因此残余适量的Al对保持催化剂的活性有显著作用[13-14]。Ni/Al比较小时,对催化剂粒子活性贡献较大的NiAl3含量较少,BYD转化率较低[15];而在更高Ni/Al下,起支撑作用的Ni2Al3物种少,试样稳定性差。综合活性与结构稳定性,Ni/Al比存在一个适宜的值。另外,由图3(d)可知,各试样中活性组分Ni元素含量均在86%以上,比浸取前试样中的Ni含量,48%,高179%,表明该浸取过程有大量的Al元素被NaOH洗去([Al(OH)4]-→Al(OH)3+OH-,以氢氧化铝形式,进一步老化为水合氧化铝沉淀)。另外,随温度的升高,助剂Fe和Cr的含量均略有下降,可能是在长时间的搅拌中使其同等程度的部分流失。
2.2.2 X射线衍射分析(XRD) 图4为不同温度催化剂加氢反应后的XRD图。
由图4可知,试样RN在2θ=44,51,75 °左右发现了Ni的特征峰[16]。试样RN具有较强的Ni特征衍射峰,经加氢反应后,活性组分Ni的特征峰出峰强度显著降低。试样RN110~RN160在2θ=51.5,75.6°未检测出活性组分Ni的特征峰,可能原因是试样在反应釜中经过3 h的剧烈高速搅拌,使Ni分散程度增加,晶面遭到破坏。
2.2.3 N2-低温物理吸附(BET)
2.2.3.1 N2吸附-脱附曲线 不同温度催化剂的N2吸附-脱附曲线表征结果见图5。
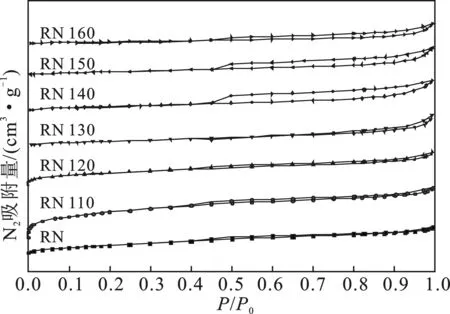
图5 不同温度催化剂N2吸附-脱附等温线
根据理论与应用化学联合会(IUPAC)分类法可以看出[16],试样等温线均为Ⅲ型,且为H3型滞后环,其形貌可能呈片状结构。为进一步说明催化剂的形貌变化,后续进行了TEM表征分析。
由图5可知,不同温度反应后催化剂的回滞环面积存在较大差异。未反应的催化剂试样回滞环极小,吸附线与脱附线几乎重合。试样RN110、RN120、RN130回滞环较为扁平;温度升高到140 ℃,回滞环明显增大;RN160回滞环面积反而略微减小,可能由于温度过高,反而造成Raney-Ni催化剂骨架结构的坍塌。
不同反应温度催化加氢反应后的催化剂的BJH孔径分布曲线见图6。

图6 催化剂孔径分布图
由图6可知,根据N2吸附-脱附等温线测试分析原理可知,各试样孔径峰值均在5~50 nm之间,说明催化剂具有介孔的特征。各试样最可几孔径具有较大的差异,试样RN为20 nm,RN110为12 nm,RN130为12 nm,RN140为15 nm,RN150为19 nm,RN160为20 nm。
2.2.3.2 孔结构参数 图7给出了反应后试样的孔结构参数。

图7 催化剂的比表面积、孔体积和平均孔径
由图7可知,温度升高,试样比表面积减小。平均孔径呈增大的变化趋势。另外,相比于反应前,试样RN120、RN130、RN140、RN150和RN160平均孔径均增大,原因可能是Raney-Ni为骨架结构,高温反应造成小孔塌陷,而大孔所受到的影响比较小,造成平均孔径变大。
2.2.4 透射电镜(TEM) 图8为不同温度催化剂加氢反应后的低倍透射电镜图。
由图5可知,各反应后试样均以片状形貌存在。由图8可知,对于RN试样,表面明显可观察到似树叶形状的结构。另外,相比于未发生反应的试样,形貌发生明显变化。试样RN120为多层片状,明显出现多重叠加的现象;试样RN140和RN150明显由多层叠加的片状形貌,转变成为较稀薄的片状形貌且表面具有较为明显的清晰纹路,使其具有更大的接触面积,催化加氢活性更好。

图8 不同温度催化剂反应后的TEM图
3 结论
本文采用10%的NaOH溶液浸取商品Ni-Al合金粉,制备Raney-Ni催化剂,考察了不同温度对1,4-丁炔二醇加氢与Raney-Ni催化剂性能与结构的影响。通过表征手段和评价试验发现,试样RN150具有较佳的催化性能,BYD转化率为51.00%,BED选择性和收率分别为94.61%,48.25%。
