电催化还原二氧化碳制甲醇的实验研究
2020-09-09刘清田戚霁周屈兰李娜
刘清田,戚霁,周屈兰,李娜
(西安交通大学 能源与动力工程学院,陕西 西安 710049)
当今全球能源需求和使用量的增加,带来经济发展的同时,也带来严重的环境问题。二氧化碳作为化石燃料的主要产物,是气候变化的主要原因[1]。因此,减少其排放并将其利用,是一项值得研究的问题。
在室温常压下,CO2的电催化反应是很好的途径,因为其反应条件较低,反应速率及转化率都较高,可以为大规模生产提供便利。80年代中期Hori等[2-3]开始利用铜箔电化学还原CO2。许多第IV族金属氧化物的还原速率低,同时还产生氢[4-6]。由于CO2的高吸附能量,Cu2O中的Cu通过电子捕获直接将CO2还原为甲醇[7-10]。
因此,本文通过溶液浸泡法制取了氧化亚铜薄膜电极,通过电沉积法制备了氧化锌薄膜,并以附着氧化锌薄膜的氧化亚铜薄膜电极作为电催化二氧化碳制甲醇的电极,并在不同的电极面积大小、不同电解液浓度、不同电极制备时间、不同Zn2+浓度、不同反应温度等条件下考察不同电极对制甲醇反应的电解反应活性。
1 实验部分
1.1 试剂与仪器
无水甲醇、无水乙醇、碳酸氢钠、氧化锌、硫酸铜、硝酸锌、盐酸等均为分析纯;工业级氮气;99.99%纯度的二氧化碳。
GC7900型气相色谱仪;ZL12-RZ1020-3P型蠕动泵;N117型质子交换膜;0142YB-24-80型直流稳压电源;HH-1型水浴锅;CPA225D型电子天平;M-50LPM-D以及D08-1F型质量流量计;玻璃反应釜等。
1.2 氧化亚铜薄膜电极的制备[11]
将铜箔片放入煮沸的饱和硫酸铜溶液中进行反应,制备氧化亚铜薄膜电极。反应方程式为:

(1)
取6片铜箔片(10 cm×5 cm),依次放入10%体积分数的稀盐酸溶液和无水乙醇中浸泡,以去除表面附着的杂质,用蒸馏水清洗干净,分别编号1~6号,将1~3号的铜箔片光滑面用胶布粘贴覆盖,只留粗糙面进行反应,编号4~6号的铜箔片不做处理,然后放入80 ℃的硫酸铜饱和溶液中,分别反应1,2,4 h。取出铜箔片,去除1~3号铜箔片粘贴的胶布,之后将1~6号铜箔片放置于80 ℃的热水中2 h,以去除铜箔片表面的硫酸铜。将铜箔片于150 ℃真空干燥2 h。得到6片附着氧化亚铜薄膜的铜箔片,见表1。

表1 氧化亚铜薄膜电极反应情况
1.3 氧化锌薄膜催化剂的制备
以Zn(NO3)2溶液作为电解液,阴极电沉积氧化锌薄膜,反应方程式如下:
(2)
取5片制备时间为2 h的氧化亚铜薄膜电极,分别编号1~5号。
称取一定量的Zn(NO3)2·5H2O,溶解于去离子水中,定容,静置,备用。浓度分别为0.04,0.05,0.1 mol/L。
取氧化亚铜薄膜电极片,反应温度设定为70 ℃,沉积电位为-1.2 V,Zn2+浓度为0.05 mol/L,反应时间30 min。氧化亚铜薄膜电极片沉积情况见表2。

表2 氧化锌薄膜电极反应情况
1.4 实验方法
反应系统见图1。

图1 反应系统图
用电子天平称适量的碳酸氢钠固体粉末,加入蒸馏水中,分别配制出20,30,40,50,60 ℃饱和碳酸氢钠溶液。将两个玻璃反应釜按照侧边开孔的位置对齐,分别向两侧反应釜中倒入适量的蒸馏水和不同温度的碳酸氢钠饱和溶液。将反应釜放入水浴锅中,开启水浴锅,设定不同的加热温度。将氧化亚铜薄膜电极接入稳压电源阴极,并放入碳酸氢钠溶液一侧的反应釜中。将Pt电极接入稳压电源阳极,并放入蒸馏水一侧的反应釜中。当反应釜中溶液的温度达到设定的温度时,封上反应釜盖板,开启二氧化碳气瓶的解压阀,用质量流量计控制气瓶内的气体以100 mL/min的速率通过反应釜盖板上方预留通气孔通入碳酸氢钠溶液一侧的反应釜中。开启稳压电源,在不同的反应时间点取样。液态产物从取样口取出,经取样针注射气相色谱仪中进行检测。
2 结果与讨论
2.1 氧化亚铜薄膜电极电化学还原二氧化碳性能测试
2.1.1 电极面积大小对于甲醇产量的影响 制备时间分别为1,2,4 h的Cu2O在不同电极面积下的甲醇产量见图2。
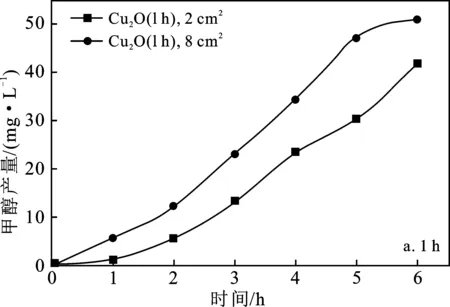
图2 甲醇产量与电极面积大小的关系
由图2可知,制备时间为2 h的氧化亚铜薄膜电极的性能要比1 h及4 h的性能更好,在电压24 V、温度为20 ℃、碳酸氢钠溶液浓度为96 g/L、反应时间6 h的条件下,2 h电极的甲醇产量比4 h的产量高出4.59%,比1 h的甲醇产量高出了41.07%;相同反应条件下,相同制备时间的氧化亚铜薄膜电极在增加面积的情况下,甲醇产量会有提升,但是制备时间为2 h和4 h的氧化亚铜薄膜电极的提升并不明显,1 h制备时间的氧化亚铜薄膜电极的提升较为明显。
2.1.2 反应温度对于甲醇产量的影响 不同温度下甲醇产量变化见图3。

图3 甲醇产量与反应温度的关系
由图3可知,温度的升高对于甲醇产量的提升有较为明显的促进作用,促进表现接近线性,反应时间6 h的甲醇产量随温度的提升接近 0.585 9 mg/(L·K)。
2.1.3 电解液浓度对于甲醇产量的影响 电解液浓度对甲醇产量的影响见图4。

图4 甲醇产量与电解液浓度的关系
由图4可知,碳酸氢钠溶液浓度的增加对于甲醇的产量及产率都有提升,并且提升表现接近为线性,反应6 h的甲醇产量随着碳酸氢钠溶液浓度每增加1 g可以提高0.258 7 mg/L。
2.2 氧化锌薄膜对于甲醇产量的影响
2.2.1 氧化锌薄膜制备时间对甲醇产量的影响 实验结果见图5。
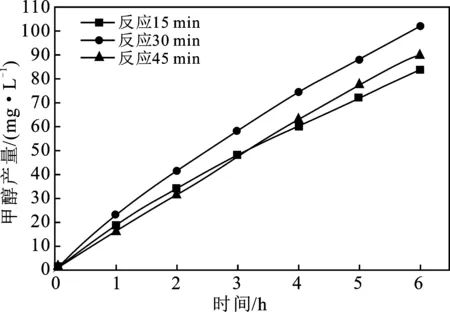
图5 甲醇产量与氧化锌薄膜制备时间的关系
由图5可知,不同制备时间生成的氧化锌薄膜电极对于甲醇产量的提升程度不同,其中,制备时间为30 min的氧化锌薄膜对于甲醇产量提升效果最优,电解反应6 h以后甲醇的产量比制备时间为15,45 min的氧化锌薄膜分别提升了21.09%和13.04%,无论是产量以及产率都在三者中最优。
2.2.2 锌离子浓度对甲醇产量的影响 实验结果见图6。
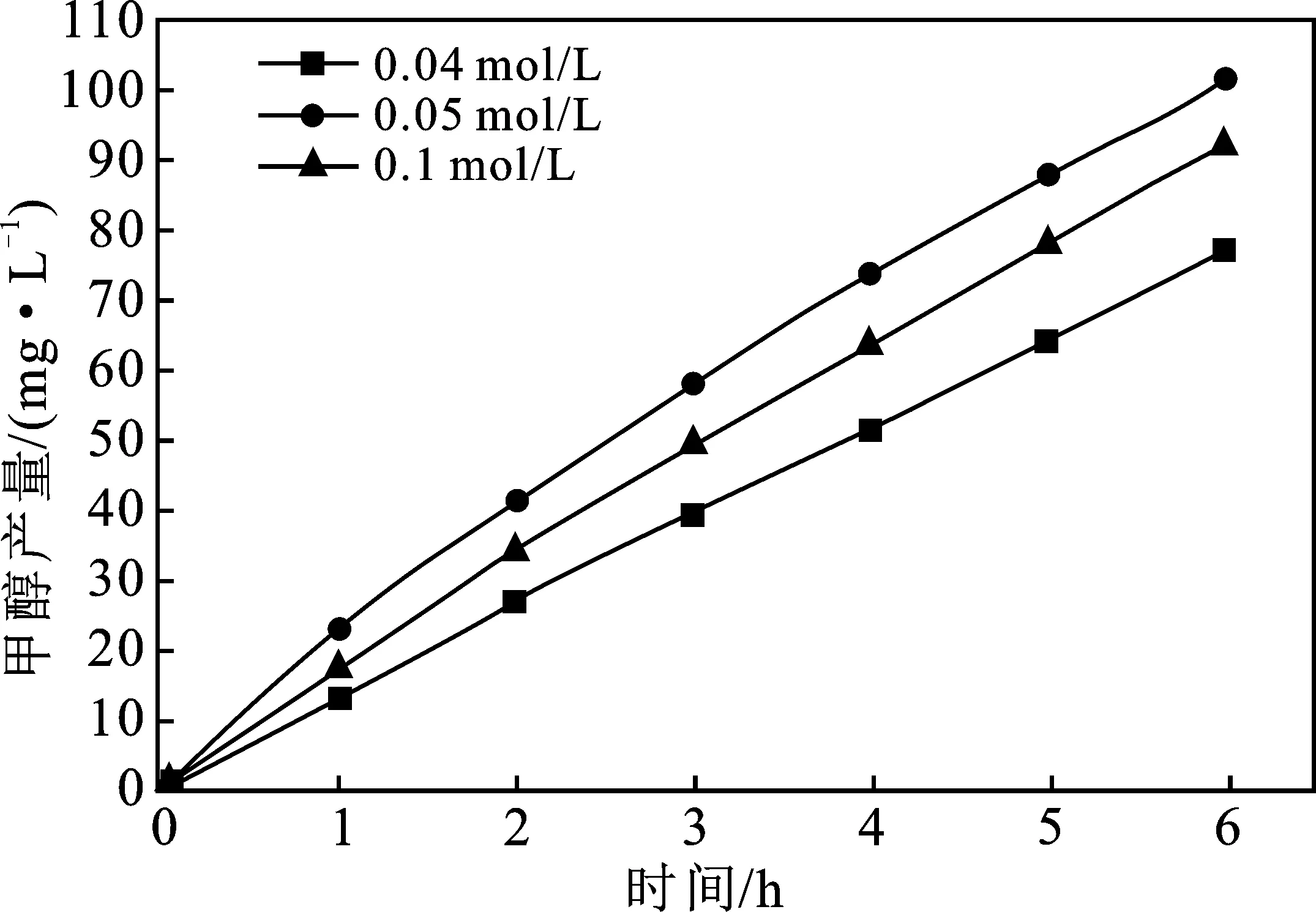
图6 甲醇产量与锌离子浓度的关系
由图6可知,在氧化锌薄膜制备时,不同锌离子浓度条件下生成的氧化锌薄膜电极对于甲醇产量的提升程度不同,Zn2+浓度为0.05 mol/L的氧化锌薄膜对于甲醇产量提升效果最优,电解反应6 h以后甲醇的产量比Zn2+浓度为0.04,0.1 mol/L的氧化锌薄膜分别提升了31.08%和10.22%。
3 结论
(1)随制备时间增大,电极表面的氧化亚铜颗粒逐渐增大,但制备时间较短又会导致电极表面覆盖程度不足,降低反应性能,2 h制备时间的氧化亚铜薄膜颗粒大小适中,表面覆盖率极高,理论上具备良好的电解性能的潜力;同样,制备时间较短生成的氧化锌薄膜颗粒晶粒尺寸过小,而且可能会有不完整的情况,而过大的晶粒尺寸会造成比表面积的减小,对催化活性有一定的伤害。所以,制备时间为30 min条件下生成的氧化锌薄膜有更优越的催化活性。
(2)无催化剂的氧化亚铜薄膜电极电解二氧化碳制备甲醇的最优条件是:氧化亚铜薄膜制备时间为2 h,反应温度为60 ℃,碳酸氢钠溶液的浓度为164 g/L(1.95 mol/L,60 ℃饱和溶液)。
(3)氧化锌薄膜对于该电解实验具有非常良好的催化促进作用。制备条件为Zn2+浓度为0.05 mol/L,制备时间为30 min的氧化锌薄膜电极的甲醇产量最多。因为这种条件下生成的氧化锌薄膜生长良好,颗粒大小适中,也较为完整,产量适中,电极覆盖密度较大的同时没有造成氧化锌的大量堆积,在电极表面存有一定空隙。
