基于质量回顾的某胃药持续质量改进分析
2020-09-08
510285广州白云山光华制药股份有限公司,广东广州
产品质量回顾
产品质量回顾是企业针对产品一系列生产和质量相关数据进行的回顾分析,以评价产品生产工艺一致性及相关物料和产品质量标准适用性,以对其趋势进行识别并对不良趋势进行控制,从而确保产品工艺稳定可靠,符合质量标准要求,并为持续改进产品质量提供依据[1]。具体应开展年度质量回顾分析的产品有:①高风险品种:如注射剂类产品、精神药品、毒性药品、放射性药品、麻醉药品、血液制品、疫苗等;②常年生产、产量较大的品种。
《药品生产质量管理规范》(以下简称GMP)在2010年版首次对其作出法规要求,第266 条规定:应当按照操作规程,每年对所有生产药品按品种进行产品质量回顾分析,以确认工艺稳定可靠及原辅料、成品现行质量标准适用性,及时发现不良趋势,确定产品及工艺改进方向。应当考虑以往回顾分析历史数据,还应当对产品质量回顾分析有效性进行自检。第267 条规定:应当对回顾分析结果进行评估,提出是否需要采取纠正和预防措施或进行再确认或再验证的评估意见及理由,并及时、有效完成整改。法规还具体规定回顾分析至少包括内容,共有12 个方面,分别为:①产品所用原辅料的所有变更,尤其是来自新供应商的原辅料;②关键中间控制点及成品的检验结果;③所有不符合质量标准的批次及其调查;④所有重大偏差及相关的调查、所采取的整改措施和预防措施的有效性;⑤生产工艺或检验方法等的所有变更;⑥已批准或备案的药品注册所有变更;⑦稳定性考察的结果及任何不良趋势;⑧所有因质量原因造成的退货、投诉、召回及调查;⑨与产品工艺或设备相关的纠正措施的执行情况和效果;⑩新获批准和有变更的药品,按照注册要求上市后应当完成的工作情况;○1相关设备和设施,如空调净化系统、水系统、压缩空气等的确认状态;○12委托生产或检验的技术合同履行情况。企业可针对产品从这12 个方面进行回顾分析,以确认产品工艺是否稳定可靠,产品质量是否稳定,有无不良趋势。因此产品质量回顾也成为企业工艺质量持续改进的重要方法之一。
产品质量年度回顾的内容包括:概述、产品批次、原辅料、变更、返工批次、包装材料、检验数据、退货、偏差、产品投诉、稳定性数据、召回、不合格批、相关设施设备、验证、其他(如质量协议、结论及建议)。药品生产企业应将风险管理的理念运用其中,先对产品进行分类,然后将具有代表性的品种或品规进行提取,进行质量回顾分析,分类的原则主要包括以下几个方面:①该年度变更工艺或关键生产设备等变更(如注射剂灌装设备变更、除菌过滤系统变更、灭菌设备改变)的产品,经质量受权人批准,可按剂型、产品或产品系列进行分类。②常年生产的产品,经质量受权人批准,可按剂型、产品或产品系列进行分类。③委托加工的产品,经质量受权人批准,可按产品或产品系列进行分类。④高风险产品,经质量受权人批准,可按品种或产品系列进行分类。⑤无菌原料药,经质量受权人批准,可按产品或产品系列进行分类。⑥生产工艺和质量控制相似、共线生产的非高风险类产品,经质量受权人批准,可按剂型或产品系列进行分类。
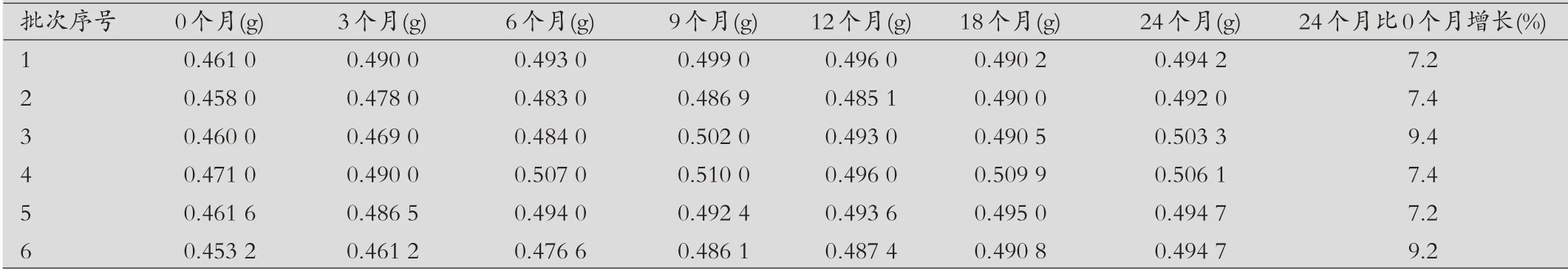
表1 某胃药持续稳定性考察平均装量数据表
产品质量回顾对某胃药的持续质量改进
笔者通过对某胃药质量回顾中持续稳定性考察数据进行分析,发现并证实影响产品质量因素,并采取有效改进措施,提高产品质量。阐述质量回顾对某胃药持续质量改进发挥的作用。
某胃药为单方化学药胶囊剂,PVC铝塑包装,有效期2年,中国药典2015年版标准规定的检验项目有性状、鉴别、检查(崩解时限和装量差异)、含量测定[2]。
发现不良趋势:在对产品进行年度质量回顾时,汇总分析其持续稳定性考察数据,考察项目性状、检查(崩解时限)、含量测定数据均符合标准规定,没有出现不良趋势,但在仔细观察含量测定时,检测相对应平均装量时,发现异常趋势。根据数据显示,平均装量每考察周期有增长趋势,对比24 个月考察周期与0 个月平均装量,均有增长,涨幅为7.2%~9.4%。药企在生产过程中会控制每粒胶囊装量不超过指标水平的6.0%,并且有严格控制和抽检,而20粒平均装量涨幅超过6.0%,且不是一批次出现偶然事件,持续稳定性考察批次均有出现,不可能是生产过程操作偏差,而其他考察项目均符合要求。经查找相关文献,某胃药原料具有引湿性,初步分析可能是产品存在水分增加现象,因某胃药标准无要求水分控制而没有发现这一趋势。见表1,图1。
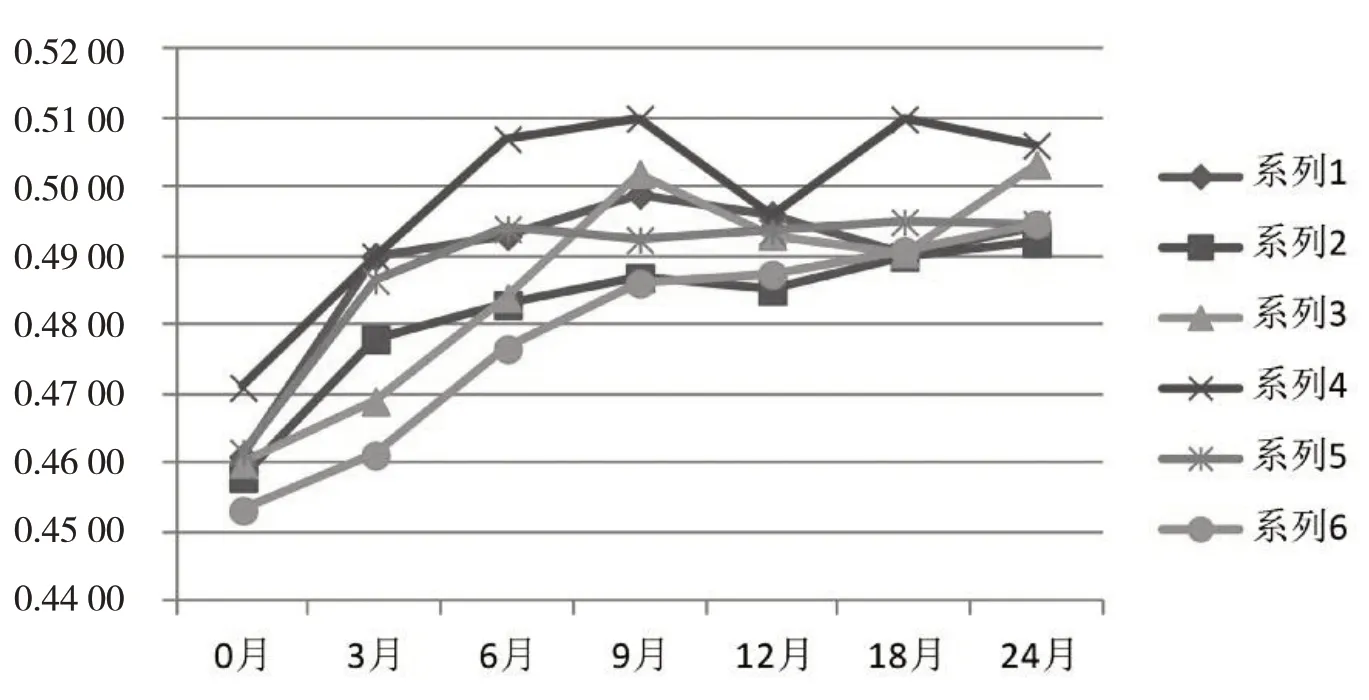
图1 某胃药持续稳定性考察平均装量折线图
影响因素确认:为证实某胃药平均装量增加是否为水分增长,对某胃药增加水分项目稳定性进行考察。数据显示,某胃药在贮存过程确中实存在水分增长趋势,且与平均装量增加水平相当,证实某胃药持续稳定性平均装量增加为水分影响。见表2。
持续质量改进:通过某胃药水分的持续稳定性考察,证实某胃药在现有PVC 吸塑包装条件下,水分有增长趋势,因此需对包装条件重新考虑。某胃药现为PVC 吸塑包装,考虑采用阻隔性能更好的PVC/PVDC 复合硬片吸塑包装进行试验,同时在现有PVC 吸塑包装上增加复合铝袋包装,使用同一批某胃药采用这3 种不同包装形式包装,再进行水分持续稳定性考察。数据显示,PVC/PVDC 复合硬片吸塑包装比PVC 吸塑包装对某胃药水分的阻隔性稍好,但也有显著的增长趋势,而增加复合铝袋包装在某胃药水分考察期内无明显差异。即说明某胃药在现有PVC 吸塑基础上,增加复合铝袋包装,可以保证产品质量。见表3。
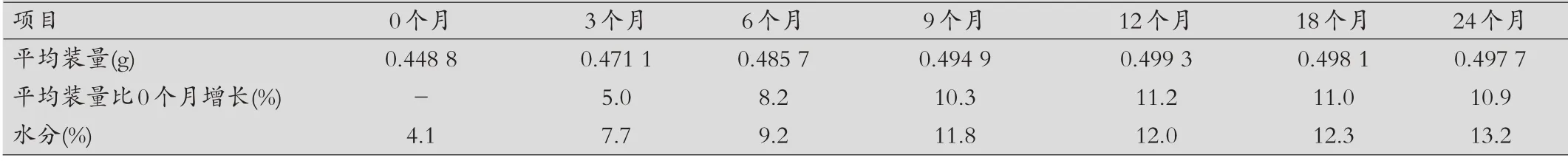
表2 某胃药持续稳定性考察平均装量与水分关系

表3 某胃药3种包装形式水分持续稳定性考察结果(%)
结 论
通过质量回顾分析某胃药持续稳定性考察数据,从而发现某胃药平均装量不良趋势,进一步试验确定为水分增加,再通过3 种不同包装形式的试验考察,得出在现有PVC 吸塑包装的基础上增加复合铝袋包装可以有效控制某胃药水分变化,保证某胃药质量。基于质量回顾分析,发挥对某胃药持续质量改进作用。
