羟考酮与舒芬太尼联合咪达唑仑在无痛结肠镜检查中的应用比较
2020-09-05赵婉莹杨晓春谢咏秋杨爱国侯新冉贺宏缘刘欢郭曲练
赵婉莹,杨晓春,谢咏秋,杨爱国,侯新冉,贺宏缘,刘欢,郭曲练
(1.广西壮族自治区妇幼保健院 麻醉科,广西 南宁530000;2.中南大学湘雅医院 麻醉科,湖南 长沙410008)
目前,结肠镜检查被认为是诊断结肠和直肠病变的金标准,是用来筛查结直肠癌的主要检查方式。结肠镜检查包括空气充入和插入器械,对肠道、肠系膜有牵拉刺激,易造成反射性痉挛和牵涉痛,患者在没有镇静镇痛的情况下难以耐受疼痛和刺激。因此,镇静和镇痛被患者广泛接受,并被许多胃肠科医生视为内镜检查的一个组成部分。在结肠镜检查过程中,需要一种有效缓解围手术期疼痛的镇痛药物,且不会产生明显的呼吸抑制。无痛结肠镜选用的阿片类药物主要以舒芬太尼、芬太尼等特异性μ 受体激动剂为主,可引起呼吸暂停、低氧血症、恶心、呕吐和胸壁强直等不良反应,对于门诊患者来说安全性差,且不利于麻醉医师术中管理。
羟考酮是一种半合成的蒂巴因衍生物强效阿片类镇痛药物,自1917年以来已在临床上使用,可有效治疗或缓解中重度疼痛[1-2]。羟考酮是阿片双受体激动剂(μ受体和κ受体),κ受体不易引起恶心、呕吐和呼吸抑制等副作用,可有效地缓解内脏疼痛。郭俊等[3]研究表明,在麻醉诱导时,羟考酮麻醉及镇痛效果与舒芬太尼相比,有相当或更好的镇痛效果。也有研究[4]表明,羟考酮比芬太尼在内脏手术术后镇痛效果更好。还有文献[5-7]表明,羟考酮比芬太尼、舒芬太尼等纯μ阿片受体激动剂在减轻内脏疼痛方面更有优势,更适合于门诊手术镇痛,但其在肠镜检查中的应用及研究较少。
本研究旨在比较咪达唑仑复合羟考酮注射液、咪达唑仑复合舒芬太尼在无痛结肠镜检查中的镇痛效果和安全性。
1 资料与方法
1.1 一般资料
选取2018年8月-2018年9月中南大学湘雅医院美国麻醉师学会分级(American Society of Anesthesiologists,ASA)I~Ⅲ级并计划行无痛结肠镜检查的患者60例,将所有患者用随机数字法分为S组(舒芬太尼组)和O 组(羟考酮组),每组30 例。年龄18~65 岁,体质指数(body mass index,BMI)18.5~27.0 kg/m2。排除标准:①有麻醉后异常恢复史者;②收缩压>180 mmHg 或<90 mmHg 者;③检查前2周有急性气道炎症、神经肌肉疾病、可能或已证实的困难气道;④疑似有麻醉药物滥用史和使用痛觉药或镇静剂;⑤对咪达唑仑、丙泊酚或类阿片药物有过敏史者;⑥无法沟通者。本研究通过医院伦理委员会审核批准,所有患者术前均签署知情同意书。两组患者一般资料,如:性别、年龄、BMI和ASA分级比较,差异均无统计学意义(P>0.05),两组患者基础生命体征比较,如:血压值、脉搏血氧饱和度(pulse oxygen saturation, SpO2)和心率等,差异均无统计学意义(P>0.05),具有可比性。见表1和2。
1.2 麻醉方法
所有患者在检查前禁食并做灌肠准备,术前立即记录生命体征。所有患者入室后建立静脉通路,均接受鼻导管吸氧(5 L/min),并连续监测心率(三导联心电图)、SpO2(SpO2测定)和血压(自动血压袖带,每5 min进行一次系列测量)。将急救药品、简易呼吸球囊及面罩、气管插管设备和麻醉机等抢救物品准备好。

表1 两组患者一般资料比较Table 1 Comparison of general data between the two groups
表2 两组患者基础生命体征比较 (±s)Table 2 Comparison of basic vital signs between the two groups (±s)

表2 两组患者基础生命体征比较 (±s)Table 2 Comparison of basic vital signs between the two groups (±s)
组别O组(n=30)S组(n=30)t值P值基础收缩压/mmHg 118.9±25.4 126.9±20.0-1.34 0.183基础舒张压/mmHg 69.0±10.1 74.3±11.8-1.84 0.070基础SpO2/%97.5±2.3 97.8±2.1-0.52 0.599基础心率/(次/min)79.3±13.2 78.1±12.8 0.35 0.722
所有患者结肠镜检查前5 min 以0.05 mg/kg 咪达唑仑缓慢静注。O组予以羟考酮0.10 mg/kg缓慢静注,如果检查时患者体动或者面部表情痛苦,可追加0.05 mg/kg;S 组结肠镜检查前2 min 予以舒芬太尼0.10 μg/kg静注,如果检查时患者体动或者面部表情痛苦,可追加0.05 μg/kg。如果两组患者追加相应的镇痛药物后仍无法配合检查,可追加10~30 mg丙泊酚。
如术中SpO2<95%的时间>30 s,则定义为轻度缺氧,给予开放气道,如托下颌等处理。如SpO2持续下降至<90%、且时间>30 s,则定义为重度缺氧。当SpO2为90%、或呼吸频率<6 次/min、或在任何时候观察到气道阻塞并停止气体交换发生呼吸窘迫的情况下,立刻予以气道操作(即下颌前推开放气道),进行面罩呼吸球囊手控辅助通气。心动过缓为心率<60 次/min;心率降至50 次/min 以下的患者予以阿托品0.3~0.5 mg。当发生低血压时(收缩压低于90 mmHg 或收缩压较基线降低30%),用麻黄碱3~5 mg治疗。
由一名不知道分组情况的独立研究人员记录患者以上所有数据和Ramsay 镇静评分(Ramsay sedation score,RSS):1分-焦虑或烦燥;2分-合作和镇静;3分-嗜睡但对命令有反应;4分-睡眠但对触觉刺激有反应;5 分-睡眠且无反应。观察并记录检查期间的副作用,包括恶心、呕吐、低血压和低氧血症等。
1.3 观察指标和随访
①观察所有患者的SpO2、心率、血压的基础值和低血压、低氧血症、恶心呕吐等不良事件的发生;②药物起效时间(自输注药物开始至达到目标镇静深度)、结肠镜操作时间(结肠镜检查开始至拔除结肠镜)、复苏时间(拔除结肠镜至患者完全清醒,RSS评分1或2分)和离室时间(苏醒时到离开结肠镜室的时间);③麻醉医生及消化内科医师(操作者)满意度(满意、不满意)及原因;术后1周电话随访患者对无痛结肠镜检查的满意度(满意、不满意)及原因。
1.4 统计学方法
选用SPSS 22.0 软件(美国芝加哥IBM 公司)进行统计分析。计量资料用均数±标准差(±s)表示,采用独立样本t检验对正态分布数据进行评价。使用Mann-WhitneyU检验比较组间等级资料。用χ2检验或Fisher 确切检验分析两组之间的分类数据。P<0.05为差异具有统计学意义。
2 结果
2.1 两组患者丙泊酚添加情况
O 组丙泊酚添加率明显低于S 组,两组比较,差异有统计学意义;两组丙泊酚添加量比较,差异无统计学意义。见表3。
2.2 两组患者术中指标比较
两组患者药物起效时间、肠镜操作时间、复苏时间和患者离开检查室时间比较,差异均无统计学意义(P>0.05)。见表4。
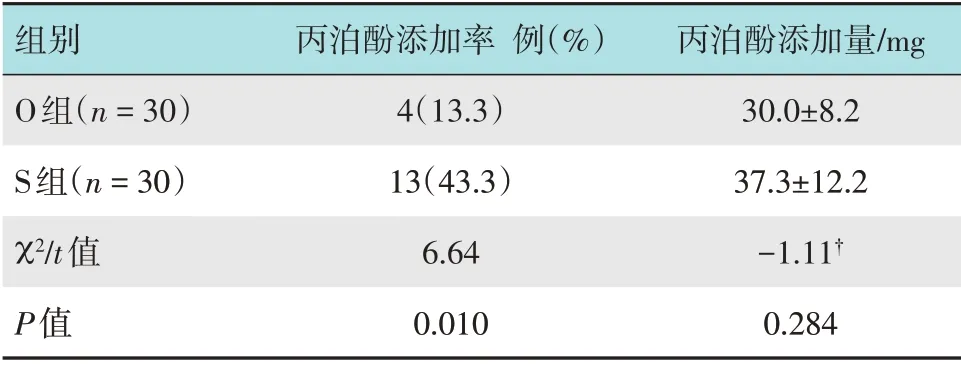
表3 两组患者术中丙泊酚添加情况比较Table 3 Comparison of propofol addition during operation between the two groups
2.3 两组患者术中不良反应发生率比较
两组患者术中心动过缓、低血压、恶心呕吐和重度缺氧等情况发生率比较,差异均无统计学意义(P>0.05);O 组术中轻度缺氧发生率明显低于S 组,两组比较,差异有统计学意义(P<0.05)。见表5。
2.4 两组满意度比较
消化内科医生不满意的原因主要为缺氧处理影响结肠镜检查操作、困难结肠镜患者体位改变不方便以及患者体动。麻醉医师不满意的原因主要为患者重度缺氧和恶心呕吐。O组消化内科医生满意度和麻醉医师满意度明显高于S组,两组比较,差异均有统计学意义(P<0.05);患者不满意的原因主要为术后眩晕或恶心,两组患者满意度比较,差异无统计学意义(P>0.05)。见表6。
表4 两组患者术中指标比较 (min,±s)Table 4 Comparison of intraoperative indicators between the two groups (min,±s)
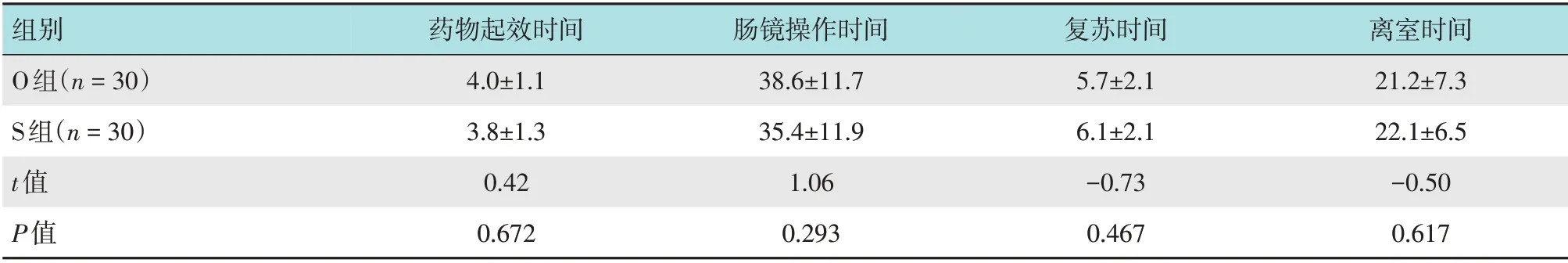
表4 两组患者术中指标比较 (min,±s)Table 4 Comparison of intraoperative indicators between the two groups (min,±s)
组别O组(n=30)S组(n=30)t值P值药物起效时间4.0±1.1 3.8±1.3 0.42 0.672肠镜操作时间38.6±11.7 35.4±11.9 1.06 0.293复苏时间5.7±2.1 6.1±2.1-0.73 0.467离室时间21.2±7.3 22.1±6.5-0.50 0.617

表5 两组患者术中不良反应发生率比较 例(%)Table 5 Comparison of adverse events during operation between the two groups n(%)
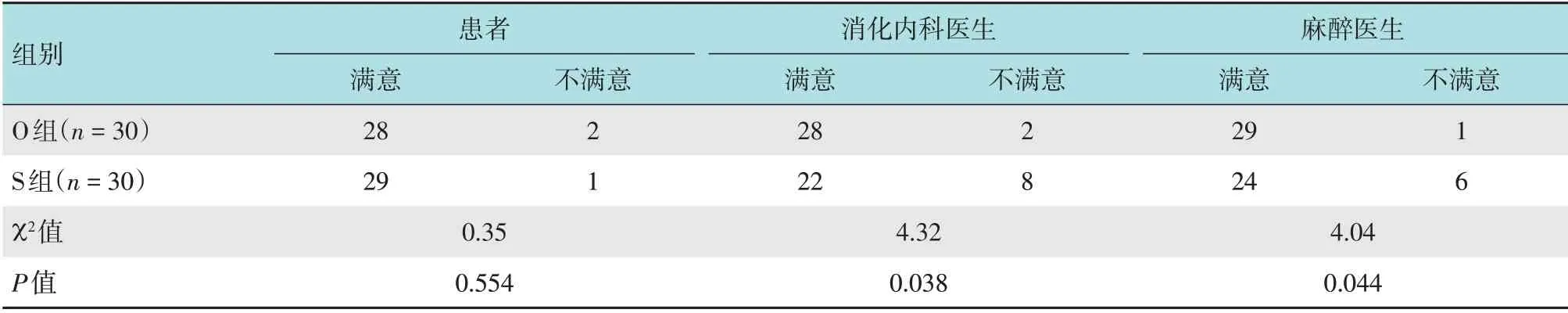
表6 两组满意度比较 例Table 6 Comparison of satisfaction between the two groups n
3 讨论
阿片类镇痛药通过阿片类受体发挥生物效应。μ、δ、κ 和ORL1 4 种亚型是目前临床和基础实验中公认的阿片受体[8],其中μ、δ和κ亚型被研究得最频繁。临床上用于无痛结肠镜检查的合成阿片类药物中,应用最广泛的是4-苯胺类阿片类药物,包括芬太尼和舒芬太尼等,它们都是μ受体选择性药物,效力是吗啡的500~10 000倍,但可能引起恶心、呕吐、心动过缓和呼吸抑制等不良反应。κ阿片受体广泛分布于下丘脑、中间隆起和黑质,也表达于肌肉、关节和内脏的神经末梢。有研究[9]发现,κ 激动剂能以剂量依赖性降低内脏疼痛。羟考酮是从天然生物碱衍生出来的半合成阿片类镇痛药。有研究[10-11]证实,羟考酮是阿片类μ 和κ 双受体激动剂,通过μ 和κ 阿片受体发挥协同镇痛作用,能够更好地缓解内脏疼痛
参照阿片类药物等效剂量换算[11],羟考酮和舒芬太尼两者效能比为1 000∶1。有研究[5,7]证明,0.10 mg/kg羟考酮是适合于门诊无痛的剂量,既能够提供良好的镇痛效果,又不影响患者的苏醒。故本研究中的舒芬太尼和羟考酮分别选择了0.10 μg/kg 和0.10 mg/kg 的剂量进行研究。本文选取的患者均需做肠镜检查,要求与胃镜检查也有所不同,肠镜检查过程中没有无法抑制的咽喉反射,且部分患者可能会有体位变化需求,以便肠镜顺利进入。既往常用的丙泊酚麻醉,患者处于全身麻醉状态无法配合体位改变,有些消化内科医生并不愿意在全身麻醉下行肠镜检查,深度镇静麻醉即可满足肠镜操作需求。故本研究采用咪达唑仑作为镇静药物,深度镇静麻醉可唤醒患者配合转换体位[12-13]。同时,咪达唑仑有明显镇静、顺行性遗忘作用,镇静程度为安静入睡但对指令有反应,检查结束即可唤醒。根据患者检查情况可适当增加少量丙泊酚,以减少血压降低、呼吸抑制等副作用[14]。因此,选用舒芬太尼或羟考酮联合咪达唑仑镇静麻醉应用于肠镜,患者可达到中度镇静状态,能唤醒配合检查,患者无术中知晓,无痛苦记忆,满意度好,肠镜操作医生及护士满意度极高。
本研究表明,羟考酮组丙泊酚添加率低于舒芬太尼组,这可能与羟考酮是阿片类μ和κ双受体激动药物有关,除了作用于μ受体,还可通过κ受体作用于脊髓水平,特别是κ2b受体,对平滑肌构成的器官可发挥镇痛作用,能更好地抑制内脏性疼痛[11;同时还可能因为κ 受体有一定的镇静作用。有研究[15-16]已证明,由κ受体激动剂介导的内脏镇痛特别有效,比舒芬太尼更适合于内脏手术的镇痛和术后镇痛。本文也支持这一结论。
本研究表明,羟考酮组轻度SpO2降低率明显低于舒芬太尼组(P<0.05)。这可能是因为抑制呼吸等副作用主要为μ2受体引起,离脑干的呼吸调节中心很近。因此,舒芬太尼较羟考酮更容易引起明显的呼吸抑制。而羟考酮μ2受体结合率较纯μ 受体激动剂舒芬太尼低,其κ受体主要分布在皮质,不影响患者呼吸。其次,由于舒芬太尼组镇静、内脏镇痛效果不足而导致更高的丙泊酚添加率,进一步导致了呼吸抑制的发生。说明羟考酮在呼吸抑制方面较舒芬太尼轻,比舒芬太尼更安全,更适合于门诊肠镜检查及治疗,这与以往的文献[17-19]报道结果相同。
以往有研究[17-19]表明,μ 受体主要分布于痛觉和呼吸(包括恶心和呕吐)等区域,而羟考酮对μ受体的亲和力较低,所以不良反应如恶心和呕吐的发生率比舒芬太尼低。在本研究中,两组恶心和呕吐等不良反应发生率比较,差异无统计学意义,可能与本研究样本量不足有关,有待进一步研究。
笔者对术后满意度的调查显示,O组麻醉医师以及消化内科医生满意度优于S 组(P<0.05),可能由于患者术中所需丙泊酚添加率低,低氧血症发生率低,生命体征平稳,所以麻醉医生满意度更高。患者丙泊酚药物使用率低,中度镇静状态可以使患者更加积极配合手术体位要求,所以内镜医师满意率也更高。术后1 周电话回访患者,两组患者满意率比较,差异无统计学意义,可能是因为咪达唑仑顺行性遗忘作用,患者体动或追加药物时并无不舒适记忆。
综上所述,在无痛肠镜检查中,与使用舒芬太尼的患者相比,羟考酮可以得到更好的疼痛控制,肠镜检查中丙泊酚添加率低,轻度低氧血症发生率也低,提示羟考酮在门诊无痛肠镜手术应用中安全有效。
