g-C3N4同质异型结对水中U(Ⅵ)及甲基橙的光催化去除性能
2020-08-21熊川宝
杨 悦,熊川宝
(安徽省核工业勘查技术总院 理化分析测试中心,安徽 芜湖 241000)
太阳能作为一种清洁、易得的持续能源,受到广泛关注[1]。石墨相氮化碳材料(g-C3N4)因其价廉易得、结构稳定、可见光相应和生物相容性良好,近年来,在光催化制氢[2-3]、CO2还原[4]、有机合成[5]、污染物去除[6-7]等方面得到了广泛应用。然而,g-C3N4有限的电子传输速度使其产生的光生电子-空穴对易在材料内部再次复合,限制了其在环境领域的进一步应用[8]。目前,常见的光催化剂改性方法有:非金属元素掺杂(如S、P、O、苯环等)调节能带结构[9]、引入金属单质、原子(如Ag、Au、Pt、Cu等)或其他导电材料(如纳米碳管、石墨烯等)改善电荷分布[10]、与其他半导体材料(CdS、TiO2、BiOI、Ag3PO4等)构建异质结促进电荷分离[11-13]、调节材料形貌增加表面反应位点[14]等。其中,利用2种材料自身的导带价带位置差异,在异质结界面处形成电位差,可有效促使光生载子在异质结内部,从高电位材料向低电位材料转移,实现电子-空穴分离,提升复合材料的光催化能力[15]。
大量含金属半导体材料与g-C3N4复合后都显著提高了光催化体系性能。但含金属材料的使用:一方面,增加了光催化剂的成本,使得催化剂易失活且具有化学毒性;另一方面,其他半导体材料与g-C3N4之间显著的物理化学差异,造成构建的催化剂系统的结界面亲和性差,严重阻碍了界面处的电荷分离传输[16]。三聚氰胺、尿素、硫脲、双氨腈等都可作为g-C3N4的合成原料;且不同原料在不同条件下合成的g-C3N4的能带隙不同,导带价带位置也各有差异[17-18]。因此,利用2种不同原料合成的g-C3N4组建一种完全由三聚三嗪结构构成的无金属同质异型结,将提高g-C3N4的实际应用范围。但如何在2种材料之间构建紧密贴合的接触面,将决定构建的异质结质量。
试验研究了以硫脲为原料合成的g-C3N4(TB)半导体1,在甲醇溶剂中与尿素混合研磨,通过TB结构中的N孤对电子与尿素分子形成氢键,促进尿素分子在TB层间表面聚集,再通过原位热聚合使尿素转化为g-C3N4型半导体2(UB);TB与UB在一定条件下构建出UTB型同质异型结光催化剂;并验证了该光催化剂对水中U(Ⅵ)的还原能力和对甲基橙的降解性能。
1 试验部分
1.1 试验原料
硫脲、尿素,均为分析纯。
1.2 g-C3N4同质异型结的构建
称取10 g硫脲置于30 mL坩埚中,放入马弗炉,以5 ℃/min的升温速率升温至520 ℃,保温2 h,自然冷却到室温,研磨,记为TB。同样,称取10 g尿素,在相同条件下得到以尿素为原料的g-C3N4(UB);再在相同条件下继续反应得到产物UTB-x(x为加入的TB质量,g)。其中,以10 g尿素为原料的g-C3N4(UB)产量约等于0.5 g。g-C3N4同质异型结构建流程如图1所示。

图1 g-C3N4同质异型结的构建流程
1.3 二次热解TB的制备
称取3 g TB,置于30 mL坩埚中,以5 ℃/min的升温速率升温至520 ℃,保温2 h,自然冷却至室温。所得样品作为对比样,排除异质结中TB二次热解的影响。
1.4 光催化反应
将常用有机染料甲基橙和无机铀酰离子(U(Ⅵ))作为降解目标。
甲基橙降解:称取30 mg光催化剂,加入25 mL质量浓度为20 mg/L的甲基橙溶液,置于黑暗环境下,磁力搅拌,预吸附20 min。打开300 W氙灯(Microsolar 300,Perfect light)模拟太阳光进行照射,在一定时间内用5 mL注射器吸取3 mL反应液,用针头过滤器过滤,在465 nm处采用紫外可见分光光度计(UVmini-1240,SHIMADZU)测定光催化剂吸光度,按式(1)计算甲基橙质量浓度。
铀酰离子降解:称取30 mg光催化剂,与25 mL铀酰离子质量浓度为40 mg/L的溶液混合(调pH至5.0)。 黑暗条件下通入N2,磁力搅拌120 min。待吸附平衡后,加入2.5 mL CH3OH作为牺牲剂,打开模拟光源,开始光催化还原。反应过程中,按一定时间移取2 mL反应液,过滤后,与4 mL、pH=2.5 的氯乙酸-乙酸钠缓冲溶液及4 mL质量浓度为0.5 g/L偶氮胂Ⅲ溶液混合并定容到10 mL, 用紫外可见分光光度计于652 nm处测定光催化剂吸光度,按式(1)计算铀酰离子质量浓度。
(1)
式中:A0—光催化剂初始吸光度;A—光催化剂吸附时间t时的吸光度;ρ0—甲基橙或铀酰离子初始质量浓度,mg/L;ρ—甲基橙在吸附时间t时的质量浓度,mg/L。
1.5 电化学性能测试
所有样品的光电流和平带电位均通过上海辰华电化学工作站测得。光电流以FTO玻璃为工作电极、Ag/AgCl为参比电极、铂丝为对电极,电解质溶液为0.5 mol/L的Na2SO4溶液。平带电位用玻碳电极作工作电极,测定前先通入20 min氮气排除电解液中的溶解氧。电化学阻抗谱利用Bio-Logic SAS的SP300型电化学工作站测得,玻碳电极作为工作电极。
2 试验结果与讨论
2.1 材料表征
g-C3N4异型结的XRD表征结果如图2所示。

图2 UTB光催化剂的XRD表征结果
由图2看出:13.1°衍射峰对应石墨相氮化碳层内三聚三嗪环基本结构的周期性排列产生的(100)晶面;27.3°衍射峰对应层与层堆积产生的(002)晶面;UB与TB复合后,UTB的主要特征峰峰位基本没变,证明UTB保持着g-C3N4的基本晶体结构;但随TB加入量增加,复合材料在27.3°的衍射峰向大角度偏移,这说明UTB材料中TB成分的增加。
采用FT-IR光谱对比研究所有样品的表面化学变化,结果如图3所示。可以看出:所有样品在810 cm-1处都保持着s—三聚三嗪环的特征吸收峰;同时,在1 200~1 700 cm-1范围内的s—三嗪环C—N键振动吸收峰也未表现出明显变化,这同样也表明原位热聚合制备的UTB材料由g-C3N4结构构成;而随TB掺杂量增加,2 800~3 500 cm-1之间的峰强逐渐降低,说明随TB掺杂量增加,同质异型结材料内的N—H键含量降低;而作为吸附位点和反应位点的表面N—H键,会显著影响光催化反应的进行。

图3 UTB光催化剂的FT-IR光谱
用扫描电镜和扫描透镜观察材料的形貌特征和结合状况,结果如图4所示。可以看出:所合成的传统g-C3N4(UB和TB)具有典型的堆叠层状结构;UB更加蓬松多孔,暴露出更多薄层表面;而复合后的同质异型结UTB-0.1则处于与UB、TB的中间状态,内部为更加多孔的团聚结构,外表面被少量薄层g-C3N4包围。这种结构可能形成于以CH3OH为溶剂的研磨过程中,CH3OH具有较低表面张力,易形成氢键,使得尿素分子与CH3OH更易一同进入层状g-C3N4内部。当CH3OH移除后,经过焙烧,原位形成的UB与TB就形成了紧密结合的同质异型结,对内部光生电荷在内电场驱动下的分离传输更有力。热聚合过程中产生的气体也进一步改善UTB的团聚状态,减小颗粒尺寸,降低光生电荷的传输距离,增加反应位点,提高光催化效果。N2吸脱附结果(表1)也证明了原位热处理过程对材料微观结构的影响,其中,UTB-0.1比表面积相较于UB和TB有明显提高。

a—UB;b—TB;c、d—UTB-0.1。图4 UTB光催化剂的SEM分析结果

材料比表面积/(m2·g-1)孔容积/(cm3·g-1)平均孔径/nmUB53.0260.37217.982TB12.4340.14326.097UTB-0.167.1160.82130.991UTB-0.538.3210.31620.347UTB-1.031.1730.0929.140
采用紫外可见漫反射和电化学测定合成材料的光吸收性能和电子能带结构特征,结果如图5所示。可以看出:合成的g-C3N4光催化剂都具有可见光响应特征,且由于UB、UTB-0.5、UTB-0.1堆叠程度更低,使其表现出量子效应,吸收边界与TB相比出现蓝移(图5(a));特别是,UTB-0.5、UTB-0.1材料的吸收边界相对于UB出现微弱红移,这也证明UB与TB材料发生了复合。
利用Kubelka-Munk方程,分别求出UB和TB的禁带宽度(Eg)为2.70、2.48 eV。尿素合成的g-C3N4(UB)与硫脲合成的g-C3N4(TB)的电子结构差异如图5(c)所示。Mott-Schottky曲线斜率为正表明,所有材料都为n型半导体,其中,TB导带(CB)为-1.42 eV,UB导带为-1.18 eV。UB与TB能带结构的差异使二者之间有形成异型结的热力学基础。光照下,UB和TB之间的电荷可以相互传输分离,延长了光生电荷的存活时间。

a—同质异型结的紫外可见漫反射光谱;b—Kubelka-Munk方程计算出的禁带宽度;c—电化学Mott-Schottky曲线。图5 UTB光催化剂的的光吸收性能和电子能带结构
光催化剂内部电荷传输分离效果的电化学阻抗谱(EIS)和瞬态光电流分析结果如图6所示。EIS Nyquist曲线(图6(a))模拟等效电路中,RCTR为工作电极的电荷传输阻抗,RSR为Na2SO4电解液阻抗,CPE为电极与电解液之间的恒相位元件。Nyquist曲线半圆环大小为RCTR,圆环半径越小,电子传输阻抗越小,电子传输速率也越快。可以看出:当TB与UB复合后,得益于二者之间的紧密结合和能带差异,UTB-0.1电子传输阻力降低。而光电流测定结果(图6(b))也说明,UTB-0.1的光电流密度在数次开关灯源循环测试中,远高于UB和TB,分别为UB和TB的4.2倍和8.6倍,这也意味着UTB-0.1有更好的电子-空穴对传输和分离效果。其他复合后的光催化剂相较于UB和TB也都表现出更高的光电流密度。

图6 催化剂的电化学阻抗谱(a)和周期光电流响应(b)
2.2 光催化性能
核能利用过程中会产生大量低浓度含U(Ⅵ)废水,这些废水用传统的吸附、萃取、沉降、膜滤等方式处理往往不经济。光催化可有效利用太阳光,将废水中移动相的U(Ⅵ)还原为不易转移的U(Ⅳ),从而抑制核素迁移,经济有效降解放射性废水[19]。对含U(Ⅵ)废水,以合成的g-C3N4同质异型结作光催化剂进行降解处理,并验证UTB在光照下的电子还原性能,试验结果如图7所示。原位复合后的UTB能有效光催化还原U(Ⅵ),在30 min内,能降解95%以上的U(Ⅵ)。为定量考察复合后光催化剂催化能力的提升效果,采用一级动力学方程,按式(3)对光催化降解污染物的速率进行拟合:
(3)
式中:c0—污染物初始浓度,mol/L;c—催化时间t时污染物浓度,mol/L;k—反应速率常数,min-1。
计算结果表明,最佳成分比的UTB-0.1光催化还原U(Ⅵ)的反应速率常数为6.38×10-2min-1,是UB(4.38×10-2min-1)、TB(9.40×10-3min-1)的1.46倍和6.79倍。这表明,采用原位生长策略构建的同质异型结g-C3N4材料能显著提高光催化性能,并有效解决实际环境中铀污染问题。
甲基橙(MO)的原位合成同质异型结的光催化活性试验结果如图8所示。
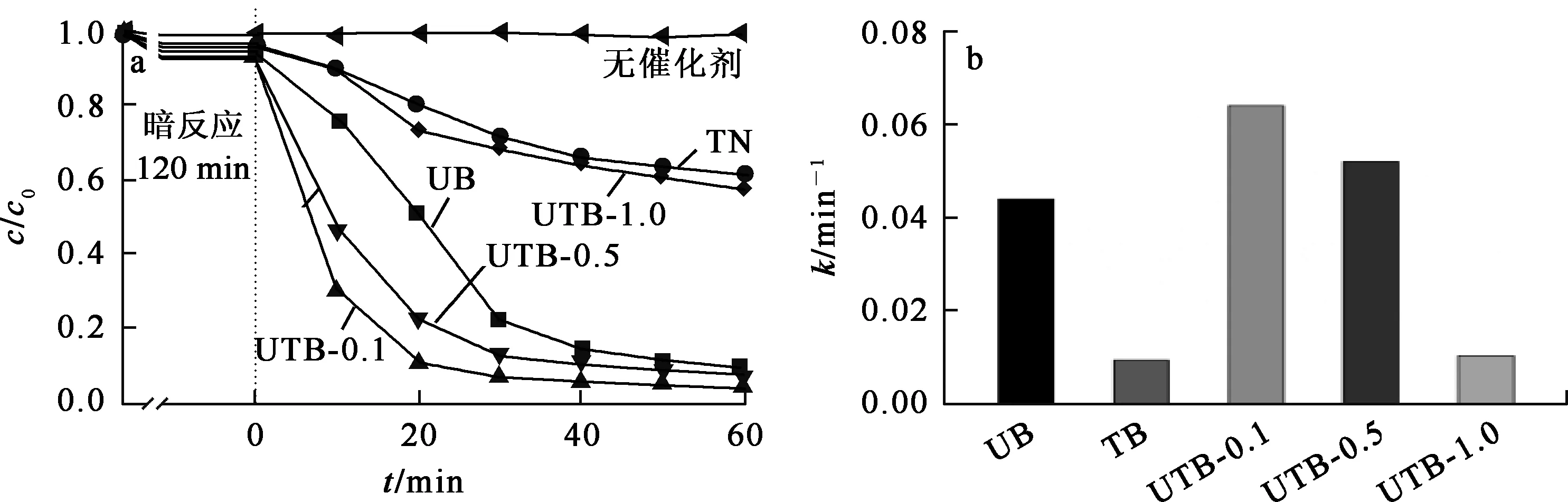
图7 UTB可见光下催化还原U(Ⅵ)的效果(a)及光催化降解速率(b)
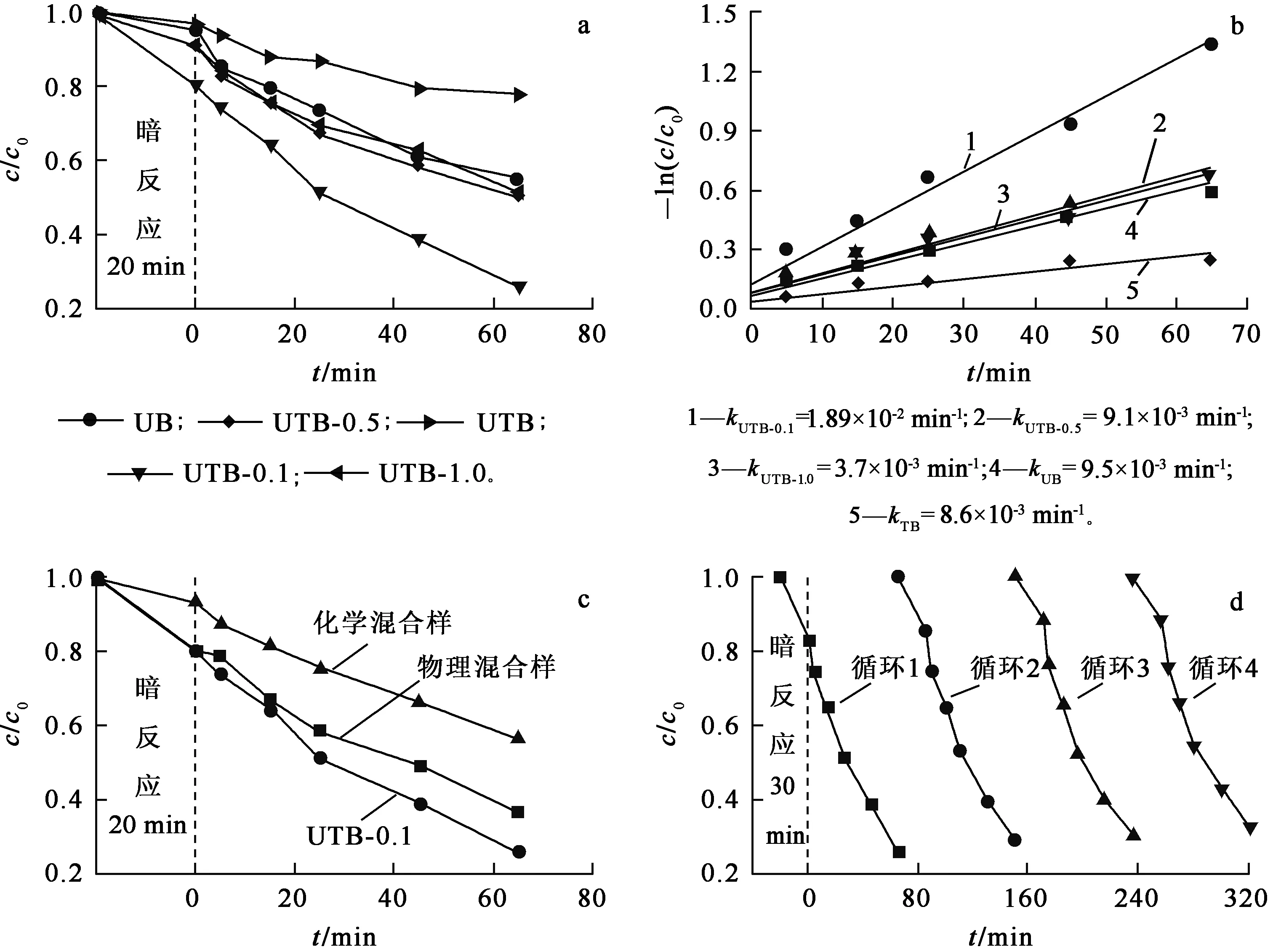
a—同质异型结对甲基橙的降解能力;b—光催化降解速率;c—不同方法制备的复合材料的催化性能;d—UTB-0.1的多次循环稳定性。图8 MO的原位合成同质异型结的光催化活性测试结果
由图8看出,光照射下,所有样品对MO都有明显降解效果:UB和TB在光照65 min后,分别去除水中45%和22.4% 的MO;而相同条件下,UTB-0.1对MO的降解率达78%;UTB-0.1、UB、TB相应的一级动力学常数分别为1.89×10-2、8.6×10-3、3.7×10-3min-1,与UB、TB相比,降解速率提高了2.2倍和5.1倍。该结果也证明了所合成的同型异质结内部的光生电荷分离传输效果得到提升,光生电荷利用率变得更高。
为验证合成的UTB同质异型结与界面的接触有效性,采用与UTB-0.1中理论的UB/TB比一致的UB和TB,将其置于100 mL去离子水中,直接超声2 h制得二者的物理混合样;同时,将一定量(该值通过原料能生成的g-C3N4的产量来确定)的硫脲和尿素直接混合焙烧制备出与UTB-0.1中的理论UB/TB一致的化学混合样。通过对比对甲基橙的处理性能(图8(c))看出,物理混合样和化学混合样的处理性能都比原位热聚合制备的UTB-0.1性能差。考虑到物理混合过程中,只是UB和TB材料的静电相互吸引和表面氢键作用,往往使得二者之间难以有效贴合,影响电荷在2种半导体之间快速转移。而对于化学混合的光催化剂,硫脲和尿素在合成过程中,都先随温度升高发生聚合反应,生成组成三聚三嗪单元的中间体。在该过程中,2种不同原料的混合,可能仅仅影响材料内部原子缺陷的含量,从而导致其对光催化性能的提升效果远远低于原位聚合手段和物理混合方法。UTB-0.1循环稳定性测试结果(图8(d))表明,经4次循环使用后,UTB-0.1对甲基橙的降解效率依然保持在64%。这说明UB与TB之间并不是通过简单的物理复合方式结合,而是形成了稳定复合体系,使得UTB光催化剂能极稳定地保持催化活性。
2.3 光催化机制
基于表征与应用结果,提出了UTB可能的光催化反应机制,如图9所示。可以看出:在太阳光照射下,UB和TB满带上的电子受到激发跃迁到空带,当UB或TB跃迁到空带上的电子不能及时转移到光催化剂表面时,被反应对象消耗;跃迁的电子又将返回满带,与满带的空穴复合,从而降低对光生电荷的利用率。当UB与TB通过原位复合形成紧密的接触界面后,由于UB和TB交叠的电子能带结构,跃迁到TB上的电子能利用CBTB和CBUB之间的电位差通过催化剂体系内部紧密接触的界面快速转移到UB上;而UB上留下的空穴则能快速转移到TB上,从而延长光生电荷的寿命,增大光生电荷参与反应的概率,最终实现光催化应用效果的进一步增强。

图9 同质异型结对水中U(Ⅵ)和MO的去除机制
3 结论
通过原位热聚合方法有效制备了具有紧密接触界面的g-C3N4同质异型结。相同的物理化学性质、适宜的能带结构与紧密接触的界面,使得UB和TB产生的电荷能在该界面处有效转移分离,抑制电荷的复合,从而提高光催化效果。其中,UTB-0.1在30 min内能实现95%以上的U(Ⅵ)还原去除,还原速率分别为UB、TB的1.46和6.79倍; 在55 min内能以0.038 min-1的降解速率降解80%左右的甲基橙,甲基橙降解率分别为UB、TB的2.2倍和5.1倍。通过对比化学混合和物理混合手段制备的UB、TB复合物,证明了该原位热聚合方法对提升光生电荷分离传输的有效性。同时,该光催化剂具有良好的循环稳定性,实际的环境治理应用前景广阔。
