灯盏花素注射剂质量控制研究进展
2020-08-21李响明孙胜斌姜国志
李响明,孙胜斌,姜国志
1.河北省中药注射液工程技术研究中心,河北 石家庄 051430; 2.神威药业集团有限公司,河北 石家庄 051430; 3.中药注射剂新药技术开发国家地方联合工程实验室,河北 石家庄 051430
灯盏花素收载于《中华人民共和国药典》2015年版一部[1]402-403植物油脂和提取物项下,由菊科植物短葶飞蓬Erigeronbreviscapus(Vant.)Hand.-Mazz.中提取分离所得,其主要有效成分为野黄芩苷(C21H18O12)。灯盏花素具有广泛、确切的药理活性,如抗组织缺血再灌注损伤、抗血栓、增加血流量、改善微循环、扩张血管、降低血黏度、调节血脂、抗氧化等[2-3]。作为临床治疗心血管类疾病的常用药,以灯盏花素为原料的制剂中口服和静脉注射液是当前制剂研究的主流[4],其中注射剂产品包括灯盏花素注射液、注射用灯盏花素、灯盏花素氯化钠注射液、灯盏花素葡萄糖注射液,前两者的临床应用较广。
灯盏花素注射液、注射用灯盏花素均以灯盏花素为原料,添加适宜辅料,应用现代制剂技术分别制成了注射用浓溶液、注射用无菌粉末,两者均有活血化瘀、通络止痛的功效。用于中风及其后遗症、冠心病、心绞痛[5]。灯盏花素注射液执行《卫生部药品标准·中药成方制剂》第二十册(WS3-B-3822-98)[6]102,注射用灯盏花素现行质量标准为《中华人民共和国药典》2015年版一部[1]1110-1111,2个质量标准差异较大。本文对比分析了以上2个产品质量标准的不同点,并整理了近20年来上述2个产品的质量控制研究文献,为规范和提高产品的质量标准提供参考。
1 现行质量标准对比分析
2个产品的现行质量标准差异较大,鉴别、检查、含量测定均有不同。下面将2个产品的质量标准进行对比分析,见表1。
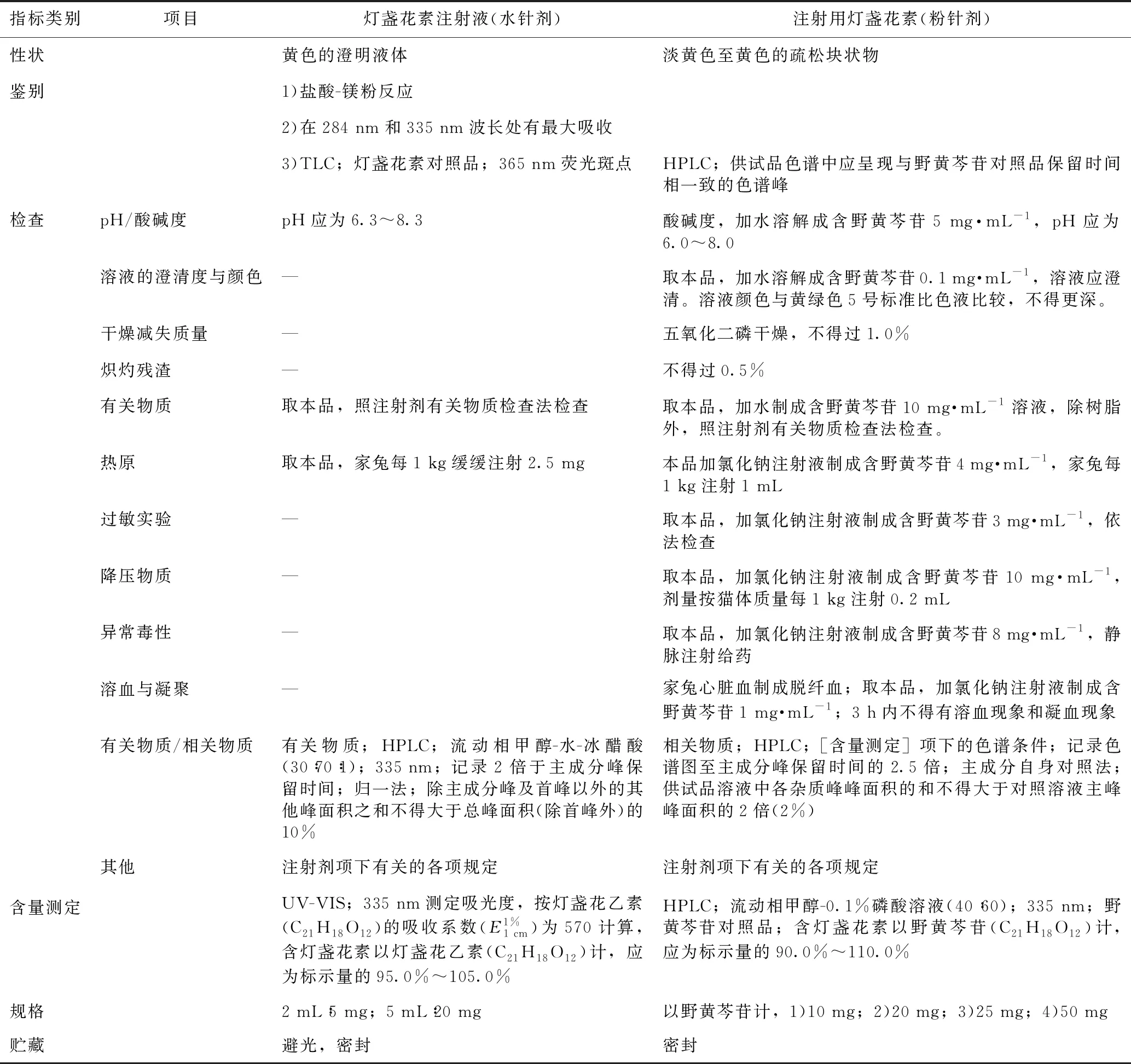
表1 灯盏花素注射液与注射用灯盏花素质量标准对比
1.1 鉴别
鉴别是根据制剂的理化特性制定的用于鉴别药品真伪的方法,因此要求方法专属性强。水针剂鉴别共3项:1)采用了黄酮类化合物经典的盐酸-镁粉还原显色反应,该鉴别专属性不够强;2)使用紫外分光光度法确认黄酮类成分苯甲酰基(284 nm附近)和桂皮酰基(335 nm附近)的最大吸收波长,标准要求的最大吸收波长为固定值,未兼顾不同设备厂家、型号的分析仪器间吸收波长稍有波动的可能性;3)利用黄酮类化合物在365 nm下的荧光特性进行薄层色谱鉴别,该鉴别中使用的灯盏花素对照品在多个标准物质目录中查询均无此标准物质,有人认为灯盏花素即为灯盏花乙素(野黄芩苷),该处表述有待进一步规范。粉针剂鉴别照“含量测定”项下的方法实验,在含量测定的同时完成鉴别,方法方便、准确,节约对照品。
1.2 检查
检查项目的设定与制剂的剂型和临床使用途径有关,除了对制剂中杂质、有关物质的质量控制外,pH/酸碱度、溶液的澄清度、不溶性微粒、热原与无菌等安全性项目的检查为临床的安全使用提供了基础性的保障,全面的质量检测是产品上市前质量控制的一个重要环节。水针剂质量标准已实施二十多年,粉针剂现行质量标准自2015年生效,整体来看,粉针剂质量标准的要求相对更高,这可能与标准建立时制剂的分析技术水平有关。粉针剂产品质量标准在安全性方面更严格,过敏试验、降压物质、异常毒性、溶血与凝聚的检测保证了上市产品的质量。2个产品均有的项目,也略有不同,比如有关物质(蛋白质、鞣质、树脂、草酸盐、钾离子)和热原。粉针剂检查时溶液中含灯盏花素(野黄芩苷)的浓度更大,其中有关物质检查时粉针剂浓度约是水针剂最大浓度的2.5倍,粉针剂热原检查家兔注射的剂量是水针剂的1.6倍。
关于灯盏花素原料相关物质的研究中,已有文献明确含有6-羟基山柰酚-7-O-β-D-吡喃葡萄糖醛酸、灯盏花甲素、野黄芩素和芹菜素4个相关物质[7-8];也有研究从注射用灯盏花素原料中分离鉴定出6-羟基芹菜素-6-O-葡萄糖-7-O-葡萄糖醛酸苷、5,7,8,3′,4′,5′-六羟基黄酮-7-O-葡萄糖醛酸苷、5,6,7,3′,4′-五羟基黄酮-7-O-葡萄糖醛酸苷及其异构体、patuletin-3-O-葡萄糖醛酸苷、甲氧基灯盏乙素、灯盏甲素、异鼠李素-7-O-葡萄糖醛酸苷、香叶木素-7-O-葡萄糖醛酸苷、野黄芩素、灯盏乙素甲酯、灯盏乙素乙酯、芹菜素13个杂质[9]。因此为了保证临床用药安全,进行相关物质的质量控制显的很有必要。2个产品有关物质/相关物质的检查均使用高效液相色谱法(HPLC),除检测波长相同外,流动相、供试品溶液和对照品溶液的浓度、计算方法均不同。主成分自身对照法是目前《中华人民共和国药典》等有关物质检查的常用方法。已有文献指出在灯盏花素注射液有关物质的色谱条件下主峰峰形拖尾[10]。
1.3 含量测定
含量测定是对目前制剂中已知的活性物质、代表性化合物或大类成分的控制,与原料的物质基础、制剂的生产工艺紧密相关,是保证临床治疗效果的前提。灯盏花素为黄酮类化合物,注射用浓溶液利用其紫外吸收的特性,采用紫外-可见分光度法检测,且利用百分吸收系数计算,省去了对照品的使用,降低了检测成本。但也有文献指出该方法专属性不强,测定的是总黄酮类化合物[11-14]。粉针剂含量测定使用以野黄芩苷为对照品的高效液相色谱法,且色谱条件与相关物质检查的条件一致,使得分析工作变得简便、高效。2个标准的限度均采用百分标示量,水针剂含量的限度范围明显窄于粉针剂的范围。
灯盏花素注射液、注射用灯盏花素均以灯盏花素为原料制成的注射剂,两者的现行质量标准存在差距,注射用灯盏花素质量控制相对更严格。其中灯盏花素注射液质量标准有待进一步规范,适当增加部分安全性方面的检查项目并优化有关物质、含量测定的方法,提高质量控制水平。
2 质控研究进展
在《卫生部药品标准·中药成方制剂》第二十册中灯盏花素注射液、注射用灯盏花素[6]174质量标准除因制剂存在状态不同,而某些检查项目不同外,大多数项目的质量控制方法类似。注射用灯盏花素在《中华人民共和国药典》2005年版、2009年增补本[15]中有了明显提高,在2010年版[16]848-849中仅修订了热原检查项注射的溶液浓度,在2015年版[1]1110-1111中未做修订。笔者查阅了近20年的文献,发现关于灯盏花素注射液的质量研究较多,涉及含量测定、有关物质、指纹图谱、安全性项目等,还有少量关于注射用灯盏花素中辅料测定的研究等,以下将分别综述。
2.1 鉴别
灯盏花素注射液鉴别(2)中,本品用甲醇稀释后,要求在284 nm及335 nm处应有最大吸收。有文献[17]指出,不同厂家、不同等级乙醇对紫外鉴别的结果有影响,主要是甲醇溶剂中的杂质干扰了供试品的吸收,提示在测定时要使用无干扰的甲醇。
2.2 有关物质/相关物质
虽灯盏花素原料纯度已经很高,但仍有约2.0%的杂质类物质,为了保证临床用药安全,开展相关物质的研究很有必要。郑金凤等[10]建立了HPLC测定灯盏花素注射液中有关物质的方法,以甲醇-0.1 mol·L-1醋酸铵溶液(用磷酸调节pH 3.0)(32∶68)为流动相,335 nm波长,柱温 30 ℃下测定,主峰和杂质峰完全分离,收集的10批样品中除溶剂峰外,各杂质峰峰面积之和占主峰峰面积3.53%~29.19%,这一结果与使用现行质量标准6[102]中有关物质检测方法所得结果相比,明显要高。申颖等[18]使用HPLC,以甲醇-水-冰醋酸(30∶70∶1)为流动相,335 nm下测定了不同厂家的3批注射用灯盏花素有关物质,按归一法计算后样品溶液除主成分峰及首峰以外的其他峰面积之和占总峰面积(除首峰外)的0.69%~0.78%。代勇等[14]采用HPLC建立了灯盏花素注射液有关物质的检查方法,以甲醇-0.1 mol·L-1醋酸铵(45∶55)(磷酸调节pH 2.4)为流动相,在335 nm下检测,记录图谱至主成分峰保留时间的2.5倍,主成分自身溶液对照法计算,收集的3批样品各杂质峰面积总和占对照溶液主峰面积7.8%~8.1%。
2.3 特征图谱
中药注射剂指纹图谱技术可以全面反映所含的化学成分,图谱的差别不仅能反映主要成分的差异,还能反映出一些含量较低甚至微量成分的差异,是全面评价产品质量的一种手段。相关研究[19-20]建立了以甲醇-0.4%磷酸缓冲液梯度洗脱,335 nm波长下测定灯盏花素注射液指纹图谱的方法,选定了7个共有峰,10批不同厂家的产品相似度为0.754~0.913,差别明显。耿家玲等[21]使用0.5%甲酸溶液-甲醇-乙腈为流动相梯度洗脱,检测波长330 nm,测定了13个厂家89批灯盏花素注射液的特征图谱和野黄芩苷含量,特征图谱相似度差距显著,野黄芩苷含量参差不齐,含量也是造成指纹图谱相似度低的主要原因。冯子男等[22]使用甲醇-0.1%磷酸溶液(40∶60)等度洗脱,在335 nm下测定了10批市售灯盏花素注射液的指纹图谱,不同厂家的指纹图谱相似度有明显差异,可能与不同厂家生产工艺的不同关系更大。
2.4 含量测定
现在研究中主要以HPLC测定灯盏花素注射液中灯盏花乙素(野黄芩苷)含量,专属性强,测定结果准确。林泳月等[23]建立了紫外法测定灯盏花素注射液含量的方法,以灯盏花乙素为对照品制备标准曲线,测定供试品溶液吸光度后从标准曲线中计算出含量。赵梅等[11]以甲醇-0.05%磷酸溶液(13∶87)为流动相,在335 nm下测得野黄芩苷含量,比紫外法测得结果稍低。张世轩等[12]以黄芩苷为内标加校正因子法测定灯盏花素注射液中野黄芩苷含量,并测定了5批样品的含量,结果均低于紫外法测得结果,与紫外测定法专属性不强的说法一致。雷灼雨[13]以甲醇-水-冰醋酸(30∶70∶1)为流动相测定了4个厂家6批灯盏花素注射液,含量为标示量的97.8%~100.2%,结果准确。彭金香等[24]建立了以甲醇-水(60∶40)为流动相测定灯盏花素注射液含量的方法,操作方便,可作为该产品含量控制的方法。还有研究者建立了灯盏花素注射液野黄芩苷含量和相关物质在同一色谱条件下测定的方法[10,14],使得分析工作变更简便、高效,可作为生产企业质量控制的方法。
灯盏花素中黄酮类化合物为主要活性成分,因此总黄酮含量也有必要控制。总黄酮含量测定多选择芦丁为对照品,使用紫外-可见分光光度法测定。方崇波[25]建立了以野黄芩苷为对照,采取离子络合方法测定注射用灯盏花素总黄酮含量的方法,测定的6批产品总黄酮含量为标示量的100.1%~105.1%。
2.5 辅料
注射剂在生产中,往往会根据药物的性状,适当地添加一定辅料来调节主药的溶解度、稳定性、酸碱性等。注射剂是一种直接注射进入血液循环系统的剂型,对其质量要求更高,安全性更好。辅料也是注射剂的一个重要组成部分,其质量与制剂的质量直接相关,因此也很有必要控制辅料的质量,目前文献中对辅料的研究有精氨酸和甘露醇。王先然等[26]建立了HPLC测定注射用灯盏花素中精氨酸含量测定的方法,以50 mmol·L-1磷酸二氢钾-乙腈(95∶5)为流动相,波长206 nm下检测,方法专属性好、准确,测定了4批注射用灯盏花素,精氨酸平均含量为11.79 mg。李金兰[27]使用不同的方法分别测定了注射用灯盏花素中甘露醇含量,参考《中华人民共和国药典》2010年版甘露醇[16]87含量测定的碘量法,测定了注射用灯盏花素中甘露醇含量,操作简单、结果准确,但滴定需在碘量瓶中进行,避免碘蒸发影响结果;建立了紫外分光光度法测定甘露醇含量,以甘露醇为对照品,与试剂反应显色后在412 nm波长处测定,实验操作相对简单,显色反应受外界pH、温度、光照等影响;还建立了使用氨基柱、蒸发光检测器,以乙腈-水(83∶17)为流动相测定甘露醇含量的高效液相色谱法,该方法专属性高、结果准确;上述3种测定方法相比,HPLC优于另外2种,可作为注射用灯盏花素中甘露醇含量测定的方法。
2.6 其他
郭红丽等[28]建立了注射用灯盏花素中13种金属元素的测定方法,HNO3和H2O2作为消解体系,采用微波消解法前处理样品后,以Sc、In、Rh、Re作为内标测定Pb、Cd、Hg、As、Cu、Fe、Mn、Ba、Zn、Al、Co、Cr、Ni 13种金属元素的含量,方法准确、灵敏度高,可作为该中药注射液质量监控的方法。
2.7 安全性研究
细菌内毒素:目前灯盏花素注射液使用家兔法检查热原,具有成本高、时间长、影响因素多、灵敏度低的缺点,目前有研究使用鲎试剂检查细菌内毒素以代替热原的检查。灯盏花素注射液细菌内毒素的检查,凝胶法和动态比浊法在文献中都有报道。中药注射剂由于成分复杂和工艺的特殊性,往往对细菌内毒素检查有干扰。高浓度灯盏花素可抑制细菌内毒素与鲎试剂的凝胶形成,通常采用稀释若干倍数的方法,排除干扰。同样使用胶凝法,不同文献中稀释倍数也不尽相同[29-34],这除了与鲎试剂灵敏度、产品规格有关外,还可能与不同厂家生产工艺不同有关。劳海燕等[35]、王璐等[36]均采用了动态比浊法测定灯盏花素注射液的细菌内毒素,细菌内毒素检测仪波长分别选择了405、660 nm。所以无论选取哪种方式测定细菌内毒素均需先开展方法学验证。
过敏反应:中药注射剂成分多且复杂,产品在上市前采用豚鼠进行过敏实验,因种属与人类存在一定差异,可能在当时实验条件下未能达到足以使实验动物产生阳性症状的剂量,以此动物实验数据推测人致敏的可能性时存在较大的风险。谭梦晖等[37]使用注射用灯盏花素诱导F344、SD、Wistar 3种品系大鼠产生被动皮肤过敏反应,3种品系大鼠随机分组后给药,大鼠同种被动皮肤过敏反应和大鼠-小鼠异种被动皮肤过敏反应结果均显示3种品系大鼠对灯盏花素的敏感性存在差异,其中以F344大鼠最为敏感,得出选择不同品系的动物至少2种以上进行过敏性安全评价,可提高检测方法的灵敏度及结果的可靠性的结论。其研究团队还用注射用灯盏花素诱导了豚鼠及大鼠的主动全身过敏反应[38],灯盏花素对两者均未表现出明显的全身过敏反应症状,反应几乎一致,BN大鼠表现出灯盏花素潜在的过敏反应,为中药注射剂过敏性评价使用不同品种的实验动物提供了参考依据。李黎明等[39]使用注射用灯盏花素比较研究了F344、BN、SD、Wistar 4种品系大鼠皮下注射后被动皮肤过敏及其致敏血清中Ⅰ型变态反应的抗体总IgE水平的差异,与谭梦晖等[37]的结果一致。谷舒怡等[40]采用腹腔致敏静脉激发、口鼻雾化致敏激发2种途径给予豚鼠灯盏花素注射液,灯盏花素注射液高、低剂量组动物均未出现明显过敏反应,高剂量组动物血清中组胺含量较阴性对照组升高,经口鼻吸入灯盏花素注射液1 mg·kg-1可能存在潜在过敏反应。谭梦晖等[41]给KM种小鼠足跖皮下注射灯盏花素,发现灯盏花素处理侧腘窝淋巴结质量和细胞计数均显著高于对侧,可知KM小鼠对灯盏花素具有一定的过敏性。
毒性研究:注射剂型灯盏花素制剂具有生物利用度高、起效快等特点,在危疾病证急救及感染性疾病治疗上具有一定的优势。近年来,临床使用该制剂的剂量有加大的趋势,为了确定增加用药剂量的安全性,观察其毒性反应症状和毒性作用靶器官,已有研究者探索性地使用不同动物开展毒性研究,发现不良反应,更好地指导临床用药。谢琛静等[42]观察了注射用灯盏花素对比格犬呼吸系统、心血管系统以及ICR小鼠协调功能和自发活性的影响,比格犬按体质量随机分成3种不同剂量组和溶媒对照组,分别给药后测定不同时间点心电图、呼吸、血压和肛温,单次静脉给予注射用灯盏花素对比格犬的呼吸、心血管系统及体温无明显影响;ICR小鼠按个体质量分成不同剂量3组和溶媒对照组,分别尾静脉给药后观察机体协调能力,单次给予注射用灯盏花素对小鼠协调功能无明显影响,500 mg·kg-1注射用灯盏花素对雌性小鼠在2 min时会产生一过性的轻度躯体运动障碍或中枢抑制作用。刘向云等[43]探讨了注射用灯盏花素对SD大鼠和比格犬的毒性病理学差异,大鼠、比格犬分别给予不同剂量注射用灯盏花素3个月,每天1次,恢复期观察1个月,麻醉采血后,取大鼠或犬大脑、小脑、骨髓、甲状腺、唾液腺、肾上腺、胰腺、气管、心肺、睾丸、附睾、子宫、卵巢、脾、淋巴结,病理制片后观察,大鼠各脏器均无明显异常改变,比格犬给药期分别在肝、胃、肺、肾、脾和淋巴结出现不同程度的损伤,损伤情况因剂量而不同,注射用灯盏花素对脏器的毒性反应存在中枢差异。梁玉记等[44]比较了比格犬和食蟹猴在使用了注射用灯盏花素后的体内毒性,2种实验动物对注射用灯盏花素的耐受性、敏感性和毒性反应均存在种属差异,两者的表现差异明显。王蓉蓉等[45]比较了不同厂家灯盏花素注射液的体外细胞毒性,不同厂家的产品细胞毒性差别较大,辅料聚山梨酯80也有细胞毒性,降低聚山梨酯80用量可提高安全性。
2.8 质量评价
注射剂型灯盏花素的生产厂家较多,不同的生产工艺、不同供应商的原料都可能影响产品的质量,为了评价不同产品的质量状况,也为进一步提高产品质量标准提供参考,开展了同品种的质量评价。何玉川等[46]使用紫外分光光度法测定了3个不同厂家的7批灯盏花素注射液质量分数为98.75%~103.3%,差异不大,均符合质量标准要求。甄健存等[47]对比研究了不同厂家灯盏花素注射液、注射用灯盏花素的质量,建立了HPLC测定上述产品中野黄芩苷含量和有关物质的方法,发现有3批产品含量不符合质量标准要求;不同厂家产品有关物质存在显著差异;注射用灯盏花素小规格产品的装量差异大,说明生产厂家小规格产品装量控制能力稍弱;颜色检查均大于标准比色液黄色10号和黄绿色10号,甚至不同批次产品的溶液颜色存在明显差异;不溶性微粒均符合质量标准要求。芮菁等[48]比较了不同厂家生产的含量测定合格的灯盏花素注射液在小鼠脑血栓形成实验和小鼠脑循环障碍实验中的反应情况,在同样的检测限值下,Ⅰ号样品对小鼠脑血栓形成有显著对抗作用,Ⅱ、Ⅲ、Ⅳ号样品则未见对抗作用;Ⅲ、Ⅳ号样品对小鼠急性脑循环障碍改善有明显作用,而Ⅰ、Ⅱ号样品则差异不显著;Ⅰ号样品无细胞毒性反应的浓度与其他3个样品无明显差异。不同厂家生产的不同规格、不同批次的灯盏花素注射液虽然含量测定均符合规定,但生物活性却存在明显差异,说明“生物活性测定”与理化分析控制反映的产品质量结果可能不一致。葛建华等[49]在检测中发现1批灯盏花素注射液紫外吸收波长产生了漂移,通过理化鉴别、薄层色谱法、紫外分光光度法、HPLC等对灯盏花素注射液中非法添加物进行了定性与定量分析,添加物呈维生素C鉴别的阳性反应,质量浓度为8.085 8 mg·mL-1。
3 结语
灯盏花素注射液、注射用灯盏花素均以灯盏花素为原料制成的供静脉注射使用的注射剂。通过对比上述2个产品的质量标准,可知两者存在一定差距,注射用灯盏花素质量控制相对严格。灯盏花素注射液水针剂建议结合现阶段质量研究进一步提高质量控制水平,可适当增加溶液的颜色、总固体、炽灼残渣、过敏反应、降压物质、异常毒性等项目的检查,优化鉴别、有关物质、含量测定的方法。水针剂、粉针剂均有的项目(如蛋白质、鞣质、树脂、草酸盐、钾离子、热原)可对比研究不同浓度的灯盏花素(野黄芩苷)对检查结果的影响,从而确定最优的检查方法,真实准确地反映产品质量;2个产品还可考虑建立指纹图谱(特征图谱)和关键辅料的质量控制方法,整体提高该产品的质量控制水平。本文质量标准的对比分析为今后同品种产品的质量控制研究提供了参考,也为以灯盏花素为原料的中药注射液质量标准提高指明了研究方向。
灯盏花素注射剂剂型的产品质量评价研究中显示,不同厂家的产品质量存在一定差距。这一现状可能主要与不同制剂企业的原料来源、生产设备、工艺参数控制等有关,最终在产品质量中表现出来。针对这一现状,建议制剂企业在固定原料来源的基础上,进一步提高工艺控制能力,把影响产品质量的关键参数、关键生产环节精细化管控,保证批间产品质量的稳定,为临床用药的有效性、安全性做好基础。
