氟苯尼考环糊精包合物的药物代谢动力学研究
2020-08-19张瑞丽李志中孙春华高伟段欣强郭文祺韩姗姗郝潇雯王恩丽秦立廷
张瑞丽,李志中,孙春华,高伟,段欣强,郭文祺,韩姗姗,郝潇雯,王恩丽,秦立廷
(山东新希望六和集团有限公司,新希望六和股份有限公司/农业部饲料及畜禽产品质量安全控制重点实验室,山东青岛 266000)
氟苯尼考(florfenicol)又称氟甲砜霉素,是由美国先灵葆雅公司于 20 世纪 70 年代末研制开发的动物专用酰胺醇类广谱抗菌药[1]。20世纪90年代我国正式批准氟苯尼考为国家二类新兽药[2]。目前国内批准的氟苯尼考制剂类型较多[3],有粉剂、可溶性粉剂、预混剂、注射液及溶液等,其中粉剂和可溶性粉剂在畜禽养殖过程中使用较方便,因此用量最大。但由于氟苯尼考在水中几乎不溶,其粉剂、可溶性粉剂产品在临床中的应用受到了一定影响。针对药物溶解性差的情况,目前国内外已有大量提高药物溶解度的固体制剂的研究报道[4-6]。有研究发现,采用分子包合、形成固体分散体等物理增溶方法来提高氟苯尼考的溶解度,可改善氟苯尼考在动物体内的吸收,提高生物利用度[7]。于欣洋等[8]研究了氟苯尼考固体分散体在大鼠的体内生物利用度,发现该固体分散体口服生物利用度与氟苯尼考原粉相比提高了15.39%。但是目前还未有氟苯尼考环糊精包合物产品与普通氟苯尼考粉产品在肉鸡体内生物利用度的比较研究。本研究建立了一种高灵敏度、高回收率的检测血浆中氟苯尼考的UPLC-MS/MS方法,并对氟苯尼考环糊精包合物的可溶性粉(以下简称氟苯尼考环糊精包合粉)在肉鸡体内的药动学特征及相对生物利用度进行了研究,以期为氟苯尼考制剂产品的临床应用提供参考。
1 材料与方法
1.1 药品和主要试剂 氟苯尼考粉:含量20%,批号1907002,由山东某药业有限公司生产;氟苯尼考环糊精包合粉:含量20%,批号1907002,由山东某药业有限公司生产;氟苯尼考对照品:购自中国兽医药品监察所,含量99.1%,批号K0301703;甲醇,色谱纯,美国天地试剂有限公司;乙酸乙酯,色谱纯,美国飞世尔试剂有限公司;超纯水由MilliQ净化系统制得,Millipore公司。
1.2 溶液配制 氟苯尼考对照品储备液:精密称取氟苯尼考对照品适量,用甲醇制成含氟苯尼考1 mg/mL的对照品储备液,-20 ℃避光保存备用。氟苯尼考对照品工作液:量取适量的1 mg/mL的对照品储备液,用甲醇-水(1∶4)稀释并配制成100 μg/mL工作溶液,-20 ℃避光保存备用。
1.3 主要仪器设备 三重四级杆液质联用仪,AB SCIEX Triple QuadTM4500,美国应用生物系统公司;BEH X-bridge C18(2.1 mm×50 mm,2.5 μm),美国沃特斯科技有限公司;TDL-5A离心机,江苏金怡仪器科技有限公司;MTN-2800D氮吹仪,天津奥特赛恩斯仪器有限公司;XW-80A型连续旋涡混合器,海门市其林贝尔公司;SB-4200DTD型超声波清洗仪,宁波新芝生物科技有限公司。
1.4 实验动物 健康白羽肉鸡24 只,体重为1~1.5 kg,饲喂不含药物添加剂及抗生素的定制肉鸡饲料,正常预饲一周,试验前采血检测血浆中是否有氟苯尼考药物干扰。给药前禁食12 h,自由饮水,给药后禁饲4 h。
1.5 给药与采样 24只白羽肉鸡,按照体重随机分为A、B两组,A组每只鸡单剂量经口灌服20%氟苯尼考粉,B组每只鸡单剂量经口灌服20%氟苯尼考环糊精包合粉,两组灌服剂量均为20 mg/kg(给药前加适量水溶解后灌服);灌服给药后,采样时间点为给药前及给药后0.083、0.25、0.5、0.75、1、1.5、2、3、4、6、8、12、24 h。每个时间点采集翅静脉血1~2 mL,置5 mL用肝素钠润洗的聚丙烯塑料离心管中,混匀, 3000 r/min离心10 min,分离血浆,置-80 ℃冰箱保存。
1.6 试验方法
1.6.1 色谱分析条件 色谱柱:BEH X-bridge C18(2.1 mm×50 mm,2.5 μm);流动相:A相为水,B相为甲醇;梯度洗脱条件见表1;流速:0.3 mL/min;柱温:30 ℃;进样量:5 μL。

表1 流动相条件Tab 1 Conditions of mobile phase
1.6.2 质谱分析条件 采用电喷雾负离子扫描的方式,多反应监控(MRM),电喷雾离子源(ESI)。母离子、子离子、碰撞能量、加速电压等质谱条件见表2。

表2 氟苯尼考质谱条件Tab 2 Mass spectrometry of florfenicol
1.6.3 血浆样品的前处理 准确吸取0.5 mL血浆于10 mL离心管中,加入4 mL乙酸乙酯,涡旋1 min,超声提取20 min,3000 r/min离心10 min,取2 mL上层乙酸乙酯上清液,氮气吹干,残留物用5 mL甲醇-水溶液(1∶4)溶解,涡旋1 min。部分采样点的样品需再进行10~20倍稀释,稀释后进样。样品溶液经0.22 μm有机滤膜过滤后,进行UPLC-MS/MS分析。
1.6.4 检测限及定量限 空白样品中添加已知浓度的氟苯尼考对照品工作液,使添加浓度依次降低,按照优化出的血浆样品预处理方法处理,重复操作5次,经测定,以能达到信噪比S/N≥3时样品的最低浓度为血浆中的检测限(LOD),以能达到信噪比S/N≥10时样品的最低浓度为血浆中的定量限(LOQ)。
1.6.5 准确度和精密度 准确吸取浓度为 10、2、0.5 μg/mL系列对照品工作液各 100 μL,添加到 500 μL 的空白血浆中,涡旋 1 min 混匀,配制成含氟苯尼考血浆终浓度分别为10、2、0.5 μg/L 的含药血浆样品,按照“1.6.3”项下的血浆样品前处理方法进行处理,每个浓度处理 5 个平行样品,与同浓度的对照品工作液产生的响应值相比较,测定准确度和精密度。
1.6.6 标准曲线及线性范围 精确量取适量的氟苯尼考对照品工作液,依次用甲醇-水溶液(1∶4)稀释成氟苯尼考含量为50、20、10、5、2、1、0.5、0.1 μg/mL系列工作液。精确吸取空白血浆500 μL加入10 mL离心管中,再分别依次加入100 μL上述系列工作液,使氟苯尼考血浆终浓度分别为50、20、10、5、2、1、0.5、0.1 μg/L。上述样品按照“1.6.3”项下的血浆样品前处理方法处理后,每个浓度配制3个平行样品,进行 UPLC-MS/MS 检测,根据仪器分析结果及相关系数,制作标准曲线。
1.7 数据处理 采用EXCEL绘制血药浓度-时间曲线。采用WinNonlin5.2.1 软件处理血浆药物浓度-时间数据,用非房室模型统计矩原理计算药代动力学参数。按公式计算两种氟苯尼考粉的相对生物利用度F,F= AUCB/ AUCA
式中,AUCA为受试药A的药时曲线下面积;AUCB为受试药B的药时曲线下面积。
2 结果与分析
2.1 方法学验证
2.1.1 线性结果 以氟苯尼考的浓度为横坐标,氟苯尼考的离子峰面积为纵坐标,建立标准曲线。结果显示,氟苯尼考在0.1~50 μg/L的浓度范围内线性关系良好,其线性方程Y=2.096e5X-1086.04,r=0.9990。
2.1.2 方法回收率与精密度 结果见表3。由表3可知,氟苯尼考在血浆样品中 10、2、0.5 μg/L 3个添加浓度水平下,其回收率在75%~110% 之间,日内和日间变异系数均小于15%,符合《兽用化学药物临床药代动力学试验指导原则》中对于回收率和精密度的要求。

表3 血浆中氟苯尼考回收率和精密度考察试验结果Tab 3 Recovery and precision test results offlorfenicol in plasma
2.1.3 方法检测限及定量限 氟苯尼考的检测限为0.025 ng/mL,定量限为0.05 ng/mL。
2.2 药动学结果
2.2.1 药时曲线 肉鸡灌服2种氟苯尼考制剂后,各给药组的平均血药浓度-时间曲线见图1。由图1可知,氟苯尼考在肉鸡体内吸收迅速,在2 h内可达到最大血药浓度;B组氟苯尼考环糊精包合粉的Cmax和AUC要显著大于A组氟苯尼考粉。
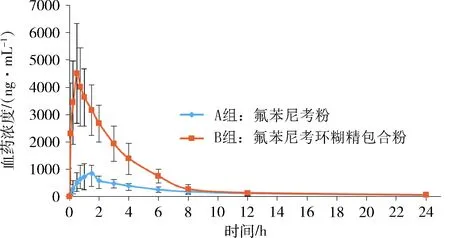
图1 肉鸡灌服氟苯尼考20mg/kg(FBNK)后平均药时曲线图(n = 12)Fig 1 Mean plasma concentration-time curves ofFBNK after oral administration of FBNK tobroilers at 20mg/kg (n = 12)
2.2.2 药动学参数 采用WinNonlin5.2.1 软件处理数据,用非房室模型统计矩原理计算药代动力学参数,结果见表4,A、B两组的T1/2λz分别为4.814±3.058 h、2.106±1.476 h;Tmax分别为1.563±0.755 h、1.417±1.683 h;Cmax分别为1043.15±391.42 ng/mL、4691.95±1597.28 ng/mL;AUClast分别为4283.53±2406.81 h·ng/mL、14911.70±2976.22 h·ng/mL;MRTlast分别为4.799±2.124 h、3.032±1.535 h。
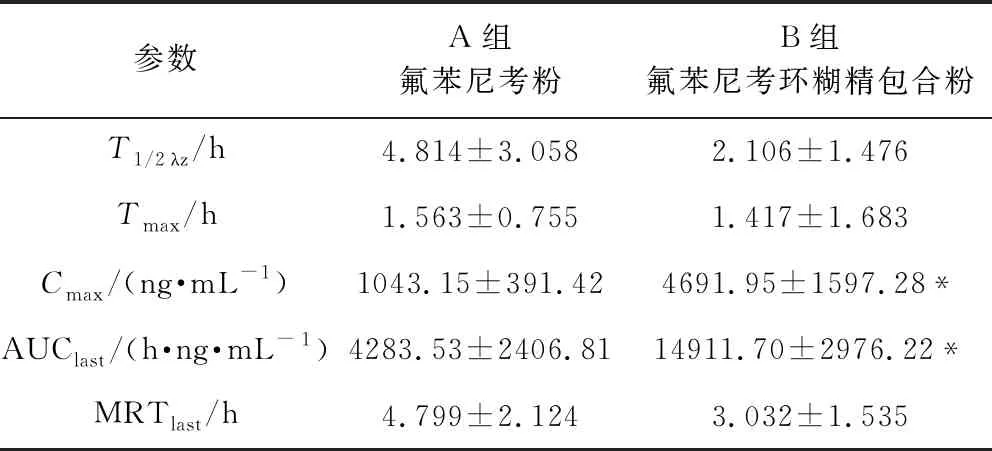
表4 肉鸡灌服氟苯尼考后的药动学参数Tab 4 Non-compartmental pharmacokinetic parametersof florfenicol in broilers plasma after oraladministration of 20 mg/kg (n=12)
2.3 生物利用度结果 按照1.7项下公式计算氟苯尼考环糊精包合粉的相对生物利用度。结果表明,采用环糊精包合工艺的氟苯尼考粉的相对生物利用度为348.12%。
3 讨论与结论
3.1 血浆样品的前处理方法 在样品前处理过程中,部分样品在乙酸乙酯吹干后用甲醇-水溶液(1∶4)振摇溶解时,并不能完全溶解,可能会造成样品中氟苯尼考检测结果偏低;为此可在样品中加入约1~2 mL正己烷,然后加入甲醇-水溶液(1∶4)振摇,底部样品可被溶解,溶液分层,吸取下层溶液进样,可避免氟苯尼考含量的损失。
3.2 氟苯尼考药动参数分析 药动学研究结果显示,采用环糊精包合工艺的氟苯尼考与普通工艺氟苯尼考产品之间的T1/2λz、Tmax均不存在显著差异(P>0.05),而Cmax、AUClast经统计分析后差异显著(P<0.001),表明经过环糊精包合后的氟苯尼考在体内吸收更好,血药浓度及药时曲线下面积显著提高。
本研究得到的药动学参数MRT与刘芳报道[9]的类似,而其他药动参数Tmax、Cmax、AUClast均存在一定的差异,这可能与刘芳选用的试验动物为黄羽肉鸡,而本试验选择的试验动物为白羽肉鸡有关;而且本试验选择的制剂与刘芳研究选用的两种氟苯尼考制剂(含量规格分别为10%、20%)工艺也不同。
3.3 氟苯尼考生物利用度分析 原料药粒径及制剂工艺的改变,均可能影响氟苯尼考药物的生物利用度。Xu Y等[10]研究了利用热熔挤压技术制备的氟苯尼考肠溶制剂的生物利用度,结果显示其生物利用度为普通商业制剂的117.2%。王加才等[11]研究了超微粉碎后氟苯尼考的生物利用度,结果与原药相比,超微粉碎后的氟苯尼考体内吸收加快,生物利用度增加。目前市面上的普通的氟苯尼考粉基本是采用氟苯尼考和辅料简单混合后得到的产品,而环糊精包合的氟苯尼考粉,则利用了环糊精具有较大的空穴结构[12]可以将氟苯尼考包合在内的特点,提高了氟苯尼考的溶解度。本研究所用的环糊精包合的氟苯尼考全部为环糊精包合物,不是与环糊精的混合物或部分包合物。研究结果表明了氟苯尼考环糊精包合物的相对生物利用度明显高于普通氟苯尼考粉。本试验氟苯尼考的灌胃剂量为20 mg/kg,远远低于胡晓军[13]研究的肉仔鸡服用氟苯尼考的半数致死量 LD50(10392.02 mg/kg),且氟苯尼考的环糊精包合物在肉鸡体内的最大血药浓度均小于10 ng/mL。在本试验结束后对试验鸡只持续观察一周,并未发现有明显的不良反应。
根据研究结果,在临床使用不同制剂工艺的氟苯尼考时,需要综合考虑药物在动物体内的药动学特征以及生物利用度;不同制剂工艺的产品不可同等应用,比如在耐药性严重的地区使用普通氟苯尼考粉治疗时,由于其血药浓度较低,其治疗效果不如氟苯尼考环糊精包合物产品。关于氟苯尼考环糊精包合物产品的临床实际应用效果需要进一步试验研究。
