β-酸-番茄红素/HP-β-CD复合包合物的制备及稳定性
2022-03-30李万茸田秉仁程建华刘玉梅
李万茸,田秉仁,许 丹,王 杰,程建华,刘玉梅,*
(1.新疆大学化学学院,新疆 乌鲁木齐 830046;2.新疆大学化工学院,煤炭清洁转化与化工过程自治区重点实验室,新疆 乌鲁木齐 830046)
作为啤酒花软树脂成分之一,β-酸具有协调啤酒风味、弥补苦味不足及抑菌、抗氧化和抗肿瘤等药理作用[1-3],研究表明β-酸对大肠杆菌、金黄色葡萄球菌、牛链球菌等菌群表现出良好的抑制性能[4-6]。番茄红素为一种天然的功能性、脂溶性红色素,广泛存在于番茄、西瓜、粉红葡萄柚等红色果蔬中,为具有11 个共轭双键的非环状类胡萝卜素[7-8],具有较强的抗氧化活性和多种功效[9],如抗凋亡、抗衰老[10],预防心血管疾病[11]和前列腺癌[12]等作用。将番茄红素作为天然的红色素应用于食品中,其呈色效果显著且食用安全[13-14]。但作为天然的活性物质,β-酸和番茄红素的化学性质均较为活泼,不稳定且不溶于水,这极大地限制了它们在更多领域的应用。
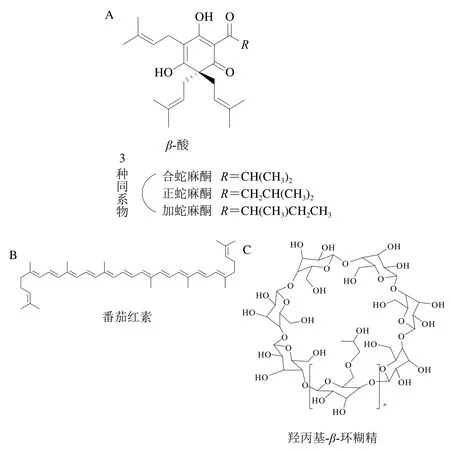
图1 β-酸(A)、番茄红素(B)及羟丙基-β-环糊精(C)结构式Fig. 1 Structural formulae of β-acids (A), lycopene (B) and hydroxypropyl-β-cyclodextrin (C)
在保持β-酸和番茄红素生物活性的基础上,增加其稳定性和溶解性,这对于提高其生物利用率、发挥功效和扩大应用范围非常重要。目前常见的解决方法是构建稳定的运载体系,如将番茄红素制备成胶囊[15-16]、乳液[17-18]、脂质体[19]、滴丸[20]、环糊精包合[21]等。环糊精包合是一种常用的制剂手段,“外亲水、内疏水”的特性使环糊精可以和多种客体分子进行包合,改善客体分子的特定性质,如增加水溶性[22]、降低毒性、缓释[23]等,其中,β-环糊精的衍生物——羟丙基-β-环糊精(hydroxypropyl-β-cyclodextrin,HP-β-CD)因具有较高溶解度和相对较高包合能力而应用最为广泛,课题组前期工作分别制备了番茄红素[24]、β-酸[25]的HP-β-CD包合物,发现包合物显著提高各自稳定性和水溶性(图1)。本实验采用HP-β-CD将β-酸和番茄红素进行包合,制备β-酸-番茄红素/HP-β-CD复合包合物,该复合包合物不仅改善β-酸和番茄红素不稳定性和水溶性差的问题,同时还兼具有防腐、抑菌、天然色素功能。本实验在对复合包合物进行表征及溶解度测定的基础上,考察光照、温度、酸碱条件的差异对复合包合物溶液稳定性的影响,旨在为开发天然来源的复合食品添加剂及探索其在水基食品加工中的应用前景提供理论参考。
1 材料与方法
1.1 材料与试剂
β-酸(质量分数≥95%),由啤酒花浸膏经碱溶-酸沉-重结晶法分离而得[26];番茄红素(质量分数>90%),由番茄红素油树脂皂化-重结晶分离而得[24]。
HP-β-CD 山东滨州智源生物科技有限公司;氢氧化钾(分析纯) 天津市致远化学试剂有限公司;乙酸乙酯、甲苯(均为分析纯) 天津市光复精细化工研究所;甲醇、95%乙醇(均为分析纯) 天津永晟精细化工有限公司;实验用水为二次蒸馏水。
1.2 仪器与设备
BS210S型电子天平 德国赛多利斯公司;HH-S4数显恒温水浴锅 金坛市医疗仪器厂;KQ5200B型超声波清洗器 昆山市超声仪器有限公司;79-1磁力加热搅拌器 江苏省金坛市医疗仪器厂;TGL-16G台式离心机上海安亭科学仪器厂;DHG-9075A电热鼓风干燥箱上海一恒科学仪器有限公司;UV-5300PC型紫外-可见分光光度计 上海元析仪器有限公司。
1.3 方法
1.3.1 复合包合物的制备及含量分析
采用研磨法[24-25]分别制备β-酸/HP-β-CD包合物和番茄红素/HP-β-CD包合物。
β-酸-番茄红素/HP-β-CD复合包合物的制备:准确称取β-酸、番茄红素各10 mg,HP-β-CD 800 mg于研钵中,加入约2 mL蒸馏水,30 ℃水浴条件下充分研磨90 min后,加入一定量的蒸馏水,8 000 r/min离心10 min,去除未包合的物质,上清液放入40 ℃烘箱烘干至恒质量,即制得红色粉末状β-酸-番茄红素/HP-β-CD复合包合物。
1.3.2 复合包合物中β-酸、番茄红素含量的测定及包合率的计算
复合包合物中β-酸、番茄红素含量的测定:称取一定质量的β-酸-番茄红素/HP-β-CD复合包合物2 份,记为m0,一份用甲醇溶解、定容,另一份用甲苯溶解、定容,记为V0,根据实际浓度稀释一定倍数,记为n。分别在各自最大吸收波长356 nm和484 nm处测定吸光度。根据标准曲线(A=0.042C+0.104 6,R=0.999 1,线性范围为2.0~14.0 μg/mL)计算样品溶液中β-酸的含量C;标准曲线(A=0.290 5C+0.060 1,R2=0.999 6,线性范围为1.0~5.0 μg/mL)计算样品溶液中番茄红素的含量C;按式(1)计算:
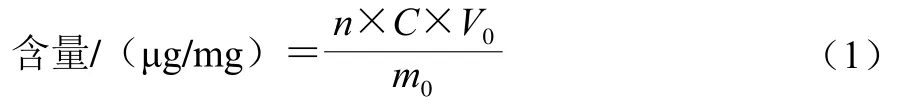
复合包合物包合率的计算方法:根据式(1)分别计算复合包合物中β-酸、番茄红素的含量,按式(2)计算其各自的包合率:
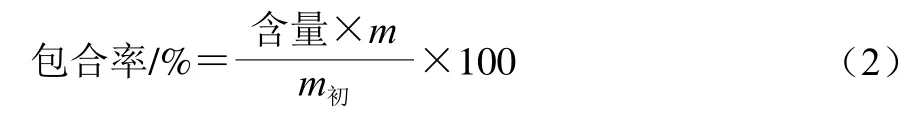
式中:m为制得包合物的质量/g;m初为制备包合物时加入的β-酸、番茄红素的初始质量/mg。
1.3.3 不同温度下复合包合物溶解度的测定
根据Tang Peixiao等[27]的方法测定。将过量的复合包合物置于5 mL蒸馏水中配制成悬浊液,并在不同温度下(20、30、40、50 ℃)不断搅拌,形成饱和溶液,离心过滤后,取1 mL稀释一定倍数,在356 nm波长下测定β-酸的吸光度;另取1 mL用甲苯萃取后,在484 nm波长处测定番茄红素的吸光度;根据标准曲线计算包合物中β-酸、番茄红素在水中的溶解度。
1.3.4 复合包合物的表征
1.3.4.1 紫外分光光度法表征
分别取β-酸、β-酸/HP-β-CD包合物、番茄红素、番茄红素/HP-β-CD包合物、HP-β-CD、β-酸-番茄红素/HP-β-CD复合包合物;β-酸、番茄红素和HP-β-CD三者物理混合物(即分别按比例称取样品后混合,无制备过程);β-酸/HP-β-CD包合物和番茄红素/HP-β-CD包合物的两者物理混合物(即先分别制备2 个包合物后按比列称取后混合),采用相应溶剂溶解,在200~700 nm波长测定各样品的吸收图谱,初步判定复合包合物的形成。
1.3.4.2 红外分光光度法表征
将β-酸、番茄红素、HP-β-CD、β-酸-番茄红素/HP-β-CD复合包合物及β-酸、番茄红素和HP-β-CD三者物理混合物样品用溴化钾压片后在400~4 000 cm-1范围内进行测试,通过比较β-酸、番茄红素、复合包合物及物理混合物的红外光谱图之间的差异判断复合包合物是否形成。
1.3.4.3 X射线衍射测试
对少量β-酸、番茄红素、HP-β-CD、β-酸-番茄红素/HP-β-CD复合包合物以及β-酸、番茄红素和HP-β-CD三者的物理混合物,进行X射线衍射测试。测定条件如下:Cu Kα射线、管电压40 kV,管电流200 mA,扫描范围10~80 °,扫描速率8 °/min,步长0.02 °。通过比较β-酸、番茄红素、HP-β-CD、复合包合物及物理混合物的X射线衍射图之间的差异判断复合包合物是否形成。
1.3.4.4 扫描电镜表征
分别取少量β-酸、番茄红素、HP-β-CD、β-酸-番茄红素/HP-β-CD复合包合物及β-酸、番茄红素和HP-β-CD三者的物理混合物、β-酸/HP-β-CD包合物和番茄红素/HP-β-CD包合物的混合物样品置于导电胶上,喷金后放入扫描电镜样品腔内观察样品的微观形态。通过比较β-酸、番茄红素、HP-β-CD、复合包合物及物理混合物的微观形貌之间的差异判断复合包合物是否形成。
1.3.4.5 核磁共振表征
分别取少量β-酸、番茄红素、β-酸-番茄红素/HP-β-CD复合包合物、β-酸/HP-β-CD包合物与番茄红素/HP-β-CD包合物的混合物样品置于核磁管中,用二甲基亚砜溶解,进行测试。通过比较β-酸、番茄红素、复合包合物、单独包合物的混合物核磁共振氢谱图之间的差异以及氢质子化学位移的变化判断复合包合物是否形成。
1.3.5 稳定性的测定
1.3.5.1 光照对复合包合物溶液稳定性的影响
称取一定质量的β-酸-番茄红素/HP-β-CD复合包合物,配制成质量浓度为14 μg/mL(以β-酸计)的溶液,此为样品中β-酸的初始质量浓度。将此初始样品溶液置于不同光照(紫外光/自然光/暗处)条件下,放置一定的时间,在356 nm波长处测定溶液的吸光度,按式(1)计算溶液中剩余β-酸的含量,按式(3)计算β-酸保存率。同时,测定溶液在可见光区(484 nm)的吸光度,以此吸光度的变化率反映溶液中番茄红素含量的变化,以此评价溶液的光稳定性。

1.3.5.2 温度对复合包合物溶液稳定性的影响
同1.3.5.1节配制复合包合物溶液,将初始样品溶液置于不同温度(10~90 ℃)条件下,放置一定的时间,其余分析和计算步骤同1.3.5.1节,评价溶液的热稳定性。
1.3.5.3 pH值对复合包合物溶液稳定性的影响
同1.3.5.1节配制复合包合物溶液,将初始样品溶液分成5 等份,分别调节溶液pH值为3、5、7、9、11,放置一定的时间,其余分析和计算步骤同1.3.5.1节,评价溶液的酸碱稳定性。
1.4 数据统计分析
所有实验均平行完成3 次以上,数据采用Excel 2010、Origin 8.6软件处理,结果均以表示(n>3)。
2 结果与分析
2.1 复合包合物中β-酸、番茄红素含量及包合率

表1 复合包合物中β-酸、番茄红素的含量及包合率Table 1 Contents and inclusion rates of β-acids and lycopene in the inclusion complex
用HP-β-CD将具有抑菌作用的β-酸与具有天然色素功能的番茄红素进行包合,制备复合包合物,改善β-酸、番茄红素的水溶性和稳定性。由表1可知,β-酸-番茄红素/HP-β-CD复合包合物中β-酸含量及包合率均较番茄红素的高,原因可能与β-酸的结构有关,β-酸中的OH更易于与HP-β-CD形成分子内OH…O氢键[28],在包合物制备的过程中其分子间的作用力使主客体分子形成了稳定的包合构象,从而使β-酸更稳定,包合率更高;也可能是番茄红素极不稳定,在制备过程中其含量会随时间、温度以及环境中氧气氧化导致其损失[29],从而使番茄红素的包合率低。
2.2 复合包合物中β-酸、番茄红素溶解度的测定

图2 β-酸-番茄红素/HP-β-CD复合包合物中β-酸、番茄红素溶解度Fig. 2 Solubility of β-acids and lycopene in the inclusion complex
β-酸在水中几乎不溶,在pH值小于7的条件下,溶解度约为2 mg/L[25];番茄红素在水中的溶解度仅为0.002 μg/mL[30]。如图2所示,在经过HP-β-CD分子包合后β-酸和番茄红素的水溶性有了明显的提升,且随着温度的升高溶解度呈现上升趋势。β-酸-番茄红素/HP-β-CD复合包合物中β-酸的溶解度最大可达到3.47 mg/mL,提高了1 735 倍;番茄红素可达0.53 mg/mL,提高了近26万倍。与β-酸/HP-β-CD包合物中β-酸的溶解度(1.73 mg/mL)[25]相比,此复合包合物中β-酸的溶解度提高了近1 倍,与番茄红素/HP-β-CD包合物中番茄红素的溶解度(0.49 mg/mL)[24]相比,也提高了0.04 mg/mL,该结果可充分说明β-酸-番茄红素/HP-β-CD复合包合物的形成,可显著提高β-酸和番茄红素的水溶性。
2.3 复合包合物的表征
2.3.1 紫外-可见光谱测定
作为一种最基本且简单快捷、经济实用的检测方法,紫外分光光度法可用来判断包合物是否形成。由图3a可知,β-酸的甲醇溶液在紫外区有明显的吸收,其中在波长224 nm和356 nm下的吸收峰最强;波长224 nm的吸收峰对应于苯环中共轭二烯的特征吸收峰,而波长356 nm为共轭烯烃和环外羟基作用的吸收峰,这2 个条带的强度和位置取决于分子中羟基的数量和位置[31-32]。β-酸/HP-β-CD包合物溶液的紫外图谱与β-酸在甲醇溶液中吸收峰的位置类似,波峰没有出现明显的位移,符合诱导光谱变化理论[33],说明β-酸/HP-β-CD包合物成功形成。如图3b所示,番茄红素在可见区有明显吸收,且484 nm波长处为其特征吸收峰;在番茄红素/HP-β-CD包合物形成后,其甲苯溶液的吸收峰与番茄红素单体吸收峰类似,说明番茄红素确实存在于包合物中。为了验证番茄红素/HP-β-CD包合物溶液的紫外吸收,从图3c可以看到,该包合物溶液尽管在可见区有吸收,但是其特征吸收峰消失[34],而在波长278 nm处有特征吸收峰出现,分析这种现象出现的原因可能是与番茄红素在甲苯溶剂中的特征吸收峰相比,特征峰发生了较大蓝移[24],番茄红素与HP-β-CD发生的相互作用使番茄红素的亲水性改善,证明番茄红素与HP-β-CD形成了一种水溶性的包合物。
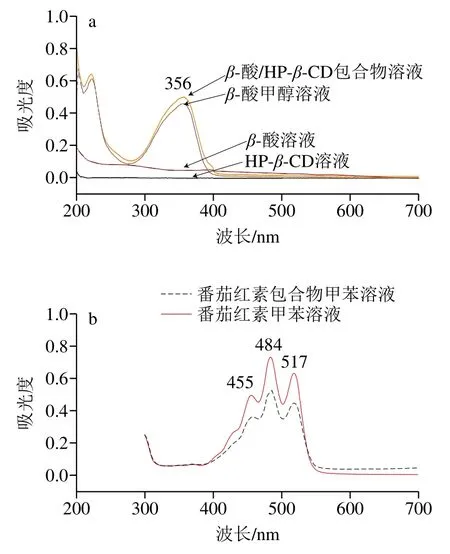
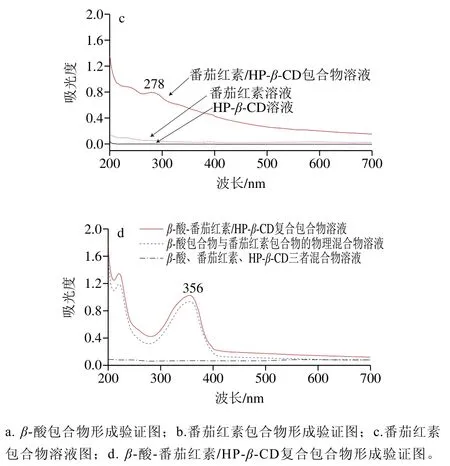
图3 紫外-可见光谱图Fig. 3 UV-Visible spectra
图3d对比图3a、c可以发现:β-酸、番茄红素、HP-β-CD三者物理混合物在200~700 nm波长无吸收,而β-酸-番茄红素/HP-β-CD复合包合物溶液图谱、β-酸/HP-β-CD包合物与番茄红素/HP-β-CD包合物的物理混合物溶液图谱与β-酸在甲醇溶液中类似,且最大吸收也均出现在波长224 nm和356 nm附近,此外,复合包合物的溶液在可见光区(400~700 nm)有吸收,可能由于β-酸在紫外区的吸收强度较大,掩盖了番茄红素的吸收峰,致使番茄红素吸收峰未呈现出来,紫外图谱可说明复合包合物的形成。
2.3.2 红外光谱测定
红外光谱可通过分子的振动和旋转跃迁识别和分析化合物,主、客体分子红外吸收峰的变化可为包合物的形成提供重要信息[35]。如图4a所示,3 500~3 200 cm-1是-OH的伸缩振动吸收带,2 967~2 914 cm-1为C-H键的伸缩振动,1 662 cm-1和1 440~1 372 cm-1处分别为C=O和C=C的骨架振动峰,1 197 cm-1处的吸收峰对应于C-O-C糖苷桥的不对称伸缩振动。如图4b所示,958 cm-1处峰是由共扼烯烃链中C-H的面外弯曲振动产生,1 628 cm-1和1 551 cm-1处峰是由C=C的伸缩振动产生,这说明C=C双键的存在;1 374 cm-1处峰是由甲基和异丙基的弯曲振动叠加产生,2 963、2 913cm-1和2 852 cm-1处峰为甲基和亚甲基的伸缩振动峰,这些说明有甲基、亚甲基和异丙基的存在;3 034 cm-1处的吸收峰是由不饱和=C-H键的伸缩振动产生,808、746 cm-1说明番茄红素为全反式,与文献[36]中番茄红素的红外光谱图基本一致。
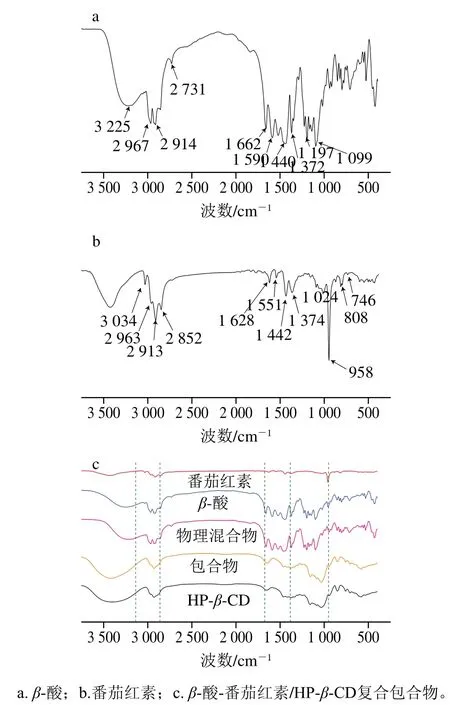
图4 红外光谱图Fig. 4 Infrared spectra
如图4c所示,3 500~3 200 cm-1是—OH的伸缩振动吸收带,2 980~2 920 cm-1为C—H键的伸缩振动,1 650、1 450~1 380 cm-1处分别为C=O和C=C的骨架振动峰;而1 020、1 070 cm-1处的吸收峰,对应CD分子中耦合C—C和C—O的伸缩振动,1 150 cm-1处的吸收峰对应于C—O—C糖苷桥的不对称伸缩振动。在3 250 cm-1波数附近,β-酸在包合物中的—OH伸缩振动吸收带变宽,在2 970 cm-1附近,β-酸、番茄红素的C—H键伸缩振动吸收峰强度明显变弱,同样在1 660 cm-1处也出现了类似的变化;此外,β-酸-番茄红素/HP-β-CD复合包合物的红外光谱图与单纯的HP-β-CD高度相似,且复合包合物中β-酸、番茄红素的特征吸收峰(2 731、1 372 cm-1和1 024、958 cm-1)消失,结果可证实β-酸、番茄红素进入到HP-β-CD分子的空腔内,并且复合包合物光谱中没有新吸收带产生,形成过程仅发生了物理作用,没有产生化学结构的改变[37]。观察到β-酸、番茄红素和HP-β-CD三者物理混合物的谱图,明显是三者谱图的简单叠加,在波数3 034、2 967~2 731 cm-1和1 662~1 099 cm-1处很容易看到一些β-酸、番茄红素的特征吸收峰(图中虚线内所示),表明β-酸、番茄红素是单纯的存在于混合物中,与HP-β-CD没有发生作用,该实验结果与文献[25]得出结论一致。
2.3.3 X射线衍射
通过X射线衍射测试比较客体分子包合前后衍射峰的变化判断包合物是否形成,被广泛应用于CD包合物的表征[38]。如图5所示,曲线b显示β-酸在2θ范围内(12~25 °)出现了比较尖锐的衍射峰,曲线c中番茄红素在16.4 °、24.7 °也出现了强度不一的峰,表明β-酸、番茄红素是以一种结晶态形式存在。相反,曲线a中HP-β-CD是非晶态物质,有2 个较明显的宽峰;β-酸、番茄红素、HP-β-CD三者物理混合物的衍射曲线d是这3 种化合物的简单叠加。然而,由曲线e可以看到β-酸、番茄红素的衍射峰消失,只在15~22.5 °处出现了一个宽的衍射峰,表明形成了1 种新的物相[25],即β-酸-番茄红素/HP-β-CD包合物成功形成,且呈无定型粉末状。Zheng等[39]在对α-硫辛酸与HP-β-CD形成的包合物研究中,得出了相似的结论。
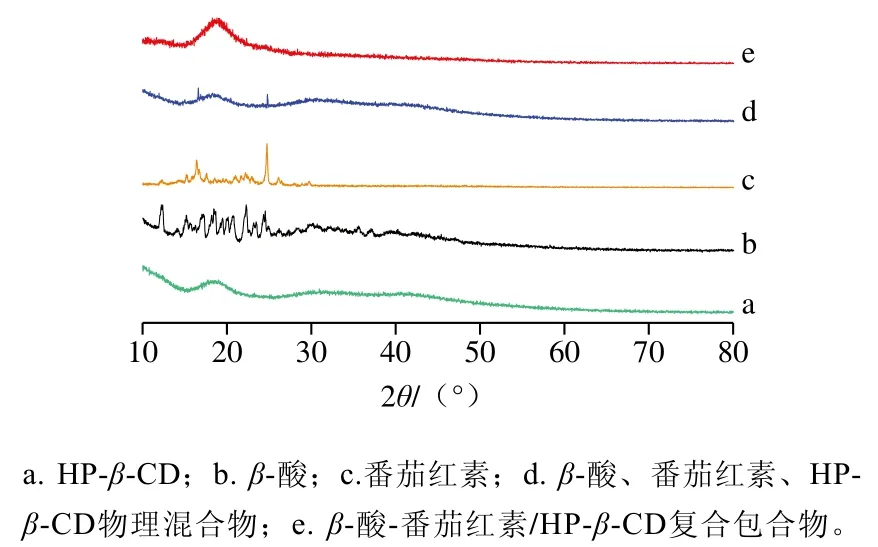
图5 X射线衍射图Fig. 5 XRD patterns
2.3.4 扫描电镜图

图6 扫描电镜图Fig. 6 Scanning electron microscopic images
扫描电镜可以直观地观察到样品的形貌,由图6可以看出,β-酸是长条状固体形态,番茄红素为片状固体形态,HP-β-CD为中空球状结构,β-酸、番茄红素和HP-β-CD三者的物理混合物则为三者的混合或黏附在一起,将这三者经过充分的研磨后,可以观察到HP-β-CD本身的球状结构已经完全消失,呈现出的许多细小、不规则的块状结构,已观察不到β-酸、番茄红素分子的存在,另外,β-酸/HP-β-CD包合物与番茄红素/HP-β-CD包合物的物理混合物也呈现不规则块状,这是各自包合物所表现出来的形貌[24-25],扫描结果进一步证实β-酸-番茄红素/HP-β-CD复合包合物成功形成。
2.3.5 核磁共振图
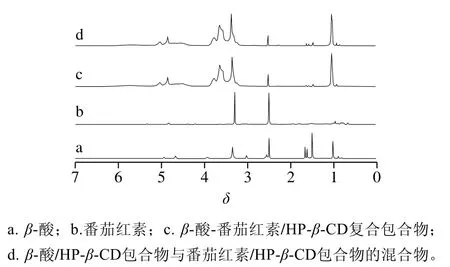
图7 核磁共振氢谱图Fig. 7 1H NMR spectra
核磁共振氢谱可以提供关于客体分子在CD腔内空间位置的有价值的信息[35]。如图7所示,β-酸中的质子出现在δ0.88~4.95之间、番茄红素的质子出现在δ0.67~5.55之间,形成复合包合物后,β-酸、番茄红素中H的化学位移均有不同程度的变化,这是β-酸、番茄红素成功进入HP-β-CD分子的表现,此外,β-酸/HP-β-CD包合物与番茄红素/HP-β-CD包合物的物理混合物表现出与β-酸-番茄红素/HP-β-CD复合包合物极度相似,此结果也进一步表明复合包合物成功形成。与本实验结果类似,Lu Na等[40]通过核磁共振氢谱测得六氢β-酸形成包合物后化学位移也发生了改变。
2.4 β-酸-番茄红素/HP-β-CD复合包合物的稳定性
2.4.1 紫外光对复合包合物溶液稳定性的影响
由图8a可知,随着时间的延长,包合物中β-酸的保存率均逐渐下降;其中,β-酸-番茄红素/HP-β-CD复合包合物中β-酸的保存率较β-酸/HP-β-CD包合物中β-酸的保存率高。β-酸对紫外线非常敏感,紫外光照射30 h后,β-酸-番茄红素/HP-β-CD复合包合物体系中β-酸的仍保留了初始值的41%,这应与番茄红素一定程度起到减缓β-酸的损失有关。由图8b可知,随着时间的延长,包合物溶液中对应番茄红素的吸光度变化率均呈下降趋势,β-酸-番茄红素/HP-β-CD复合包合物与番茄红素/HP-β-CD包合物变化较一致,也说明与β-酸相比,番茄红素的活性更强,然而包合物的形成也增强了番茄红素对紫外线的耐受性,30 h后番茄红素的含量仍能保留在60%以上。由此可见,紫外光对复合包合物中β-酸的稳定性影响较大,因此,复合包合物在保存时应避免紫外光的长时间照射。
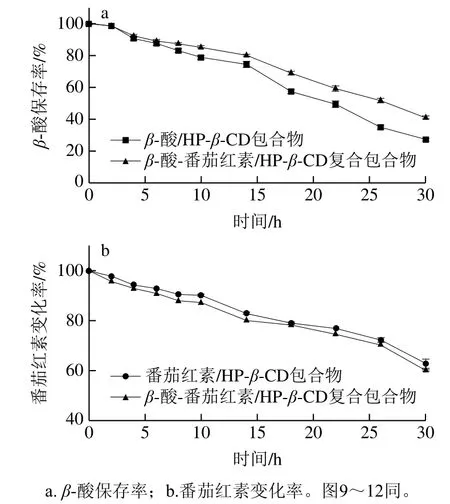
图8 紫外光对复合包合物溶液稳定性的影响Fig. 8 Effect of UV light on the stability of aqueous solution of the inclusion complex
2.4.2 自然光对复合包合物溶液稳定性的影响
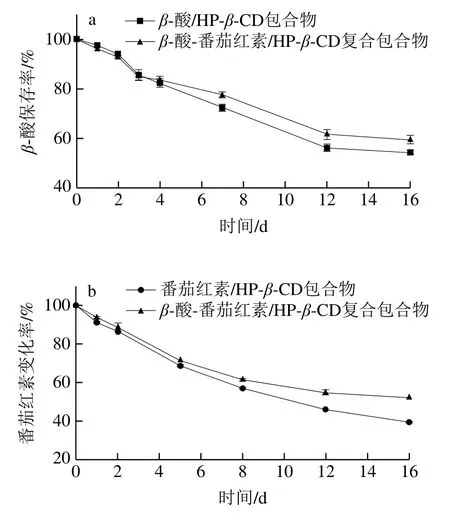
图9 自然光对复合包合物溶液稳定性的影响Fig. 9 Effect of natural light on the stability of aqueous solution of the inclusion complex
由图9a可以看出,随着时间的延长,β-酸的保存率与紫外光照射下相似,均呈下降趋势,但下降的速度明显减缓,24 h后β-酸的保存率可达97.6%,48 h后仅仅减少了6.1%,说明复合包合物中β-酸在自然光条件下保持了很好的稳定性,放置16 d后,复合包合物溶液中β-酸的保存率仍能达到50%以上。由图9b可知,与紫外光照射相似,随着时间的延长,2 种包合物体系中对应的番茄红素吸光度也均呈下降趋势,但复合包合物的变化缓慢,24 h后变化率为93.7%,16 d后仍为初始量的52.3%,而番茄红素/HP-β-CD包合物仅为39.4%,说明复合包合物中的番茄红素在自然光条件下损失较慢,这可能一定程度上与β-酸在该条件下较为稳定有关。
2.4.3 暗处对复合包合物溶液稳定性的影响
相比较于紫外光、自然光照射条件,避光条件下(图10a)复合包合物中β-酸的保存率均较高,避光放置24 h后β-酸的保存率为99.2%,48 h后保存率为97.9%,16 d后仍可保持在80%以上;如图10b所示,复合包合物溶液中对应番茄红素吸光度的变化率呈下降趋势,24 h后变化率为98.2%,16 d后也维持在60%以上,说明在长时间避光保存条件下,β-酸-番茄红素/HP-β-CD复合包合物显示出更好的稳定性。
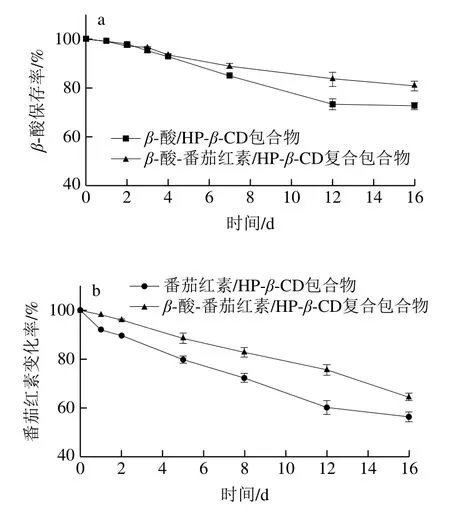
图10 暗处对复合包合物溶液稳定性的影响Fig. 10 Effect of darkness on the stability of aqueous solution of the inclusion complex
综上所述,不同光照条件对复合包合物中β-酸的稳定性及对应番茄红素的稳定性影响程度是不同的,但相比较β-酸/HP-β-CD包合物、番茄红素/HP-β-CD包合物,β-酸和番茄红素一起制备的复合包合物(β-酸-番茄红素/HP-β-CD复合包合物)呈现出更好的稳定性,这可能由于它们相互的协同作用[41],使番茄红素保护了β-酸,减少了损失,β-酸也在一定程度也保护了番茄红素,总体来说,复合包合物在避光条件的稳定性较好,因此应在避光处进行保存。Kamimura等[42]在探讨自然光和避光条件下,香芹酚/HP-β-CD包合物的抗氧化稳定性,得出该包合物抗氧化活性在避光保存比自然光条件下的效果好;刘国荣等[43]制备并研究了栀子蓝色素β-环糊精包合物在阴暗避光、室内散射(230 lx)、灯光直射(3 000 lx)、阳光照射(40 000 lx)及紫外照射(170 lx)5 种条件下放置7 d的稳定性,得出日光照射和紫外照射对色素及其包合物的稳定性影响都较大,而在阴暗避光、室内散射条件下,栀子蓝色素及包合物保存率7 d内均高于99.2%,说明包合物在阴暗避光、室内散射条件下较为稳定,色素变化不显著。
2.4.4 温度对复合包合物溶液稳定性的影响
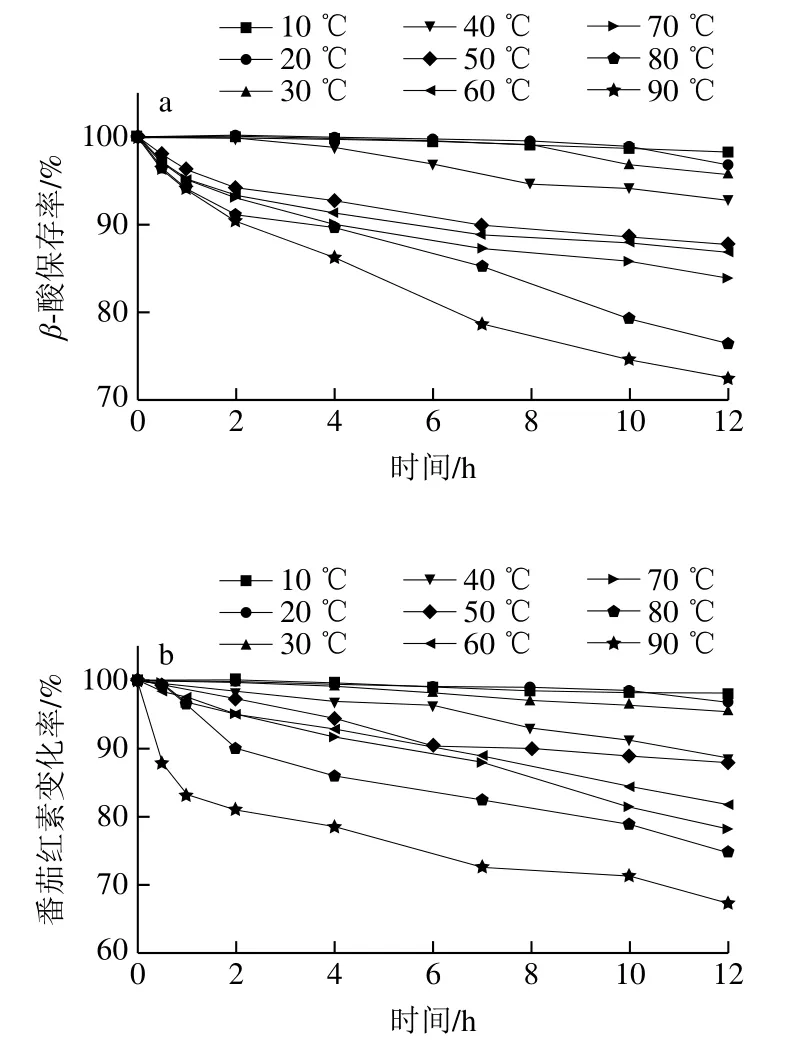
图11 温度对复合包合物溶液稳定性的影响Fig. 11 Effect of temperature on the stability of aqueous solution of the inclusion complex
温度对啤酒花中活性成分的含量[44,25]和番茄红素的稳定性[45]均有一定的影响,因此,考察温度对β-酸-番茄红素/HP-β-CD复合包合物溶液稳定性的影响。图11a显示,在较低温度(10~40 ℃)范围内处理12 h,β-酸的保存率可达90%以上,随着温度的升高,β-酸的保存率逐渐降低,在较高温度(80、90 ℃)保温12 h后,其保存率仍可达到70%以上,稳定性优于相同条件下啤酒花中β-酸[46]以及β-酸/HP-β-CD包合物[25]的稳定性。而图11b观察到的同样条件处理后,复合包合物溶液中对应番茄红素吸光度变化率的趋势与β-酸(图11a)基本一致,进一步说明复合包合物溶液在10~90 ℃范围内具有较好的热稳定性。由此可见,β-酸、番茄红素经HP-β-CD包合在低于90 ℃环境中,其热稳定性显著提高,尤其是番茄红素的加入使β-酸的热稳定性相比较于β-酸/HP-β-CD包合物著提高,说明经环糊精包合后的β-酸-番茄红素复合包合物在改善水溶性的同时也增强了热稳定性。
2.4.5 pH值对复合包合物溶液稳定性的影响
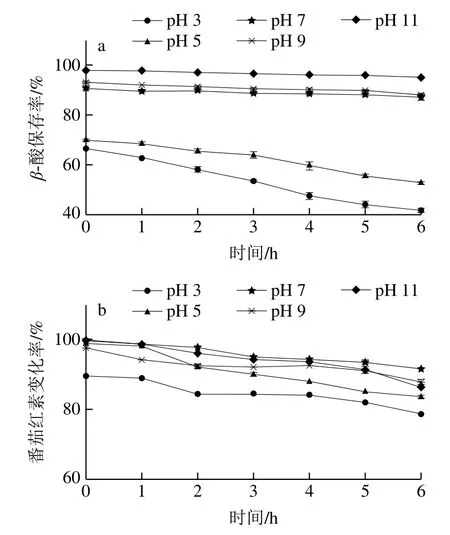
图12 pH值对复合包合物溶液稳定性的影响Fig. 12 Effect of pH on the stability of aqueous solution of the inclusion complex
如图12a所示,在酸性条件下,复合包合物溶液不稳定,这与β-酸自身的化学性质有关;β-酸在酸性条件下易析出,可溶于水的部分减少,在初始溶液中,β-酸的保存率就发生了明显下降,降为70%左右,经6 h放置后为40%左右;而在中性、碱性环境中,复合包合物的稳定性较好,维持在90%以上。由图12b可以看到,pH值对复合包合物溶液中对应番茄红素的影响较小,经6 h放置后吸光度的变化率在80%以上。上述结果表明,在酸性条件下,复合包合物中β-酸的保存率会受到酸度的影响,而番茄红素受酸碱度影响不明显,因此,该β-酸-番茄红素/HP-β-CD复合包合物更适用于中性或偏碱性的食品体系。
3 结 论
本研究成功制备了β-酸-番茄红素/HP-β-CD复合包合物,其中β-酸的包合率可达78.76%,番茄红素的包合率为43.07%;该复合包合物在50 ℃条件下β-酸的溶解度可达3.47 mg/mL,番茄红素溶解度可达0.53 mg/mL,相比较于β-酸包合物和番茄红素包合物,较大程度提高β-酸和番茄红素的水溶性。稳定性评价发现,复合包合物溶液中β-酸和番茄红素均表现出较好的光稳定性和热稳定性,其中,避光条件下,复合包合物中的β-酸保存率最高,经16 d贮藏仍可达80%以上,但紫外光照下β-酸的稳定性改善有限。其次,复合包合物溶液中β-酸在较低温度(10~40 ℃)下含量基本稳定,随着温度的升高保存率逐渐下降,然而即使温度达到90 ℃,复合包合物溶液中β-酸的保存率也可达70%以上,相较于单独的β-酸包合物,其热稳定性显著提高[25];中性或碱性条件对复合包合物溶液中β-酸和番茄红素的影响均较小。β-酸-番茄红素/HP-β-CD复合包合物制备对于将天然来源的防腐剂与天然色素相结合有一定的指导意义,并且两者都具有一定的生物活性,在改善颜色同时还能有效延缓食品腐败,不仅安全性高也更方便使用。最后,制备的复合包合物拓宽了β-酸和番茄红素在水基食品体系中应用范围,为复合食品添加剂的开发提供研究基础和新思路。
