外泌体在各型糖尿病及其并发症中作用的研究进展
2020-08-13吕佳蓉麦一峰
吕佳蓉 麦一峰
糖尿病是一种常见的慢性代谢性疾病,据统计,截至2017年全世界约有4.51亿患者,到2045年,患者的人数可能会上升到6.93亿[1]。糖尿病的显著特点是由于胰岛素产生不足或胰岛素抵抗导致血糖升高。长期高血糖不但会引起糖尿病视网膜病变、糖尿病肾病以及糖尿病周围神经病变等各种并发症的发生,而且也是冠状动脉粥样硬化的独立危险因素。有研究报道糖尿病还会增加多种恶性肿瘤的发病风险[2]。因此,糖尿病的流行已成为全球人类健康的一大危机。近几年,关于外泌体的研究越来越广泛,涉及外泌体的论文数量呈指数级增长。外泌体是一类由各种细胞分泌的纳米级的细胞外囊泡,它通过携带脂质、核酸等特异性物质进行细胞与细胞间的信号传导,参与了多种疾病的发生、发展,有可能成为一种新的生物标志物。Diamant等[3]发现在2型糖尿病(T2DM)患者血浆中微小囊泡较正常人有所增加,揭示了外泌体可能参与了糖尿病的发生。笔者通过收集近年来关于外泌体和糖尿病的相关文献,就外泌体在各型糖尿病及其并发症发生、发展中的作用作一综述,旨在为糖尿病的早期诊断和治疗提供新的方向。
1 外泌体概述
细胞膜上生物物质的转运是细胞维持自身内环境平衡的重要步骤,细胞通过胞外膜小泡(EVs)释放分子,进行细胞间信号传导、细胞分化、炎症和免疫反应等多种生理功能。EVs不仅存在于人体中,在细菌、植物中也曾发现它们的存在[4]。这些小泡在过去被命名为内泌体、脱落小泡、微粒等,然而外泌体这一术语是由Trams等[5]在研究正常和肿瘤细胞系脱落囊泡时首次提出的。外泌体的直径范围约30~150 nm[6]。外泌体的发生始于质膜的向内出芽,随之形成含有膜蛋白的早期内吞体,随着内吞体的内陷和特定蛋白质、RNA的封闭,进一步产生多泡体,随后这些多泡体与质膜融合形成外泌体并释放到细胞外[7]。外泌体通过携带各种生物分子,介导自身及远处细胞间的信息交流,最终完成生理和病理过程。此外,由于有脂质双层结构的保护,外泌体能稳定存在于各种生物液体(例如血液、尿液、唾液和细胞培养基)中而不被降解[7]。
2 外泌体参与各型糖尿病的发生、发展
2.1 外泌体与1型糖尿病(T1DM) T1DM是一种自身免疫性疾病,其特征是存在循环的自身抗体、胰岛的淋巴细胞浸润以及β细胞的特异性破坏,最终导致胰岛素缺乏。目前,已有多项研究结果表明外泌体在T1DM的发生过程中起关键作用,作用机制见图1。有学者发现大鼠和人类的胰岛能释放出富含β细胞自身抗原(如谷氨酸脱羧酶65抗体、胰岛抗原2抗体和胰岛素原)的外泌体,这些被释放出来的外泌体可以被树突状细胞摄取并使其激活,产生细胞因子,而高水平的细胞因子可诱导β细胞的内质网发生应激,导致外泌体进一步分泌增加,从而产生恶性循环[8]。Tang等[9]和Zhu等[10]发现高浓度的细胞因子可促进大鼠β细胞瘤细胞的凋亡,而低浓度的细胞因子可刺激大鼠β细胞瘤细胞释放富含中性神经酰胺酶的外泌体,其可保护β细胞免受高剂量细胞因子或高浓度游离脂肪酸诱导的细胞凋亡。此外,有学者发现胰岛素瘤细胞释放的外泌体可刺激非肥胖糖尿病(NOD)小鼠的自身免疫反应,同时他们发现NOD小鼠胰岛中的间充质干细胞可释放免疫刺激性外泌体,从而激活NOD小鼠自身反应性B细胞和T细胞。同时,他们还发现血清中外泌体的水平和外泌体诱导产生的干扰素-γ与早期糖尿病进展呈正相关[11]。T细胞产生的富含 miRNA-142-3p、miR142-5p和miR-155的外泌体活化后可促进β细胞凋亡,但是通过灭活这些外泌体可缓解NOD小鼠糖尿病的发展。此外,有学者发现T淋巴细胞分泌的外泌体不仅在β细胞中触发细胞凋亡,同时还可以促进趋化因子(趋化因子-2、趋化因子-7和趋化因子-10)信号传导基因的表达[12]。
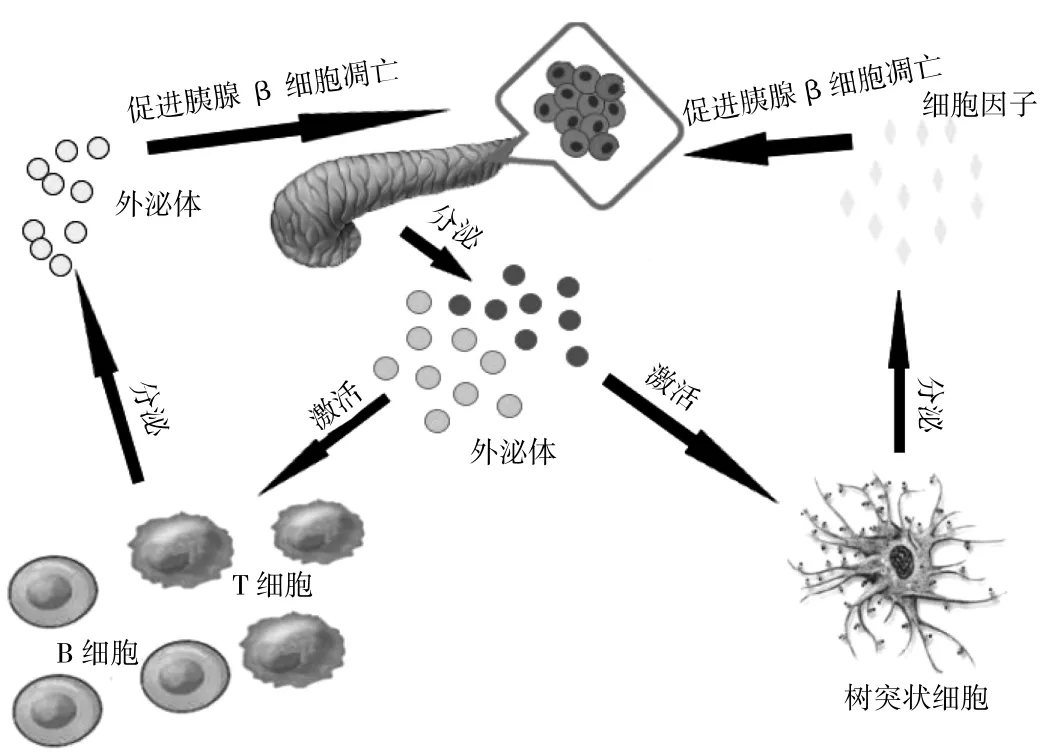
图1 外泌体在1型糖尿病中的作用过程
2.2 外泌体与T2DM T2DM与肥胖密切相关,以胰岛素抵抗为主要特征。脂肪组织被认为是一种动态的内分泌器官,它可以通过释放多种调节糖和脂代谢的激素来调节全身能量代谢平衡。此外,脂肪组织也是循环外泌体miRNA的重要来源,它可以调节远处组织中基因的表达。研究发现脂肪组织特异性敲除miRNA加工酶Dicer(ADicerKO)的小鼠模型中,循环外泌体miRNA以及组织中的成熟miRNA的表达水平显著下降[13];同时,有研究发现这些模型小鼠表现出严重的胰岛素抵抗[14]。然而,白色和棕色脂肪组织的移植可恢复许多循环外泌体miRNA的表达水平(尤其是在ADicer KO小鼠中)从而改善糖耐量。这可能与肝脏成纤维细胞因子-21和循环成纤维细胞因子-21水平的降低有关[13]。Mori等[15]发现随着年龄的增长,脂肪组织的Dicer表达水平随之降低,ADicer KO使小鼠对氧化应激反应过敏。因此,调控脂肪组织中外泌体miRNA的表达在机体对环境变化的反应能力上起着重要作用,可能直接导致老年人糖尿病等代谢性疾病的发病率增加。近年来,有学者发现脂肪细胞产生的外泌体可将单核细胞诱导分化成巨噬细胞,然后巨噬细胞干扰人脂肪细胞中的胰岛素信号传导,最终导致胰岛素抵抗[16]。同时,Song等[17]发现脂肪组织衍生的携带有音猬因子的外泌体可以诱导巨噬细胞向M1极化。降低脂肪细胞中的胰岛素抵抗底物-1和激素敏感性脂肪酶的表达可以促成脂肪细胞的胰岛素抵抗。此外,Ying等[18]发现给正常小鼠注射肥胖小鼠的脂肪组织巨噬细胞(ATMs)分泌的外泌体后,正常小鼠会发生胰岛素抵抗;而给肥胖小鼠注射正常小鼠ATMs分泌的外泌体后,肥胖小鼠的胰岛素抵抗能得到改善,提示ATMs分泌的外泌体参与了靶细胞的血糖不耐受和胰岛素抵抗过程。
2.3 外泌体与妊娠期糖尿病(GDM) GDM是妊娠期间最常见的代谢物紊乱,其病因复杂,涉及遗传、环境等多种因素。与T2DM一样,随着肥胖症的流行,GDM的发病率日益增加。虽然大多数GDM在分娩后大多能恢复正常,但怀孕期间的代谢异常仍然会给母体带来严重的健康风险。研究表明患有GDM的母体在分娩过后患T2DM的风险较正常人增加[19]。此外,研究还发现将发育中的胚胎暴露于受干扰的代谢环境可能会改变生殖细胞的表观遗传谱,从而影响下一代,提示GDM可能会使后代患肥胖及糖尿病的风险增加[20]。Liu等[21]发现GDM孕妇血浆中的外泌体水平显著高于对照组,这些外泌体可促进内皮细胞释放炎性细胞因子,但是外泌体在GDM发展中的具体作用机制尚不明确。除此之外,GDM与胎儿胎盘内皮细胞功能障碍有关。Saez等[22]发现在高浓度高葡萄糖环境中的人脐静脉内皮细胞会产生更多的外泌体,这些外泌体可以增加一氧化氮合酶、人阳离子氨基酸转运蛋白、血管内皮生长因子、细胞内黏附分子的表达,导致内皮细胞功能障碍,但目前具体机制尚未完全阐明。Nair等[23]在研究正常葡萄糖耐量妊娠女性和GDM女性时发现,从GDM妊娠女性绒毛膜绒毛外植体中分离的外泌体能降低骨骼肌细胞的胰岛素敏感性以及其摄取葡萄糖的能力。
3 外泌体与糖尿病并发症
3.1 外泌体与糖尿病肾病(DN) DN是一种严重的糖尿病微血管并发症,是全球终末期肾病的主要原因。DN的临床特征是蛋白尿,其最终的病理表现是肾纤维化。肾小球内皮细胞(GEC)、肾小球系膜细胞(GMC)以及足细胞之间异常的相互作用被认为在DN的发病机制中起关键作用[24-26]。Wu等[24]发现在高糖环境中,GEC会发生内皮-间充质转化(EMT),而EMT的肾小球内皮细胞会分泌富含转化生长因子-β1(TGF-β1)mRNA 的外泌体,这些外泌体可以被足细胞摄取导致足细胞EMT及屏障功能受损,足细胞的EMT过程可能涉及经典的Wnt/β-连环蛋白信号传导途径。同时,这些外泌体还可以作用于GMC,通过TGF-β1/Smad3信号通路促进GMC中的α-平滑肌肌动蛋白表达,系膜细胞增殖以及胞外基质蛋白过量产生,最终导致肾纤维化[25]。总而言之,GEC、GMC、足细胞之间通过外泌体进行旁分泌相互作用可促进DN的发生、发展。
3.2 外泌体与糖尿病性大血管病变 糖尿病性大血管病变是指主动脉、冠状动脉、肾动脉等大血管发生动脉粥样硬化,其是糖尿病患者的主要死因。与正常人群相比,糖尿病患者动脉粥样硬化的发病率更高、发病年龄更轻、病情更重、病死率更高。内皮细胞功能障碍在糖尿病血管病变的发展中起着至关重要的作用,但其机制尚不完全清楚。有研究报道显示从糖尿病患者或肥胖型糖尿病小鼠的血浆中分离的富含精氨酸酶-1的外泌体,可以从体外和体内两种途径转移至内皮细胞,通过减少内皮细胞NO的产生,从而导致血管功能障碍[27]。同时,也有学者发现富含miRNA-155的外泌体可以从平滑肌细胞向内皮细胞转移,破坏细胞间的紧密连接和内皮细胞屏障的完整性,最终导致内皮细胞通透性增加,从而促进动脉粥样硬化的进展[28]。这些都提示了外泌体可能参与内皮细胞的损伤过程,促进了糖尿病性大血管病变的发生与发展。
3.3 外泌体与糖尿病性视网膜病变(DR) DR是糖尿病主要的常见并发症,它也是全球中青年人群视力下降和失明的主要原因。对DR的发病机制的研究虽已有很多,但其最根本的发病机制尚不明确。目前大家普遍认为DR的发生与视网膜细胞变性(包括视网膜细胞凋亡、胶质细胞功能障碍)和视网膜微血管功能障碍(视网膜无血流灌注、血管通透性改变和视网膜新生血管形成)有关[29]。Kamalden等[30]发现在高浓度葡萄糖培养基中培养的大鼠胰腺β细胞会分泌富含miRNA-15a的外泌体,这些外泌体进入血液后能靶向作用于丝氨酸/苏氨酸蛋白激酶-3,从而引起视网膜细胞氧化应激,最终导致细胞凋亡;在糖尿病患者的血浆中,富含miRNA-15a的外泌体水平呈显著增加,且与疾病的严重程度成正比。Huang等[31]发现糖尿病患者血浆中含有免疫球蛋白-G的外泌体是负责激活经典补体途径的重要部分,从而使促炎因子和趋化因子上调,最终导致视网膜血管损伤。而Hajrasouliha等[32]发现视网膜星形胶质细胞分泌的外泌体具有抑制巨噬细胞的迁移和小鼠视网膜脉络膜新生血管的形成。这提示抑制外泌体诱导的补体途径以及促进视网膜星形胶质细胞分泌抗血管生成的外泌体可能可以阻止DR的发展进程,为治疗DR提供了新的途径。
4 展望
糖尿病及其相关并发症的治疗对世界上所有国家来说都是一个巨大的经济负担。目前,最为普遍的糖尿病确诊手段是测量血糖水平。但在其出现血糖升高之前,已有潜在的血管损伤及胰岛素敏感性下降存在。近年来,随着对外泌体研究的不断深入,已有学者提出了将外泌体作为糖尿病早期诊断的一种新的生物标志物。不仅如此,因外泌体可在细胞间传递生物活性分子从而影响靶细胞的胰岛素敏感性,将外泌体作为治疗剂和载体来增强β细胞增殖和修复也为糖尿病的治疗提供了新的方向。虽然现在外泌体在糖尿病发生、发展中的机制还未完全清楚,但是随着对外泌体和糖代谢功能障碍机制的深入研究,其定能在糖尿病的临床应用中发挥重要作用。
