薏苡仁油软胶囊的急性毒性和亚急性毒性研究
2020-08-12黄样增
黄样增
(福建仙芝楼生物科技有限公司 药用菌栽培与深加工国家地方联合工程研究中心,福州 350002)
薏苡仁被国家卫生健康委员会列为药食兼用品,具有健脾利湿、除痹止泻、清热排脓的功效,可以用于水肿、小便不利、脚气、脾虚泄泻、湿痹拘挛、肠痈、肺痈、扁平疣等的治疗。作为一种药食两用的功能性食品原料,人们对薏苡仁的关注日益增加,开发薏苡仁类保健产品成为发展的必然趋势。薏苡仁油是从禾本科植物薏苡(Coixlacryma-jobi. var.ma-yuan(Roman.)Stapf)的干燥成熟种仁[1]中提取的活性物质。薏苡仁含有2%~7%的薏苡仁油,薏苡仁油富含不饱和脂肪酸,主要成分为油酸[2-3]、亚油酸,具有抗肿瘤[4]、抗白血病[5]、镇痛止血[6]的作用。薏苡仁油软胶囊为增强机体免疫力的保健品[7],但是目前对于薏苡仁油软胶囊的安全性报道较少。为科学评价其安全性,本文对薏苡仁油软胶囊进行了急性毒性和亚急性毒性研究,以期为薏苡仁的进一步研究提供基础数据。
1 材料与方法
1.1 试验材料
1.1.1 试验样品
薏苡仁,购买于福建省浦城县,按照《中国药典》(2015年版一部)检测合格后,经超临界CO2萃取分离,得薏苡仁油(密度为0.87 g/mL),直接经压丸后得到薏苡仁油软胶囊。软胶囊内容物组成是纯薏苡仁油(99.5%)和0.5%维生素E,其中甘油三酯含量大于等于90%。薏苡仁油软胶囊内容物,成人日推荐剂量为2.0 g,相当于0.033 3 g/kg(成人体重以60 kg计),临用前分别称取样品(薏苡仁油软胶囊内容物)16.66、33.4、66.6 g加大豆油至100 mL,搅拌均匀,作为低、中、高剂量组受试物。
大豆油(非转基因),购于福州金满福粮油贸易有限公司。
1.1.2 试验动物
由上海斯莱克实验动物有限责任公司提供的清洁级ICR小鼠20只,体重18~22 g,雌雄各半;清洁级SD大鼠80只,体重67~85 g,雌雄各半。试验动物许可证号为SCXK(沪)2012-0002。
1.1.3 饲养环境
福建省疾病预防控制中心SPF级动物实验室,许可证号为SYXK(闽)2012-0008。
1.1.4 仪器与设备
日立7060C全自动生化分析仪,SHANDON EXCELSIOR全自动密封脱水机,美国雅培CELL-DUN3700血球分析仪,LEICA EG 1150石蜡包埋机,CS-IV摊片烤片机,SHANDON Finesse325石蜡切片机,电热鼓风干燥箱,LEICA ST5020全自动染片机,OLYMPUS BX51显微镜,电子天平。
1.2 试验方法
按照《保健食品检验与评价技术规范(2003版)》,进行小鼠经口急性毒性试验和大鼠30 d喂养试验,分别观察薏苡仁油软胶囊的急性毒性和亚急性毒性。
1.2.1 急性毒性试验
急性毒性试验若LD50大于或等于100倍者,则可以考虑进入下一阶段毒理学试验。选取18~22 g健康ICR小鼠20只,雌雄各半。试验前小鼠隔夜禁食16 h,不禁水。取薏苡仁油软胶囊内容物以经口方式灌胃,灌胃剂量为17.4 g/(kg·d)。成人日推荐剂量为2.0 g,相当于0.033 3 g/(kg·d)(成人体重以60 kg计)。则试验倍数为17.4/0.033 3≈522,远大于100倍。灌胃后,连续观察14 d,每天观察并记录动物中毒的表现和死亡情况。室内保持温度18~22℃,相对湿度50%~60%,噪声60 dB以下,照明10~14 h,换气8~20次/h;每3 d洗1次饮水瓶,每天下午加满全价营养块状饲料和饮水。
1.2.2 大鼠30 d喂养试验
1.2.2.1 分组及给予受试物
按照《保健食品检验与评价技术规范(2003版)》的要求,若30 d喂养试验未观察到有害作用的最大剂量大于或等于人的可能摄入量的100倍,综合其他各项试验结果可初步做出安全性评价。将雌雄大鼠按体重随机分成4组,每组各10只。试验按受试物成人日推荐量的25、50、100倍,设3个剂量组分别为0.833、1.67、3.33 g/(kg·d),另设大豆油为对照组。按5 mL/(kg·d)经口灌胃给予不同浓度受试物及对照物1次。试验期间动物单笼喂养,自由进食饮水,每天观察动物形态,记录饲料洒漏量,每周记录1次体重和2次食物摄入量。喂养30 d禁食过夜后称重,采血做血常规及生化指标测定,取出脾、肝、睾丸、肾称重,并对胃肠、脾、肝、肾、睾丸、卵巢做病理学检查。室内保持温度18~22℃,相对湿度50%~60%,噪声60 dB以下,照明10~14 h,换气8~20次/h;每3 d洗1次饮水瓶,每天下午加满全价营养块状饲料和饮水。
1.2.2.2 观察指标
(1)动物的一般表现、体重、进食量、食物利用率。
(2)血常规及生化指标:红细胞计数、白细胞计数、白细胞分类、血红蛋白、谷丙转氨酶、谷草转氨酶、肌酐、尿素、甘油三酯、总胆固醇、血糖、总蛋白、白蛋白。
(3)病理解剖:脏体比、大体观察及病理组织学检查(胃肠、肝、脾、肾、睾丸和卵巢)。
1.2.3 数据统计
试验数据以SPSS软件进行单因素方差分析。经方差齐性检验,方差齐的试验数据采用LSD法进行统计分析,方差不齐的试验数据采用Tambane法进行统计分析。
2 结果与分析
2.1 急性毒性试验(见表1)
由表1可知,试验期间动物未见异常;受试物属无毒级。
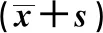
表1 薏苡仁油急性经口毒性试验
2.2 大鼠30 d喂养试验
2.2.1 一般形态观察
该样品3个剂量组的大鼠毛质白、有光泽,外观形态与对照组比较无区别,也无死亡现象。
2.2.2 动物体重增长与食物利用率(见表2~表4)
由表2~表4可见,试验期间,各剂量组每周体重、进食量、食物利用率及试验结束时各剂量组大鼠体重及体重增量、总进食量、总食物利用率与对照组比较,差异均无统计学意义(P>0.05)。

表2 薏苡仁油对大鼠体重的影响
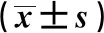
表3 薏苡仁油对大鼠进食量的影响
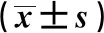
表4 薏苡仁油对大鼠食物利用率的影响
2.2.3 血常规检查结果(见表5)
由表5可见,各剂量组大鼠的血红蛋白、红细胞计数、白细胞计数和白细胞分类与对照组比较,差异均无统计学意义(P>0.05)。

表5 血常规检查结果
2.2.4 血清生化检验结果(见表6)
由表6可见,与对照组比较,雄性高剂量组大鼠血清谷草转氨酶、雌性低剂量组大鼠血清血糖差异有统计学意义(P<0.05),但均在本实验室正常值范围内。其余各剂量组大鼠的血清谷丙转氨酶、谷草转氨酶、尿素、肌酐、血糖、总胆固醇、甘油三酯、总蛋白、白蛋白与对照组比较,差异均无统计学意义(P>0.05)。
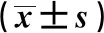
表6 血清生化检验结果
2.2.5 对大鼠脏体比的影响(见表7)
由表7可见,各剂量组大鼠禁食后体重、脏体比与对照组比较,差异均无统计学意义(P>0.05)。
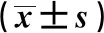
表7 薏苡仁油对大鼠脏体比的影响
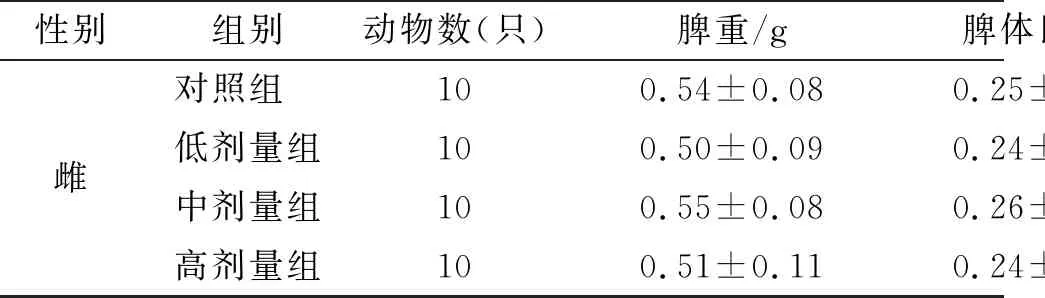
续表7
2.2.6 病理组织学检查
(1)各剂量组动物大体检査未发现明显病变,且生化指标未见异常,因此仅选高剂量组和对照组做组织病理学检查。
(2)结果描述
肝:正常肝小叶结构存在,个别肝细胞轻度变性肿胀。个别肝细胞胞浆内出现少许细小的脂肪空泡,呈轻度脂变,这种脂变肝细胞范围小,呈散在小灶分布。肝细胞无坏死改变。个别肝汇管区见淋巴细胞等炎症细胞浸润,胆管未见异常,无纤维组织增生。大鼠肝脏病理检测结果见表8。
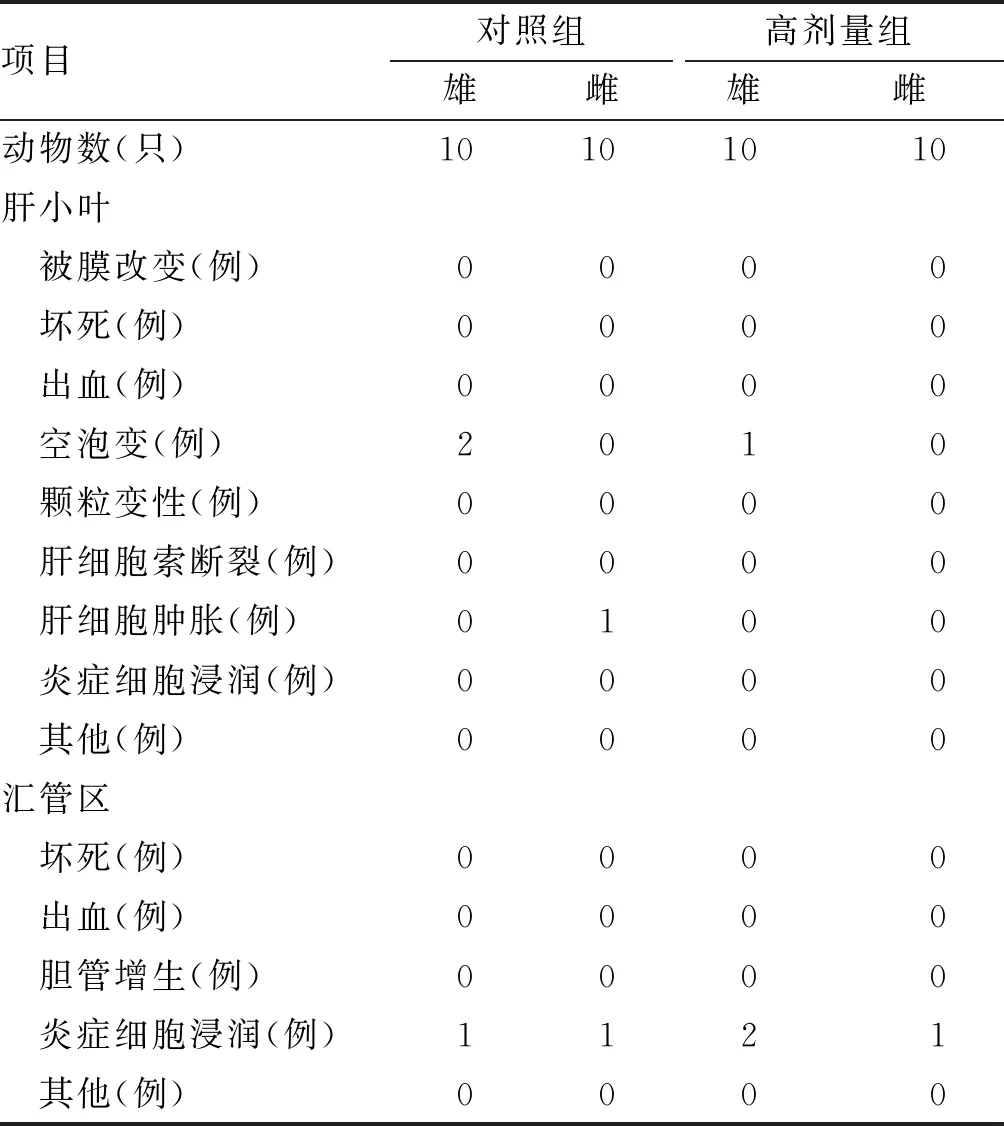
表8 大鼠肝脏病理检测结果
肾:肾皮髓质结构清楚,个别肾小管轻度肿胀及空泡变性,个别肾间质中有灶性炎症细胞浸润,个别肾小管内可见管型,少数肾髓质部可见小囊肿。大鼠肾脏病理检测结果见表9。

表9 大鼠肾脏病理检测结果
胃和十二指肠:未见异常,黏膜完整,无明显出血、糜烂、坏死、溃疡及炎症细胞浸润,无明显腺体增生萎缩改变。
脾:未见异常,脾白髓、红髓结构清楚,红髓、白髓无眀显扩张或萎缩现象。
睾丸:未见异常,曲细精管正常,可见各级生精细胞及成熟精子。
卵巢:未见异常,发育正常,可见各级卵泡和成熟黄体。
总之,在胃、脾、睾丸、卵巢和十二指肠中未发现病理学改变,仅在个别大鼠的肝脏和肾脏中发生病理学改变,各组标本病理变化无明显差异,因此认为被检脏器未见与受试物有关的病理学改变。
3 结 论
急性毒性试验结果提示薏苡仁油软胶囊内容物按灌胃剂量17.4 g/(kg·d)灌胃小鼠未产生毒性,表明薏苡仁油的最大耐受量大于17.4 g/(kg·d)(相当于成人日推荐量的522倍),根据急性毒性分级属无毒级。
薏苡仁油软胶囊内容物各剂量组给予大鼠喂养30 d,试验期间,各组动物生长活动正常,各剂量组每周体重、进食量、食物利用率及试验结束时各剂量组大鼠体重、体重增量、总进食量、总食物利用率、脏体比与对照组比较,差异均无统计学意义(P>0.05)。雄性高剂量组谷草转氨酶、雌性低剂量组血糖与对照组比较,差异有统计学意义(P<0.05),但均在本实验室正常值范围内。其余各剂量组大鼠的血清谷丙转氨酶、谷草转氨酶、肌酐、尿素、血糖、甘油三酯、总胆固醇、白蛋白、总蛋白、血红蛋白、红细胞计数、白细胞计数和白细胞分类与对照组相比差异均无统计学意义(P>0.05),对受检脏器做组织病理学检查,未见特异性病变。因此,可以认为薏苡仁油软胶囊内容物30 d喂养大鼠,未出现毒性反应,即薏苡仁油软胶囊无亚急性毒性。
