基于质量源于设计理念的山参饮提取工艺研究*
2020-08-12何云华石红霞刁本恕
何云华,石红霞,刁本恕,杨 林△
(1. 四川大学华西医院临床药学部,四川 成都 610041; 2. 四川省成都市第七人民医院刁本恕名医工作室,四川 成都 610072)
山参饮为四川省名中医刁本恕主任医师的临床验方,由山药、山楂、郁李仁、人参等10 味中药组方,具有开胃健脾、润肠通便功效,用于肿瘤放化疗、老年病、术后食欲不振、肠道功能差、消化不良、便秘等。该方临床使用已有10 余年,疗效显著,安全性好,为方便服用,将其研制成质量可控的中药颗粒剂。质量源于设计理念是应用质量风险管理知识,重点控制产品的生产工艺,以达到预定目标的产品研发过程,其主要途径是根据关键质量属性,确定关键工艺参数,然后采用多种试验设计方法和数据分析方法开发产品生产工艺[1-4]。目前,质量源于设计理念已应用于中药的干燥[5-6]、包衣[7]等生产过程。本研究中基于质量源于设计理念,优化山参饮提取工艺。现报道如下。
1 仪器与试药
1.1 仪器
1260 型高效液相色谱仪(包括DAD 检测器,美国安捷伦科技有限公司);BT25S 型电子分析天平(北京赛多利斯科学仪器有限公司,精度为十万分之一);JA2003 型电子分析天平(上海良平仪器仪表有限公司,精度为千分之一);YPR -10T 型超纯水器(北京英普瑞环保设备有限公司);AS20500T 型超声波清洗器(天津奥特赛恩斯仪器有限公司,功率为300 W,频率为40 kHz)。
1.2 试药
山药饮片(批号为18060806,四川禾一天然药业有限公司);山楂饮片(批号为180927-8),郁李仁饮片(批号为180528-8),麦芽饮片(批号为180829-8),均购自泸州百草堂中药饮片有限公司;人参饮片(批号为180301941),白扁豆饮片(批号为180100032),薏苡仁饮 片(批 号 为 180800871),砂 仁 饮 片(批 号 为180701701),火麻仁饮片(批号为180800781),均购自成都康美药业有限公司;生姜饮片(自制)。所有药材经四川大学华西医院杨林副主任药师鉴定为正品。苦杏仁苷对照品(批号为110820 -201506,质量分数为93.4%,中国食品药品检定研究院);乙腈(色谱纯,赛默飞世尔科技有限公司);其他试剂均为分析纯。
2 方法与结果
2.1 有机酸含量测定
参照2015年版《中国药典(一部)》山楂含量测定方法[8],按处方比例称取药材(山药30 g,山楂12 g,郁李仁10 g,人参3 g,麦芽15 g,白扁豆15 g,火麻仁15 g,薏苡仁30 g,砂仁3 g,生姜3 g)进行煎煮,过滤,取滤液适量,置容量瓶中,加纯水定容,摇匀,加酚酞指示液2 滴,用氢氧化钠滴定液(0.1 mol/L)滴定[每l mL 氢氧化钠滴定液(0.1 mol/L)相当于6.404 mg 的枸橼酸(C6H8O7)],即得有机酸含量。
2.2 苦杏仁苷含量测定
2.2.1 色谱条件
色谱柱:Agilent extend -C18柱(250 mm×4.6 mm,5 μm);流动相:乙腈-水(12∶88,V/ V);流速:1.0mL/min;检测波长:210 nm;柱温:25 ℃;进样量:10 μL。
2.2.2 溶液制备
取苦杏仁苷对照品(质量分数为93.4%)20.02 mg,精密称定,置25 mL 容量瓶中,加甲醇溶解至刻度,制成质量浓度为0.747 947 2 mg/mL 的溶液,即得对照品溶液。按处方比例称取药材(山药30 g,山楂12 g,郁李仁10 g,人参3 g,麦芽15 g,白扁豆15 g,火麻仁15 g,薏苡仁30 g,砂仁3 g,生姜3 g)进行煎煮,过滤,取适量滤液,置水浴上蒸干,加甲醇溶解于容量瓶中,并稀释至刻度,摇匀,滤过,取续滤液,即得供试品溶液。按处方比例称取郁李仁以外的其他药材,按供试品溶液的制备方法制备阴性对照品溶液。
2.2.3 方法学考察
专属性试验:分别精密吸取2.2.2 项下3 种溶液,按拟订色谱条件进行测定,记录色谱图。可见,阴性对照无干扰,表明该方法专属性良好。详见图1。
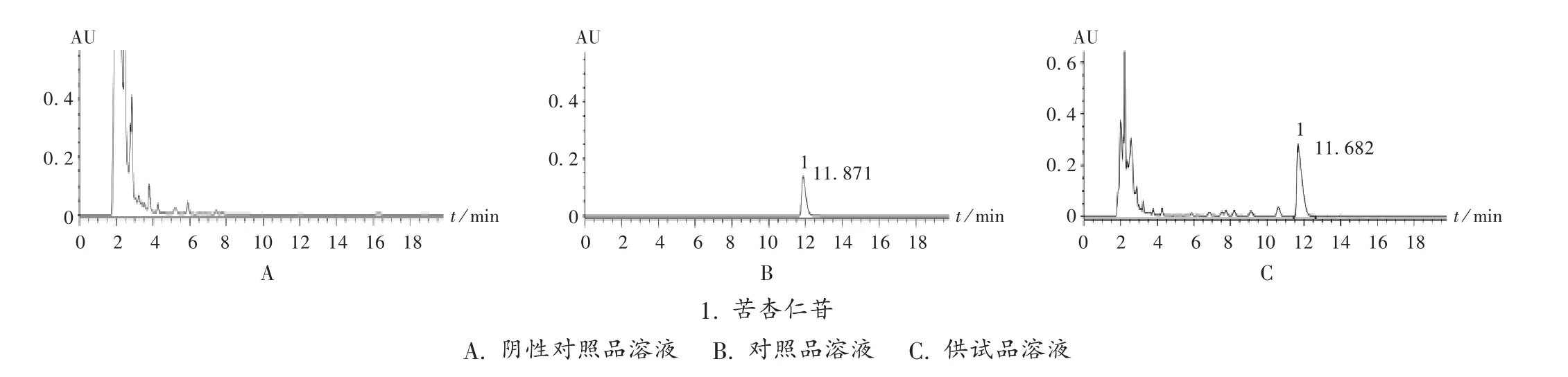
图1 高效液相色谱图
线性关系考察:精密吸取2.2.2 项下对照品溶液,加甲醇稀释成质量浓度为74.794 72,149.589 44,299.178 88,448.768 32,598.357 76,747.947 20 μg/mL的对照品溶液,按拟订色谱条件进行测定。以质量浓度(X)为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程Y=1 324.6X-19.127,r=0.999 1(n=6)。结果表明,苦杏仁苷质量浓度在74.79472 ~747.94720μg/mL范围内与峰面积线性关系良好。
精密度试验:取2.2.2 项下的对照品溶液,按拟订色谱条件连续进样6 次,记录峰面积。结果苦杏仁苷峰面积的RSD为1.13%(n=6),表明仪器精密度良好。
稳定性试验:取样品(批号为180528-8),按2.2.2项下方法制备供试品溶液,分别于制备后0,2,4,6,8,12,24 h 时按拟订色谱条件测定,各进样10 μL,记录峰面积。结果苦杏仁苷峰面积的RSD为1.56%(n=7),表明供试品溶液在24 h 内稳定。
重复性试验:取样品(批号为180528-8),按2.2.2项下方法平行制备供试品溶液6 份,按拟订色谱条件进样测定,记录峰面积。结果苦杏仁苷峰面积的RSD为2.52%(n=6),表明方法重复性良好。
加样回收试验:取同一批(批号为180528-8)样品0.2 g,精密称定,共6 份,精密加入对照品溶液4 mL(质量浓度为1.850 067 2 mg/mL),按2.2.2 项下方法制备供试品溶液,按拟订色谱条件进样测定。结果苦杏仁苷的平均回收率为99.61%,RSD为1.60% (n=6)。
2.3 吸水率计算
吸水率(%) =(处方饮片浸泡后质量-处方饮片浸泡前质量)/处方饮片浸泡前质量×100%
2.4 浸膏得率测定
参照2015年版《中国药典(四部)》浸出物测定法项下方法,精密吸取各试验项下滤液25 mL,置已干燥至恒重的蒸发皿中,水浴蒸干,于105 ℃干燥3 h,置干燥器中冷却30 min,迅速精密称定质量,计算供试品中水溶性浸出物含量和浸膏得率。

2.5 数据处理
根据本研究指标有机酸、苦杏仁苷的含量和浸膏得率在处方中的地位,设定满分为100 分,其权重系数分别为苦杏仁苷含量50,有机酸含量30,浸膏得率20,进行综合评分[9]。综合评分=(苦杏仁苷含量/最大值) ×50+ (有机酸含量/最大值) ×30+ (浸膏得率/最大值) ×20。
2.6 影响因素分析
中药提取过程中会受到多种因素影响,根据预试验研究,结合生产环境,将山参饮提取过程的影响因素归结为5 个方面,将其细化分类绘成鱼骨图(见图2)。其中,环境、饮片、设备和溶剂为客观因素,故本试验对工艺参数进行考察[10]。
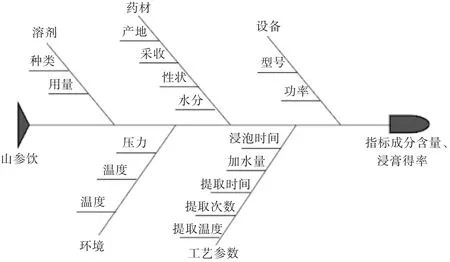
图2 山参饮提取工艺鱼骨图
2.7 单因素考察
浸泡时间:以吸水率为指标考察。按处方比例称取饮片100 g,分别置同一规格烧杯中,加10 倍量水,浸泡30,60,90,120,150,180 min,按2.3 项下公式计算饮片的吸水率。结果见图3 A。可见,90 min 前吸水率呈上升趋势,超过90 min 后趋于平稳,故选浸泡时间为60 min和90 min。
加水量:以有机酸、苦杏仁苷的含量和浸膏得率为指标考察。按处方比例称取饮片100 g,置烧杯中,分别加水8,10,12,14 倍,浸泡90 min,提取2 次,每次60 min,依法测定有机酸含量,测定苦杏仁苷含量及浸膏得率。结果见图3 B。可见,加8 ~12 倍水时,各指标呈上升趋势,超过12 倍水后趋于平稳,故选加水量为12 倍和8 倍。
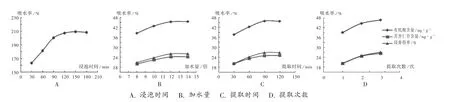
图3 提取影响因素考察结果
提取时间:以有机酸、苦杏仁苷的含量和浸膏得率为指标考察。按处方比例称取饮片100 g,置烧杯中,加水12 倍,浸泡90 min,分别提取30,60,90,120 min,提取2 次,依法测定有机酸含量、苦杏仁苷含量及浸膏得率。结果见图3 C。可见,提取时间为30 ~90 min 时,各指标呈上升趋势,超过90 min 后下降,故选提取时间为90 min 和30 min。
提取次数:以有机酸、苦杏仁苷的含量和浸膏得率为指标考察。按处方比例称取饮片100 g,置烧杯中,加水12 倍,浸泡90 min,提取90 min,分别提取1,2,3 次,依法测定有机酸含量、苦杏仁苷含量及浸膏得率。结果见图3 D。可见,提取次数为1 ~3 次时,各指标呈上升趋势,故选提取次数为3 次和1 次。
提取温度:提取方法为煎煮提取法,根据生产经验,提取温度为100 ℃和90 ℃进行试验。
2.8 Plackett-Burman 试验设计筛选关键工艺参数
试验设计:采用Plackett -Burman 试验设计方法,根据检测指标筛选显著影响的因素[11]。以有机酸的含量、苦杏仁苷的含量和浸膏得率为指标,以浸泡时间(因素A)、加水量(因素B)、提取时间(因素C)、提取次数(因素D)、提取温度(因素E)为影响因素。根据单因素试验结果,选择各影响因素水平,采用Plackett-Burman 设计筛选关键工艺参数,因素水平见表1。本试验中采用综合评分作为响应值,采用Mintab 16.0 软件进行分析。

表1 Plackett-Burman 试验因素水平表
试验结果:试验见表2 和表3。由表3 可见,因素B,C,D 有显著影响,因素A,E 无显著影响,故筛选加水量、提取时间和提取次数为关键工艺参数。浸泡时间根据单因素筛选结果选浸泡90 min;根据生产经验,提取加热方式采用先武火后文火。
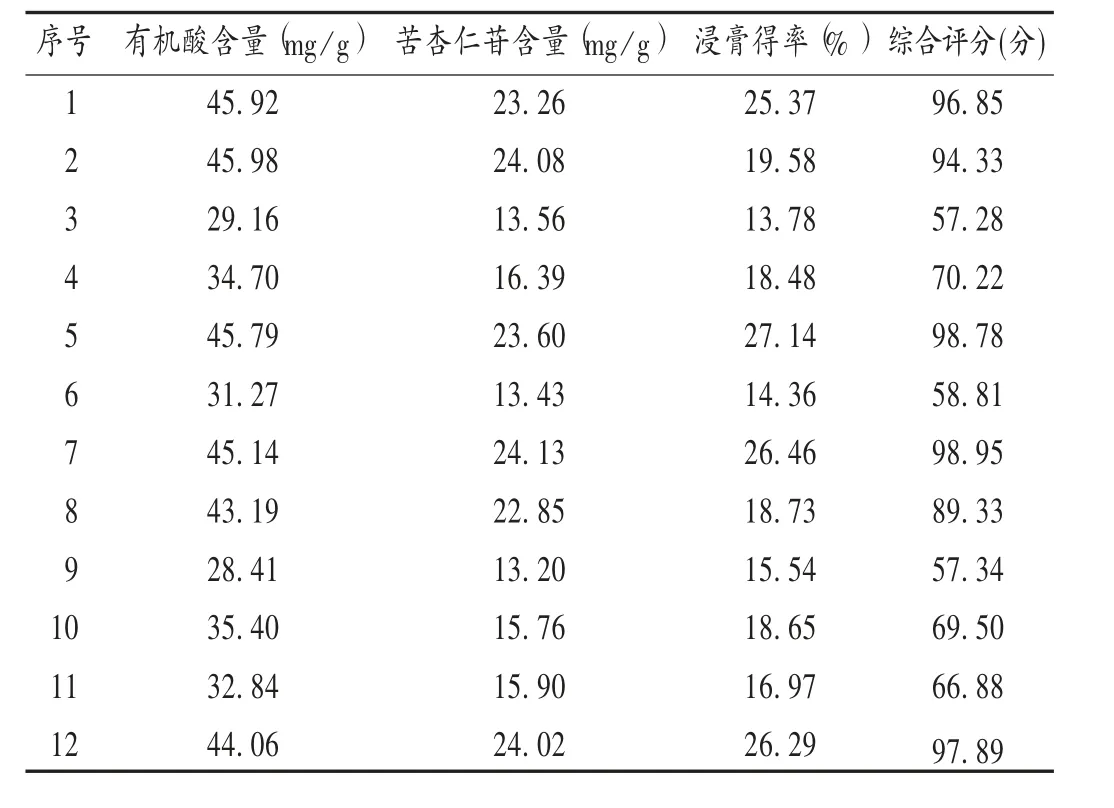
表2 Plackett-Burman 试验结果
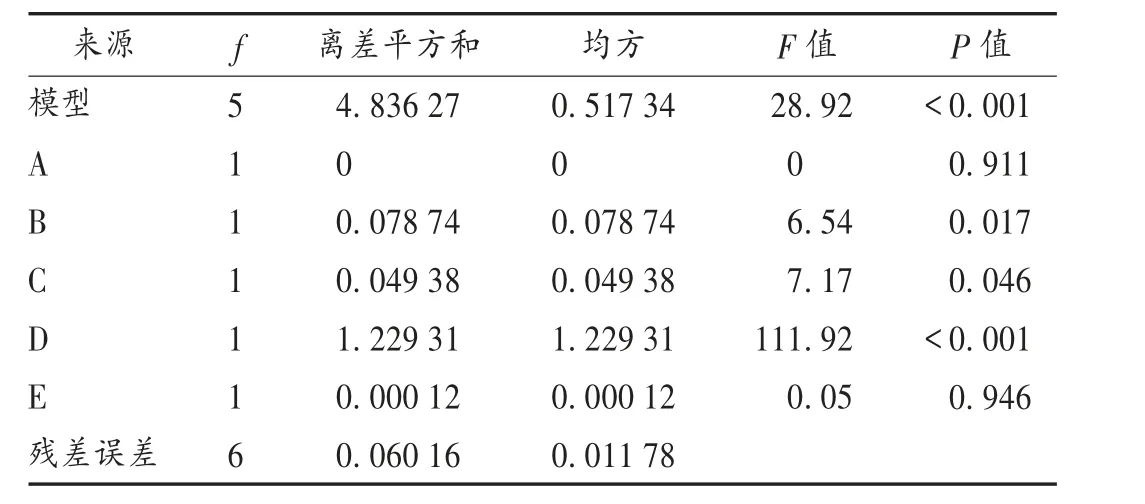
表3 Plackett-Burman 试验方差分析结果
2.9 Box-Behnken 优化提取工艺
根据Plackett-Burman 试验结果,采用Box-Behnken 试验设计[12-14],以综合评分为响应值[15-18],优化山参饮提取工艺。试验设计及结果见表4。
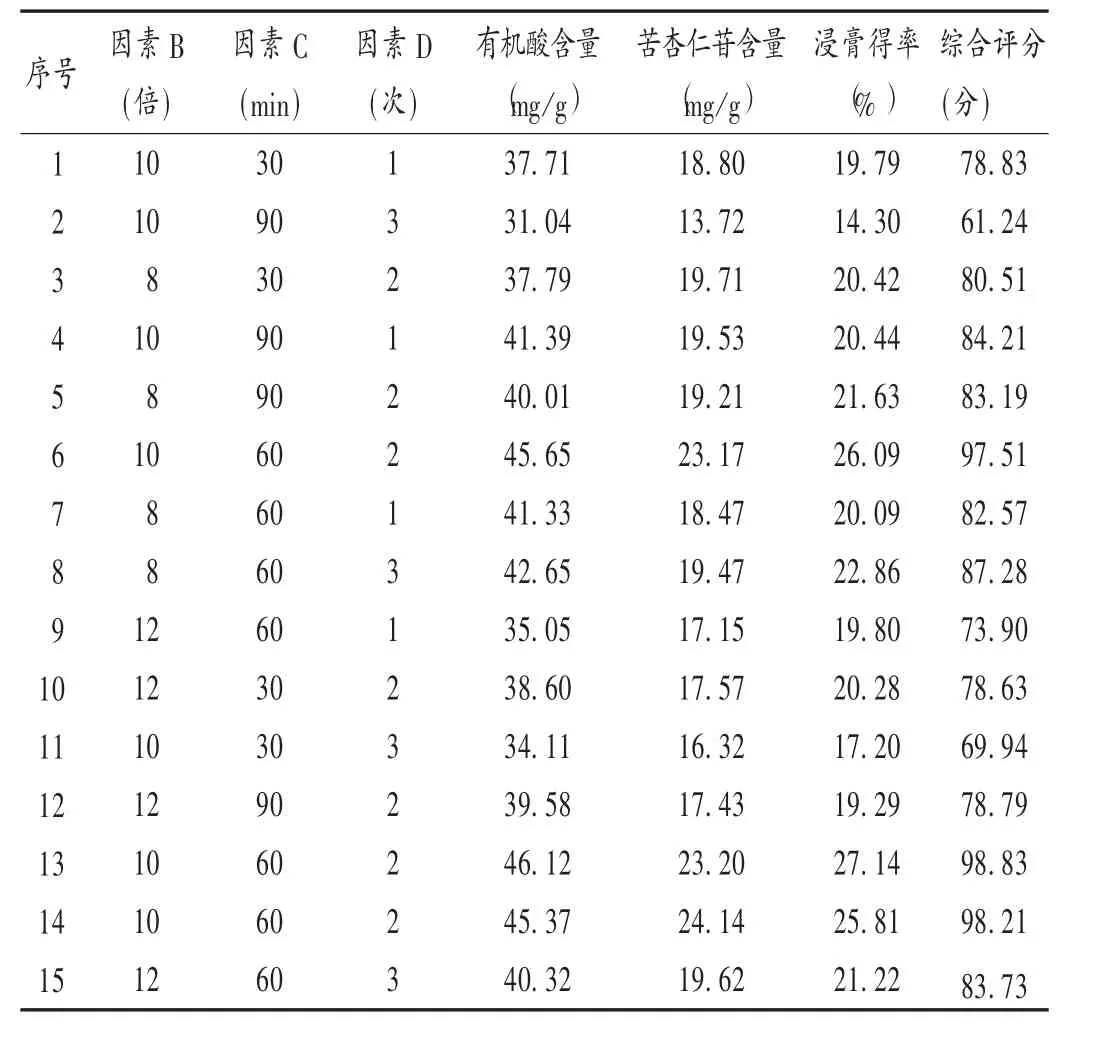
表4 Box-Behnken 试验设计及结果
采用Mintab 16.0 软件,对Box-Behnken 试验数据进行响应面分析,由响应面分析得回归方程Y=98.43-2.29B-0.038C-2.16D-0.58BC+1.28BD-3.52CD-4.89B2-13.21C2-11.66D2,P<0.01 表明模型拟合度较好。结果见表5,响应面3D 图见图4。可见,优选的最佳工艺为加9.96 倍量水,提取62.47 min,提取2.14 次。依据实际生产情况,修正提取参数为加10 倍量水,提取60 min,提取2 次。
2.10 验证试验
通过以上试验及数据分析,得到山参饮最佳提取工艺条件为加10 倍量水,提取60 min,提取2 次。结合实际操作,将优化后的工艺参数修正为加水量、提取时间、提取次数,重复试验3 次。结果有机酸含量分别为45.52,44.78,45.36 mg/g,平均值为45.22 mg/g;苦杏仁苷含量分别为23.87,23.96,23.51 mg/g,平均值为23.7 mg/g;浸 膏 得 率 分 别 为27.09% ,27.15% ,26.86%,平均值为27.03%。与理论预测值相比,相对误差小于1.0%。表明该方法所建立的数学模型具有良好的预测性,优化工艺条件重复性好。
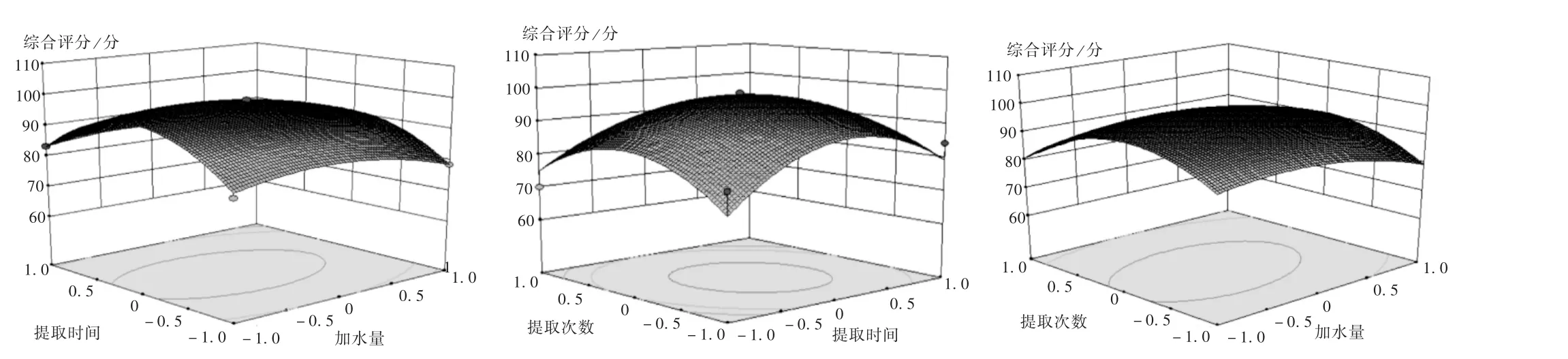
图4 Box-Behnken 试验响应面3D 图
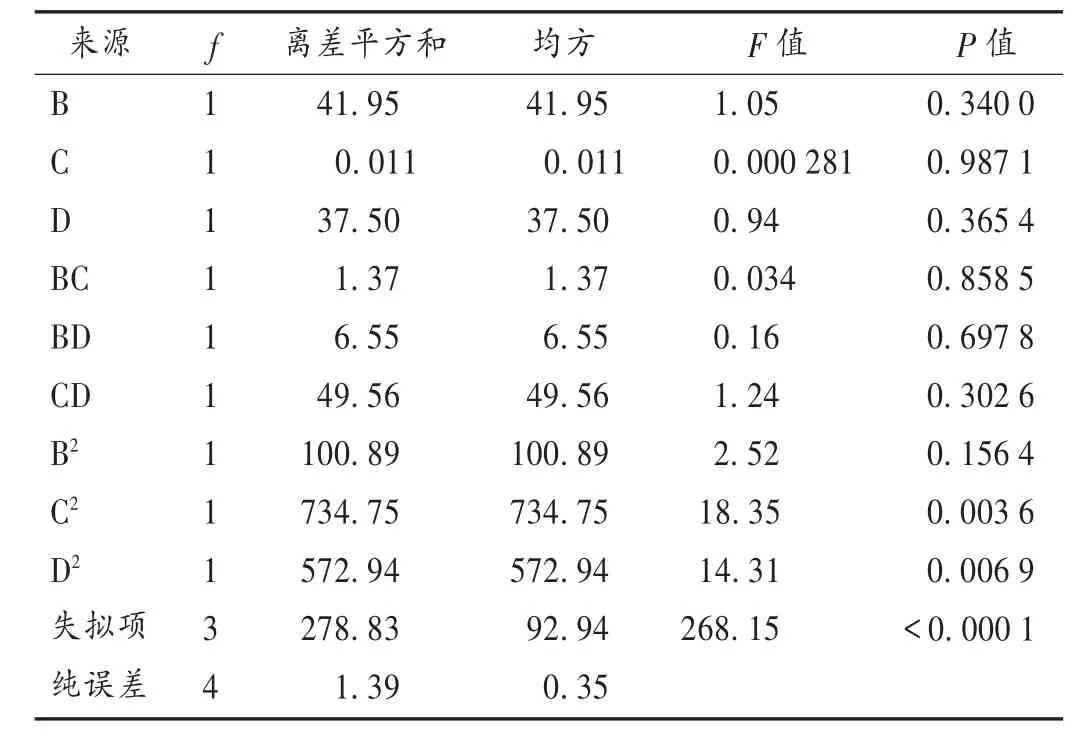
表5 Box-Behnken 试验方差分析结果
3 讨论
采用鱼骨图列出各因素,筛选主要影响因素,再进行单因素影响试验,根据试验结果确定各影响因素试验水平,采用Plackett-Burman 试验设计筛选显著影响因素,对显著影响因素采用Box -Behnken 试验设计进行优化。最终得到最优提取工艺为加10 倍量水,浸泡90 min,提取2 次,每次60 min,先武火后文火。通过验证,该工艺稳定、可靠。
质量源于设计作为一种先进的国际制剂研究理念,能完成药品质量从检验出来到设计出来的策略要求,采用一系列科学推理和分析方法,达到药品质量批间一致性高的目的。本研究中基于质量源于设计理念优化山参饮提取工艺,可推广到实际生产中,提高提取产物质量的稳定性,保证制剂质量稳定、可控。
