四种去内毒素试剂盒提取质粒中内毒素水平的比较
2020-08-12杨振苹张静静邢体坤宋路萍荆新蕊宋彦君王亚萍潘若文
杨振苹 张静静 邢体坤 王 斌 宋路萍 荆新蕊 宋彦君 黄 帅 王亚萍 潘若文▲
1.华兰生物工程股份有限公司研发中心,河南新乡 453003;2.华兰基因工程有限公司质量控制部,河南新乡 453000
近年来,建立在DNA基础上的基因疗法和DNA疫苗已成为一个热门的研究方向,有望成为解决全球卫生问题的最有前景的方法之一。与重组病毒比较,重组质粒因具有免疫原性低、安全等特点而占有更大的优势。
质粒(plasmid)是独立于染色体外的双链闭合环状DNA分子,大小范围为0.8~120kb,具有自主复制和转录能力,常以超螺旋状态存在,广泛存在于细菌、放线菌和真菌中[1]。质粒作为基因工程的常用载体,能够将目的基因通过DNA重组技术转入宿主细胞中。
内毒素(Endotoxin)最早于十九世纪由Richard Pfeiffer在研究发热物质过程中发现并提出[2]。内毒素是革兰氏阴性细菌细胞壁外膜上的特有结构,其主要化学成分是脂多糖。脂多糖由核心寡糖、杂多糖链、菌株特异性O抗原和疏水的脂质A组成,其中脂质A是其主要的活性位点[3]。研究表明,内毒素是诱发炎症反应、胰岛素抵抗、肺损伤等的主要致病成分[2,4-5],对哺乳类动物有显著的致热性[6]。内毒素的检测常用家兔热源法和鲎试剂法[7],其中,鲎试剂法是目前最常用的方法,已被列入《中华人民共和国药典》[8]。
由于试验目的不同,质粒DNA的质量也有不同的要求,尤其是在细胞转染的过程中,质粒中的内毒素水平会明显影响细胞的转染效率,所以对质粒的质量要求更为苛刻。而面对市售的种类繁多的质粒DNA提取试剂盒,正确的选择会成为试验成功的关键。本研究选取了四种市售的去内毒素试剂盒进行质粒提取,并用鲎试剂凝胶法和动态浊度法测定所提质粒DNA的内毒素水平,为细胞转染用质粒DNA提取试剂盒的选择提供依据。
1 材料与方法
1.1 材料
质粒pCGS3保存于华兰生物工程股份有限公司实验室,DH5α感受态细胞购自生工生物工程股份有限公司。
1.2 试剂
四种去内毒素试剂盒为:(A)Thermo公司的GeneJET Endo-Free Plasmid Maxiprep Kit,货号:K0861;(B)生工的UNIQ-500无内毒素质粒大量提取试剂盒,货号:B511249;(C)QIAGEN的EndoFree Plasmid Maxi Kit,货号:12362;(D)TaKaRa的 MidiBEST Endo-free Plasmid Purification Kit,货号:9783S。
凝胶法鲎试剂(批号:1904083,λ=0.06EU/mL)、动态浊度法鲎试剂(批号:1809270)、细菌内毒素国家标准品(批号:1612010,80EU/支)、细菌内毒素检查用水(批号:1812040)均购自湛江安度斯生物有限公司。
1.3 仪器
超净工作台(苏净集团有限公司,SW-CJ-1F),全温摇瓶柜(太仓市实验设备厂,HYG-A),NanoDrop分光光度计(Thermo公司,NanoDrop ONE),电热恒温水浴锅(上海一恒科学仪器有限公司,HWS-28),动态试管检测仪(湛江安度斯生物有限公司,LKL-164-03)。
1.4 方法
1.4.1 质粒DNA提取 用pCGS3质粒转化大肠杆菌DH5α感受态细胞,培养获得携带pCGS3质粒的菌液,之后分别用四种无内毒素质粒提取试剂盒提取质粒,每组做3个平行管。提取的质粒用NanoDrop ONE分光光度计测定质粒DNA浓度、A260/A280、A260/A230,进行质粒DNA的质量评价。
1.4.2 凝胶法 鲎试剂灵敏度的复核:根据《中华人民共和国药典》2015年版[8]中收录的细菌内毒素检测法,首先将细菌内毒素国家标准品稀释成四个浓度的内毒素标准溶液,浓度分别为:0.12、0.06、0.03、0.015EU/mL。然后分别吸取100μL上述内毒素标准溶液,加入100μL待复核的鲎试剂中,每组做4个平行管。同时,取100μL细菌内毒素检查用水加入100μL待复核的鲎试剂中,用作阴性对照,阴性对照平行做2管。封闭管口,轻轻混匀,垂直放入37℃恒温水浴锅中,保温60min。观察凝胶凝结情况,并按公式λc=lg-1(ΣX/4)计算鲎试剂的实际灵敏度(λc)。其中,X为反应终点浓度的对数值,反应终点浓度是指梯度稀释的内毒素浓度中最后一个呈阳性结果的浓度。
当λc在0.5λ~2λ(包括0.5λ和2λ)范围内,表示该鲎试剂可用于细菌内毒素的检测。
1.4.3 动态浊度法
1.4.3.1 标准曲线的可靠性实验 用细菌内毒素检查用水将细菌内毒素国家标准品稀释成1.00、0.10和0.01EU/mL三个梯度的内毒素标准溶液。分别吸取100μL上述内毒素标准溶液,加入100μL的鲎试剂溶液,每组做3个平行管。同时,取100μL细菌内毒素检查用水作阴性对照,阴性对照平行做2管。轻轻混匀,放入动态试管检测仪中于37℃自动采集数据。将内毒素浓度C对达限时间T进行线性回归分析。所得线性回归方程的相关系数r的绝对值≥0.980,则试验有效。
1.4.3.2 供试品的干扰试验 将四种去内毒素试剂盒所得质粒用细菌内毒素检查用水进行适度稀释,参照《中华人民共和国药典》2015年版[8]中细菌内毒素检测法进行干扰实验。根据所得线性回归方程,分别计算供试品溶液中的内毒素含量Ct和含标准内毒素的供试品溶液中的内毒素含量Cs,然后按下列方程式计算回收率(R):

当回收率在50%~200%时,则认为供试品溶液不存在干扰。
1.4.4 质粒内毒素水平测定 (1)凝胶法测定质粒DNA中的内毒素水平。首先将质粒DNA进行梯度稀释,然后向鲎试剂中加入100 μL的细菌内毒素检查用水和100 μL质粒混匀,每组重复3管。同时,取100 μL的细菌内毒素检查用水作为阴性对照,阴性对照做2个平行管。轻轻混匀,置于37℃水浴锅中孵育60min。将试管从水浴锅中轻轻取出,缓缓倒转180°,观察凝胶形成情况。若管内形成不变形、不滑脱的凝胶,则为阳性;若管内没有形成凝胶或形成的凝胶不坚实、变形易滑脱则为阴性。(2)动态浊度法测定质粒DNA中的内毒素水平。参照动态浊度法鲎试剂说明书检测质粒DNA中内毒素水平,每组做3管平行,然后根据回归方程计算内毒素含量。
1.5 统计学分析
试验所得数据用统计学软件SPSS17.0进行分析,数据以()的形式表示。
2 结果
2.1 四种去内毒素试剂盒提取质粒DNA结果
质粒DNA提取操作步骤详见试剂盒说明书。分别取质粒样品5μL,用洗脱液作为空白对照,用NanoDrop ONE分光光度计测定质粒的浓度、A260/A280值、A260/A230值。结果显示,四种去内毒素试剂盒所提质粒的得率、纯度均与说明书一致。测定结果见表1。

表1 四种无内毒素试剂盒提取质粒DNA测定结果
2.2 凝胶法鲎试剂灵敏度的复核
用细菌内毒素检查用水作为稀释液,将细菌内毒素国家标准品稀释成2λ、λ、0.5λ和0.25λ四个浓度的内毒素标准溶液,以细菌内毒素检查用水做2支阴性对照,参照《中华人民共和国药典》2015年版[8]中细菌内毒素的检测法,进行鲎试剂的λ复核。结果显示,λc=0.05EU/mL,在0.5λ~2λ范围内,表明该鲎试剂可用于内毒素检测。复核结果见表2。
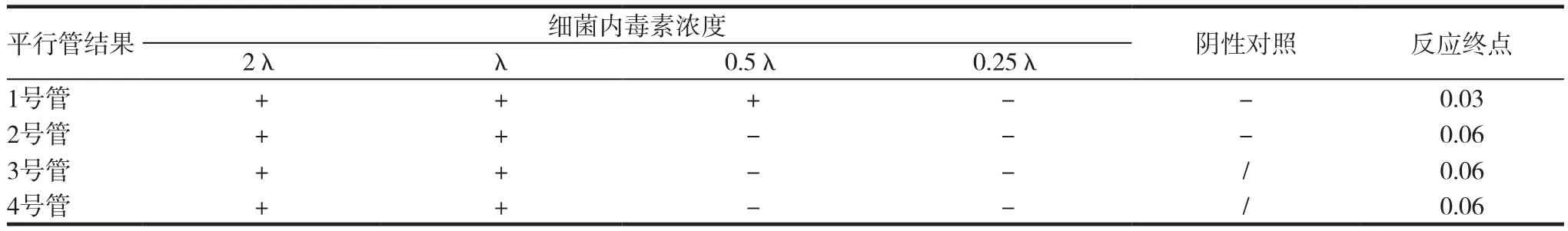
表2 鲎试剂的灵敏度λ复核结果
2.3 动态浊度法
2.3.1 标准曲线的可靠性实验 将内毒素国家标准品进行3个梯度稀释,浓度分别为:1.00、0.10、0.01EU/mL。然后根据说明书操作,测定3个标准浓度达到预设的浊度值所用的时间。结果如表3所示。将内毒素浓度C对达限时间T进行线性回归分析,得回归方程:lgT=2.8008-0.3100lgC,其中,相关系数︱r︱=0.9973>0.980,最低检测浓度为0.01EU/mL,平行管的变异系数小于10%,NC反应时间>3600s,在检测时间外,综上所述,标准曲线成立,可用于后续结果计算。

表3 标准曲线可靠性试验数据
2.3.2 供试品的干扰试验 以质粒样品稀释倍数8为例,进行回收率计算,计算结果如表4所示。内毒素的回收率均在50%~200%之间,所以在此试验条件下供试品溶液不存在干扰作用。

表4 供试品的干扰试验回收率结果
2.4 四种去内毒素试剂盒提取质粒DNA中内毒素水平检测结果
分别用鲎试剂凝胶法和动态浊度法检测四种不同去内毒素试剂盒所提质粒DNA内毒素的水平。首先,将质粒样品稀释后用于凝胶法检测,记录凝胶形成情况;再用动态浊度法测定质粒样品中内毒素,根据回归方程计算内毒素水平,结果见表5。结果表明,凝胶法和动态浊度法检测结果一致,且内毒素含量均符合试剂盒说明书要求,小于0.1EU/μg。

表5 质粒DNA内毒素水平测定结果
3 讨论
内毒素是革兰氏阴性细菌细胞壁外膜上的特有结构,通常会在细菌生长、死亡中被释放。内毒素表面带负电荷、易形成微囊结构,其分子量、电荷性和疏水性都与质粒DNA相似,使用常规的质粒提取方法很难将其与质粒DNA完全分开[9]。此外,在细胞转染过程中,内毒素与质粒DNA竞争转染试剂,阻碍质粒DNA进入细胞膜和核孔复合物,能显著降低内毒素敏感细胞株的转染效率[10-11]。在用电穿孔进行细胞转染中,内毒素含量与细胞转染率、细胞凋亡率有极强的相关性[12]。因此,应尽可能降低用于细胞转染的质粒DNA中内毒素的含量。
在国外,基因治疗用质粒DNA制品的细菌内毒素残留量标准为不超过0.1EU/μg[10]。在本实验中,采用凝胶法和动态浊度法检测四种质粒提取试剂盒所提质粒的内毒素水平,检测结果表明,4种试剂盒所提质粒的内毒素含量均小于0.1EU/μg,均能满足后续细胞转染实验的要求。从质粒得率、内毒素残留量和性价比综合分析,C试剂盒质粒得率最高,内毒素含量最低,但价格也最贵;而B试剂盒虽然质粒得率不及其他3个,但内毒素含量仅次于C,性价比也最高。
本实验采用的凝胶法和动态浊度法检测结果相符,内毒素水平均小于内毒素的限值。凝胶法只能定性地判定结果是否符合《中华人民共和国药典》规定,而动态浊度法可以定量地测出样品中的内毒素含量。除此之外,随着我国鲎资源的逐年减少[13],一种新的内毒素检测方法-重组C因子法正在推广使用。重组C因子法将鲎试剂中的C因子采用生物技术重组获得,以此来替代海洋生物鲎作为鲎试剂原料的唯一来源[14]。该方法已得到欧洲药典、美国食品药物管理局(FDA)的官方认可,其列入《中华人民共和国药典》也指日可待。
疫苗生产过程中的每一个环节都有可能污染内毒素导致制品不合格,不仅给生产企业造成严重的经济损失,也会直接影响该企业的口碑。并且,随着GMP、ICH等文件对生物制品质量要求的规定不断提高,对内毒素的要求也越来越严格[15-16]。因此,疫苗生产人员必须采取有效措施控制产品内毒素含量,保证接种者的人身安全。而质粒生产作为疫苗上游研发过程中的重要环节,其质粒内毒素水平直接影响后续的细胞转染、稳定细胞株的筛选等。因此,获得内毒素水平符合要求的质粒至关重要。
本研究结果为细胞转染用质粒提取试剂盒的选择提供基础。本实验所选的4种去内毒素质粒提取试剂盒所提质粒均能满足细胞转染的要求,但不同的试剂盒质粒得率、内毒素含量和价格不同,使用时应根据实际情况综合考虑。
