原发性高血压尿钠排泄量与左室肥厚的关系探讨
2020-08-07秦晋梅孙宁玲
秦晋梅,孙宁玲
高血压是常见心血管疾病,流行病学研究表明高钠摄入与高血压发病密切相关。钠主要经肾脏排泄,饮食稳定时钠摄入量约等于尿钠的排泄量,因此,24 h尿钠(24 hUNa)是反映机体钠摄入量的最佳指标。左室肥厚(LVH)是高血压常见的靶器官损害,是冠心病、心律失常、心力衰竭、猝死等心血管不良事件的独立危险因素[1-3]。本研究分析原发性高血压病人24 hUNa排泄量与LVH的关系,以探讨盐摄入量与LVH的关系。
1 资料与方法
1.1 研究对象 回顾性分析2015年1月—2017年2月在北京大学人民医院高血压病区住院的原发性高血压病例,诊断标准参照《2010中国高血压防治指南》[4],排除继发性高血压、肥厚型心肌病、瓣膜性心脏病、急性心肌梗死、急性脑血管病、重症感染、严重肝肾功能不全、结缔组织病、恶性肿瘤等病人及资料不全者,最终纳入1 044例病人。
1.2 研究方法 ①记录病人一般临床资料,包括性别、年龄、身高、体重,计算体质指数(BMI)=体重/身高2,体表面积(BSA)= 0.006 1×身高+0.012 8×体重-0.152 9。②收集病人动态血压资料,包括24 h平均收缩压(24 hSBP)、24 h平均舒张压(24 hDBP)、白天平均收缩压(dSBP)、白天平均舒张压(dDBP)、夜间平均收缩压(nSBP)、夜间平均舒张压(nDBP)。③收集病人生化指标,包括空腹血糖(FBG)、血肌酐(Cr)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)、24 hUNa。④记录心脏彩超结果,包括左房内径(LA)、左室舒张末期内径(LVDd)、室间隔舒张末期厚度(IVSTd),左室后壁舒张末期厚度(LVPWTd),按Devereux公式[5]计算左室质量(LVM)=1.04×[(LVDd+LVPWTd+IVSTd)3-LVDd3]-13.6,并计算左室质量指数(LVMI)=LVM/BSA。满足以下任一条件即可诊断LVH[6]:男性LVMI≥115 g/m2,女性LVMI≥95 g/m2;男性IVSTd或LVPWTd≥11 mm,女性IVSTd或LVPWTd≥10 mm。

2 结 果
2.1 高血压合并LVH与不合并LVH病人临床资料比较 研究共纳入1 044例原发性高血压病人,年龄18~92岁,其中不合并LVH 458例(高血压非LVH组),合并LVH 586例(高血压LVH组)。结果显示:高血压LVH组性别比例、年龄、24 hDBP、dDBP、nSBP、nDBP、Cr与高血压非LVH组比较,差异均有统计学意义(P<0.05);高血压LVH组LA、LVDd、IVSTd、LVPWTd、LVM、LVMI均较高血压非LVH组明显升高(P<0.05)。详见表1。
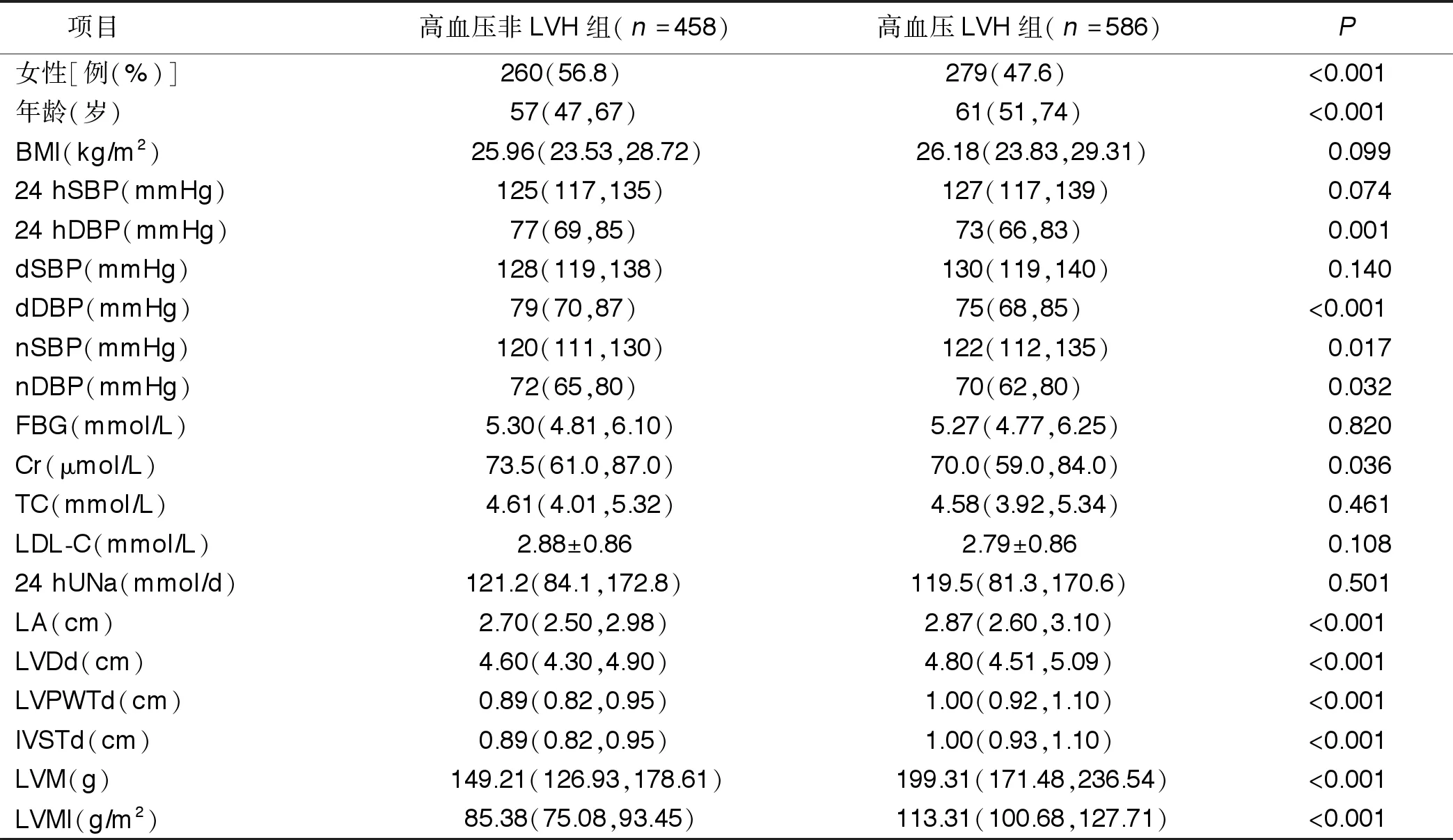
表1 高血压LVH组与高血压非LVH组临床资料比较
2.2 24 hUNa与LVMI的单因素分析 Spearman相关分析显示,24 hUNa与LVMI呈非线性相关(r=0.074,P=0.017)。依据24 hUNa水平将入选病人分为6组:组1(24 hUNa<50 mmol/d)、组2(24 hUNa 50~<100mmol/d)、组3(24 hUNa 100~<150 mmol/d)、组4(24 hUNa 150~<200 mmol/d)、组5(24 hUNa 200~<250 mmol/d)、组6(24 hUNa≥250 mmol/d)。6组LVMI比较差异有统计学意义(P<0.01);组间两两比较显示:组2、组3、组4 LVMI与组6比较差异均有统计学意义(P<0.05或P<0.01)。详见表2、图1。

图1 24 hUNA与LVMI的关系曲线图

表2 6组LVMI比较[M(Q1,Q3)] 单位:g/m2
2.3 24 hUNa与LVH的多因素Logistic回归分析 将高血压是否合并LVH作为因变量(0=高血压不合并LVH,1=高血压合并LVH),结合24 hUNa与LVMI的关系曲线(见图1),将24 hUNa进行3分类(1:24 hUNa 50~<200 mmol/d;2:24 hUNa<50 mmol/d;3:24 hUNa≥200 mmol/d),并设置24 hUNa为亚变量(1为对照),将性别、年龄、BMI、24 hSBP、24 hDBP、dSBP、dDBP、
nSBP、nDBP、FBG、Cr、TC、LDL进行赋值后作为自变量共同引入回归模型(赋值表见表3)。结果显示,女性、高龄、肥胖、肾功能不全、24 hUNa≥200 mmol/d是高血压合并LVH的独立危险因素,24 hUNa<50 mmol/d有危险性增高倾向,但未达统计学意义(RR=1.351,P=0.215),详见表4。

表3 Logistic回归赋值表

表4 LVH与24 hUNa的多因素Logistic回归分析
3 讨 论
盐是人们生活不可或缺的调味品,是生命的必需营养物质。流行病学研究显示盐摄入量远高于生理需要量,盐摄入量增加和血压增高密切相关[7-9],各国开展的限盐干预研究进一步证实了高盐摄入在高血压发生、发展中的重要作用。Hajjar等[10]研究推测,钠摄入量每天减少50 mmol(1.15 g),可以减少50%需要降压治疗、22%的脑卒中死亡、16%的冠心病死亡人数。因此,各国高血压指南都建议高血压病人限制钠盐摄入。但是盐作为人体必需的营养物质,限盐以多少为宜一直在探索中。一些研究显示,盐摄入量和心血管风险间存在J型或U型曲线。Alderman等[11]研究发现,每日钠摄入量<2.5 g或>6.0 g都可能增加心血管疾病风险。O′Donnell等[12]对28 880例年龄大于55岁有明确心血管疾病或糖尿病的心血管疾病高危人群(其中70%患高血压)进行了估测24 hUNa排泄量与心血管风险的研究,研究开始时24 hUNa排泄量为(4.77±1.61)g/d,中位随访56个月,结果显示:与基线尿钠排泄量4.00~5.99 g/d相比,尿钠排泄量>7 g/d与所有心血管事件(包括心血管死亡、心肌梗死、卒中、因心力衰竭住院)危险性增加相关,尿钠排泄<3 g/d与心血管死亡和因心力衰竭住院危险性增加相关。2016年在 Lancet发表的一项汇总分析也发现,对于高血压人群,24 hUNa排泄<3 g或≥7 g均增加全因死亡及心血管事件发生风险[13]。然而这和各国高血压指南所建议的每日钠摄入量控制在1.5 g或2.0 g以下相距甚远。
高血压LVH是临床常见的靶器官损害,表现为左室室壁增厚、质量增加,伴或不伴左心室心腔扩大,心脏收缩、舒张功能减退,可导致心律失常、心力衰竭、猝死等不良心血管事件。目前,高血压发生LVH的机制未完全阐明。血压增高所导致的心脏压力负荷和容量负荷增加是高血压发生LVH的重要因素。然而,临床上部分高血压病人LVH 程度与血压水平并不相关,一些长期血压控制良好的高血压病人仍会出现LVH甚至进展。因此,血流动力学并非导致LVH 的唯一因素。目前研究认为,交感神经-肾上腺素系统和肾素-血管紧张素-醛固酮系统(RAAS)激活、内皮细胞功能障碍、氧化应激和炎症反应、胰岛素抵抗、细胞内钙超载、遗传和基因突变等均和LVH的发生发展密切相关[14]。
目前已有的一些动物实验表明高盐和低盐摄入均可诱导LVH[15-17]。周宁等[17]观察了不同浓度钠盐饮食对自发性高血压大鼠(SHR)血压及LVH的影响,将SHR分为高盐饮食组(饮用4%氯化钠溶液)、正常盐饮食组(饮用0.9%氯化钠溶液)、低盐饮食组(饮用0.4%氯化钠溶液),Wistar大鼠为对照,实验喂养12周,结果显示:与Wistar大鼠相比,SHR血压明显增高,LVMI明显增高,高盐饮食组和低盐饮食组LVMI较正常盐饮食组明显增高,高盐饮食组LVMI增加更明显。Frohlich等[18]用不同盐浓度的饲料喂养SHR和WKY大鼠10周发现,SHR动脉血压和外周阻力进行性升高,心脏指数、心率、内脏血流降低,LVMI明显升高,而WKY血流动力学无明显变化,LVMI亦明显升高。从而得出结论:高盐摄入可能是LVH的独立危险因素。目前研究表明,高盐摄入可以通过容量增加、血压增高、激活RAAS系统、细胞内钙超载、氧化应激等引起LVH[19-21],而低钠摄入亦可以增加交感神经活性,促进肾上腺素分泌,上调血浆肾素、醛固酮水平,产生胰岛素抵抗,最终产生心肌损伤和LVH[22-23]。
本研究研究结果显示,24 hUNa与LVMI呈非线性相关,24 hUNa≥200 mmol/d(4.6 g)是高血压合并LVH的独立危险因素,而24 hUNa<50 mmol/d(1.15 g),虽LVH相对危险度增高,但未达统计学意义,可能与在本组病例中24 hUNa<50 mmol/d病例数相对较少相关。综合目前临床研究,高盐摄入的危害是人们普遍接受的,而低盐摄入的危害也有了一些证据,盐作为人们日常生活最重要的调味品,多少量最有益身体健康,需要更多研究支持。
