肺动脉环缩术在先天性心脏病分期手术中的应用效果观察
2020-08-07刘爱军刘承虎王执一范祥明苏俊武
刘爱军,刘承虎,王执一,范祥明,程 沛,苏俊武
1952年Muller和Dammann首先对合并肺动脉高压的先天性心脏病患儿施行肺动脉环缩(pulmonary artery banding,PAB)术,以减少肺血流量[1]。随着小儿心脏外科技术的提高,PAB术逐渐拓展应用于合并重度肺动脉高压的先天性心脏病患儿在行双心室矫治或者单心室矫治前的分期手术治疗中以及大动脉调转术前期的左心室功能锻炼中。2008年1月—2018年12月我院小儿心脏中心对205例拟行分期手术治疗的合并有重度肺动脉高压的先天性心脏病患儿进行PAB术,回顾性总结其临床应用经验及手术效果。现报道如下。
1 资料与方法
1.1 临床资料 选取2008年1月—2018年12月我院小儿心脏中心收治的合并有重度肺动脉高压的先天性心脏病患儿共205例,男101例,女104例;年龄0.3~73.0个月,中位数0.6个月;体重2.5~26.0 kg,中位数6.6 kg。按实施PAB手术目的分为双心室矫治组(97例)、单心室矫治组(72例)和左心室训练组(36例)。双心室矫治组,男47例,女50例;年龄2~38个月,中位数0.5个月;体重3.2~22.0 kg,中位数5.9 kg;经皮血氧饱和度(SpO2)为(96.6±9.7)%;病种包括完全性房室间隔缺损34例,右心室双出口23例,多发室间隔缺损35例,室间隔缺损合并主动脉缩窄5例。单心室矫治组,男35例,女37例;年龄3~42个月,中位数0.8个月;体重3.8~22.3 kg,中位数7.9 kg;SpO2为(91.8±2.3)%;病种包括肺动脉高压型单心室27例,三尖瓣闭锁16例,三尖瓣重度狭窄7例,右心室双出口(室间隔缺损远离两大动脉)15例,十字交叉心3例,矫正型大动脉转位4例。左心室训练组,男19例,女17例;年龄0.3~73个月,中位数0.5个月;体重2.5~19.0 kg,中位数6.2 kg;SpO2为(73.1±10.3)%;病种均为室间隔完整型完全型大动脉转位(TGA-IVS),其中合并房间隔缺损29例,卵圆孔未闭7例,动脉导管未闭15例,小型室间隔缺损2例。
所有患儿胸片均提示肺血明显增多,肺充血,胸部X线平片显示心胸比值(C/T)0.60~0.78(0.67±0.08),术前均进行超声心动图检查,49例患儿行右心导管造影,76例行心脏CT血管造影(CTA)。术前出现肺部感染42例,心功能不全3例,因动脉导管近闭合出现严重缺氧5例。心电图检查全部为窦性心律,右心室肥厚62例,双心室肥厚64例,左心室肥厚79例。3组患儿临床资料见表1。
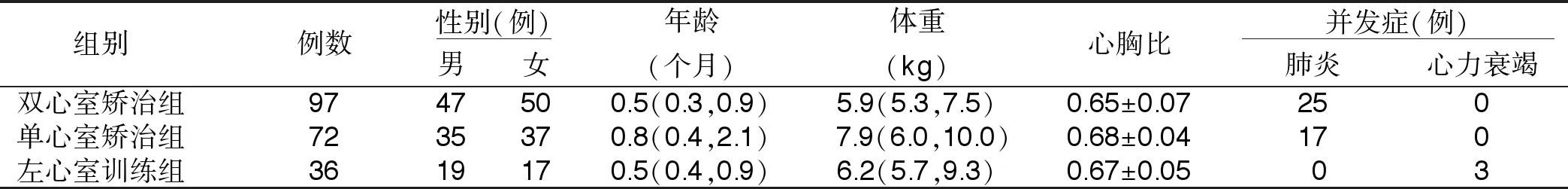
表1 3组患儿临床资料比较
1.2 手术方法 PAB术均在静脉复合全身麻醉下施行,术中保持吸入氧浓度(FiO2)在30%~50%。采用胸骨正中或胸骨左缘第2肋间径路手术。切开心包后充分游离显露升主动脉、主肺动脉,双心室矫治组和单心室矫治组在主肺动脉远端置入测压管监测肺动脉压;左心室训练组主肺动脉环缩带近心端置入测压管监测肺动脉压(左心室压力)。在肺动脉瓣交界上方1.0~1.5 cm处放置Gore-Tex 3~5 mm宽血管条,逐渐收紧达到预计效果后,以5-0 Prolene 线或者4×12涤纶编织线贯穿缝合血管条和肺动脉外膜固定,防止移位。
1.3 环缩标准 3组患儿肺动脉环缩程度的标准有所不同。肺动脉环缩带周长度大小原则上按照Trusler经验公式[2]进行计算。双心室矫治组患儿术中调整肺动脉环缩带远心端肺动脉收缩压与体循环收缩压的比值(sPAP/sBP)为0.3~0.5,SpO2降至90%左右;单心室矫治组患儿尽可能使远端肺动脉平均压(mPAP)达到20 mmHg(1 mmHg=0.133 kPa)以下,SpO2维持在80%~85%;左心室训练组患儿术中监测肺动脉环缩带近心端mPAP,或者直接测量解剖左心室收缩压与体循环收缩压的比值,一般要达到 0.6以上,为避免PAB术后SpO2过低及动脉导管过早闭合,进行体肺分流术,维持SpO2为80%~85%。
二期双心室修复手术及大动脉调转手术均在静脉复合全身麻醉体外循环辅助下施行,均采用胸骨正中切口径路,经升主动脉及上腔静脉、下腔静脉插管建立体外循环后,游离拆除原肺动脉环缩带后,完成相应心内畸形矫治。行单心室修复手术者,先期在非体外下完成单侧/双侧腔肺吻合(Glenn)手术后,再择期在体外循环辅助下完成全腔静脉-肺动脉连接术(Fontan术)。
1.4 围术期治疗 术后患儿入重症监护室(ICU)治疗,呼吸机辅助呼吸,吸入氧浓度40%~60%。应用芬太尼2~5 μL/(min·kg) 镇静,多巴胺和/或多巴酚丁胺3~8 μL/(min·kg)和/或盐酸肾上腺素0.02~0.1 μL/(min·kg)维护心脏功能及血流动力学平稳。严格无菌操作,应用抗菌药物防治感染。
1.5 术后随访 术后1个月、3个月、6个月及1年门诊复查SpO2、胸部X线片、超声心动图检查等,收集数据。

2 结 果
2.1 3组术前、术后mPAP、SpO2比较 单心室矫治组、双心室矫治组术后mPAP、SpO2均较术前明显下降(P<0.05);左心室训练组术后mPAP、SpO2均较术前明显上升(P<0.05)。详见表2。

表2 3组术前、术后mPAP、SpO2比较(±s)
2.2 3组呼吸机使用时间、ICU停留时间、住院时间及住院期间死亡情况 3组住院期间死亡7例,死亡率3.4%。其中双心室矫治组死亡2例,1例死于术后低心排血量综合征、重症感染;1例术中心室颤动术后死于低心排血量综合征。单心室矫治组死亡3例,1例死于重症感染、多脏器功能衰竭、弥散性血管内凝血(DIC);1例死于术后低心排血量综合征;1例死于感染性休克、心力衰竭。左心室训练组死亡2例,1例死于重症感染、多脏器功能衰竭;1例死于术后低心排血量综合征。详见表3。单心室矫治组术后有1例患儿术后因环缩带过紧,再次手术调整环缩带。术后并发心包积液2例,经治疗后痊愈出院。胸骨左缘第2肋间进胸25例,余手术切口均经胸骨正中进胸。
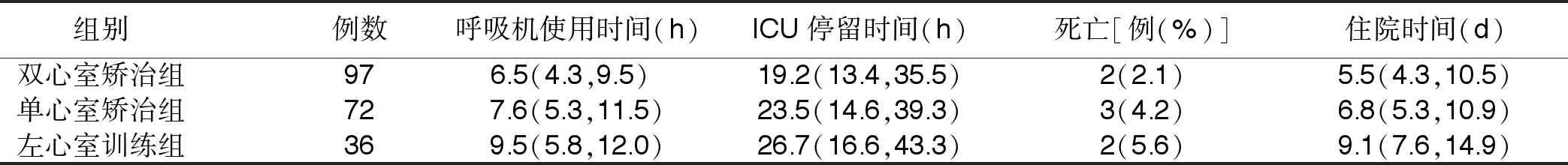
表3 3组呼吸机使用时间、ICU停留时间、住院时间及住院期间死亡情况
2.3 3组Ⅱ期及Ⅲ期手术资料比较 PAB术后实施二期手术117例(57.1%)。其中双心室矫治组有 47例,男26例,女21例,距PAB术间隔时间5~40个月,中位数时间17.6个月。单心室矫治组行Glenn术43例,男23例,女20例,距PAB术间隔时间15~53个月,中位数时间18.3个月;后期3次行Fontan术13例,距PAB术间隔时间52~112个月,距二期Glenn手术间隔27~52个月。左心室训练组完成大动脉调转术(ASO)27例,距PAB手术间隔时间6 d至35个月,中位数时间0.3个月。详见表4。
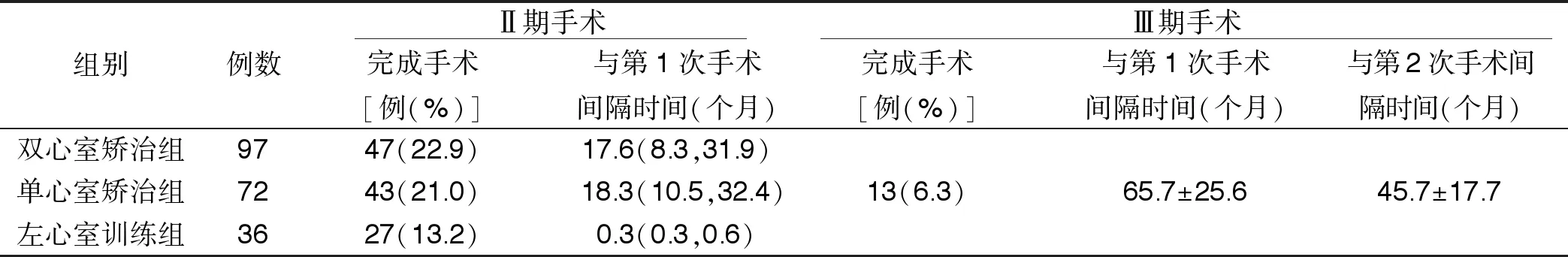
表4 3组Ⅱ期及Ⅲ期手术情况
2.4 随访 PAB术后随访5~63个月,无死亡病例。其中双心室矫治组随访5~43个月,单心室矫治组随访15~53个月,其中1例因需要调整环缩带松紧程度而分别于术后1年和3年再次手术收紧环缩带。左心室训练组随访1~45个月。
3 讨 论
早期PAB术是作为减少肺血流量的姑息手术,后来逐步拓展应用于因年龄、体重限制和/或病情严重暂时不能进行Ⅰ期根治手术;需要分期完成Fontan类手术的肺血流量过多的功能性单心室、远离两大动脉的右室双出口等[3];超过适宜手术年龄拟行大动脉调转术前的左心室功能锻炼的患儿[4-5],为Ⅱ期手术创造条件。
随着小儿心脏外科的进展以及相关科室技术水平的提高,更多的先天性心脏畸形均可以在更小的年龄成功实现双心室矫治[6-7],但是对于一些年龄、体重过小及心内畸形暂不适于解剖矫治的先天性心脏病,如多发性室间隔缺损,非均衡型完全性房室间隔缺损、室间隔缺损位于主动脉瓣下的右心室双出口、病情危重的主动脉弓缩窄以及幼儿临床状态暂不适合体外循环手术的重症患儿,可以选择Ⅰ期行PAB术,以减少肺动脉血流量,保护肺血管床,为Ⅱ期根治提供机会,同时减轻手术风险,保障患儿安全。本研究中97例患儿,因年龄小、体重低、生长发育及营养状况差,均不适于一次行根治手术,故早期先予PAB治疗,手术死亡2例,另有47例Ⅱ期根治,取得了良好的手术效果。
对于肺血多且只能行单心室矫治的先天性心脏病患儿,目前采用的策略是在尽可能小的月龄先施行PAB术,以限制肺血流灌注,为后期再次手术提供更低的肺循环阻力,在6月龄后施行双向Glenn手术,并最终完成Fontan手术。国外文献报道PAB手术患儿年龄为2 d至8个月,最终64%~87%的患儿完成了 Fontan手术治疗[8-9]。本研究中72例患儿PAB手术中位数年龄0.8个月,58%完成双向格林手术,16%最终完成Fontan类手术。完成Ⅱ/Ⅲ期手术率明显低于国外文献报道[10],与患儿接受PAB手术时年龄偏大,导致肺血流限制结果欠满意有关。从这方面来看,对于合并重度肺动脉高压且仅能行单心室修复的患儿,应该尽早行PAB手术。
1977年,Yacoub等[11]提出TGA/IVS患儿采用肺动脉环缩术锻炼左心室功能,进行二期大动脉调转(switch)手术取得成功。对于就诊相对延迟的D-TGA/IVS患儿经PAB训练改善解剖左心室(mLV)功能,提高Ⅱ期动脉转位术成功率也已获得国内外绝大多数学者的认同[10,12-13]。行左心室锻炼的指征是:解剖左心室与解剖右心室的压力比值(mLVp/ mRVp)<0.5,需实施PAB训练;mLVp/ mRVp为0.5~0.6,如年龄>3个月,亦考虑PAB训练。PAB术后,为维持足够的血氧饱和度或者防止动脉导管过早闭合所引起的血氧饱和度下降,往往需要同时进行体肺分流术。本研究中,左心室训练组6例患儿中4例患儿PAB手术同期行体肺分流术,另外2例术中保留动脉导管;术后27例Ⅱ期根治,死亡2例,治疗效果满意。
对于主动脉、肺动脉解剖位置相对正常的患儿,可以经左侧开胸行PAB手术,优点是防止再手术时前纵隔的粘连。而正中胸骨切口的优点是安全,而且在复杂畸形(如内脏异位、心房反位)肺动脉位置发生变异时也很容易显露肺动脉。
环缩带的位置、松紧至关重要,直接影响手术效果。环缩部位既不能太靠近肺动脉分叉处也不能太靠近肺动脉根部。太靠近肺动脉分叉处有可能导致左/右肺动脉起始部折曲狭窄;太靠近肺动脉根部容易造成肺动脉瓣环扩张或者扭曲,引起肺动脉瓣关闭不全。尤其对于二期拟行大动脉调转术的患儿,调转术后会导致主动脉瓣关闭不全。因此,必须保证肺动脉瓣叶功能完好。
PAB术中同步监测心率、血压、动脉血氧饱和度变化10~20 min,以确定血流动力学稳定。在PAB过程中若患儿尚未达到环缩标准就出现动脉血氧饱和度过低,心率过快或变慢,心脏胀满等不耐受表现时,常提示环扎过紧,需及时调整肺动脉环缩程度。如果动脉收缩压力上升5~10 mmHg,心率、SpO2无明显波动,复查动脉血氧饱和度与SpO2基本一致,pH、动脉氧分压(PaO2)、动脉血二氧化碳分压(PaCO2)、剩余碱(BE)、乳酸(LAC)值正常,则环缩满意。肺动脉环缩术后早期如果出现顽固性的低氧血症、低心排血量综合征,要考虑与环缩带过紧导致肺血流量过少、右心室压力负荷过重有关,常常会危及患儿生命,需要急诊手术调整环缩带。另外,环缩带随着患儿的生长环缩程度会相对变得更紧,血氧饱和度和远端肺动脉压力会进一步下降。因此,术后应该定期随访,尽早发现,尽早治疗。本研究中有2例患儿入ICU后SpO2上升至90%以上,超声心动图发现脉压小于40 mmHg,遂再次手术进行环缩。术中环缩带应精细调节至理想的肺动脉压力且不发生不可接受低氧或循环波动,观察20 min,一般此时为最佳环缩周径。目前可调节式肺动脉环缩带开始在临床中应用,可以按需调整松紧程度,有望解决环缩过松过紧问题[14]。本研究有1例拟行单心室修复的患儿远期出现环缩带移位,导致肺动脉扭曲,一侧肺动脉狭窄和一侧肺血过多。因此,保证环缩带的牢固固定至关重要[15]。
有文献报道,PAB术后远期还可能出现球室孔狭窄和心室肌肉肥厚等问题[16],而在部分完全性大动脉转位患儿还可能造成主动脉瓣下的狭窄。本研究中有1例主动脉缩窄合并肌部大型室间隔缺损患儿在PAB术后反复缺氧发作,超声心动图提示右室流出道肌肉肥厚,停用洋地黄药物加β受体阻滞剂后缓解。
一般Ⅱ期手术时机取决于不同的病种。对于双心室修补患儿,如完全性房室间隔缺损、右室双出口等,各个中心经验不同,一般患儿体重在5 kg以上可考虑进行根治;国内有学者建议PAB两次手术间隔时间在6个月以内,避免缺氧加重、流出道梗阻等PAB手术相关并发症[17]。本研究患儿的手术中位数年龄0.5个月,两次手术间隔中位数时间17.6个月,门诊随诊超声心动图检查没有发生缺氧加重、流出道梗阻等相关并发症。对于拟行单心室矫治的患儿,由于肺动脉环缩程度较大,一般在肺动脉环缩术后3个月,月龄满6个月后即行心导管检查,明确肺动脉压力<20 mmHg、阻力低于4 woods/unit,即可以考虑进行双向腔肺分流术[18]。而对于完全性大动脉转位的患儿行肺动脉环缩术者,一般术后10~14 d进行左心室功能超声心动图评价,如室间隔位置凸向右室面和左心室质量指数>50 g/m2等可考虑进行Ⅱ期大动脉调转术[19]。
有文献报道,PAB是一种风险较高的姑息治疗手段,其手术死亡率为5%~20%[20],本研究中住院死亡率为3.4%,低于文献报道。PAB术后再次手术率57.1%,其中双心室修复占22.9%,行左心室锻炼完成大动脉转位调转再次手术率13.2%,而行单心室矫治的患儿完成二次手术(Glenn)的比率占21.0%,完成Fontan占6.3%。说明PAB术在保护肺血管床、实施心室功能训练、完成复杂先天性心脏病的分期矫治方面具有重要作用。
