原发性骨质疏松症发病及诊治的现状和展望
2020-08-07汪纯
汪 纯
(上海交通大学附属第六人民医院骨质疏松和骨病专科 上海市骨疾病临床研究中心,上海 200233)
原发性骨质疏松症是好发于绝经后妇女和老年男性的复杂疾病,患者骨密度下降、骨骼细微结构破坏导致骨骼脆性增加,特征为易发生骨折,其最终表现和最严重的并发症是骨质疏松性骨折。骨质疏松性骨折的定义为轻微外伤(如站立或走平路时跌倒的损伤力度)所导致的桡骨远端、髋部、椎体等部位发生的任何类型骨折,其中尤以髋部骨折危害最大,是导致老年人死亡和致残的主要疾病。患者发生过1次骨质疏松性骨折后,再次发生骨折的风险会明显增加。如初发骨质疏松性骨折的女性患者中有26%会再发骨折,其中23%发生于初次骨折后的第1年,54%发生在初次骨折后5年内。本文介绍目前我国原发性骨质疏松症的诊疗现状并作展望。
原发性骨质疏松症发病的现状和药物作用机制
一、我国原发性骨质疏松症的发病现状
我国是人口大国,目前已进入老龄化社会,近年来骨质疏松症患病人数不断增加,随之而来的骨质疏松性骨折发病率也上升迅猛。北京最新的一项流行病学调查结果显示,2002年至2006年间北京男性、女性髋部骨折的发病率分别为138/10万和243/10万,显著高于1990年至1992年的97/10万和87/10万,其中2002年至2006年间50岁以上男性的髋部骨折发病率为1990年至1992年同年龄段男性的1.61倍,而相应的女性髋部骨折发病率则为1990年至1992年间的2.76倍[1]。2018年10月19日,国家卫生健康委员会发布了首个中国骨质疏松症流行病学调查结果,提示我国50岁以上人群的骨质疏松症患病率为19.2%,其中中老年女性的骨质疏松问题尤为严重,50岁以上女性的骨质疏松症患病率达32.1%,远高于同龄男性(6.0%),65岁以上女性的骨质疏松症患病率更是达到了51.6%。此外,我国男性的骨质疏松症患病率与其他国家间差异不大,但女性的患病率显著高于欧美国家,与日韩等亚洲国家相近。骨质疏松症及其导致的骨折不仅给患者带来严重的健康问题,也给社会、个人造成了巨大的经济负担。因此,如何有效、科学地防治骨质疏松症是当前老龄社会亟待解决的公共健康问题。
二、目前治疗药物的作用机制
尽早确诊骨质疏松症,进行有效的药物治疗,降低骨转换、增加骨密度、改善骨质量,是降低患者骨折风险的关键。根据2017年中华医学会骨质疏松和骨矿盐疾病分会发布的《原发性骨质疏松症诊疗指南(2017)》[2](以下简称“2017年指南”),目前临床上治疗骨质疏松症的药物根据作用机制,主要分为以下四类。①骨吸收抑制剂,包括双膦酸盐、降钙素、选择性雌激素受体调节剂、雌激素和核因子-κB受体活化因子配体(receptor activator of nuclear factor of kappa B ligand,RANKL)抑制剂;②骨形成促进剂,如甲状旁腺激素片段1~34(parathyroid hormone 1-34,PTH1-34),该药物的使用疗程最长为2年;③其他机制类药物,包括活性维生素D及其类似物、维生素K2类和锶盐;④中药,如骨碎补总黄酮制剂、淫羊藿苷类制剂和人工虎骨粉制剂。
临床应根据患者的双能X线吸收法(dual energy X-ray absorptiometry,DXA)检测骨密度结果、既往脆性骨折病史、骨折危险因素的评估和骨转换指标测定结果,制定针对不同患者的合理治疗方案。
原发性骨质疏松症的诊断面临的主要问题
一、原发性骨质疏松症的诊断
原发性骨质疏松症的诊断主要基于2个要点,即DXA骨密度测定结果和(或)脆性骨折发生情况。其中,基于DXA测定骨密度进行诊断是目前公认的诊断标准。临床上常用的DXA骨密度测定部位是中轴骨(腰1至腰4椎体、股骨颈或全髋),或非优势侧的桡骨远端1/3[只适用于髋骨和(或)脊椎的骨密度无法测定或分析时,以及甲状旁腺亢进或过于肥胖超过检查床负荷的患者]。对于绝经后女性、50岁及以上男性则建议参照世界卫生组织(World Health Organization,WHO)推荐的诊断标准进行判断(见表1)。当患者的骨密度降低程度符合骨质疏松症的诊断标准,同时伴有一处或多处骨折时可诊断为严重骨质疏松症。
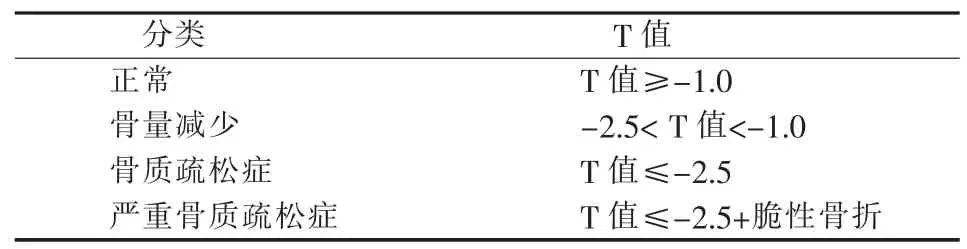
表1 WHO推荐的基于DXA测定骨密度的骨质疏松症诊断标准
基于脆性骨折的诊断,该标准则明确指出,这种骨折是低能量或者非暴力导致的骨折。如果患者的髋部或椎体发生脆性骨折,则可不依赖于骨密度测定,临床直接诊断为骨质疏松症。此外,如果DXA测定骨密度结果显示骨量减少(-2.5 由于目前各地区的卫生资源不平衡,DXA的拥有率在大、中、小城市中存在很大差异。因此,对没有发生过脆性骨折的绝经后妇女及老年男性普遍进行DXA检测骨密度存在很大困难。目前一些社区卫生服务中心和体检中心配置了定量超声进行超声骨密度检测,但定量超声检查的有效部位仅为跟骨,且不能作为诊断标准和判断药物疗效的手段,仅可用于骨质疏松风险人群的筛查和骨质疏松性骨折的风险评估。 此外,2017年指南还推荐将胸椎、腰椎X线侧位影像作为判定骨质疏松性椎体压缩性骨折的首选检查方法。骨质疏松性椎体压缩性骨折最常发生的部位为腰1椎体,之后依次是胸12椎体、胸7至胸9椎体。因此,常规胸椎、腰椎X线侧位摄片范围应分别包括胸4至腰1椎体和胸12至腰5椎体。此项检查有助于发现临床上无症状的脊柱压缩性骨折患者,可将这部分骨质疏松症患者纳入正规的临床诊治和随访。 由于抗骨质疏松药物治疗是一个持久的过程,双膦酸盐的疗程更可长达5~10年[2],因此尽管有充足的循证医学证据,患者长期治疗的依从性仍较差[3],已成为一个全球问题。早在2016年,来自梅奥诊所(Mayo Clinic)的Khosla和Shane教授发表了题为“A crisis in the treatment of osteoporosis”的论文[4]。随后,又有多位专家撰文指出,患者对于药物安全性(特别是双膦酸盐相关下颌骨坏死和非典型股骨骨折)的关注[5],导致患者擅自停药或者减量,从而使髋部骨折发病率增高。因此,需要从患者和卫生专业人员的教育、新药开发以及加大骨质疏松基础研究等多方面出发,才能解决目前骨质疏松症的治疗危机[5-11]。 笔者结合临床实践,总结目前治疗面临的问题(困境)有以下几方面。 根据目前的指南建议,在患者治疗前需进行骨吸收指标和骨形成指标检测,以评估患者的骨转换情况[2]。但骨转换指标(bone turnover markers,BTMs)并不能作为药物选择的依据,且目前也没有其他手段可以指导临床抗骨质疏松药物的选择。 判断抗骨质疏松药物疗效最主要的手段是每年进行1次DXA测定和比对骨密度[2],如骨密度值变化百分比大于等于最小有意义变化,则判定为治疗有效。关于抗骨质疏松药物的疗效评估,目前仍面临监测手段单一、监测周期长的窘境,导致患者的依从性也受到很大影响,部分患者由于短期看不到治疗效果而放弃治疗。 与DXA这一相对静态的指标相比,BTMs在抗骨质疏松药物治疗过程中的变化明显早于骨密度。当患者采用抗骨吸收药物治疗时,其BTMs会快速下降,并于数个月内降至较低平台期[12],且这种BTMs短期下降与后续持久的骨密度变化及骨折风险的下降间存在一定的相关性[13-15]。但一旦进入平台期后,患者的BTMs将基本保持平稳,不会再随着治疗时间的延长而发生显著变化,也无法预示长期治疗的疗效及骨折风险。 双膦酸盐药物最主要的不良反应包括双膦酸盐相关下颌骨坏死和非典型股骨骨折。目前尚没有相关标志物可以判断药物不良反应的高危人群,也没有相关标志物可以起到预警作用。 2017年指南明确指出,骨质疏松症药物治疗的目的是显著提高患者的骨强度,从而降低其发生新发骨折的风险[2]。但目前在治疗过程中尚没有合适的指标可以预示患者的新发骨折风险。临床上对骨质疏松治疗疗效的监测主要依靠DXA测定骨密度,但无论患者选择使用抗骨吸收药物还是促进骨形成的药物治疗,其骨密度变化并非是预测新发骨折风险的灵敏指标,而早期监测骨密度的变化对于预测抗骨吸收药物治疗反应的价值也很有限。多个研究显示,骨密度增加仅能解释双膦酸盐治疗降低新发骨折风险的7%~18%[16]、雷诺昔芬治疗降低新发脊椎骨折风险的4%[17]、特立帕肽治疗降低新发脊椎骨折风险的30%~41%[18],而迪诺塞麦治疗36个月后全髋骨密度变化可解释其降低新发椎体骨折风险的35%和其降低新发非椎体骨折风险的84%[19],因此骨密度变化解释新发骨折风险的下降在不同药物之间存在显著差异,这也表明除骨密度外可能存在更合适的、与新发骨折风险相关的新指标。 双膦酸盐治疗超过5年的获益证据有限,且使用超过5年可能会增加罕见的不良反应(如下颌骨坏死或非典型股骨骨折)的风险[20-21],因此2017年指南建议患者在接受双膦酸盐治疗3~5年后考虑进入药物假期[2];而对于患者应于何时重启治疗,2017年指南没有提出明确建议。目前临床主要是根据患者的骨折风险进行综合判断,如患者为骨折高风险者则需继续治疗。 基于以上问题,临床医师对于抗骨质疏松治疗没有充分信心,而患者的依从性也难以提高。个体化精准医疗对于原发性骨质疏松症患者而言,无法实现。因此,如何着手将骨质疏松症的遗传机制研究、流行病学调查、新药开发以及药物基因组学、蛋白质组学和代谢组学等多组学研究相结合,并将研究成果向临床转化是亟待解决的问题。 近年来,国内多个中心已针对双膦酸盐类药物的疗效与其作用通路以及成骨、破骨细胞功能调控相关的关键基因进行了多项研究,包括药物基因组学研究[22-26]、上海社区的脊柱压缩性骨折流行病学调查[27]、骨质疏松及其骨折易感基因筛查[28-30]、25-羟维生素D水平和BTMs的研究等[31-33],也已获得一定的研究成果。 2019年,在抗骨质疏松治疗新药开发方面也有了新的突破,同时具有抑制骨吸收和促进骨形成双向调节作用的单抗类抗骨质疏松药物romosozumab,在日本和美国先后获得批准上市。该药通过拮抗骨硬化蛋白的活性,从而提高骨密度并降低骨折风险,这为临床治疗骨质疏松症等疾病提供了新思路和新方法[34-35]。 自2009年开始,在上海市医学会骨质疏松专科分会、卫生健康委员会和各级医院的大力支持下,医疗系统开展了社区与三级医院联动转诊新模式的探索,为社区培养了一批专病医师和专职护士的同时,在部分社区开展了骨质疏松专病门诊,初步构建了二、三级医院与社区卫生服务中心的骨质疏松症防治网络和转诊系统,建立了原发性骨质疏松症规范诊治体系,为切实推动骨质疏松防治工作、降低骨折发病率打下坚实基础。二、目前存在的问题
原发性骨质疏松症药物治疗所面临的主要问题
一、缺乏合适的指标指导临床医师选择治疗方案(抗骨吸收药物或促进骨形成药物)
二、缺乏合适的指标在治疗早期监测药物疗效
三、缺乏合适的指标预警药物不良反应
四、缺乏合适的指标预示新发骨折风险
五、缺乏合适的指标作为依据决定患者何时进入“双膦酸盐治疗假期”及何时重启治疗
展望
