离子色谱法同时测定生鲜乳中碘离子、硫氰酸根离子
2020-08-05
(北京市饲料监察所,北京 100107)
碘是具有重要生物效应的微量元素之一,与人体的生长发育、新陈代谢密切相关,是一种多形态的非金属元素。临床发现,碘的缺乏可引起甲状腺疾病[1],对婴幼儿脑损伤有至关重要的影响[2,3]。然而高碘或一次性摄入过量,同样可造成机体的甲状腺功能紊乱,如甲亢、甲状腺功能减退及自身免疫性甲状腺疾病等[1]。同时,碘还是一种常用的消毒剂,具有杀菌速度快、杀菌谱广的特点,常用于奶牛挤奶前牛乳头的清洁消毒。碘制剂消毒乳头后需要用毛巾或一次性纸巾擦拭后方可进行挤乳,但免不了部分碘随之进入生鲜乳中[4]。随着生乳中不断检出碘,碘已经成为了影响生鲜乳质量安全的风险因子。
硫氰酸根离子是参与动物生命活动的一种保护性抗菌因子[5],可抑制生鲜乳中的细菌活动,使其失去繁殖能力,以保证生鲜乳的新鲜度[6,7]。过量的硫氰酸钠会对人体健康造成危害,引发中毒[8],还会妨碍机体对碘的吸收利用,引起甲状腺疾病[9~11]。其主要来源于动物、饲料及人为添加[12]。在2008年,卫生部发布的《食品中可能违法添加的非食用物质和易滥用的食品添加剂品种名单(第一批)》中明确规定,硫氰酸钠属于违法添加的非食用物质。目前已经禁止人为添加到生鲜乳中,但由于生鲜乳中硫氰酸钠存在动物源性本底值,所以相关部门并未对生鲜乳中硫氰酸钠含量进行限值规定。
因此,确定一种能够同时检测生鲜乳中碘离子和硫氰酸根离子的方法,有利于我国生鲜乳质量安全的进一步提升,强化生鲜乳质量安全监管维度,从而为生鲜乳质量安全风险预警、打造优质乳工程提供技术支持和理论基础。
1 材料和方法
1.1 材料与试剂
生鲜乳样品:来自当地养殖场;乙腈:赛默飞世尔科技(中国)有限公司(色谱纯);硫氰酸钠(NaSCN):西格玛奥德里奇贸易有限公司(优级纯);I-单元素标准溶液:国家有色金属及电子材料分析测试中心提供,国家标准样品(GSB04-2834-2011),1000μ g/mL;超纯水:电阻率18.2MΩ·cm,德国默克密理博Milli-Q;OnGuard RP柱:赛默飞世尔科技(中国)有限公司。
1.2 仪器与设备
Dionex ICS-1100 离子色谱仪(Dionex AERS 500型阴离子抑制器、电导检测器、Dionex EGC III KOH 型淋洗液自动发生装置):戴安公司(USA);CF-RN型多用途冷冻离心机:日本HITACHI 公司;VORTEXGENIE2 型漩涡振荡器:美国Scientific Industries 公司;ME204/02 型电子天平:梅特勒-托利多仪器(上海)有限公司。
1.3 方法
1.3.1 SCN-标准储备液
将NaSCN固体于烘箱内烘干2h,准确称取干燥后的NaSCN 0.1397g。用水定容于100mL容量瓶中,浓度为1 000mg/kg,混匀。0~4℃保存,有效期6个月。
1.3.2 I-标准储备液
I-单元素标准溶液,为国家有色金属及电子材料分析测试中心提供的国家标准样品,浓度为1 000mg/L。
1.3.3 I-、SCN-混合标准溶液
分别移取1mL I-、SCN-标准储备液于同一100mL容量瓶中,用纯水定容至刻度线,即浓度为10mg/kg。分别移取上述溶液10、20、50、100、500、1000μL于10mL容量瓶中,定容后得I-、SCN-混合标准溶液,浓度分别为0.01、0.02、0.05、0.10、0.50、1.00mg/kg。
1.3.4 色谱条件
色谱柱:IonPacAS-16型色谱柱(4mm×250mm)和IonPac AG-16型保护柱(4mm×50mm)。抑制器:AERS500,电流149mA。淋洗液:氢氧化钠溶液,浓度为45~60mmol/L,梯度淋洗,淋洗梯度条件见表1。流速1.0mL/min。柱温:30℃。进样量:100μL。
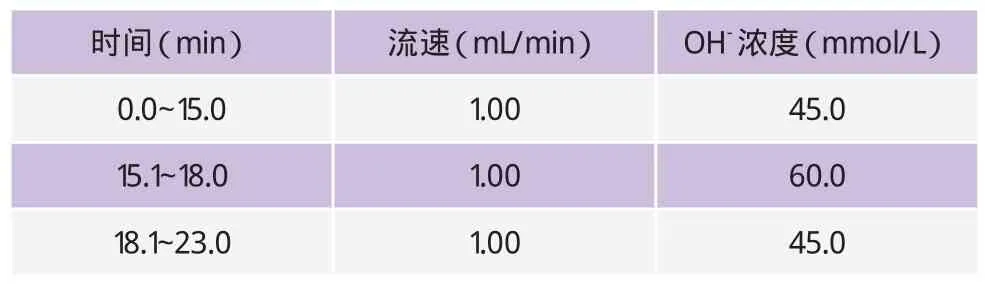
表1 离子色谱氢氧根淋洗液梯度条件
1.3.5 样品前处理
准确称取4g(精确至0.01g)生鲜乳样品,用乙腈定容至10mL,摇匀后静置沉淀蛋白20min,以8 000r/min离心10min,取上清液,稀释10倍并混匀。取上述溶液依次过0.22μm过滤器和OnGuard RP柱后,去掉前3mL溶液后收集溶液用于检测。
2 结果与讨论
2.1 色谱柱的选择
I-和SCN-是易激化和疏水性的阴离子,IonPac AS-16型色谱柱是亲水性较强的高容量柱,具有分离时间短、分离度好、峰形对称等优点,而IonPac AS-11型色谱柱和IonPac AS-19型色谱柱在测定I-和SCN-时出现峰形拖尾严重、干扰峰多现象,检测时间长。所以选择IonPac AS-16型色谱柱(图1)。
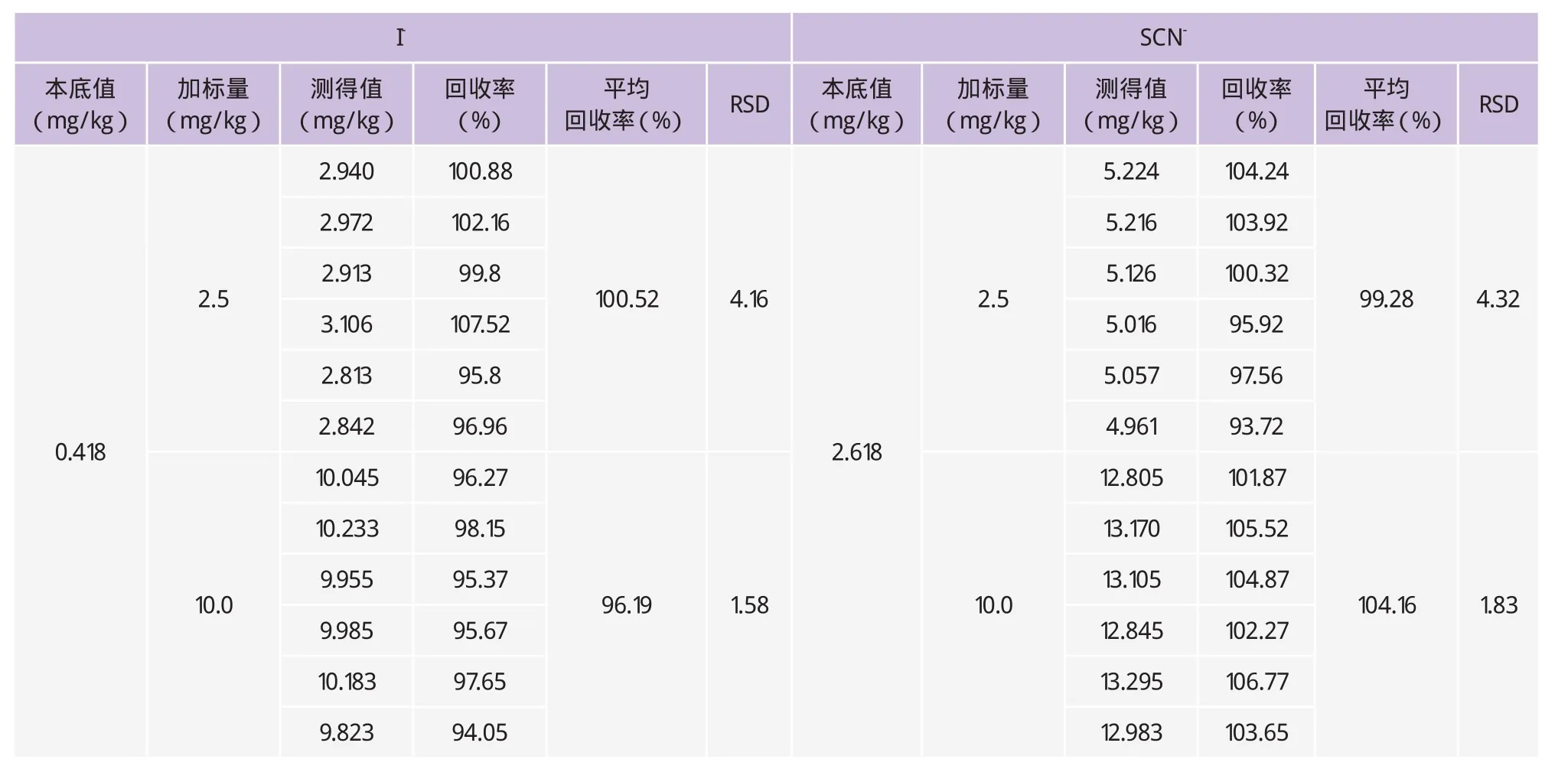
表3 生鲜乳中I-和SCN-的加标回收率
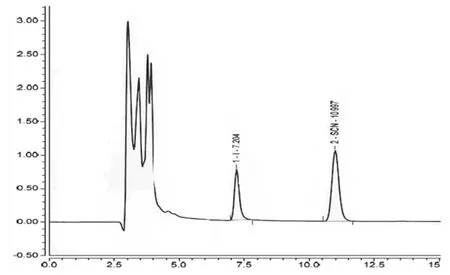
图1 I-和SCN-混合标准溶液上机图谱
2.2 线性范围、相关系数、检出限
对碘离子、硫氰酸根离子6个浓度的标准混合溶液进样,碘离子、硫氰酸根离子浓度在0.01~1mg/kg内与各自峰面积呈线性关系,线性方程分别为Y=0.335X+0.003,r=0.9994和Y=0.688X-0.002,r=0.9995。以信噪比3:1为检测限,碘离子和硫氰酸根离子检测限为0.20mg/kg和0.16mg/kg。
2.3 重复性
取碘离子和硫氰酸根离子混合浓度为0.5mg/kg的混合标准溶液,连续进样6次,其电导检测器测定结果的RSD值分别为1.38%、0.36%,RSD值均小于2.0%。由此可见,利用离子色谱法测定生鲜乳中I-和SCN-含量的精密度较高,所得的检测结果准确性和重复性好。检测结果见表2。
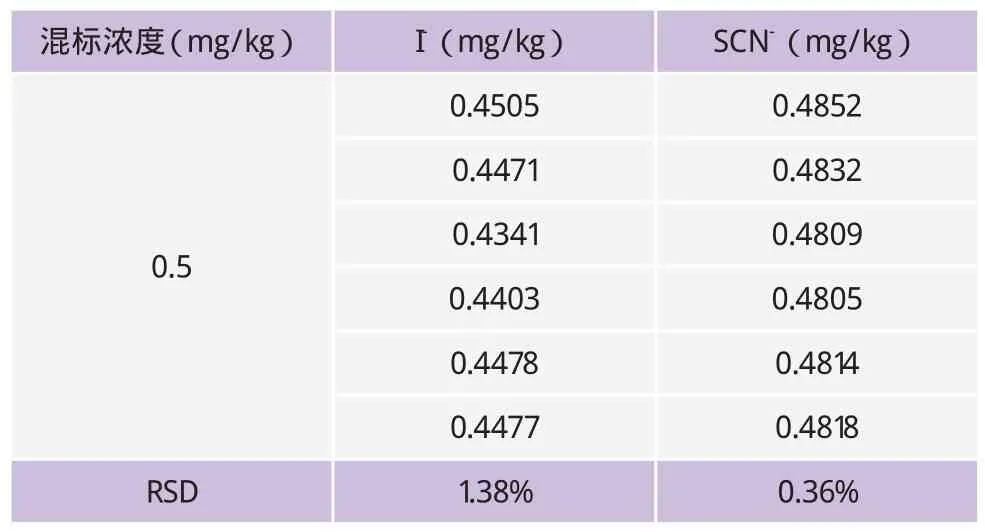
表2 I-和SCN-的重复性
2.4 加标回收率
对生鲜乳中I-和SCN-进行加标回收率的测定,I-和SCN-的添加量分别为2.5mg/kg、10mg/kg,所得加标回收率为96.19%~104.16%(n=6),本方法测定生鲜乳中I-和SCN-含量回收率较高,说明该方法检测结果可靠。测定加标结果见表3。

表4 样品中碘离子和硫氰酸根离子的检测结果(n=2)
2.5 实际样品分析
采集6份生鲜乳样品进行碘和硫氰酸钠检测,检测结果见表4。
由表可见,实际样品中均检测出硫氰酸根离子,但是检测的样品浓度均低于国家食药监总局风险监测参考值10mg/kg,可判定为生鲜乳本底值。样品中碘离子含量最高值为1.24mg/kg,高于在《动物科学杂志》中关于牛奶中碘含量的研究报道,夏季牛奶中的碘含量平均为143μg/kg,冬季牛奶中碘含量平均为183μg/kg,所以为避免生鲜乳中碘离子与硫氰酸根离子非法添加,防范潜在风险,有必要加强监督管理,为此,该方法提供了很好的检测技术支持。
3 结论
该方法通过利用离子色谱柱分离机理,能够同时对生鲜乳中碘离子、硫氰酸根离子进行定量分析,且两种离子分离效果良好,分析方法灵敏度高、准确可靠,为生鲜乳质量安全风险监测提供了良好的技术支持。
