重度呼吸窘迫综合征早产儿撤机后行经鼻同步间歇指令通气临床疗效的分析
2020-08-03吴守业张余转
吴守业 张余转
呼吸窘迫综合征(respiratory distresssyndrome,RDS)是由于肺泡表面活性物质减少所致,是早产儿主要死亡原因之一[1]。目前研究显示,早产儿RDS越来越受到临床儿科医师的关注[2]。临床上,重度RDS必须进行机械通气,但是机械通气的时间过长则可出现各种呼吸道相关并发症,所以将呼吸机辅助通气改为无创通气,成为必然的选择[3]。nCPAP是既往早产儿常用的无创通气方式,但是临床数据显示其具有较高的撤机失败率[4];nSIMV能协调患儿的呼吸频率、增加通气效率,也被临床上应用于重度RDS早产儿的治疗[5],但是有关撤机后行nSIMV失败率的研究并不多见。本文以此为切入点,选取海南省妇幼保健院2015年4月~2017年4月儿科NICU收治的160例重度呼吸窘迫综合征早产儿作为研究对象,探讨nSIMV与nCPAP在重度RDS患儿撤机后的呼吸支持效果、撤机失败率和并发症发生率,旨在为重度RDS早产儿撤机后的治疗提供理论指导。
资料与方法
一、一般资料
选取海南省妇幼保健院2015年4月~2017年4月儿科NICU收治的160例重度呼吸窘迫综合征早产儿作为研究对象,按照撤机后的呼吸支持方式分为nSIMV组和nCPAP组,各80例。nSIMV组中,男46例,女34例,胎龄31~34周,平均胎龄(32.55±1.43)周,出生体重1815~2113 g,平均体重(1973.62±128.63)g;nCPAP组中,男41例,女39例,胎龄31~34周,平均胎龄(32.68±1.52)周,出生体重1801~2155g,平均体重(1979.62±130.75)g。两组早产儿基线资料(性别、胎龄、出生体重、有创通气时间、剖宫产率、产前使用激素情况、Apgar评分[6]及呼吸窘迫情况等)差异不大(P>0.05),具有可比性(见表1)。本研究经患儿父母知情并签字,经本医院伦理委员会批准并通过。

表1 两组早产儿基线资料的比较[n(%)或
二、纳入与排除标准
纳入标准:⑴符合重度呼吸窘迫综合征的诊断标准[7];⑵胎龄不足36周;⑶机械通气超过24 h。排除标准:⑴出生后先天畸形;⑵出生后重要脏器功能不全;⑶重度贫血、感染等。
三、方法
1 有创通气:所有入选早产儿给予肺表面活性剂(100 mg/kg,气管插管内滴入),通气模式采用SIMV或A/C,以血气分析为依据调整呼吸机参数。撤机指标如下:吸气峰压(Peak Inspiratory Pressure,PIP)<18 cmH2O,呼气末正压(positive end-expiratory preassure,PEEP)<3 cmH2O,吸入氧浓度(Fraction of inspiration O2,FiO2)<0.4,动脉血氧饱和度(arterial oxygen saturation,SaO2)>88%,呼吸频率<20次/min且呼吸平稳,无三凹征。拔气管插管后,分别给予nCPAP或nSIMV。
2 nCPAP:采用STEPHAN CPAP B Plus持续正压通气系统。初始参数为:CPAP为4~6 cmH2O,Flow为4~8 L/min,FiO2为0.2~0.5。当CPAP降至2~3 cmH2O、FiO2<0.4的时候,可停止nCPAP。
3 nSIMV:采用STEPHAN Christina型小儿呼吸机。初始参数为:PIP 15~20 cmH2O,PEEP 4~6 cmH2O,FiO20.20~0.50,呼吸频率25~30次/min。当PEEP<3 cmH2O、FiO2<0.4的时候,可停止nSIMV。
4 撤机失败标准[8]:撤机后72 h内SaO2不能达到88~92%;24 h内呼吸暂停超过4次;血气分析显示pH<7.20、氧分压(PaO2) <50 mmHg、二氧化碳分压(PaCO2)>60 mmH2O。
四、观察指标
1 血气分析:对比两组早产儿行机械通气之前以及nSIMV和nCPAP之后4 h的主要血气指标如pH、PaO2、PaCO2、SaO2和氧合指数(OI)。
2 撤机失败率:按照撤机失败标准记录并计算失败率,失败率=撤机失败例数/该组早产儿总数×100%。
3 并发症发生率:主要并发症有腹胀、营养喂养不耐受、脑室内出血、支气管发育不良、视网膜病变以及坏死性肠炎等[9]。比较两组早产儿各种并发症发生率。
五、统计学分析

结 果
一、比较两组早产儿行机械通气之前和之后4 h的主要血气指标
结果显示,两组早产儿在行机械通气之前各项血气指标均无统计学意义(P>0.05);治疗结束4 h后,两组早产儿各项血气指标均发生变化,pH、PaO2、SaO2和OI均较之前升高(均P<0.05),PaCO2均较之前下降(P<0.05),差异具有统计学意义;但是nSIMV组较nCPAP组变化更加显著(P<0.05),差异具有统计学意义(见表2)。

表2 两组早产儿行机械通气之前和之后4 h主要血气指标的比较
二、比较两组早产儿的撤机失败率
结果显示,nCPAP组撤机失败25例(31.25%),分别为低氧血症6例,高碳酸血症11例,呼吸暂停8例;nSIMV组撤机失败7例(8.75%),分别为低氧血症2例,高碳酸血症3例,呼吸暂停2例;nCPAP组早产儿的撤机失败率明显高于nSIMV组,差异有统计学意义(P<0.05)(见表3)。
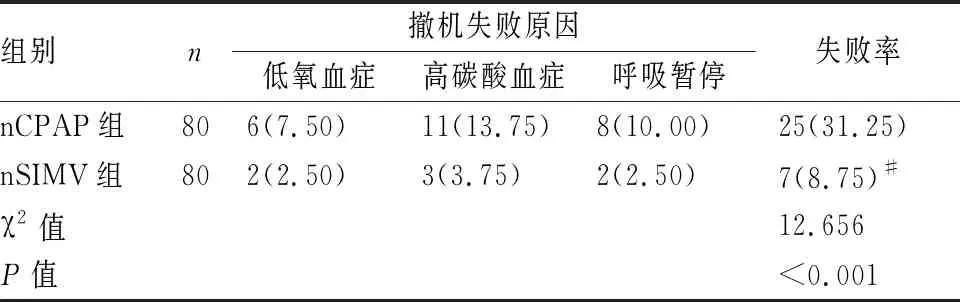
表3 两组早产儿撤机失败率的比较[n(%)]
三、比较两组早产儿各种并发症发生率
结果显示,nSIMV组早产儿腹胀的发生率明显低于nCPAP组,具有统计学意义(P<0.05);其他并发症发生率在两组间差异不大,无统计学意义(P>0.05)(见表4)。

表4 两组早产儿各种并发症发生率的比较[n(%)]
讨 论
临床上除产前使用激素以及出生后应用肺表面活性物质外,以机械通气来改善通气、促进氧合是重要的治疗手段,但常规气管插管存在多种并发症(呼吸机相关性肺炎、肺损伤、肺出血及支气管发育不良等)[10-11],所以,减少常规机械通气的时间、预防再次上机显得格外重要。
既往在机械通气达到撤机标准后大多使用nCPAP进行过渡,对于可以自主呼吸的患儿,nCPAP可以提高功能残气量、预防肺泡萎陷、防止呼吸暂停[12],然而,临床上还是有约30%的患儿因为频发呼吸暂停或低氧血症及高碳酸血症,再次插管机械通气[13]。nSIMV具备某种频率的同步间歇正压,在患儿自主呼吸的同时触动呼吸机的同步正压通气,让自主呼吸与呼吸机相结合,提高了通气量和通气效率[14]。此外,nSIMV以非侵入方式提供稳定压力、以同步正压通气减少气道阻力,既维持了通气效果也减少了通气相关并发症;对于可能存在严重呼吸暂停的患儿,使用nSIMV可通过设定某种呼吸频率给予通气支持;同步正压通气还提供了稳定的PIP和PEEP,有效地扩张了小气道、预防了肺泡萎缩、减少了呼吸做过、提高了呼吸效率[15]。有学者对比nSIMV和nCPAP后发现,nSIMV能明显减少早产儿的呼吸暂停发生率,减少低氧血症和高碳酸血症,提高疗效[16]。
本文显示,采用无创通气后,nSIMV组与nCPAP组早产儿的血气指标都有改善,表明无论哪种支持方式均可以改善通气效果;但是治疗4 h以后,nSIMV组的改善状况明显优于nCPAP组,pH、PaO2、SaO2和OI均高于nCPAP组(均P<0.05),PaCO2低于nCPAP组(P<0.05),证实了nSIMV改善通气的效果优于nCPAP,与前文分析一致。
本研究发现,nSIMV组的撤机失败率低于nCPAP组(P<0.05),失败原因显示低氧血症、高碳酸血症和呼吸暂停在nCPAP组中更高,可能与nSIMV通过扩张气道降低了气道阻力、协同了呼吸频率、改善了通气效果有关,从而最终改善了缺氧和CO2潴留、减少了呼吸性酸中毒以及呼吸暂停的发生[17]。
关于并发症,本研究只发现nSIMV组早产儿的腹胀发生率较nCPAP组低(P<0.05),其他并发症于两组早产儿之间差异不明显,说明nSIMV和nCPAP的安全性均较好,但总体而言,nSIMV的安全性更好。
综上所述,重度RDS早产儿撤机后给予nSIMV能改善通气效率,维持了血气指标稳定,减少了撤机失败率,进一步减低了相关发生率,值得临床推广。
