离子液体N-丙基-吡啶二氰胺盐[C3py][DCA] 水溶液的体积和表面性质
2020-07-31邢楠楠王莉雨刘可峰牛凯旋
*邢楠楠,王莉雨,余 意,姚 健,刘可峰,牛凯旋
(黄山学院化学化工学院,安徽,黄山 245041)
随着世界各国对环境保护的日益重视,绿色化学已成为化学发展的必然趋势。与传统的有机溶剂相比,离子液体具备很多传统有机溶剂不具备的优点,如热稳定性好、蒸气压几乎为零、熔点低、液程宽、催化性能好、溶解性能强、具有可设计性、对许多有机物和无机盐有特殊溶解性等特点[1-3]。目前正在被成功应用于催化[4-5]、生物[6]、萃取[7]、药物化学[8-9]和二氧化碳捕捉[10]等多个领域。离子液体凭借独特性能已被各国研究者公认为是最理想的绿色溶剂,近年来,越来越多的学术团体开展了离子液体二元体系的研究。通过不同离子液体和不同溶剂的组合可以提供无限多数量的、性质连续变化的反应介质,为实际的特殊需要提供精细的选择,既是对离子液体可设计性的有效补充,而且还提高了离子液体的应用范围。离子液体由于阴阳离子各异,数量及其庞大,若仅通过实验合成并测定其物性,又耗时又耗力,而且成本非常高,所以需要有效而可靠的方法对含离子液体的体系进行热力学性质的估算。
在前期研究离子液体水溶液的基础上[11-13],我们研究了离子液体[C3py][DCA]水溶液的物化性质,为离子液体今后能更好的应用提供了理论依据。本研究做了如下的工作:1) 在T= (288.15~318.15) K温度范围内间隔5K测定[C3py][DCA]水溶液的密度和表面张力。2)根据密度值,求出[C3py][DCA]水溶液的平均摩尔体积和热膨胀系数。3)提出估算[C3py][DCA]水溶液表面张力的经验方程。
1 实验部分
1.1 试剂和仪器
[C3py][DCA](此样品同于前期工作所用的离子液体[C3py][DCA][13])、去离子水(电导率小于 1.0/ μS·cm-1)、FA2104N电子分析天平(上海民桥精密科学仪器有限公司)、CL-1A型磁力搅拌器(巩义市予华仪器有限责任公司),奥地利AntonPaar公司生产的DMA4500型振动管数字密度计,DP-AW型表面张力计(南京桑力电子设备厂生产),GDH-2008W型超级恒温水浴(上海比朗仪器有限公司)。
1.2 [C3py][DCA]水溶液密度和表面张力的测定
用电子分析天平使用重量法配制质量浓度m=(0.0135~0.4447)mol·kg-1范围内一系列离子液体[C3py][DCA]水溶液样品,每个样品新鲜配制,然后用搅拌器搅拌均匀,待用。在T= (288.15~318.15)K温度范围内间隔5K使用DMA4500型振动管数字密度计测定上述样品的密度。样品测量前,密度计需要用干燥的空气和去离子水对仪器进行校正。利用最大气泡法使用DP-AW型表面张力计测定上述样品的表的面张力,用超级恒温水浴控制测量温度。表面张力使用前需要用去离子水对其进行校正。
2 结果与讨论
2.1 [C3py][DCA]水溶液的密度和表面张力
样品测定后的密度和表面张力值分别列入表1和表2 中,表中的每一个值都是三次测量的平均值。由表1 和表2 可以看出,离子液体水溶液的密度随着温度的升高而降低,随着质量浓度的增加而增大;离子液体水溶液的表面张力随着温度的升高而降低,随着质量浓度的增加而减小。
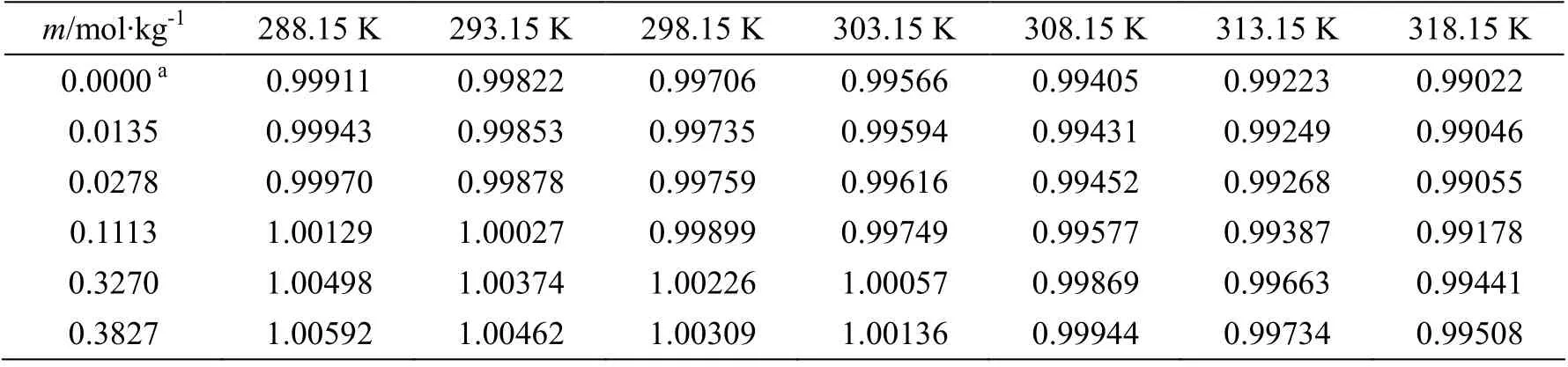
表1 在T =(288.15~318.15)K温度范围内[C3py][DCA]水溶液的密度(ρ /g·cm−3) Table 1 Values of density for aqueous [C3py][DCA] with various molalities at T =(288.15~318.15)K

表2 在T =(288.15~318.15)K温度范围内[C3py][DCA]水溶液的表面张力(γ/ mJ·m-2) Table 2 Values of surface tension, for aqueous [C3py][DCA] with various molalities at T =(288.15~318.15)K
根据测得的密度数据可计算[C3py][DCA]水溶液的平均摩尔体积:

其中,M代表摩尔质量,x代表摩尔分数,角标1 和2 分别代表溶质和溶剂。[C3py][DCA]水溶液的平均摩尔体积列于表3 中。从表3 可以看出体积随着温度和质量浓度升高而明显增大。
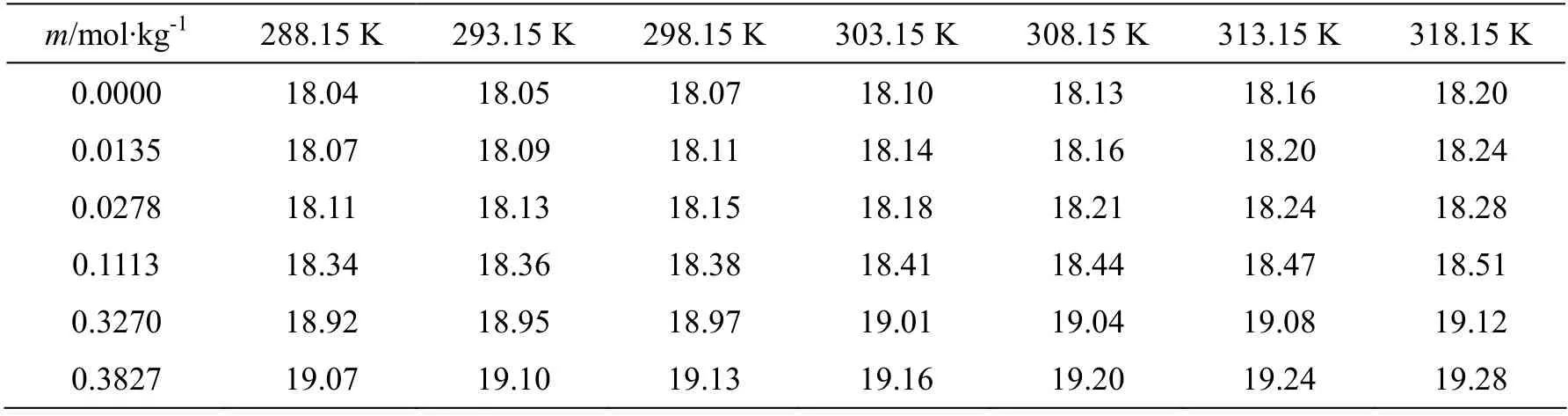
表3 在T =(288.15-318.15)K温度范围内[C3py][DCA]水溶液的平均摩尔体积(V/cm3·mol-1) Table 3 The values of the average molar volume for aqueous solutions of [C3py][DCA] with various molalities at T=(288.15~318.15)K
2.2 [C3py][DCA]水溶液的热膨胀系数
[C3py][DCA]水溶液的密度ρ与温度T的关系可用下面的经验方程表示:

其中Bi是经验参数。根据方程(2)用ρ对(T-298.15)拟合,将拟合得到的参数Bi值、相关系数平方r2和标准偏差sd都列入表4 中。另外,把用水的文献密度值[14]对(T-298.15)拟合得到的Ai值也列入了表4。根据热膨胀系数α的定义[15]:

其中下角标p和m分别为压力和质量浓度。借助方程(2)可得到计算α的方程:


表4 [C3py][DCA]水溶液的密度ρ 对(T-298.15)拟合得到的各参数值 Table 4 The parameters values of the fitting for the densities and (T-298.15)
按照方程(4)计算得到不同温度下各个浓度的[C3py][DCA]水溶液热膨胀系数α,并列入表5中,从表中可以看出,热膨胀系数随着温度的升高而增加。
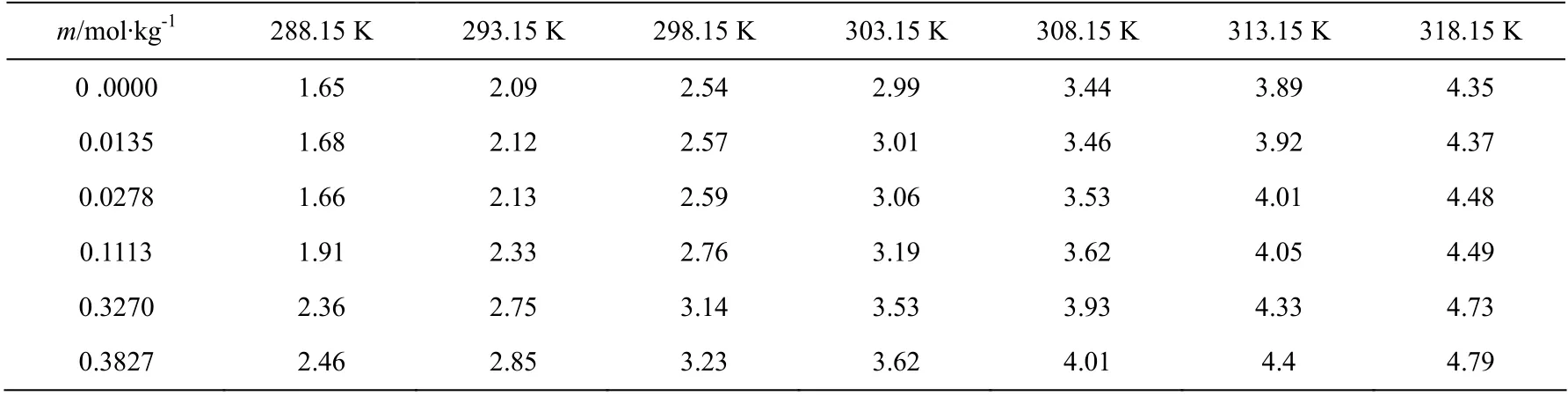
表5 [C3py][DCA]水溶液的热膨胀系数(104α/K-1) Table 5 Values of the thermal expansion coefficient of aqueous [C3py][DCA]
2.3 [C3py][DCA]水溶液的表面张力与浓度和温度的关系
从表2 中数据可以看出,在固定温度下,[C3py][DCA]离子液体水溶液的表面张力γ随溶液的浓度m呈线性变化,可用下面的经验方程表示:

其中Ci是经验参数。用γ对m作图,可得到一组很好的直线,相关系数平方r2都在0.99 以上。将γ对m线性拟合得到的参数值列入表6 中。

表6 根据经验方程(5)拟合得到的参数值Ci,相关系数平方r 2和标准偏差sd Table 6 The values of Ci in equation (5) with standard deviation, sd, and the correlation coefficient square, C, for the mixtures of aqueous [C3py][DCA]
从表6 中数据可以看出,C0随T呈线性变化,而C1基本不随T变化,可用下面的经验方程表示:

将方程(6)和(7)代入方程(5)中,得到了预测[C3py][DCA]离子液体水溶液表面张力的工作方程:

通过工作方程拟合可以得到q0=71.74,q1= - 0.15,q2= - 12.39,r2= 0.9994,sd=0.05。将利用工作方程估算的[C3py][DCA]离子液体水溶液的表面张力γest列入表7 中。
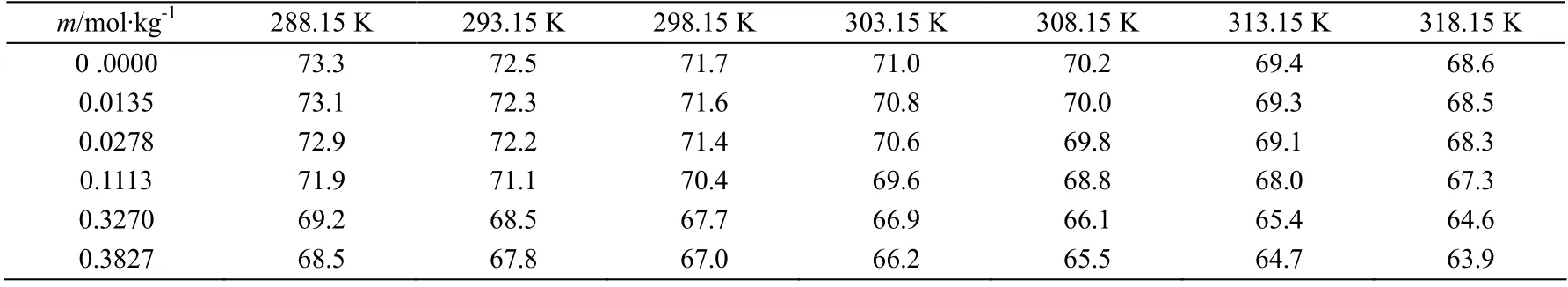
表7 在T =(288.15~318.15)K温度范围内[C3py][DCA]水溶液的表面张力估算值(γest/ mJ·m-2) Table 7 Values of surface tension for aqueous [C3py][DCA] with various molalities at T =(288.15~318.15)K
用表面张力估算值γest对表2 中实验值γ作图(见图1),得到一条很好的直线,其斜率接近1,截距接近零,r2=0.9999。说明表面张力的估算值和实验值高度相关并十分相似。
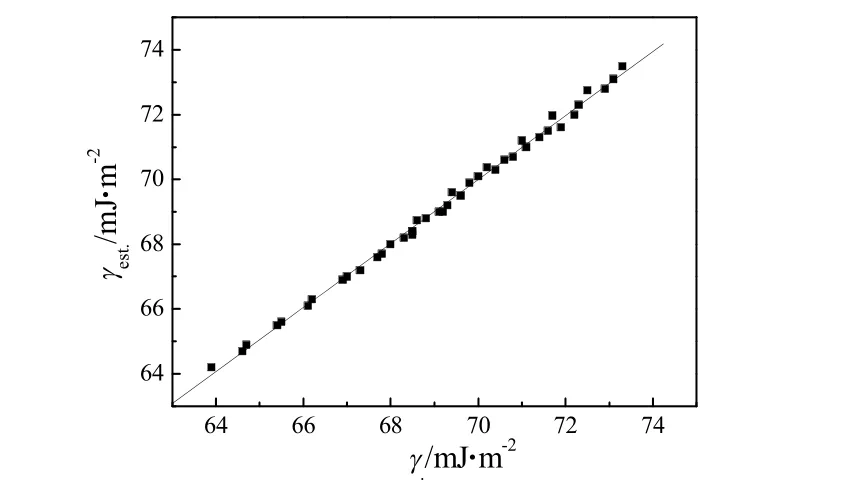
图1 [C3py][DCA]离子液体水溶液估算的表面张力值γ(est.)对相应的实验值γ 作图 Fig. 1 Plot of γest. vs. γ obtained from experiments for aqueous [C3py][DCA] γest. = 0.8194 + 0.9882 γ, r2=0.9999, sd =0.14.
3 小结
在T= (288.15~318.15) K 温度范围内,每隔5 K 测定了质量摩尔浓度0.01~0.04 mol·kg-1的离子液体[C3py][DCA]水溶液的密度和表面张力。计算了不同浓度不同温度下[C3py][DCA]水溶液的平均摩尔体积和热膨胀系数。水溶液平均摩尔体积随着温度和质量浓度的升高而增大。热膨胀系数随着温度的升高而增大。本研究提出了一种估算水溶液表面张力的经验方程,预测值与实验值具有较好的一致性。
