罗丹明6G 与罗丹明6G 酰肼测汞的对比研究
2020-07-31盛新凤董彦杰
盛新凤,董彦杰
(1.安庆师范大学化学化工学院,安徽,安庆 246001;2.安徽省功能配合物重点实验室,安徽,安庆 246001)
汞离子(Hg2+)是一种常见的重金属,也是最具毒性的重金属之一,任何形式的汞对人体都有毒害作用。它主要来源于以下几个方面:工业排放的“三废”中;空气中的汞蒸气以及被空气氧化而溶于水的Hg2+;而水中的Hg2+会沉积到土壤或地下中,当被动植物吸收后就会转化成甲基汞,随着这些动植物在食物链中循环,甲基汞也会随食物链的循环而不断传递下去,危害人类的健康[1]。因此对定量检测Hg2+方法的研究是很重要的研究课题。目前对金属离子的具体测定方法有原子荧光光谱法(AFS)[2]、紫外可见分光光度法(UV)[3]、原子吸收光谱(AAS)[4]、电化学法[5]、X 荧光光谱法(XRF)[6]、荧光分析法[7-8]、磷光分析法[9]和光度法[10]。其中因为荧光分析法的灵敏度高、选择性强和使用简便的优点而被广泛使用[11-14]。而以罗丹明为母核的酰胺螺环结构具有“敞开-闭合”的特点,当加入某种金属离子时会让酰胺螺环结构打开,从而使化合物本身的荧光增强或猝灭,以达到检测金属离子的目的。罗丹明6G 酰肼是罗丹明类化合物最重要的中间体,但是尚未报道罗丹明6G 和罗丹明6G 酰肼的对比研究。本研究将围绕罗丹明6G与罗丹明6G 酰肼在测Hg2+条件和检出限等方面进行对比研究。
1 实验
1.1 仪器
LKTC-C 型DF-101S 集热式磁力加热搅拌器(金坛市白塔新宝仪器厂);SH3PA00004 型超纯水机(默克密理博实验室设备有限公司,上海);SHB-3型循环水式多用真空泵(郑州长城科工贸有限公司);Hitachi F-4500 型荧光光谱仪(日本Hitachi公司);PHSJ-3F 型pH 计(上海精密仪器仪表有限公司)。
1.2 试剂
罗丹明6G(R6G)、水合肼、乙醇;THF、36%醋酸溶液、NaAc、Na2HPO4·12H2O、NaH2PO4·2H2O、HCl、六次甲基四胺(C6H12N4)及实验中所用的无机盐均来自上海阿拉丁试剂有限公司,试剂均为AR 级。整个实验过程使用的纯净水来自SH3PA00004 型超纯水机。
1.3 分析方法
取一定量1.0×10-3mol/L R6G 或R6GH 或溶液,2.00 mL 缓冲溶液(磷酸缓冲溶液、醋酸缓冲溶液和六次甲基四胺缓冲溶液)和一定量1.0×10-4mol/L金属盐溶液,放入10 mL 容量瓶,用去离子水稀释到刻度,摇匀。并用Hitachi F-4500 型荧光光谱仪测定其荧光强度。
2 结果与讨论
2.1 罗丹明6G 酰肼的合成
根据参考文献[11]合成罗丹明6G 酰肼,合成路线见图1。
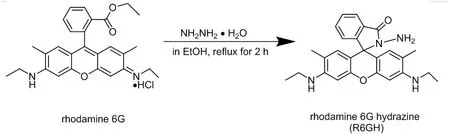
图1 R6GH 的合成路线 Fig. 1 Synthesis route of R6GH
2.2 荧光试剂、缓冲溶液和金属离子溶液的配置
称取R6G(95%)12.6053 g,用水溶解后再转移至250 mL 容量瓶中,加水稀释至刻度线,摇匀,配置成0.1000 mol/L 的溶液。
称取R6GH 4.2822 g,用THF 和水混合溶液(V:V=1:1)溶解后再转移至100 mL 容量瓶中,加混合溶液稀释至刻度线,摇匀,配置成0.1000 mol/L的溶液。
称取NaH2PO4·2H2O 1.9501 g,Na2HPO4·12H2O 4.4768 g,用水溶解后再转移至250 mL 容量瓶中,加水稀释至刻度线,摇匀,配置成0.10 mol/L 的磷酸缓冲溶液体系。
称取质量分数为36%的HAc 2.0850 g,NaAc 1.03775 g,用去离水溶解后再转移至250 mL 容量瓶中,加水稀释至刻度线,摇匀,配置成0.10 mol/L的醋酸缓冲溶液体系。
称取质量分数为37%的HCl 1.2318 g,C6H12N41.7700 g,用去离子水溶解后再转移至250 mL 容量瓶中,加水稀释至刻度线,摇匀,配置成0.10 mol/L的盐酸缓冲溶液体系。
各种金属盐溶液均依照上述方法配置成1.0 mol/L,实验时根据需要再稀释至所需浓度。
2.3 金属离子和缓冲溶液体系的选择
为了考察R6G 和R6GH 选择性识别金属离子的性能,我们按分析方法配制好溶液,在激发波长(ExR6G=527 nm,ExR6GH=524 nm)下用F-4500 型荧光光谱仪测定。R6G 磷酸缓冲溶液体系的实验结果见图2a,R6G 醋酸缓冲溶液体系的实验结果见图2b,R6G 六次甲基四胺缓冲溶液体系的实验结果见图2c;R6GH 磷酸缓冲溶液体系的实验结果见图3a,R6GH 醋酸缓冲溶液体系的实验结果见图3b,R6GH 六次甲基四胺缓冲溶液体系的实 验结果见图3c。

图2 R6G对金属离子的选择性识别 Fig.2 Selective recognition of metal ions by R6G

图3 R6GH 对金属离子的选择性识别 Fig.3 Selective recognition of metal ions by R6GH
从图2(a、b、c)中可以看出R6G 对金属离子的识别能力不佳,但在醋酸缓冲溶液中荧光效果最好。从图3(a、b、c)中可以看出R6GH 对Hg2+的识别最好,且在醋酸缓冲溶液体系中R6GH 的荧光效果最佳。
2.4 HAc/NaAc 缓冲溶液pH 对测Hg2+的影响
为了考察醋酸缓冲溶液体系pH 对R6G 和R6GH 检测Hg2+的影响,在分析方法中,使用不同pH 的0.1mol/L 醋酸缓冲溶液体系配制好待测溶液,测定其溶液的荧光强度,结果见图4(a、b)。
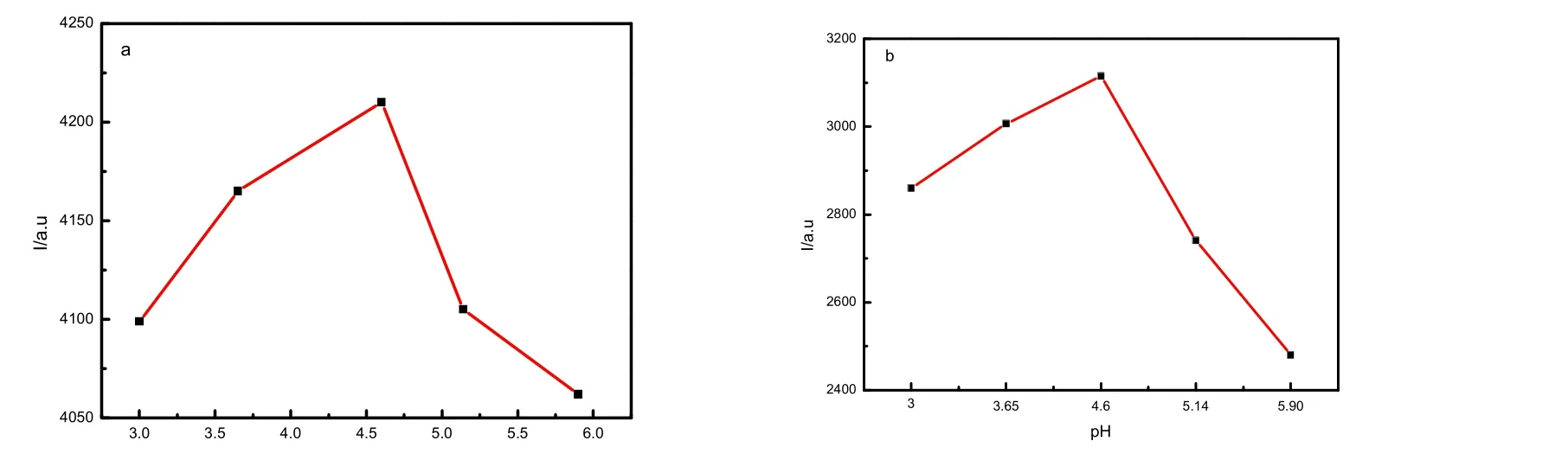
图4 HAc/NaAc 缓冲溶液pH 对测Hg2+的影响 Fig.4 Effect of pH of HAc/NaAc buffer solution on Hg2+ measurement
由图4(a、b)可以看出,R6G/Hg2+溶液和R6GH/Hg2+溶液均在醋酸缓冲溶液体系(pH=4.60)时荧光最强,故在后续实验中,R6G 和R6GH 检测Hg2+,选定醋酸缓冲体系(pH = 4.60)。
2.5 HAc/NaAc 缓冲溶液的浓度对测Hg2+的影响
为了考察缓冲溶液浓度对测定Hg2+的影响,固定醋酸缓冲溶液体系的pH 为4.60,改变醋酸缓冲溶液的浓度,配制总浓度为0.001、0.005、0.01、0.05、0.1 mol/L 这五种醋酸缓冲溶液体系,按分析方法配制待测溶液。实验结果见图5(a、b)。
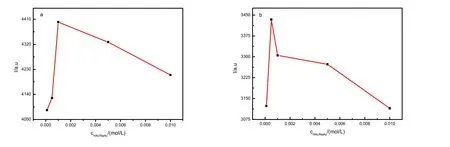
图5 HAc/NaAc 缓冲溶液的浓度对测Hg2+的影响 Fig.5 Influence of HAc/NaAc buffer solution concentration on Hg2+ measurement
通过图5(a、b)可知,R6G 在醋酸缓冲溶液体系总浓度为0.01mol/L 检测Hg2+效果最佳,而R6GH 则在醋酸缓冲溶液体系总浓度为0.005 mol/L时检测Hg2+的效果最佳。
2.6 荧光试剂的浓度对测Hg2+的影响
为了考察R6G 和R6GH 浓度对测定Hg2+的影响,配制1.0×10-5、2.0×10-5、4.0×10-5、6.0×10-5、8.0×10-5、1.0×10-4mol/L 六个浓度的R6G 和R6GH 溶液,按分析方法配置待测溶液,实验结果见图6(a、b)。

图6 荧光试剂的浓度对测Hg2+的影响 Fig.6 Influence of R6G and R6GH concentration on Hg2+ measurement
从图6(a、b)可以看出,随着R6G、R6GH溶液浓度的增加,荧光强度也增加,为了保证实验的顺利进行,后续实验中R6G、R6GH 的浓度选定为1.0×10-4mol/L。
2.7 测Hg2+检测范围、回归方程和检测限
在最佳条件下,Hg2+的浓度(0.1~1.0×10-5mol/L)范围内,R6G 测定Hg2+的线性回归方程为:lg(I/I0) = 0.0503-0.00974lgc(Hg2+),相关系数R2= -0.9951,检测限为6.0×10-6mol/L(11 次),实验结果见图7a;在最佳条件,Hg2+的浓度(1.0×10-5~1.0×10-11mol/L)范围内,R6GH 测定Hg2+的的线性回归方程为lg(I/I0) = 0.0474+0.009387lgc(Hg2+),相关系数R2= 0.9993,检测限为5.0×10-12mol/L(11 次),实验结果见图7b。
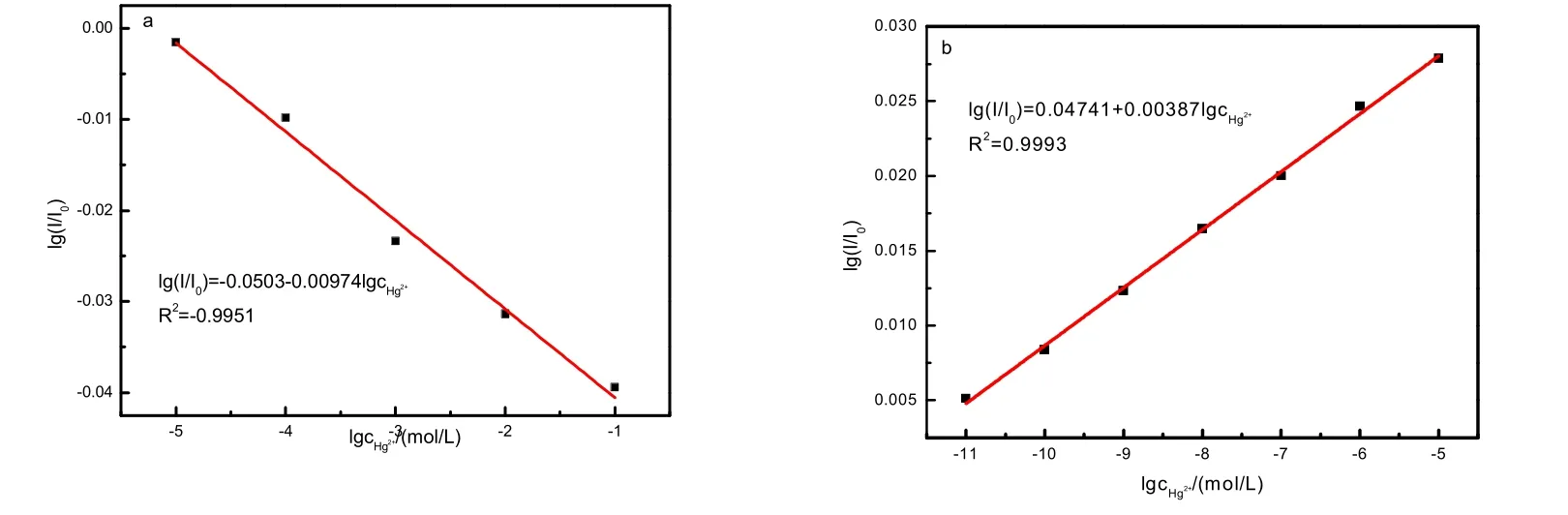
图7 R6G 和R6GH 测Hg2+回归分析 Fig. 7 Regression analysis of Hg2+ measured by R6G and R6GH
图7a 可见,当Hg2+浓度从1.0×10-5mol/L 升高至0.1mol/L 时,Hg2+对R6G 溶液的荧光有猝灭作用。图7b 可见当Hg2+浓度从1.0×10-5mol/L 降至1.0×10-11mol/L 时,R6GH 的荧光强度也逐渐线性降低。由图7a 和图7b 比较可知,R6GH 检测Hg2+线性范围要比R6G的要大,且检出限要高6个数量级。
2.8 常见金属离子的干扰
为了考察常见阳离子对R6G、R6GH 检测Hg2+的干扰,在最佳条件下,±5%荧光强度范围内,R6G/Hg2+体系测定结果为:Na+(550),K+(500),Cr3+(175),Ni2+(50),Fe2+(13),Zn2+(10),Mg2+(5),Ba2+(5),Pb2+(5),Ca2+(5),Cd2+(5),Al3+(5),Co2+(3),Ag+(3)。R6GH/Hg2+体系测定结果为:K+(500),Na+(500),Ag+(175),Co2+(150),Ni2+(90),Cd2+(50),Ba2+(40),Zn2+(25),Cr3+(25),Ca2+(15),Mg2+(10),Al3+(5),Fe2+(5),Pb2+(5)。括号中的数值为干扰离子与待测离子的浓度比。通过14 种阳离子的干扰实验发现,阳离子对R6G 测定Hg2+的影响大于对R6GH 测定Hg2+的影响。
3 小结
以R6G 为原料合成了R6GH,利用荧光法考察了R6G 和R6GH 酰肼选择性识别金属离子、适合的缓冲溶液体系、最佳缓冲溶液pH 及浓度、R6G和R6GH 的浓度、Hg2+的浓度以及阳离子的干扰等七个因素的影响。实验确定了R6G 测定Hg2+的最佳条件为:R6G 浓度为1.0×10-4mol/L,0.01mol/L醋酸缓冲体系(pH=4.60);R6G 测定Hg2+的线性回归方程为:lg(I/I0) = 0.0503-0.00974lgc(Hg2+),相关系数R2= -0.9951,检测限为6.0×10-6mol/L(11 次)。R6GH 测定Hg2+的最佳条件为:R6GH 浓度为1.0×10-4mol/L,0.005mol/L 醋酸缓冲体系(pH = 4.60);R6GH 测定Hg2+的线性回归方程为:lg(I/I0) = 0.0474+0.009387lgc(Hg2+),相关系数R2=0.9993,检测限为5.0×10-12mol/L(11 次)。通过14 种阳离子的干扰实验发现,阳离子对R6G 测定Hg2+的影响大于对R6GH 测定Hg2+的影响。实验结果表明:R6GH 比R6G 能更好的识别Hg2+。
