中国骨肿瘤大手术静脉血栓栓塞症防治专家共识
2020-07-29中华医学会骨科学分会骨肿瘤学组
中华医学会骨科学分会骨肿瘤学组
韩秀鑫1 初同伟2△ 董扬3△ 郭世炳4△ 郭卫5△ 郭征6△ 郝永强7△ 胡勇8△ 胡永成9△ 黄纲10△李浩淼11△ 李亚平12△ 刘勇13△ 陆俭14△ 吕智15△ 孙保胜16△ 汤小东5△ 同志超17△ 屠重棋18△王晋19△ 吴玉仙20△ 杨彩虹21△ 张春林22△ 张晓晶23△ 张伟滨24△ 郑伟25△ 周勇26△ 朱夏27△邵增务28* 李建民29* 肖建如30* 牛晓辉31* 王国文1* 林建华27*
(1.天津医科大学肿瘤医院,天津 300060;2.陆军军医大学新桥医院,重庆 400037;3.上海交通大学第六人民医院,上海 200233;4.内蒙古医科大学第二附属医院,呼和浩特 010030;5.北京大学人民医院,北京 100044;6.空军军医大学西京医院,西安 710032;7.上海市第九人民医院,上海 200011;8.安徽医科大学第一附属医院,合肥 230022;9.天津医院,天津 300211;10.中山大学附属第一医院,广州 510080;11.南方医科大学第三医院,广州 510635;12.宁夏医科大学附属第一医院,银川 750000;13.北京协和医院,北京 100730;14.苏州大学附属第一医院,苏州 215006;15.山西医科大学第二医院,太原 030001;16.北京儿童医院,北京 100045;17.西安红会医院,西安 710054;18.四川大学华西医院,成都 610041;19.中山大学肿瘤医院,广州 510080;20.山东大学齐鲁医院青岛院区,山东青岛 266035;21.华中科技大学同济医院,武汉 430030;22.上海第十人民医院,上海 200070;23.辽宁省肿瘤医院,沈阳 110092;24.上海瑞金医院,上海 200025;25.西部战区总医院,成都 610083;26.空军军医大学唐都医院,西安 710038;27.福建医科大学附属第一医院,福州 350005;28.华中科技大学协和医院,武汉 430022;29.山东大学附属齐鲁医院,济南 250012;30.海军军医大学长征医院,上海 200433;31.北京积水潭医院,北京 100035)
静脉血栓栓塞症(venous thromboembolism,VTE)是指血液在静脉内异常凝结,使血管完全或不完全阻塞而引起静脉回流障碍,从而导致相应的机体变化。常见的类型包括深静脉血栓形成(deep vein thrombosis,DVT)及肺动脉血栓栓塞症(pulmonary embolism,PE)。国内90 家医院2007~2016 年统计数据显示,因VTE 住院的患者从3.2/10 万人增加至17.5/10万人,VTE相关的死亡率约为2.1%[1]。肿瘤确诊后2 年内相关的VTE 发生率为1%~10%[2]。此外,23%~60%非致命的VTE 患者会出现血栓后综合征,需要长期护理[3]。
既往研究认为恶性肿瘤及骨科手术是VTE的高风险因素,二者同时出现会增加患者VTE 的风险[4,5]。研究显示原发性骨肿瘤的VTE 发生率达5.2%,转移性骨肿瘤的VTE可增加至7.0%[6]。然而,目前国内尚无相应的骨肿瘤静脉血栓栓塞症防治共识可供借鉴。为此,中华医学会骨科学分会骨肿瘤学组组织全国30多位专家,参考国内外相关领域的最新指南、共识,经反复讨论形成《中国骨肿瘤大手术静脉血栓栓塞症防治专家共识(2019 版)》。本专家共识将骨肿瘤大手术定义为脊柱、骨盆、髋、膝、肩关节周围恶性肿瘤进行的切除、重建手术。本专家共识仅为成人骨肿瘤深静脉血栓栓塞症防治提供指导意见,具体实施方案需根据临床具体情况而定。
1 骨肿瘤相关VTE的流行病学
一项回顾性研究发现252 例原发性骨与软组织肉瘤术后DVT 及PE 的发生率分别为4%和1.2%[7]。另有研究显示骨与软组织肿瘤VTE的整体发生率为2.7%,但恶性肿瘤患者可增高至6.7%[8]。也有研究报道了相对较高的骨肿瘤术后VTE发生率。不同部位骨肿瘤术后静脉血栓发生率不尽相同,股骨近端骨肿瘤术后血栓发生率高于股骨远端,胫骨近端VTE发生率略低[9]。综合既往骨与软组织肿瘤术后VTE的研究报道,骨肿瘤VTE 的发生率为5.7%±1.5%,软组织肿瘤术后VTE的发生率为7.0%±2.0%。
2 骨肿瘤相关VTE的风险因素及评估
静脉血栓形成包括三方面主要因素:高凝状态、静脉内膜损伤及静脉血流淤滞。恶性肿瘤细胞及其产物与宿主相互作用产生高凝状态,化疗引起血管内皮细胞的毒性反应及损伤[10],患者活动能力下降、下肢静脉血液回流差,这些情况均会增加血栓形成的概率[11]。
骨肿瘤大手术患者术后发生VTE的风险因素可分为患者相关因素、肿瘤相关因素以及治疗相关因素。患者相关因素包括老年患者(>60岁[12])、糖尿病、既往VTE 病史[13]及脑血管疾病[12]等。肿瘤相关因素涉及肿瘤的性质、是否为转移性肿瘤、是否合并内脏转移等。研究发现恶性肿瘤(4.8%)较良性肿瘤(0.95%)出现VTE 的风险更高[12],转移性肿瘤是术后出现VTE的独立因素[14],合并肺部转移也会增加VTE的风险[15]。治疗相关因素包括手术、化疗及放疗等。手术通常会增加VTE 的发生率,骨与软组织肿瘤术后VTE 常发生在下肢及骨盆的手术[12]。肿瘤体积较大或需要切除后重建,亦增加VTE的风险[8]。患者行化疗后VTE发生率可从1%(1/100例)增加至8.5%(6/71 例)[16]。术前较低的血红蛋白水平[17]、术中氧饱和度下降[15]、失血量较多及输血[13]、术后伤口并发症[18]以及较长的住院时间[17]等也都是VTE 发生的相关风险因素。
鉴于骨肿瘤术后较高的VTE 发生率,临床上应积极行VTE 的风险评估并予相应的预防措施。目前,针对VTE 的风险有多种的评估工具,包括Khora⁃na 评分[19]、Padua 风险评分[20]、Rogers 评分[21]及Caprini风险评估模型[22]等。其中,Caprini风险评估模型广泛应用于外科系统及静脉血栓预防指南[23-25]。因此本专家共识亦采用该模型评估骨肿瘤患者术后发生VTE的风险,详见表1。

表1 Caprini风险评估模型及VTE风险分级
3 骨肿瘤相关VTE的诊断
临床需要加强对患者的巡视及检查,及时发现VTE 的早期症状及体征,如DVT 患者通常会出现下肢肿胀、疼痛及压痛等临床症状;PE患者通常会出现不明原因的呼吸困难、胸痛、咳嗽、咯血、心动过速、情绪不安、晕厥、氧饱和度下降等临床症状。当怀疑患者出现VTE时,应该尽快完善相应的检查。
3.1 验前概率及评估
根据Bayes 理论,疾病发病率越低阴性预测价值越高;反之,发病率越高阳性预测价值越高。医师可以据此判断患者的验前概率(pretest probability,PTP),从而提高检查的针对性。对于PTP 较低的患者,简单的检查方案即可达到满意的结果。例如,低PTP 的患者可疑出现VTE 时,阴性的D-二聚体结果可以较放心地排除VTE,这样可使约30%可疑VTE的患者无需影像检查即可安全地排除VTE[26]。但是,对于高PTP 的患者,阴性的D-二聚体结果并不能安全地排除VTE。此外,使用PTP还可以指导抗血栓治疗的时机。ACCP 抗血栓治疗指南建议:对于高PTP的患者,如果检查结果要4 小时后报告,可即刻开始抗血栓治疗;对于低PTP的患者,可以等到24小时结果报告后开始相应治疗[25]。
文献报告了多种PTP 的评估工具[27],其中Wells PE 评分[28]或改良Geneva 评分[29]适用于可疑PE 的患者;Wells DVT 评分[30]适用于可疑DVT 的患者。具体工具见表2。
3.2 DVT、PE的辅助检查及流程
3.2.1 DVT辅助检查及流程
超声:简单便捷,是四肢DVT 诊断的首选方法,彩色多普勒超声检查还可以提高盆腔内血管血栓的检测能力。CT 静脉造影:适用于病情危重或肢体采用夹板固定等不便超声检查的患者,可同时检查腹部、盆腔、下肢深静脉的情况。静脉造影:该技术是DVT 诊断的金标准,但部分患者可能出现造影剂过敏等情况。在其他检查难以确定诊断时,如无静脉造影禁忌证,可行该项检查。血浆D-二聚体:其变化反映了凝血激活及继发性纤溶的过程,对诊断急性DVT具有较高的灵敏度。临界值目前多用500 μg/L,但是癌症患者的D-二聚体水平普遍较高,手术干预也会对结果造成明显干扰,判定值有待进一步研究确定[31]。
依据一项采用Wells 评分评估DVT 发病率的荟萃分析结果[32],2018年美国ASH指南[33]估计低、中、高PTP的DVT发病率为≤10%(低)、≤25%(中)及≤50%(高)三级。当患者可疑DVT 时,首先评估PTP,根据PTP分级采取不同的检查策略。低PTP患者先行D-二聚体检查,阴性结果可排除DVT;如果无法检测D-二聚体,可直接行下肢超声检查,阴性超声结果亦可排除DVT;阳性D-二聚体联合阳性超声方可确诊DVT。中PTP患者直接行下肢超声检查,阳性结果可诊断下肢DVT;下肢超声阴性结果可排除DVT;近端超声阴性结果需后期复查超声。对于高PTP 患者直接行下肢超声检查,阴性结果必须后期复查超声。具体流程见图1。
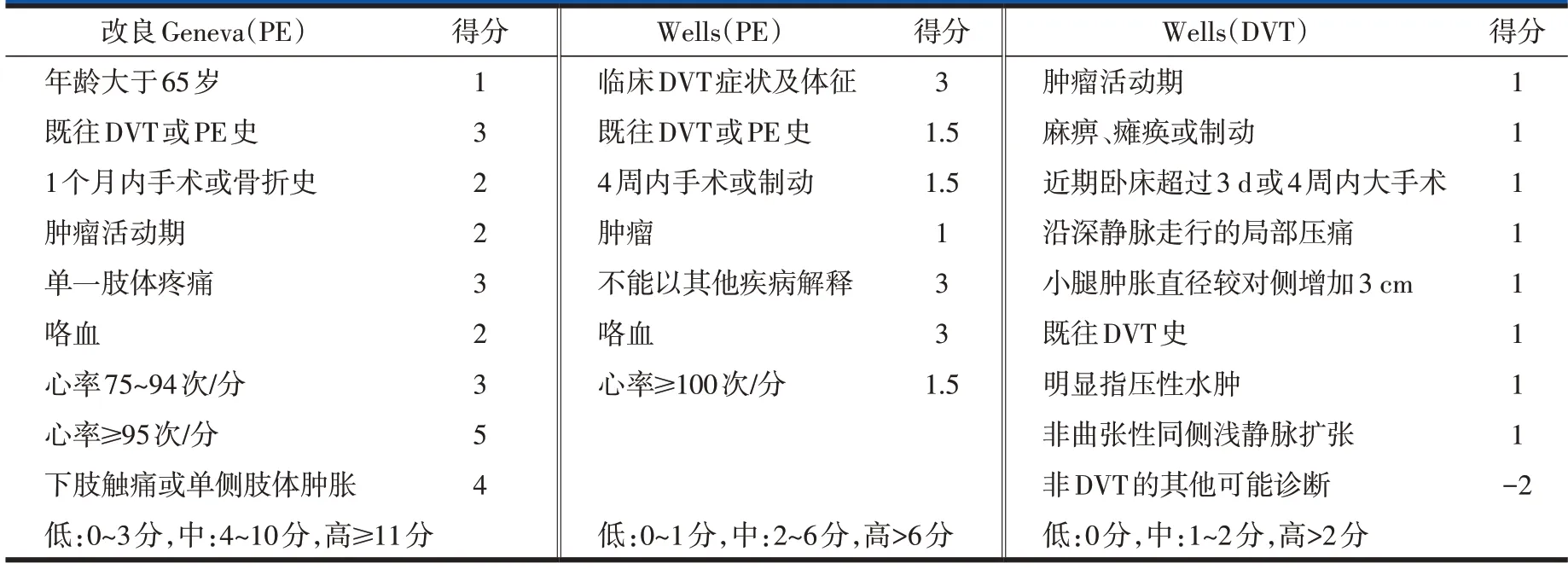
表2 患者PTP评估工具
3.2.2 PE辅助检查及流程
CT肺动脉造影:是一项有创检查,是诊断肺栓塞的金标准;在其他检查难以确定诊断并且无静脉造影禁忌证时,可行该项检查。肺通气灌注扫描:敏感度较高,与其他检查结合可提高诊断的特异度和敏感度。CT或增强CT可判断肺动脉栓塞大小及位置,但对亚段及以远肺动脉血栓的敏感性较差。经胸超声心动检查:对于临床怀疑PE 并伴有休克或低血压患者,通常无条件行肺动脉增强CT,此时可行床旁经胸多普勒超声心动检查,观察右心高负荷表现,并明确诊断。血浆D-二聚体:可辅助诊断PE。
依据一项采用Wells 评分评估PE 的荟萃分析结果[27],2018年美国ASH预防指南估计低、中、高PTP的PE 发病率分别为≤5%(低)、≤20%(中)及≤50%(高)三级。当患者可疑PE时,首先评估PTP,低PTP患者先行D-二聚体检查,阴性结果可排除PE;如果无法检测D-二聚体或其结果阴性,可行肺通气灌注检查,正常结果可排除PE,高度阳性结果诊断PE,模棱两可的结果需进一步完善下肢近端超声检查,阳性结果确诊PE,阴性结果排除PE。当肺通气灌注扫描或近端超声无法施行时,还可直接行CT肺动脉造影,阴性结果排除PE,阳性结果确诊PE。对于中PTP 患者,模棱两可的肺通气灌注检查结果进一步行CT 肺动脉造影检查,阴性结果排除PE,阳性结果确诊PE。对于高PTP 患者,应直接行CT 肺动脉造影检查,阳性结果确诊PE。当结果为阴性或无法施行该检查时,需辅助肺通气灌注扫描、D-二聚体及超声检查,从而明确有无PE。具体流程见图2。

图1 可疑DVT诊断流程图
当患者出现高危DVT 或PE 时,应及时与专科医师沟通,寻求诊疗指导。
4 骨肿瘤VTE的预防
根据Caparini评分,骨肿瘤大手术患者VTE的风险级别高,建议高危风险的恶性骨肿瘤患者围手术期在无禁忌证情况下,常规预防VTE[34]。临床医师应根据具体情况制定基本预防、机械预防和药物预防综合方案[35]。
4.1 基本预防
应对住院骨肿瘤大手术患者进行血栓预防知识的宣教,使其充分认识VTE 防治的重要性和必要性[36,37]。宣教内容包括:①讲解静脉血栓知识,鼓励并指导患者勤翻身,早期功能锻炼,下床活动等;②术后抬高患肢,加强肌肉锻炼,促进深静脉回流;③术后适度补液,多饮水,避免脱水;④建议患者改善生活方式,如戒烟、戒酒、控制血糖及血脂等。

图2 可疑PE诊断流程图
4.2 机械预防
机械预防包括间歇性气动压缩装置(intermittent pneumatic compression,IPC)、足底静脉泵(venous foot pump,VFP)和分级弹力加压袜(graduated compres⁃sion stockings,GCS)等,可促进静脉血回流,降低VTE的发生率。机械预防具有操作简单、并发症少及不增加出血等优点[36,37]。对于中、高VTE 风险的骨肿瘤患者应联合应用机械和药物进行预防。存在药物预防禁忌证的患者可暂时给予机械预防,禁忌证消失后,建议继续与药物联合预防[37]。对于脊柱、骨盆肿瘤手术患者在围手术期无禁忌证情况,应予机械预防。术前和术后可使用IPC/VFP 和GCS,术中使用GCS[37]。对于髋、膝关节周围肿瘤切除重建手术患者,应用椎管内麻醉时,可选择单独使用机械预防[38]。对于不能早期下地活动的患者,出院后继续使用机械预防,直至VTE 风险消失。在临床应用过程中应避免错误的使用方法,否则可能会增加相关并发症(如GCS 加重皮肤溃疡和坏死)[34]。使用各种机械预防过程中,应特别注意观察皮肤情况[39]。机械预防禁忌证[34]:分为绝对和相对禁忌证,详见表3。
4.3 药物预防
恶性骨肿瘤大手术患者在无药物禁忌证的情况下,符合指征的患者需要接受VTE药物预防[34]。因骨肿瘤患者个体情况及手术方式差别较大,应充分考虑抗凝药物使用和VTE 风险的利弊,合理选择抗凝药物。常用药物包括:普通肝素、低分子肝素、Ⅹa因子抑制剂及维生素K拮抗剂等[40]。
普通肝素(unfractionated heparin,UFH):是严重肾功不全患者的首选抗凝药物,该药有增加患者出血甚至大出血风险,需要常规监测活化部分凝血酶原时间从而调整其剂量。因某些患者可发生肝素诱导的血小板减少症(heparin induced thrombocytope⁃nia,HIT),现临床较少使用[40]。UFH 禁用于HIT 患者,有HIT病史的患者慎用[41]。
低分子肝素(low molecular weight heparin,LM⁃WH):是临床一线最常见的VTE 防治药物,也是癌症患者首选的抗凝药物[42]。其特点是抗凝效果稳定,通常不增加患者大出血风险,一般无需常规凝血监测。对于髋、膝关节周围肿瘤切除重建手术患者起始给予预防剂量(依诺肝素:4000 IU),术前12 h开始给药,也可以根据具体情况调整药物或剂量。其中依诺肝素可用于VTE 的紧急治疗[42]。达肝素钠可用于癌症患者症状性VTE 的延长治疗。若LM⁃WH需长期使用(超过3个月),需将其剂量减少至初始量的3/4[43]。
Ⅹa因子抑制剂:可分两类:①间接Ⅹa因子抑制剂:如磺达肝癸钠,适用于HIT 患者或代替LM⁃WH[44]。由于磺达肝癸钠代谢增加肾脏排泄负担,所以严重肾功能不全患者禁用;体重<50 kg 患者或年龄>75岁老年患者慎用[34];慎用于严重肝功能损害的患者。②直接Ⅹa 因子抑制剂:如利伐沙班,一般用于髋膝关节置换手术患者VTE的预防和治疗[40],其特点是应用方便、效果肯定,但应注意其可能引发出血[45]。严重肾功不全患者禁用,中度肾功不全慎用[34]。虽然国内外利伐沙班在恶性骨肿瘤患者应用的安全性和有效性的证据较少[34],但现有证据支持其可能是将来替代LMWH 的潜力药物。对于髋、膝关节周围肿瘤切除重建手术患者不适合注射给药和机械预防的患者,可考虑口服Ⅹa因子抑制剂如利伐沙班(10 mg 起始,术后6~10 h 开始使用),并根据具体情况酌情调整药物剂量[34]。
维生素K 拮抗剂(VKA):华法林适合癌症患者VTE的长期治疗,但要和肠外抗凝药物(UFH、LMWH或磺达肝癸钠)同时使用≥5 d,直到INR≥2,停用肠外抗凝药物[34,45]。用于治疗HIT 时需每周两次监测INR。华法林可安全用于肾功能不全患者,不建议肝功能异常患者使用。
抗血小板药:阿司匹林,骨肿瘤患者不建议使用[34,46]。国内外多项研究发现,阿司匹林预防VTE的效果与安慰剂并无明显区别[46]。此外,研究数据表明VTE 治愈后,不推荐应用阿司匹林预防VTE 的复发[47]。

表3 机械预防禁忌证
选择药物预防时还应该考虑以下情况:①对于VTE风险级别低的恶性骨肿瘤患者,术前不建议药物预防;VTE级别高的恶性骨肿瘤患者术前给予抗凝药物预防VTE,但应在术前12~72 h 前停用,并改用桥接药物。桥接药物一般选择低分子肝素,预防剂量根据出血风险和VTE 发生风险评估来综合制定[48]。术后12~72 h 根据患者具体情况(如引流量、抗凝药物药理等)予以抗凝药物。持续时间一般10~14 d,特殊情况可延长至术后1个月[49,50]。各种抗凝药物的半衰期、清除率等药理性质不同,应根据药物说明书选择药物具体应用时间。②椎管内麻醉手术患者,不建议术前应用抗凝药物预防VTE。若非肿瘤原因使用抗凝药物,术前应与麻醉医师沟通,了解抗凝药物与硬膜外置管拔出时间的关联性,必要时改用全麻或其他麻醉方式。③长期服用氯吡格雷或阿司匹林的患者,应在术前停用此类抗凝药物(氯吡格雷7 d;阿司匹林5 d),桥接应用低分子肝素[51]。④对于骨肿瘤大手术患者建议动态监测D-二聚体,评估出凝血风险,选择合适的治疗方案。
5 骨肿瘤VTE的治疗
5.1 DVT的治疗
对于明确DVT 的患者,建议根据体重予以普通肝素、低分子肝素治疗;对于恶性肿瘤合并DVT患者长期应用低分子肝素能够获得较好的治疗结果;排除禁忌证后,还可以用于急性期治疗。在应用普通肝素、低分子肝素或磺达肝素等药物期间,如拟更换华法林,应与华法林叠加使用至少5 d,直至INR≥2。对于DVT 患者,用低分子肝素或华法林治疗持续时间最短3个月;对于存在危险因素或高VTE级别的癌症患者建议长期抗凝并监测出血风险;对于急性DVT 有抗凝绝对禁忌证的患者建议放置下腔静脉滤器,具体使用情况可咨询相关专科[42]。详细DVT治疗流程图见图3。

图3 DVT治疗流程图
5.2 PE的治疗
对于确诊PE 的患者,建议首先对患者进行风险分层,对无抗凝禁忌证的患者,确诊后应立即予以抗凝治疗;对有抗凝禁忌证且PE来自下肢、骨盆或腹部的深静脉血栓,建议放置下腔静脉滤器[25,52];对于大块肺栓塞、中或重度右心室增大或心功能障碍的患者,酌情予以溶栓或取栓治疗[52-54]。详细PE 治疗流程见图4。

图4 PE治疗流程图
6 其他
6.1 复发性VTE
恶性肿瘤患者尽管接受了抗凝治疗,但是较高的VTE复发率依然是临床常见的问题。参考治疗措施:在治疗期间VTE复发的癌症患者,首选低分子肝素,需增加剂量1/4,延长抗凝治疗超过3个月[34]。
6.2 无症状偶发性VTE
无症状偶发性VTE指通过影像学或其他检查无意中发现的DVT 或PE,其治疗参考常规预防抗凝治疗,定期专科复查[55]。
