特发性膜性肾病患者高尿酸血症的相关因素分析
2020-07-17陈小妹杨沿浪刘慧婷
陈小妹,杨沿浪,刘慧婷,金 月
(皖南医学院第一附属医院 弋矶山医院 肾脏内科,安徽 芜湖 241001)
膜性肾病(membranous nephropathy,MN)是成人肾病综合征常见的一种病理类型,在原发性肾小球疾病中比例在增加[1],常隐匿起病,约1/3患者治疗无效,肾功能进展至终末期肾脏,需行肾脏替代治疗,增加了患者家庭经济负担和社会负担。众多临床研究[2-3]发现,高尿酸血症(hyperuricemia,HUA)是导致慢性肾脏病的危险因素,但其确切机制仍不明确,且HUA在MN中相关影响因素分析研究甚少,本研究回顾性分析151例特发性膜性肾病(idiopathic membranous nephropathy,IMN)中HUA患者的临床资料和肾脏病理资料,探讨IMN中HUA的影响因素,为该疾病早期治疗和预后改善提供理论基础。
1 资料与方法
1.1 研究对象 选取2016年1月~2019年3月在弋矶山医院肾内科住院,经肾活检确诊的IMN患者151例,其中HUA组65例,血尿酸正常组86例。两组患者的临床资料、实验室检查及病理资料等均完整。纳入病例时剔除肿瘤、自身免疫性疾病、过敏性紫癜、病毒性肝炎及其他感染等继发性因素以及服用影响尿酸代谢药物者。
1.2 临床及病理资料 收集患者临床及病理资料。①基本资料:年龄、性别、体质量指数(body mass index,BMI)、收缩压(SBP)、舒张压(DBP)、有无水肿。②实验室资料:血浆白蛋白(Alb)、前白蛋白(PA)、空腹血糖(BS)、总胆固醇(CHOL)、甘油三酯(TG)、低密度脂蛋白(LDL)、高密度脂蛋白(HDL)、血尿素氮(BUN)、血肌酐(Scr)、胱抑素C(CYS-C)、血尿酸(BUA)、血红蛋白(Hb)、24 h尿蛋白定量(24 h-pro)。③病理资料:所有患者均在B超引导下行肾活检术,肾脏病理行常规光镜、免疫荧光和电镜检查。IMN的病理分期参考《肾活检病理学》第4版[4],分为 5 期(I~V期)。如同时有两个分期,则以较高分期为最终分期。 根据Katafuchi半定量积分标准评价肾小管间质病变程度。肾小管按病变范围:阴性0,≤5%为轻度,26%~50%为中度,≥50%为重度;肾间质:阴性0,≤25%为轻度,26%~50%为中度,≥50%为重度。系膜增生如同时有2个分期,以较高分期为最终分期。④肾小球滤过率(eGFR):eGFR计算采用慢性肾脏病流行病合作工作组(CKD-EPI)方程[5]。CKD分期(分为1~5期)标准参考《内科学》第9版。
1.3 HUA诊断标准 在正常嘌呤饮食状态下,非同日两次空腹血尿酸水平男性高于420 μmol/L,女性高于360 μmol/L。

2 结果
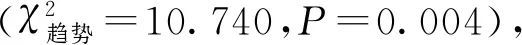
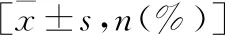
表1 两组患者一般资料及临床资料比较
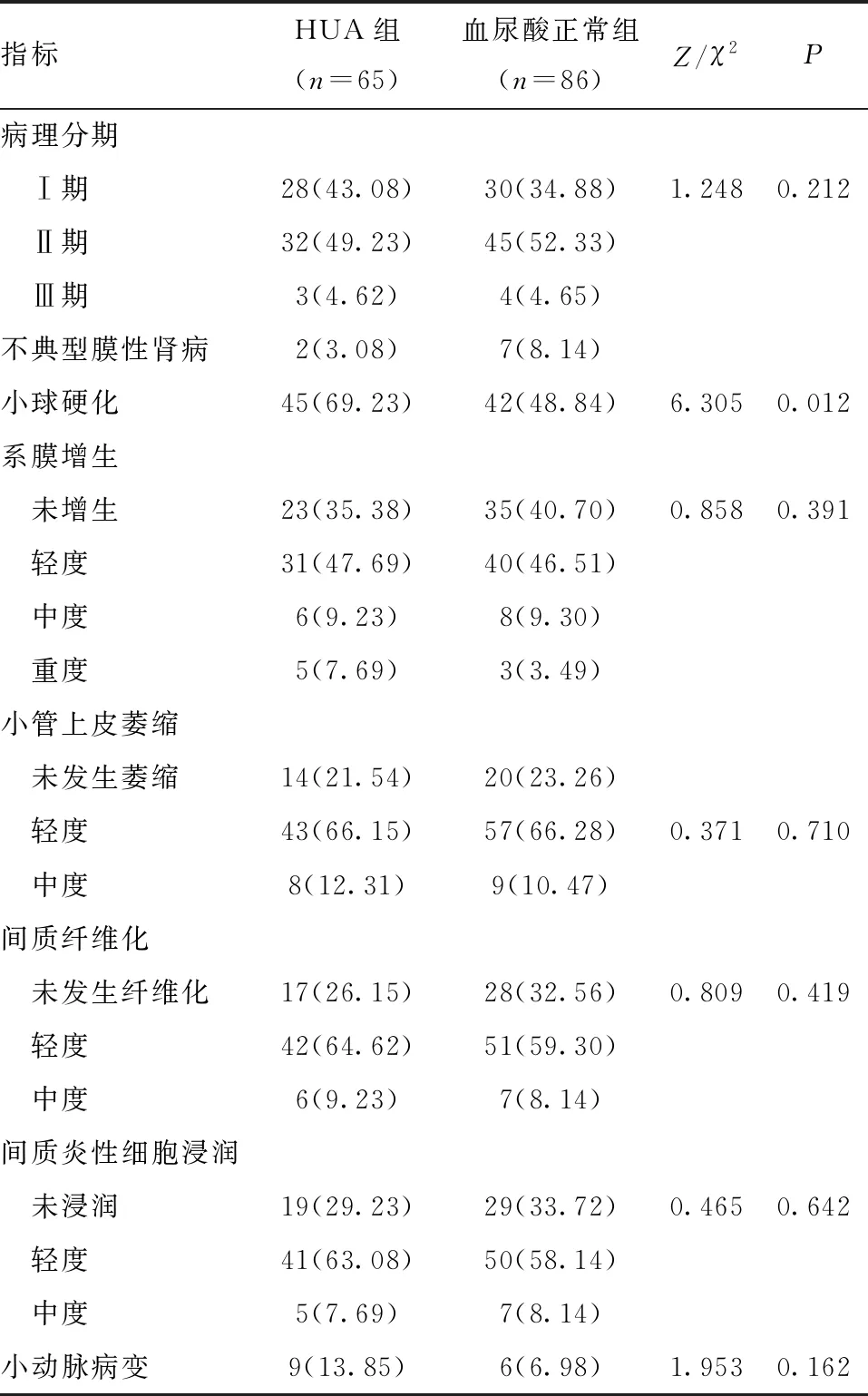
表2 两组患者光镜资料比较[n(%)]
2.2 HUA组与血尿酸正常组患者光镜资料比较 HUA组肾小球硬化发生率高于血尿酸正常组(P<0.05),两组患者在病理分期、系膜增生、小管上皮萎缩、间质纤维化、间质炎性细胞浸润及小动脉病变上差异无统计学意义(P>0.05)。见表2。
2.3 HUA组与血尿酸正常组患者免疫荧光资料比较 免疫荧光结果显示,两组患者均以IgG及C3沉积为主,部分病例伴IgA、IgM 及补体C1q沉积,但两组间各指标差异均无统计学意义(P>0.05)。见表3。
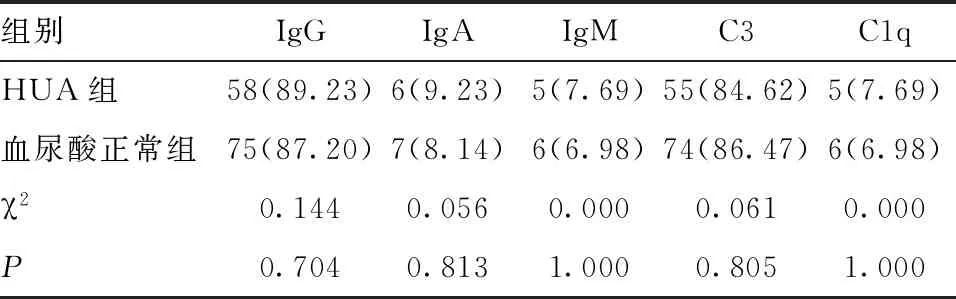
表3 两组患者免疫荧光资料比较[n(%)]
2.4 IMN中HUA危险因素分析 根据单因素分析结果,按照P<0.10的标准共有13个指标纳入多因素Logistics回归模型。结果显示,CKD3期(OR=8.147,95%CI:2.278~29.141)、BMI增高(OR=1.660,95%CI:1.364~2.021)、TG增高(OR=2.705,95%CI:1.726~4.240)和BUN增高(OR=1.234,95%CI:1.046~1.457)是HUA发病的危险因素。见表4。
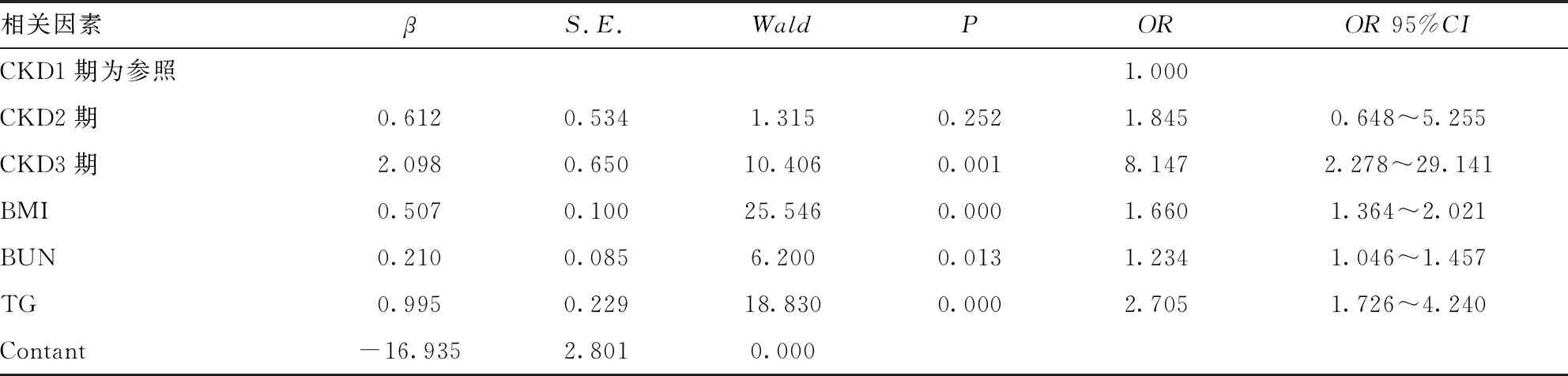
表4 IMN中HUA影响因素分析
3 讨论
近年来,MN的发病率迅速增加[6]。HUA的发病率日渐上升[7]。有研究报道[8-9],IMN中HUA的发生率为23.2%~38.4%。本研究结果显示,151例IMN中HUA者65例,HUA的发生率为43.05%,较相关报道高,可能与患者饮食习惯、生活方式有关。
分析两组患者临床资料发现,HUA组患者BMI、高血压占比、BUN、Cystatin C、血脂水平比血尿酸正常组高(P<0.05),血浆白蛋白及估算eGFR水平较血尿酸正常组低(P<0.05),提示高尿酸与肾功能损伤有一定关系。华明[10]研究也发现,随着尿酸水平的升高,CKD患者的eGFR水平逐渐降低。Mende[11]研究发现,HUA 患者的肾脏损伤风险比血尿酸正常患者高9.3倍。
本研究发现,两组患者肾组织病理分期均以Ⅰ、Ⅱ期为主。HUA组肾小球硬化发生率高于血尿酸正常组(P<0.05)。随着CKD分期的增加,HUA所占比例有增高的趋势(P<0.05)。多因素回归分析发现CKD3期是IMN中HUA危险因素,提示高尿酸可能加重CKD3期患者肾功能恶化,与Moriyama等[12]研究一致。Romi等[13]在动物实验研究中同样也发现HUA小鼠肾小球硬化较重。这可能与氧化应激、内皮细胞NO合成不足、激活肾素血管紧张素系统、损害足突上皮细胞有关。此外,高尿酸通过调控TLR4 /NF-κB 信号通路诱导肾小管上皮细胞-间充质细胞转化(epithelial-mesenchymal transition,EMT),导致小管间质纤维化[14],而肾脏纤维化是慢性肾脏病进展的共同途径。但本研究中两组间小管间质纤维化差异无统计学意义,这可能与所入组病例数较少及均为CKD1-3期患者有关。
多因素回归分析发现,较高的BMI、高血脂是IMN中HUA的危险因素。肥胖可导致胰岛素抵抗,激活肾素-血管紧张素-醛固酮系统,引起肾脏血流量减少,导致尿酸排泄减少。高尿酸可致PCSK-9水平升高,使肝脏降解脂蛋白减少,诱发血脂代谢紊乱[15]。血脂异常时LDL在血管内皮沉积和氧化加速,激活炎症细胞,释放炎症介质、细胞因子,刺激肾脏固有细胞增殖以及细胞外基质的大量合成,导致肾损伤加重,肾功能进展。因此临床上对IMN中HUA患者,控制体质量及降脂治疗可能对改善肾脏预后有一定益处。
综上所述,IMN中HUA发生率较高,合并HUA的IMN患者临床及病理损伤更严重,CKD3期、较高的BMI、较高的血脂及BUN水平是IMN合并HUA的相关危险因素,降脂、控制体质量及改善肾功能治疗对改善肾脏预后可能有一定益处。但本研究样本量有限,为单中心横断面研究,考虑到肾活检风险,入组病例为CKD1-3期的患者,研究结果尚需更大样本研究证实。
