干扰素联合替诺福韦治疗慢性发作乙型肝炎效果及对肝功能、乙肝病毒脱氧核糖核酸阴转率的影响*
2020-07-10蔡庆贤李海凤
蔡庆贤,夏 章,罗 芳,李海凤
深圳市第三人民医院肝病一科,广东 深圳 518000
慢性乙型肝炎病毒(HBV)感染可导致急性发作的肝损伤、肝衰竭、肝硬化和肝癌。其中慢性乙型肝炎急性发作患者出现乏力、纳差、恶心、腹胀、尿黄等消化道症状及肝功能失代偿的表现,如处理不当可进展为肝衰竭及肝硬化[1-2]。目前针对慢性HBV感染采用口服核苷/核苷酸类类药物(如:拉米夫定、替比夫定、恩替卡韦、替诺福韦、丙酚替诺福韦)或者聚乙二醇干扰素治疗,两种方案各有利弊[3]。对于急性发作的慢性乙型肝炎患者,如何选择治疗方案存在争议[4]。近期有学者在研究中提出,干扰素联合替诺福韦治疗急性发作乙型肝炎效果显著,临床应用价值较高[5]。为探讨上述报告的可行性我们开展了后续研究分析,现报告如下。
1 资料与方法
1.1 一般资料
研究对象均为深圳市第三人民医院近期收治的慢性乙型肝炎急性发作患者,共80例,随机分为观察组(40例)与对照组(40例)。观察组,男性23例,女性17例;年龄为21~67岁,平均年龄(41.15±5.48)岁;病程为1~8年,平均病程(5.71±1.30)个月;BMI指数为21~27 kg/m2,平均(23.95±3.08)kg/m2。对照组,男性22例,女性18例;年龄为22~65岁,平均年龄(41.21±5.50)岁;病程为1~9年,平均病程(5.65±1.31)个月;BMI指数为20~27 kg/m2,平均(23.82±3.11)kg/m2。两组上述资料对比差异无统计学意义(P>0.05),具有可比性。
1.2 入选标准
慢性乙型肝炎诊断依据《慢性乙型肝炎防治指南(2015年版)》[6]的标准,急性发作定义为谷丙转氨酶升高超过10倍正常值上限(the upper limit of normal,ULM),所有患者均为HBeAg阳性(大三阳)。排除:胆红素升高超过34.2 umol/L(干扰素治疗的禁忌),晚期纤维化、肝硬化和肝癌患者;合并其他类型病毒性肝炎,如:丙型肝炎病毒、丁型肝炎病毒、戊型肝炎者;HIV感染、酗酒、自身免疫性或代谢性肝病者;需要使用皮质类固醇或免疫抑制剂的严重内科或精神疾病的患者。
1.3 治疗方法
对照组,均单独采用替诺福韦治疗,替诺福韦片(安徽贝克生物制药有限公司国药准字H20193014)每次取量300 mg,进行1次/d口服治疗,长期连续治疗。观察组,采用替诺福韦与聚乙二醇干扰素α-2a联合治疗,其中替诺福韦用药方案与对照组基本无异,聚乙二醇干扰素α-2a(批准文号:H20030011,生产厂商:上海罗氏品牌:派罗欣,180 ug/0.5m l/支)1次/周,皮下注射,疗程48周。
1.4 观察指标
对比两组各项临床资料的差异,两组不同用药方案下临床疗效、肝功能指标、用药安全性以及HBV-DNA转阴情况的差异。疗效判断指标:在治疗开始后48周比较两组的应答情况。(1)完全病毒学应答(Complete virological response):定义为HBV-DNA水平<100 IU/m l,HBV-NDA采用荧光定量聚合酶链反应技术(试剂盒购自广州达安基因股份有限公司,检测下限<100 IU/mL)。(2)HBeAg转阴/血清学转换:定义为HBeAg转阴伴或不伴HBeAb转阳。HBV标记物采用美国Abbott公司第2代试剂微粒子酶联免疫法(MEIA)进行检测,其中基线HBsAg采用罗氏电化学发光全定量检测系统(The Elecsys HBsAg IIQuant系统)。(3)生化应答转氨酶ALT降低到正常。(4)联合应答:生化应答+病毒学应答。肝功能指标检测项目包括:白蛋白(ALB)、天冬氨酸转氨酶(AST)、丙氨酸转氨酶(ALT)、总胆红素(TBIL),上述指标表达水平具体检测方法为:取患者晨间肘静脉血液5 m l,在恒温条件下凝聚20~30 min,后在3 000 r/min条件下进行15 min离心处理,获取血清样本后放置于-20℃条件下保存待检,检测仪器选用日本Olympus2700型全自动生化分析仪,检验方法选用免疫比浊法,检验试剂盒由上海晶抗生物工程有限公司生产提供,具体检验操作严重按照说明书规范执行。HBV-DNA采用美国ABI 7700型荧光定量PCR仪进行检测,若HBV-DNA定量检测水平低于1 000 copies/m l则可判定为阴性,统计两组患者HBV-DNA转阴例数。通过统计患者治疗过程中出现的不良反应对用药安全性进行评价,不良反应统计项目包括:头晕、胃肠道反应、血液系统异常、过敏反应等。
1.5 统计学方法
数据采用SPSS 20.0软件进行统计学分析,计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料用例数和百分比(%)表示,组间比较采用χ2检验,并行Spearman相关分析;以P<0.05为差异有统计学意义。
2 结果
2.1 临床资料
所有患者入院后均进行性别、年龄、病程、体质量指数及血压水平统计对比,结果表明:两组患者临床资料差异无统计学意义(P>0.05),具有可比性。见表1。
表1 两组临床资料对比(±s)

表1 两组临床资料对比(±s)
注:1mmHg=0.133kPa。
组别分类观察组(n=40)对照组(n=40)χ2/t P性别男性[例(%)]23(57.50)22(55.00)0.216 0.839女性{例(%)}17(42.50)18(45.00)年龄(岁)41.15±5.48 41.21±5.50 0.049 0.961病程(月)2.71±0.30 2.65±0.31 0.88 0.382 BMI(kg/m2)23.95±3.08 23.82±3.11 0.188 0.852收缩压(mmHg)125.52±11.49 125.18±12.05 0.129 0.898舒张压(mmHg)80.73±6.22 80.60±6.18 0.094 0.926 HBV-DNA定量(×103 copies/ml)4.25±0.38 4.30±0.34 0.165 0.873 ALT(U/L)452.24±35.33 454.91±34.28 0.343 0.732乙肝家族史[例(%)]12(30.00)11(27.50)0.09 0.903
2.2 临床疗效分析
此次研究所选取的所有患者均顺利完成临床治疗,未出现研究数据脱落。在治疗后48 h对疗效进行判断,观察组,患者在联合用药治疗后共33例被判定为生化应答,36例被判定为完全病毒学应答,20例判定为HaveBeAg转阴/血清学转换;对照组,患者在单一用药治疗后共33例被判定为生化应答,28例判定为完全病毒学应答,10例判定为HaveBeAg转阴/血清学转换。两组联合应答率对比差异有统计学意义(P<0.05);观察组治疗3个月后共21例患者HBV-DNA定量检测判定为阴性,对照组治疗3个月后共16例患者HBV-DNA定量检测判定为阴性;观察组治疗6个月后共29例患者HBV-DNA定量检测判定为阴性,对照组治疗6个月后共27例患者HBV-DNA定量检测判定为阴性。两组联合应答率对比差异无统计学意义(P>0.05),两组患者治疗3个月、6个月后HBV-DNA转阴率对比差异均无统计学意义(P>0.05),见表2。
2.3 肝功能指标分析
两组治疗前ALB、AST、ALT及TBIL指标表达水平对比差异均无统计学意义(P>0.05);两组治疗后ALB、AST、ALT指标水平对比差异无统计学意义(P>0.05),TBIL指标水平对比差异有统计学意义(P<0.05),观察组均低于对照组,见表3。
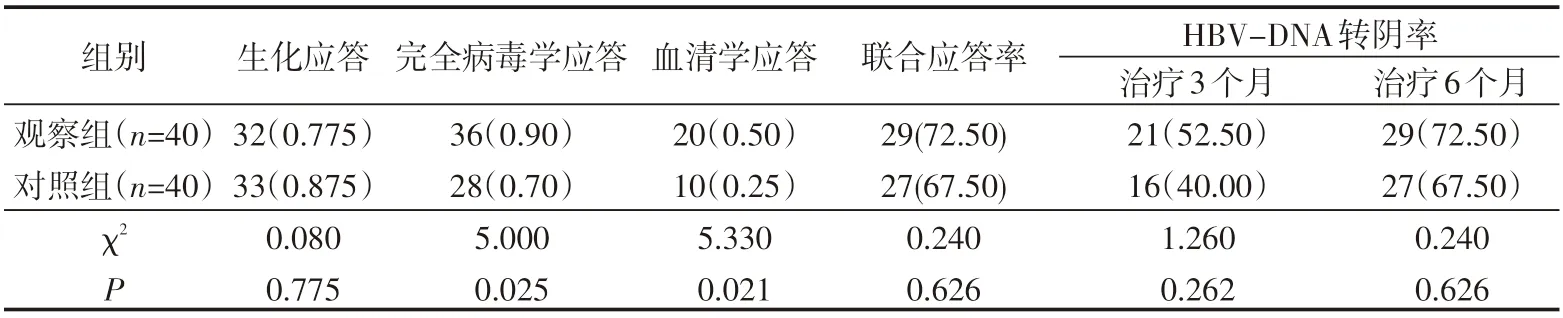
表2 两组临床治疗效果对比 例(%)
表3 两组治疗前后各项肝功能指标水平对比(±s)

表3 两组治疗前后各项肝功能指标水平对比(±s)
肝功能指标ALB(U/L)t P AST(U/L)ALT(U/L)TBIL(U/L)时间治疗前治疗后治疗前治疗后治疗前治疗后治疗前治疗后观察组(n=40)42.15±4.60 43.14±4.58 154.81±11.52 38.61±5.87 220.51±30.18 40.01±8.11 37.56±4.52 15.81±2.02对照组(n=40)42.20±4.56 43.02±4.81 155.02±11.94 36.48±5.04 219.92±29.87 39.52±8.64 37.65±4.37 20.58±2.43 0.049 0.114 0.080 1.741 0.088 0.262 0.091 9.547 0.961 0.909 0.936 0.043 0.930 0.794 0.928 0.000
2.4 用药安全性分析
观察组,患者用药治疗后共22例出现血液系统异常反应,3例出现胃肠道反应,8例出现流感样症状;对照组40例患者用药治疗后3例出现头晕反应,2例出现胃肠道反应。观察组不良反应总发生率显著高于对照组,差异有统计学意义(P<0.05),见表4。

表4 两组不良反应总发生率对比 例(%)
3 讨论
慢性乙型肝炎急性发作是临床治疗常见病,该病属于HBV感染引起的传染性疾病,该病具有起病急、病情进展快的特点,患者发病后肝功能损害程度严重,疾病进展后自身生命安全也可能受到严重威胁[7-8],因此及时对患者病情进行诊断,并制定合理治疗方案显得尤为重要。目前临床针对慢性乙型肝炎患者具有多种治疗方案,其中以恩替卡韦和替诺福韦等核苷/核苷酸类抗病毒治疗方案最为常见[9]。由于核苷类药物抑制病毒见效快、副作用小,常被用于慢性乙型肝炎急性发作的患者。但是同其他核苷类一样,恩替卡韦与替诺福韦同样存在低HBeAg血清学转换、停药后病毒反弹、耐药、长期用药有增加肾损伤、骨质疏松、肌酸激酶升高等不良事件的风险[10-12],因此,有必要探索更佳的治疗方案。
研究结果表明:联合用药方案所获得的临床疗效明显优于单一用药方案;联合用药治疗可提高患者HBeAg血清学转化率和HBV-DNA转阴率,使得患者肝功能指标显著改善,但联合用药同样显著提高了患者不良反应发生率。为进一步探讨上述治疗方案临床应用优势,我们参考了其他研究结论进行综合分析:目前临床针对慢性乙型肝炎患者的治疗多以抗病毒为主,而诸多抗病毒药物在初次使用后虽能较好缓解患者临床症状,但普遍存在低HBeAg血清学转化率、疗效不持久、需要长期用药和耐药等问题[13]。本次研究中所采用的替诺福韦属于一种核苷酸类逆转录酶抑制剂,其对多种病毒均具有显著的抵抗作用,该药物在进入患者机体后可使病毒聚合酶的产生受到抑制,同时还能进入病毒DNA中对其DNA复制产生抑制作用,起到抑制病毒复制、阻止疾病进展的作用。替诺福韦本身具有较好的水溶性,在进入机体后生效时间短,并在短时间内可达到血药峰值,最大程度提高药物利用率[14]。除此之外,有学者[15]研究中指出,替诺福韦在抵抗HBV病毒上具有重要作用,且不会出现耐受情况,因此通常可作为慢性肝炎患者耐药情况发生后的补救治疗药物。但事实上,单独应用替诺福韦进行临床治疗所获得的效果仍旧存在局限性,部分患者在经替诺福韦治疗后,仍然出现病情进展的现象,病情控制并不显著,故此次研究考虑加用干扰素与替诺福韦联合用药治疗。
研究结果显示,观察组联合用药后肝功能TBIL指标水平改善程度显著优于对照组,推测造成该项结果的原因为:研究所采用的聚乙二醇干扰素α-2a是目前临床公认的抗乙型肝炎重要药物,其主要通过提高机体免疫能力而起到清除病毒的作用。该药物在进入患者机体后可直接阻碍病毒基因的复制与表达,再通过对患者机体免疫能力进行调节,实现双链抗病毒作用。聚乙二醇干扰素α-2a的应用显著提升了常规药物抗病毒的效果,避免了肝炎病毒大量产生对患者肝功能造成严重损伤,因此可以说聚乙二醇干扰素α-2a的应用对患者肝功能改善价值重大。另外,研究发现,联合用药方案的应用增加了患者不良反应发生风险,因此针对此类患者需密切监视,一旦发现患者出现明显不良反应需及时进行处理,最大程度提升其临床用药安全程度。最后,我们对联合用药后HBV-DNA转阴率进行统计,结果提示,观察组HBV-DNA转阴率高于对照组,推测造成该项结果的原因为:聚乙二醇干扰素α-2a的应用显著提升了常规药物抗病毒的效果,不仅抑制病毒复制,对肝细胞内的共价闭合环状DNA(cccDNA)也能起到清除作用,在机制上补充了替诺福韦抗病毒的不足,随着治疗时间延长,患者HBV-DNA转阴率也呈现出明显提升趋势。
综上所述,干扰素与替诺福韦在慢性乙型肝炎急性发作患者临床治疗中的应用价值较高,联合用药方案除具有较高的临床应用安全性外,还具有临床疗效、改善患者肝功能的作用,患者经治疗后HBeAg血清学转化率、HBV-DNA转阴率较高,治疗结局及预后改善价值较大,可考虑临床推广应用。
