不同手术方案对脊髓型颈椎病合并椎管狭窄症患者术后疗效及颈椎矢状位参数的影响
2020-06-30彭爱明
刘 果,俞 勇,刘 辉,阮 翔,张 聃,彭爱明
咸宁市中心医院(湖北科技学院附属第一医院)脊柱外科,咸宁 437100
脊髓型颈椎病(CSM)是骨科常见疾病之一,超过30%的此类患者合并颈椎椎管狭窄症[1]。目前临床上对CSM 合并椎管狭窄症多推荐手术治疗,以前路椎体次全切除术和后路椎管扩大椎板成形术最为常用。相关回顾性研究结果提示,以上2 种手术方案在改善患者肢体活动及神经功能方面效果令人满意,但后路手术导致的颈部软组织复合体损伤可引起矢状位失代偿,进而导致后凸畸形,严重影响患者生活质量[2-3]。已有研究证实,脊柱特别是颈椎矢状位状态是影响身体平衡及视野水平的关键因素,同时矢状位平衡(SVA)受损还可诱发腰腿疼痛等多种症状[4]。本研究旨在探讨前路椎体次全切除术和后路椎管扩大椎板成形术治疗CSM 合并椎管狭窄症的术后疗效及对颈椎矢状位参数的影响,为手术方式的选择提供参考。
1 资料与方法
1.1 临床资料
纳入标准:①符合CSM 及椎管狭窄症诊断标准[5];②病变累及节段≥2 个;③年龄18 ~ 75 岁;④采用前路椎体次全切除术或后路椎管扩大椎板成形术治疗;⑤患者及家属知情同意。排除标准:①既往颈椎手术史;②合并严重骨质疏松;③颈椎畸形;④随访资料不全。本研究经医院伦理委员会批准(2010 科研第3 号)。根据以上标准,纳入2010年3 月—2015 年8 月收治的CSM 合并椎管狭窄症患者147 例,其中80 例采用前路椎体次全切除术治疗(A 组),67 例采用后路椎管扩大椎板成形术治疗(B组)。A 组男51 例、女29 例,年龄(52.84±6.21)岁,双节段病变57 例、三节段病变23 例;B 组男44 例、女23 例,年龄(53.10±6.24)岁,双节段病变50 例、三节段病变17 例。2 组一般资料比较差异无统计学意义(P > 0.05),具有可比性。
1.2 治疗方法
前路椎体次全切除术[6]:在全身麻醉下,患者取仰卧及颈部自然后伸位,于颈前外侧切开,清除椎体相邻椎间盘及病变髓核至后纵韧带;切除椎体骨质但保留椎体后壁(厚约2 mm),有效扩大减压椎间隙,切断后纵韧带后摘除脱出髓核;将填有碎骨的钛网装入减压槽,与椎体后壁紧密结合后行钢板固定。
后路椎管扩大椎板成形术[7]:在全身麻醉下,患者取俯卧位,行后正中纵切口,剥离暴露棘突、椎板及关节突内侧;开槽位置在椎板关节突内侧缘,仅保留门轴侧内层皮质,将开门侧椎板掀至门轴侧再行小钢板固定。
1.3 观察指标[5]
术后随访18 ~ 27个月,中位随访时间为24.3个月。采用日本骨科学会(JOA)评分[8]对肢体活动及神经功能进行评价。由2位对本研究方案不知情的医师在MRI上测量Cobb角、SVA及T1倾斜角。Cobb角为C2与C7椎体下缘连线间的夹角,SVA为C1前结节和C7椎体后上角两者垂线间的距离,T1倾斜角为T1椎体上缘连线与水平线间夹角。T1倾斜角≥25°的患者归入高T1倾斜角亚组,T1倾斜角< 25°的患者归入低T1倾斜角亚组。后凸畸形判定标准为Cobb 角 < 0°。
1.4 统计学处理
应用SPSS 24.0 软件对数据进行统计学分析。符合正态分布的计量资料以表示,组间比较采用t 检验;计数资料以例数和百分数表示,组间比较采用χ2检验或Fisher 确切概率法;以P < 0.05 为差异有统计学意义。
2 结 果
2 组末次随访JOA 评分和Cobb 角均高于术前,差异有统计学意义(P < 0.05,表1)。A 组术后SVA低于术前,差异有统计学意义(P < 0.05,表1),B 组术后SVA 与术前相比差异无统计学意义(P > 0.05)。A 组术后JOA 评分和Cobb 角均高于B 组,SVA 低于B组,差异均有统计学意义(P < 0.05,表1)。A组中,高T1倾斜角亚组和低T1倾斜角亚组JOA 评分改善效果和后凸畸形发生率比较差异无统计学意义(P > 0.05,表2);B 组中,低T1倾斜角亚组JOA 评分改善效果和后凸畸形发生率优于高T1倾斜角亚组,差异均有统计学意义(P < 0.05,表2)。典型病例影像学资料见图1,2。
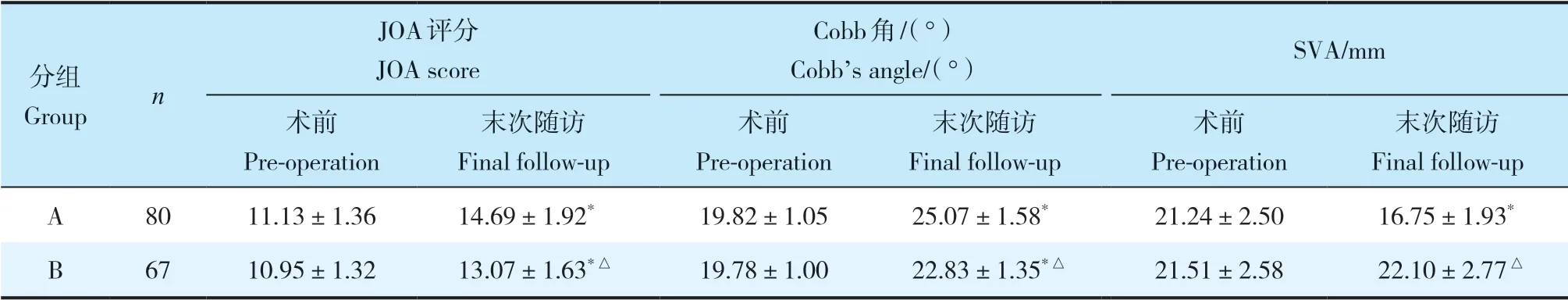
表1 2组手术前后JOA 评分、Cobb角和SVATab. 1 JOA score,Cobb’s angle and SVA before and after surgery in 2 groups
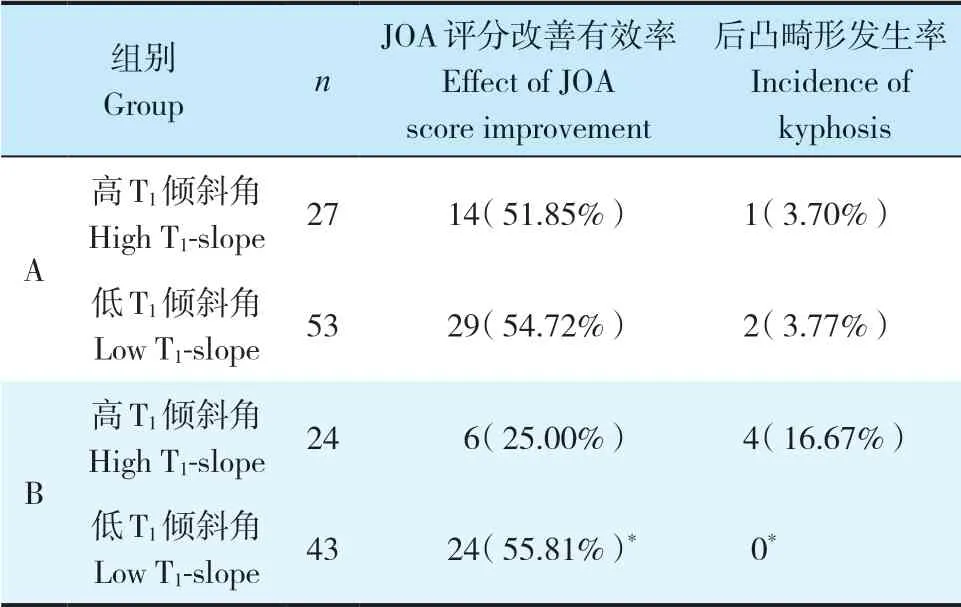
表2 2组不同T1倾斜角亚组JOA评分改善效果和后凸畸形发生率Tab. 2 JOA score improvement effect and incidence of kyphosis in high- and low-T1-slope subgroup in 2 groups
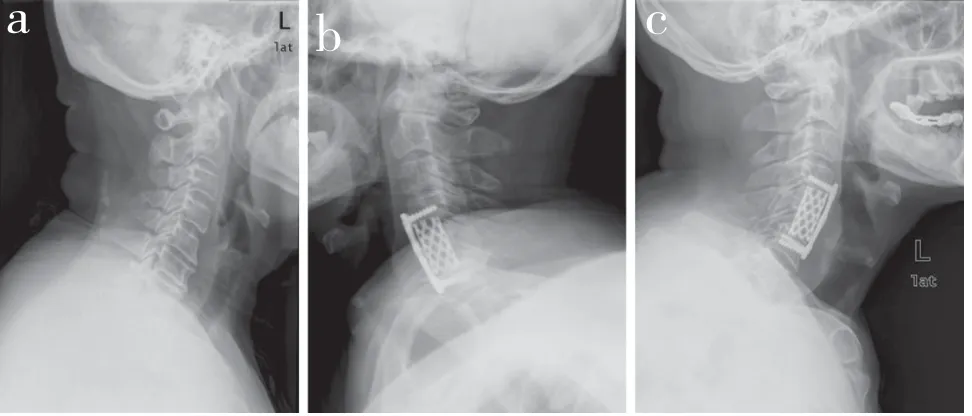
图1 A 组典型病例影像学资料Fig. 1 Imaging data of a typical case in group A
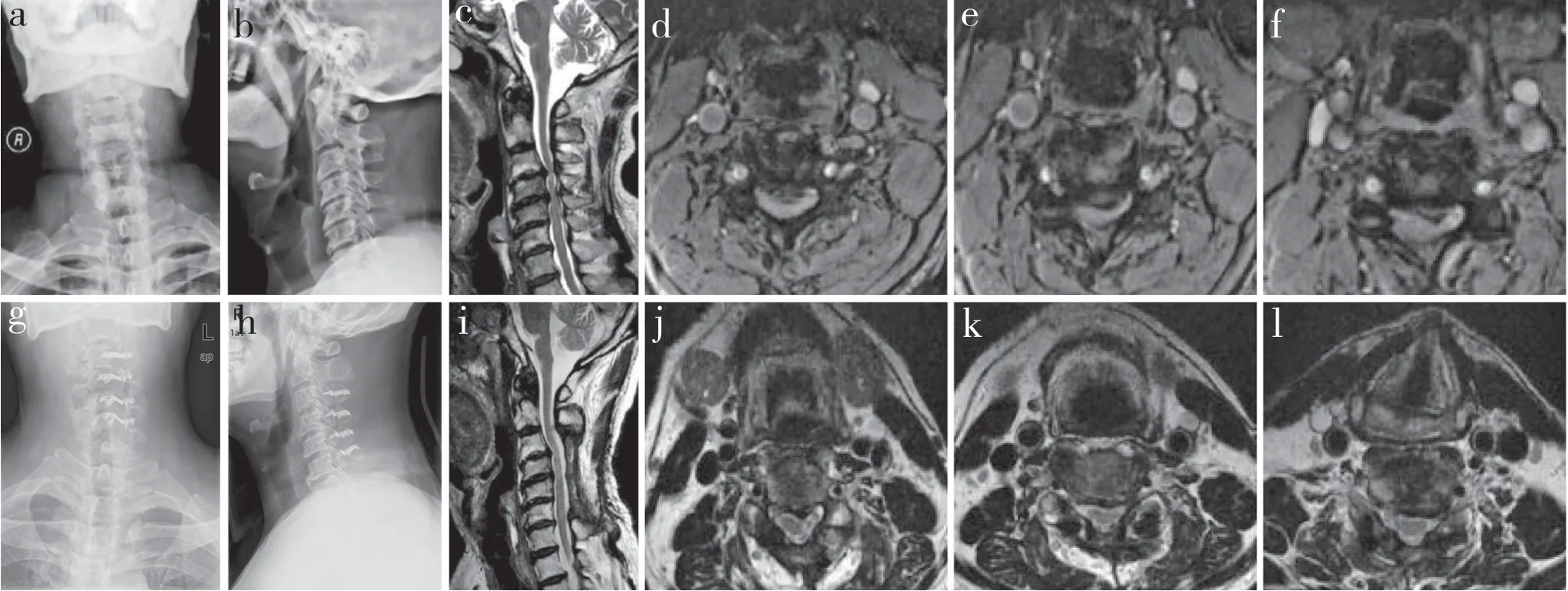
图2 B 组典型病例影像学资料Fig. 2 Imaging data of a typical case in group B
3 讨 论
近年来,国外学者提出采用SVA 对颈椎手术疗效进行评价,并逐渐获得医学界的认可[9]。已有研究显示,颈椎手术对于颈椎曲度的重建及周围肌肉-韧带复合体的损伤较易引起术后颈椎矢状位失衡,进而导致颈椎曲度变直、后凸畸形等问题,不利于颈椎功能及远期生活质量改善[10]。近年来,前路椎体次全切除术和后路椎管扩大椎板成形术均被用于CSM 及椎管狭窄症的临床治疗,但两者对于SVA 的影响有无差异尚有待证实[11]。
已有研究提示,颈椎术后矢状位失衡是诱发术后疼痛及功能受限的关键原因;而SVA 与术后功能恢复预后密切相关,其术后重建及维持备受国内外学者的关注[12]。既往采用胸椎后凸角对颈椎曲度进行评价,但往往难以解释术后实际颈椎曲度的变化;在此基础上,颈椎矢状位参数开始进入人们的视野,其中SVA 已被证实能够准确反映颈椎矢状面是否平衡[13]。本研究发现,前路椎体次全切除术后JOA 评分和Cobb 角水平均高于后路椎管扩大椎板成形术,SVA 水平低于后路椎管扩大椎板成形术,证实前路手术治疗CSM 合并椎管狭窄症在促进颈椎活动功能和生理曲度恢复、维持矢状位平衡状态方面更具优势。
国外学者报道显示,T1倾斜角与SVA 相关性最高,可被用于评估颈椎矢状位是否平衡[14-15]。T1作为颈椎底座,其倾斜度与颈椎前倾角具有明确相关性,当颈椎前倾过多时人体被动通过过伸颈椎实现颈椎前倾,代偿并维持视线水平,T1倾斜角≥25°者应保持较大的颈椎前凸曲度及肌肉负荷以避免颈椎矢状位失衡,但手术治疗后因颈椎后方软组织结构和功能遭到破坏,矢状位的平衡失代偿及远期颈椎后凸改变风险显著增加[16]。术前T1倾斜角对于后路手术后神经功能恢复影响已被证实,高 T1倾斜角者总体疗效逊于低T1倾斜角者,即T1倾斜角较高者行后路手术需谨慎,应综合评价选择更为合适的其他术式以改善临床预后[17-19]。
本研究发现,行前路椎体次全切除术治疗的患者,高T1倾斜角者和低T1倾斜角者JOA评分改善效果和后凸畸形发生率无显著差异;而行后路椎管扩大椎板成形术治疗的患者,低T1倾斜角者JOA 评分改善效果和后凸畸形发生率均优于高T1倾斜角者。上述结果表明,CSM 合并椎管狭窄症患者行前路手术治疗时其总体疗效并未受术前T1倾斜角影响,而后路手术中高T1倾斜角者预后更差。结合相关文献分析,笔者认为前路手术对相关椎体软组织损伤较小,经钛网和钢板塑形后能够纠正颈椎生理曲度、提高颈椎稳定性,更有助于预防颈椎矢状位失衡出现[20-21]。提示临床医师术前应注意评估患者T1倾斜角,对于≥25°者,为有效缓解术后矢状位的平衡失代偿需尽量选择前路手术。
综上所述,相较于后路椎管扩大椎板成形术,前路椎体次全切除术治疗CSM 合并椎管狭窄症具有更佳的临床疗效,且有助于改善颈椎SVA;同时对于高T1倾斜角的患者,应尽可能采用前路椎体次全切除术治疗。但本研究纳入样本量相对较少、且为单中心研究,所得结论尚有待更大规模随机对照研究证实。
