血清CEA、CA19-9、CA242对结直肠癌转移及预后的评估价值
2020-06-29王奇龙陈南征吕铁升
王奇龙,陈南征,吕铁升
结直肠癌是我国发病率位居第3位的恶性肿瘤,据国家癌症中心发布的最新数据显示,我国结直肠癌的发病率为9.88%,相比于往年有明显增长趋势[1]。尽管目前结直肠癌的5年生存率有了很大提高,但这一数据在近十年来少有突破,究其原因为结直肠癌患者就诊时疾病已发展至晚期,且治疗后复发、转移率较高[2-3]。肿瘤标志物是恶性肿瘤的诊断参考指标,已被广泛应用于恶性肿瘤的临床诊断。癌胚抗原(CEA)、糖类多肽抗原19-9(CA19-9)、糖类多肽抗原242(CA242)是临床常用的恶性肿瘤标志物,在结直肠癌诊断中有较高的应用价值[4-6],但其对结直肠癌转移、预后的评估价值仍有待进一步研究证实。本研究收集了行结直肠癌手术治疗患者的临床资料,测定患者血清CEA、CA19-9、CA242水平,并进行术后随访,探讨各血清肿瘤标志物对结直肠癌患者术后转移及预后的预测价值,旨在为结直肠癌的术后治疗、预后评估提供参考。具体内容报告如下。
1 资料与方法
1.1一般资料 选择2014年2月—2017年1月于西安交通大学第一附属医院接受手术治疗的325例结直肠癌患者作为研究对象。①纳入标准:年龄≥18岁;经临床、病理学检查明确诊断为结直肠癌,均行结直肠切除术;临床资料以及随访资料均完整。②排除标准:合并其他恶性肿瘤者;并发感染、糖尿病、高血压病等全身性疾病者;临床或随访资料不完整者。根据结直肠癌患者是否出现转移分为转移组和未转移组。
1.2方法
1.2.1资料收集:查阅电子病历,收集患者的一般资料(年龄、性别、家族史等)以及临床资料(肿瘤部位、肿瘤直径、分化程度、临床分期、浸润深度等)。
1.2.2血清学检查:采集术前晨起空腹静脉血,离心分离血清,CEA、CA19-9、CA242采用蛋白芯片检测试剂盒进行测定,检测试剂盒均购自上海数康生物科技有限公司,检测严格按照试剂盒说明书进行操作。检测指标参考值:CEA<5.0 μg/L、CA19-9<35 kU/L、CA242<20 kU/L为阴性,超过上述参考值为阳性。
1.2.3术后随访:术后对所有患者进行随访,以门诊随访为主,随访检查项目主要包括血常规、血清肿瘤标志物、肺部CT、腹部增强CT及肠镜检查。总生存时间为患者手术时间至随访死亡、失访或最后1次随访时间。

2 结果
2.1患者临床资料及术后转移情况 本研究共入组325例结直肠癌患者,其中男186例,女139例;年龄23~75(57.41±10.27)岁;肿瘤位于直肠174例,位于结肠151例;肿瘤直径≤5 cm者188例,>5 cm者137例;病理浸润深度:黏膜和肌层62例,浆膜55例,全层208例;分化程度:高分化28例,中分化267例,低分化30例;术前血清CEA浓度为(14.02±4.12)μg/L,阳性率为64.92%(211/325);术前血清CA19-9浓度为(39.68±10.24)kU/L,阳性率为30.15%(98/325);术前血清CA242浓度为(54.75±14.71)kU/L,阳性率为52.00%(169/325);共有152例患者出现转移,其中肝脏转移42例,淋巴结转移109例。
2.2血清学指标比较 转移组血清CEA、CA19-9、CA242水平显著高于未转移组(P<0.01)。见表1。

表1 转移组和未转移组结直肠癌患者的血清CEA、CA19-9和CA242水平比较
注:CEA为癌胚抗原,CA19-9为糖类多肽抗原19-9,CA242为糖类多肽抗原242
2.3血清CEA、CA19-9、CA242单独或联合预测结直肠癌患者术后转移的价值 ROC曲线分析结果显示,血清CEA、CA19-9、CA242单独预测结直肠癌患者术后转移的曲线下面积(AUC)分别为0.799、0.678、0.750,其中CEA预测效能最高;CEA+CA19-9、CEA+CA242、CA19-9+CA242以及三者联合预测结直肠癌患者术后转移的AUC分别为0.830、0.870、0.807、0.895,三者联合预测效能最高。见图1、2和表2。

图1 CEA、CA19-9、CA242单独预测结直肠癌患者术后转移的ROC曲线
CEA为癌胚抗原,CA19-9为糖类多肽抗原19-9,CA242为糖类多肽抗原242
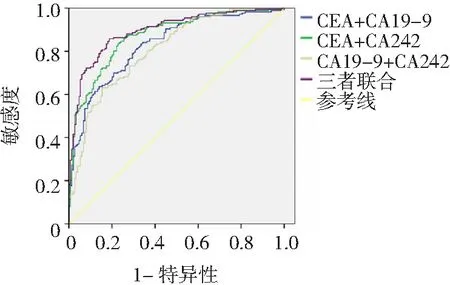
图2 CEA、CA19-9、CA242水平联合预测结直肠癌患者术后转移的ROC曲线
CEA为癌胚抗原,CA19-9为糖类多肽抗原19-9,CA242为糖类多肽抗原242

表2 CEA、CA19-9、CA242水平单独或联合预测结直肠癌患者术后转移的价值
注:CEA为癌胚抗原,CA19-9为糖类多肽抗原19-9,CA242为糖类多肽抗原242
2.4血清CEA、CA19-9、CA242与结直肠癌患者预后的关系 所有入组患者的随访截止时间为2019年12月,随访时间为7~62个月,中位随访时间为32个月。经Kaplan-Meier法绘制生存曲线及Log-rank检验分析结果显示,血清CEA阴性、CA19-9阴性以及CA242阴性结直肠癌患者的总体生存率均显著高于血清CEA阳性、CA19-9阳性以及CA242阳性的患者,差异有统计学意义(P<0.05)。见图3~5。

图3 CEA阳性和阴性结直肠癌患者Kaplan-Meier生存曲线
CEA为癌胚抗原

图4 CA19-9阳性和阴性结直肠癌患者Kaplan-Meier生存曲线
CA19-9为糖类多肽抗原19-9

图5 CA242阳性和阴性结直肠癌患者Kaplan-Meier生存曲线
CA242为糖类多肽抗原242
2.5结直肠癌患者的预后影响因素分析 经多因素Cox模型分析显示,在矫正肿瘤直径、分化程度、术后转移、化疗等因素后,血清CEA、CA19-9、CA242阳性均为影响结直肠癌患者预后的独立危险因素(P<0.05或P<0.01)。见表3。
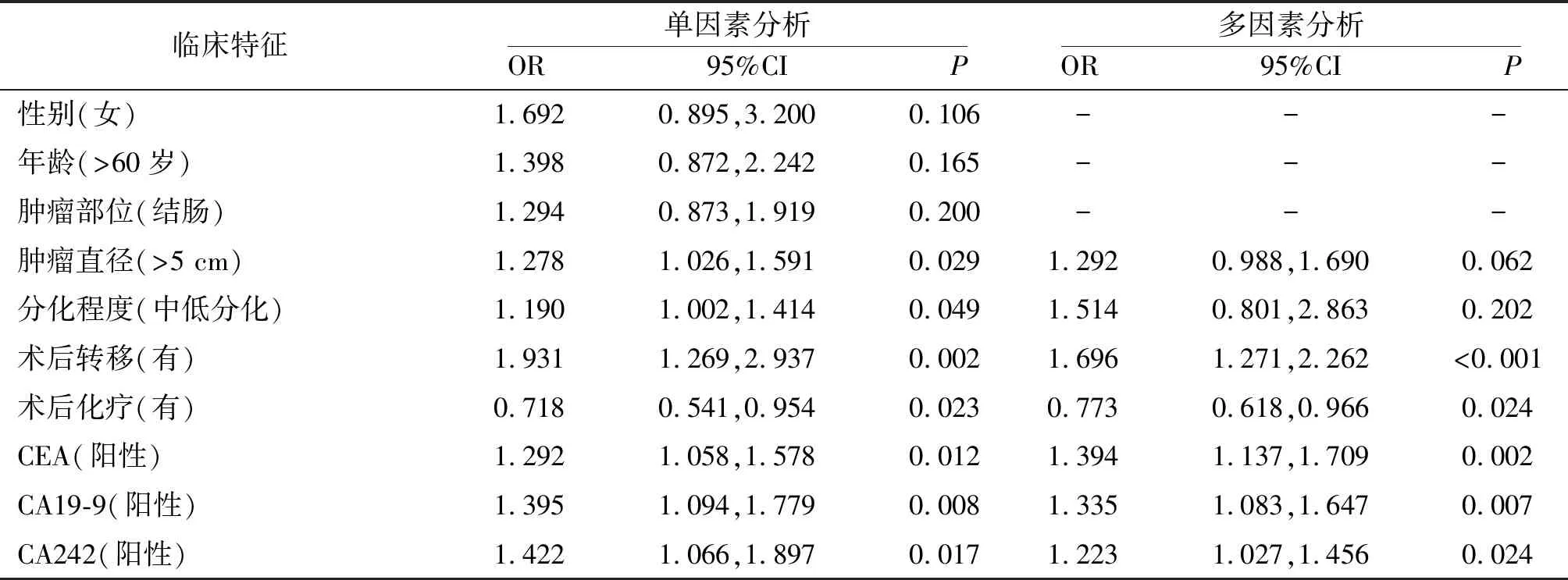
表3 影响结直肠癌患者预后的单因素和多因素Cox模型分析
注:CEA为癌胚抗原,CA19-9为糖类多肽抗原19-9,CA242为糖类多肽抗原242
3 讨论
肿瘤标志物临床应用的基本原理为这些标志物在恶性肿瘤中具有较高的表达,释放入血后可引起血液中分子浓度的升高,通过检测这些分子的水平即可为临床诊断提供参考。目前认为,恶性肿瘤转移、复发、预后情况与肿瘤负荷、侵袭性等密切相关,检测这些肿瘤标志物水平或可为患者病情、复发、转移的临床评估提供一定参考[7-9]。本研究结果显示,发生肝脏转移及淋巴结转移的结直肠癌患者血清CEA、CA19-9、CA242水平较高,提示上述肿瘤标志物水平可能与结直肠癌患者术后复发相关。CEA是一种具有胚胎抗原决定簇的大分子酸性蛋白,在内胚层来源的恶性肿瘤中均可检出[10-11]。国内有研究证实,高水平CEA表达与结直肠癌患者转移具有相关性[12]。CA19-9是一种神经节糖苷酯,属于类黏蛋白糖蛋白,但该分子识别谱相对较窄,在结肠癌诊断中特异度不理想[13]。CA242是一种唾液酸化黏蛋白脂类抗原,在多种恶性肿瘤患者血液中均能检出,在诊断方面的特异度不佳[14]。既往刘以俊等[15]研究证实,血清CEA、CA19-9水平与原发性十二指肠癌患者的分化程度、淋巴结转移、远处转移等均显著相关。刘启志等[16]研究证实,术前CEA、CA19-9水平是影响直肠癌患者生存预后的独立因素,但并非患者复发的独立因素。本研究与前者研究结果类似,与后者研究结果有一定差异的原因可能为患者病情差异及血清指标检测水平差异所致。本研究结果显示,血清CEA、CA19-9、CA242单独预测结直肠癌患者术后转移的AUC分别为0.799、0.678、0.750,其中CEA预测效能最高;CEA+CA19-9、CEA+CA242、CA19-9+CA242、三者联合预测的AUC分别为0.830、0.870、0.807、0.895,其中三者联合预测效能最高。提示在临床应用中可结合多种指标进行预测及评估,从而指导结直肠癌患者的临床治疗[17]。
本研究结果还显示,血清CEA、CA19-9、CA242阴性患者总体生存率显著高于阳性患者,提示较高的血清CEA、CA19-9、CA242水平或预示不良的预后;多因素Cox模型分析也提示,在矫正其他与预后相关的因素后,血清CEA、CA19-9、CA242阳性患者预后不良风险分别是阴性患者的1.394、1.335、1.223倍,这一结果与刘启志等[16]、张鑫东等[18]提出的血清CEA、CA19-9是影响结直肠癌患者生存时间的危险因素的结论类似,可能原因为血清CEA、CA19-9、CA242水平与肿瘤负荷、病情分期相关,较高水平提示患者病情处于中晚期阶段,必然会导致患者预后欠佳。
综上所述,血清CEA、CA19-9、CA242与结直肠癌患者术后转移及预后密切相关,上述指标可单独或联合用于评估患者术后转移风险及预后情况,在一定程度指导术后的辅助治疗,帮助改善患者预后。本研究局限性在于样本量较小,且缺乏对患者术后饮食、其他治疗情况资料的分析,这些因素也可能对患者转移、预后造成一定影响,未来仍有待进一步扩大样本量进行研究。
