基于生活情境的探究式教学
——以“乙醇的催化氧化反应”教学为例
2020-06-22广东夏娜娜
◇ 广东 夏娜娜
化学是一门贴近生活,改善生活的学科,具有实用性和创造性,也就是我们所说的来自于实际生活,又改善了我们的生活.但是有些高中化学老师对化学这门学科的教学理念缺乏正确的认识,片面地重视理论教学,忽略了它的实用性,导致化学课堂枯燥乏味.当自主选科的新高考政策实施后,如果教师的教学方式仍然不改变,会使更多的学生选择放弃化学,因此教学方式的转变迫在眉睫.我们可以利用化学这门学科的实用性、创造性特点,将抽象、精深、复杂的知识融于实际的生活,通过创设熟悉的情境,逐步启发学生思考、猜想、探究,在探究中构建知识体系.这样的探究式教学不仅仅将知识传达给了学生,还提高了学生对化学学习的积极性,更培养了学生的动手能力和创新能力,并且整个课堂教学中学生参与度很高.当学生真正成为课堂的主人,他们就会对这个科目的学习充满兴趣.本文是通过对情境问题的探究来构建知识体系并应用于实际的教学模式讲解乙醇的催化氧化反应.
1 教材分析
在人教版的化学课本中,这一节的标题叫作“生活中两种常见的有机物”,从题目就可以看出乙醇、乙酸这两种物质与实际生活联系非常紧密.这一节可以分为3个课时,其中乙醇的学习需要2个课时.第一课时围绕乙醇的物理性质和结构进行探究,第二课时是对乙醇催化氧化反应的探究.第二课时是这一整节的重点和难点.在第一课时的讲解中,教师可以用“我国的酿酒技术与文化”的相关视频作为导入,也可以通过一些谚语,如“酒香不怕巷子深”等讲述乙醇的相关性质.以生活现象作为乙醇章节学习中激趣、引课环节的情境具有合理性.在“乙醇的催化氧化反应”课时教学中,如何创造情境引入教学能将实用性和创造性结合起来,如何将孤立的知识与生活实际相结合,引发学生思考创新,这是本文论述的重点.
2 设计思路
设计流程见图1.

图1
3 教学过程
3.1 根据生活实际创设情境,体现化学的实用性
【视频展示】 喜庆的春节,某条大路上出现一抹忙碌而又可爱的身影,交警叔叔要求司机对着手里的仪器吹气.这是交警叔叔在查酒驾.
【问题】 为什么要查酒驾呢?酒驾有什么危害呢?各小组讨论后回答.
【第一组回答】 因为喝酒后会头晕、呕吐、脸色发红,并且大脑会不受控制,为避免酒后驾驶发生车祸所以交警才会查酒驾.猜测出现以上现象的原因可能是酒精在体内发生了化学变化,生成了其他物质导致的.
【知识拓展】 乙醇进入体内后,在肝脏中乙醇脱氢酶的作用下转化成乙醛,乙醛又会被乙醛脱氢酶催化转化成二氧化碳和水.但是由于肝脏中的乙醛脱氢酶的量有限,当饮酒过量时,酒精变成了乙醛存在体内.乙醛会使人产生头晕、头痛、呕吐等中毒症状.

【结论】 喝过多的酒会有损健康,酒驾更不可取.
【评价】 根据生活实际创设情境,既体现了化学的实用性,也激起了学生的学习兴趣,并且为讲述乙醇的催化氧化反应做了铺垫.
【过渡】 在人体内存在乙醇脱氢酶,可以使乙醇变成乙醛,那我们在实验室怎样将乙醇变成乙醛呢?
3.2 创设实验情境,由现象引发思考
【实验探究】 请同学们取出两根大小相同洁净的螺旋状铜丝,将铜丝分别放在酒精灯外焰和内焰上加热.
【问题】 铜丝在酒精灯的外焰和内焰加热产生的现象一样吗?请同学们仔细观察并提出猜想.
【第二组同学回答】 猜想1:现象不同,外焰加热后铜丝变黑色,内焰加热后铜丝依旧是红色,可能是因为外层的氧气比较充足发生了氧化反应,而内焰氧气不充足,所以没有发生氧化反应.
【第三组同学回答】 猜想2:现象不同,可能因为外焰温度比较高,促使Cu氧化成了CuO,而内焰温度比较低,所以没有发生此反应.
【第四组同学回答】 猜想3:根据乙醇在体内酶的作用下可以变成乙醛,而酶是一种催化剂.由于乙醇易挥发,内焰上乙醇的浓度比较大,而实验过程中内焰铜丝没有变化,联想到催化剂的性质,所以猜测铜丝应该和乙醇脱氢酶一样作了催化剂.
【教师】 每个组都提出了猜想,请各组设计实验验证自己的猜想.
【验证猜想1】 设计实验证明铜丝在外焰和内焰加热后产物不同是由于外焰、内焰氧气浓度导致的.
【设计实验】 将铜丝置于不同浓度的氧气中,加热.
【结论】 铜丝均变黑色,猜想1不正确.
【验证猜想2】 设计实验证明铜丝在外焰和内焰加热后产物不同是由于外焰、内焰温度不同导致的.
【设计实验】 将铜丝放在火柴的外焰和内焰上加热后观察现象.
【结论】 发现铜丝均变黑色,那说明和外焰内焰没有关系,和加热的原料酒精有关系,既说明了猜想2不正确也证明了猜想1不正确.
【验证猜想3】设计实验证明酒精灯内焰加热后的铜丝没有变红是因为铜丝作了催化剂.
【问题】是否能根据二氧化锰催化过氧化氢的实验,将铜丝放入乙醇中加热来进行实验呢?
【回答】不可以,乙醇易燃,会引起火灾.
【继续启发】乙醇有哪些物理性质?是否可以加热铜丝呢?
【回答】乙醇易挥发,可以试着使低浓度的乙醇挥发到铜丝上,加热,观察铜丝是否变色.
【设计实验】经过尝试后发现图2实验操作方便,现象明显.
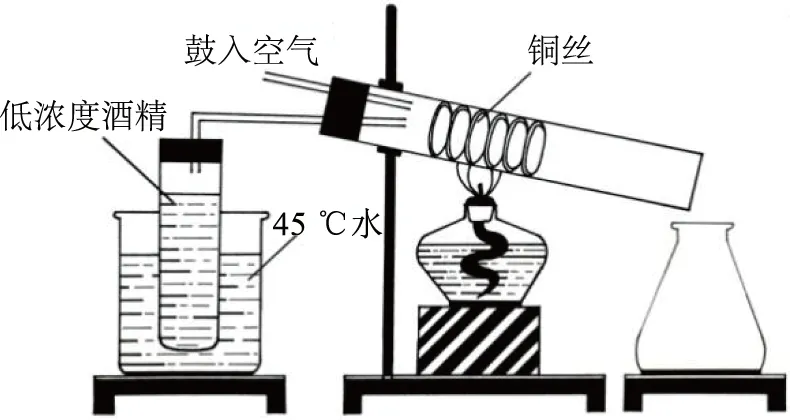
图2
【实验现象】加热铜丝,铜丝依旧是红色,同时产生有刺激性气味的油状液体.这个过程中发生了化学变化.
【学生代表总结】铜丝在空气中加热会生成氧化铜变成黑色,但是由于酒精易挥发,内焰酒精燃烧不充分,有大量乙醇存在,乙醇在铜丝的催化作用下会发生化学变化.催化剂反应前后性质不变,所以铜丝依旧是红色.具有刺激性气味的油状液体恰好符合乙醛的性质.
【评价】化学是一门以实验为主的自然科学,对于观察到的现象,启发学生提出猜想,引导学生再通过实验的方式验证猜想,提高学生的课堂参与度,使他们成为课堂的主人.
3.3 引入反应原理,用微观知识解释宏观现象
【过渡】 从刚才的现象中我们可以总结乙醇在铜的催化作用下变成了乙醛,那么这个反应究竟是怎么发生的呢?
【PPT展示】 利用动画展示乙醇变成乙醛的过程中H原子的轨迹,如图3所示.

图3
①
②
总反应方程式:

【评价】通过动画形象生动地模拟了乙醇催化氧化的具体过程,使得学生对断键位置以及反应原理清晰明了,记忆深刻,突破了本节学习的难点.
4 结合所学知识,解决生活问题
【提问】我们学习了乙醇的催化氧化,知道了Cu在乙醇的催化氧化过程中起到催化剂的作用,那么这个知识是否能应用到我们的生活中呢?
【学生回答】可以用来除铜锈.
【继续启发】哪个学生描述一下具体的做法呢?这种除铜锈的方法能不能推广?有没有缺点呢?
【学生回答】可以将铜锈放在酒精灯上加热.这种方法不能推广,因为在反应过程中会产生乙醛这种有刺激性气味的有毒物质.
【评价】学以致用,将学习的知识应用到解决实际生活问题中,充分体现了化学的实用性,也拓展了学生的思维,引导学生辩证地看待问题,善于思考问题的两面性.
5 反思
高中化学的特点是抽象、零碎、复杂.教师如果仅仅简单地将知识传授给学生,学生会觉得化学的学习很枯燥,再加上高中化学的抽象性,会使很多学生在学习化学的过程中比较吃力,慢慢地就失去了学习的积极性.这就要求教师在上课时,不能仅仅将知识单一地传达给学生,而是要尽可能地将教学内容以生活实际作为出发点,创设熟悉的情境,化抽象为具体,引发学生思考,提高学生对化学学科的兴趣,提高学生的课堂参与度.乙醇的催化氧化是乙醇章节的重点,本节课通过对生活中常见现象的思考,引发学生到对铜丝加热现象的探究,一步步启发学生完成了乙醇催化氧化知识的学习,构建了知识体系.整个教学过程彰显出新课标强调的“素养为本”的教学理念,将教学内容置于相关情境中,用情境作载体,引发思考,最后又将学习的知识应用到实际生活中,提高了学生在特定环境中解决化学相关问题的能力,也发展了学生各方面的素养.
