COVID-19疑似病例合并肝母细胞瘤多学科临床讨论
2020-06-19
目前新型冠状病毒肺炎(corona virus disease 2019,COVID-19)疫情依然严峻,全球病确诊病例数日益增长[1]。虽然有证据表明多数COVID-19患儿临床症状较成人轻,重症及危重症病例相对成人少,但危重患儿救治难度亦较大[2]。成人中有基础疾病的COVID-19患者危重症的发生率及死亡率较高[3],因此须警惕有严重基础疾病患儿的潜在死亡风险。肝母细胞瘤(hepatoblastoma,HB)是常见儿童恶性实体肿瘤,其恶性程度较高,若未及时规范的治疗,临床进展极快。而严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)感染则可能将肝母细胞瘤的诊治复杂化。现介绍2020年2月浙江大学医学院附属儿童医院收治的1例COVID-19疑似病例合并HB的多学科协作体系(multidisciplinary team,MDT)诊治过程,供儿科临床工作者参考。
1 材料与方法
1.1 临床资料
患儿女性,3岁6个月,因反复发热6天,发现肝占位4天于2020年2月收入浙江大学儿童医院,入院前患儿在湖北省襄阳市居住。发热,体温波动37.5~38.8℃,伴有腹胀、胃纳减少,无咳嗽,无气促,无呕吐、腹痛、腹泻等表现。体检:T 38.3℃,P1 25次/分,R 34次/分,BP 106/56 mmHg,神志清,精神可,皮肤黏膜略苍白,咽部充血,胸骨无压痛,呼吸平稳,双肺呼吸音粗,无明显干湿啰音,心音中等,心律齐,心率125次/分,腹部膨隆,右上腹包块可及,质地中偏硬,边界不清,脾肋下未及,全腹无压痛及反跳痛。神经系统病理征阴性,全身皮肤无皮疹。外院腹部+胸部CT检查显示:肝脏巨大占位性病变。患儿入院后第1、2、7、14天检测咽拭子、大小便SARS-CoV-2核酸均阴性;第1、7、14天SARS-CoV-2 病毒抗体阴性;2020年2月24日血常规显示:WBC为12.52×109/L,N为6.79×109/L,L为4.64×109/L,Hb为71g/L,PLT为375×109/L;CRP为112.6 mg/L,第13天复查CRP为37.51 mg/L;化疗后第1天血小板106×109/L,第2天降至37×109/L,行骨髓涂片未发现肿瘤细胞。予重组人血小板生成素治疗2天后血小板开始上升,住院第13天复查PLT为358×109/L;肿瘤标记物:AFP为173 151 ng/mL,神经元特异烯纯化酶65.41 ng/mL;血气、电解质、肝、肾功能及心肌酶谱无异常;本院行CT(胸部平扫+腹部增强)显示:肝右叶巨大占位性病变(图1),肝脏强化不均匀,下腔静脉受压推移,门脉周围积液,腹腔、盆腔、双侧胸腔(右侧为主)积液,右肺上叶磨玻璃影(图2);超声:肝脏巨大占位,双侧胸腔、腹腔积液,心脏结构正常。入院第13天复查B超:未见胸腔及腹腔积液,肝脏巨大包块同前。
1.2 治疗方案
化疗方案:C5V方案:顺铂(CDDP),第1天;5-氟脲嘧啶(5-FU),第2天;长春新碱(VCR),第2天。其他治疗:重组人血小板生成素升血小板;头孢噻肟抗感染7天;复合辅酶保护心肌;帕洛诺司琼止吐;碳酸氢钠碱化尿液及静脉补液。
2 结果
患儿化疗第2天出现血小板显著降低,经上述治疗后血小板逐步上升,化疗后第8天血小板升至正常范围。入院第13天血常规:WBC 4.51×109/L,N 1.26×109/L,L 2.53×109/L,Hb 76 g/L,PLT 358×109/L;CRP 37.51 mg/L。复查B超:未见胸腔及腹腔积液,肝脏巨大包块同前;多次咽拭子、大小便SARS-CoV-2 核酸及病毒抗体检测均阴性,排除SARS-CoV-2感染。共隔离治疗14天,住院1周后患儿体温恢复正常,精神胃纳转好,生命体征平稳,各项指标恢复良好,予出院并解除隔离,按计划进行后续治疗。
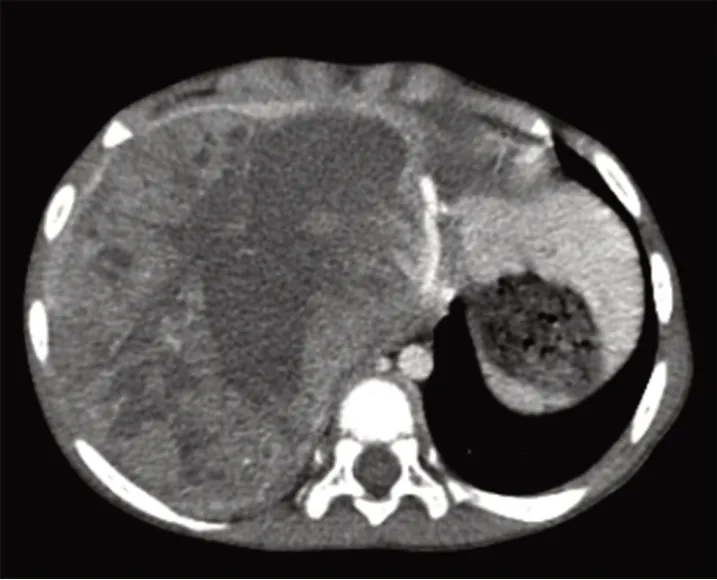
图1 腹部增强CT(右肝叶巨大占位)
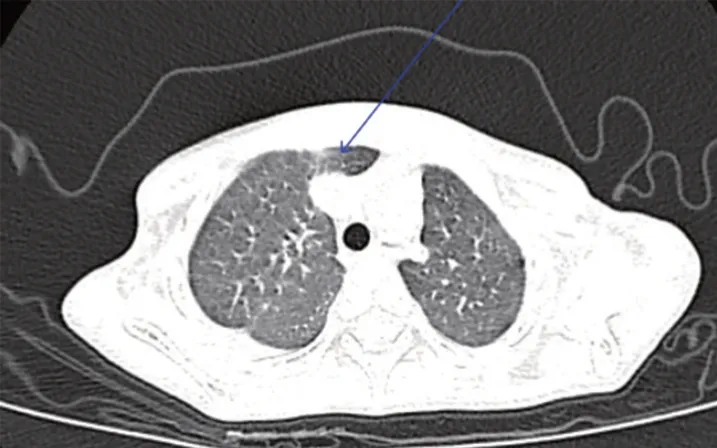
图2 肺部高分辨CT(右肺上叶少许磨玻璃影,箭头示病变部位)
3 讨论
COVID-19诊治专家组(感染科、呼吸科、重症医学科):对于COVID-19 的诊断需结合流行病学史和临床表现,参考《新型冠状病毒感染的肺炎诊疗方案(试行第六版)》[3]。本例患儿来自湖北省襄阳市,有发热,肺部CT提示右上肺磨玻璃影,符合方案中流行病学史第1条及临床表现的第1、2条,故诊断为COVID-19 疑似病例。纵观疫情,儿童COVID-19 的临床表现往往不典型,多以轻症或无症状感染为主[4-5],血常规中白细胞及淋巴细胞大多正常[6],因此对于有流行病学史的患儿应行全面的排查。
目前SARS-CoV-2 核酸检测仍然为确诊COVID-19 的主要手段,但由于患儿在取样过程多不配合,核酸假阴性更高。随着研究的不断深入,病毒血清学检测逐渐成为重要的补充手段,发病3~5 天抗体可出现。但儿童尤其是婴儿,由于其自身免疫特点,产生抗体的能力较正常成年人相对较弱,因此在对患儿进行检测时需要根据年龄以及基础疾病来评估,可能需要多次检测。儿童SARS-CoV-2感染的肺炎CT表现多样性,磨玻璃影不如成人典型,早期胸腔积液少见[7-8],大多数患儿临床症状轻,肺部病灶较少,往往诊断难度较大,需要对其肺部影像学表现慎重评估。结合本例患儿临床特点及病毒性监测结果,其胸部CT“胸腔积液及右上肺少许磨玻璃影”考虑为巨大瘤体挤压导致血液及淋巴回流障碍所致,最终排除SARS-CoV-2感染。
因巨大肿瘤消耗,本例患儿营养状况欠佳,血CRP 明显升高,存在细菌感染的可能性大,但在不明确是否存在SARS-CoV-2感染的情况下,为了防止病毒扩散,可暂不行血、痰及大小便培养等检测。患儿病程中无头痛、呕吐,无尿频尿痛,无腹泻等表现,体检见咽部充血,因此首先考虑为上呼吸道感染,给予广谱抗生素控制感染。同时需严密监测化疗后继发感染情况。
实体肿瘤MDT 组(包括肿瘤外科、肿瘤内科、放射科、超声科、病理科及介入治疗组):影像学检查在实体肿瘤的诊断中意义重大。腹部增强CT除了可以观察肿块的来源、密度以及强化方式是否符合典型的肝母细胞瘤外,还能观察门静脉、腔静脉等是否有瘤栓累及,判断肿瘤侵犯的肝段,是治疗前分期(PRETEXT 分期)以及危险度分组的基本依据[9-11]。胸部平扫在观察是否存在肺部感染的同时,还能判断是否有胸部转移病灶,也是临床分期和危险度分组的重要指标。超声检查可初步判断肿瘤性质,评估肝脏主要血管的受累情况[12]。此外,AFP水平升高为HB 重要的诊断标准之一,大多数HB 患者AFP 水平异常升高[9]。根据患儿临床症状表现、AFP异常增高及典型的影像学表现,临床诊断符合HB;肝脏关键血管无肿瘤侵犯,肺内无明确转移病灶,临床危险度分组为低危组。在活检存在极大风险时,根据中国抗癌协会小儿专业委员会推荐的诊疗专家共识建议,暂不行肿瘤活检,可根据临床诊断制定治疗方案[10]。同时,尽量减少手术和有创操作,避免医疗人员与患儿的接触和暴露,降低病毒传播风险。
化疗是儿童恶性实体肿瘤重要治疗手段之一,但化疗有客观存在的风险和并发症。而在化疗后导致免疫紊乱的基础上,若存在SARS-CoV-2感染可能更容易进展成为重症病例。疫情期间避免超大剂量化疗方案的应用,尽量减少易诱发重度骨髓抑制的化疗方案应用,以降低发生严重骨髓抑制的风险[13]。治疗过程中发生严重粒细胞减少或缺乏的患儿,可使用长效粒细胞刺激因子[14];出现严重血小板减低的患儿,可使用重组人血小板生成素,血小板<20×109/L时输注血小板;血红蛋白<60 g/L以下必须输注悬浮红细胞[9]。必要时也可以考虑适当减低化疗剂量,以保障特殊时期患儿的安全[13]。此外需密切监护可能出现的其他并发症,如消化道及泌尿系统不良反应、心肌损害、肝功能损害、继发感染等。本例患儿采用C5V 方案相对比较缓和,MDT 讨论后认为适合患儿目前状况。患儿首次化疗结束并完成隔离后可收入肿瘤科病房继续行3周化疗方案。
隔离病房:患儿由救护车接至隔离病房,进行单人隔离,由1名身体健康的家长陪护。为减少隔离期人员在院内的病毒传播风险,所有出入院手续可线上完成。进入隔离病房所有工作人员的防护措施严格按照《医疗机构内新型冠状病毒感染预防与控制技术指南(第一版)》[15]执行。尽可能利用远程会诊、视频及语音等形式及时联络相关科室,共同制定应急方案,从而减少医护人员进入隔离病房与患儿直接接触。本例患儿的多次MDT讨论、病情告知、化疗知情同意等均利用远程视频完成,不但降低了感染扩散风险,也减少了防护物资的消耗。此外,入院后需首先行病毒相关检测明确感染情况,以降低医务人员在之后的诊疗活动中受感染风险。血气机、心电图机、普通X 线及超声设备已在本院隔离病房配备,除超声外其他均由隔离病房医生在培训后使用,心电图及放射科医生电脑读片提供报告。对疑似患儿进行其他必要的实验室、CT检查时,人员防护及设备消毒严格参照相关管理条例执行[16-17]。陪护家长必须身体健康,入院前未接触除患儿外其他的疑似或确新冠状肺炎患者,陪护期间不得外出,并进行每日体温监测及定期病毒检测。
综上所述,疫情期间对于来源于疫情高发地的特殊疾病患儿的救治需要多个科室共同参与,相互配合完成,根据病情及疫情防控要求为患儿制定个体化诊治方案。为了防止院内病毒扩散,诊治过程的各个环节均需要提前制定预案,根据风险等级进行安全防护,在救治患儿的同时避免医务人员感染。
