废旧滤袋重金属元素成分分析及清洗技术研究
2020-06-15倪箐魏峰俞秋虹刘基俊陈宇岳
倪箐,魏峰,俞秋虹,刘基俊,陈宇岳
(1.苏州大学 纺织与服装工程学院,江苏 苏州 215123;2.无锡海关,江苏 无锡 214100;3.南京海关纺织工业产品检测中心,江苏 无锡 214100)
袋式除尘技术作为治理PM2.5污染的有效手段之一,已在电力、水泥、钢铁等重污染行业中得到广泛的应用[1],而因此产生的大量废旧滤袋的回收再利用过程却难以起步。究其原因,滤袋大多是由难以降解的多种合成化纤制成,使用后其表面及内部附着的粉尘含有大量重金属元素[2],相对于废旧服装、布料等的回收和利用[3-5],废旧滤袋的回收处理难度极高。目前大部分废旧滤袋主要采取填埋、焚烧等方法进行处理,不仅浪费资源,处理不当还易对环境造成污染[6-7]。因此,如果将其进行清洗处理,降低重金属含量,可以扩大再生料的使用范围,提高经济效益,促进废旧滤袋回收再利用。本文在分析了不同工况下废旧滤袋中所含有重金属元素的基础上,通过改变实验条件对其进行清洗,探讨更合理的化学清洗方式,为废旧滤袋的资源化利用提供参考。
1 实验部分
1.1 试剂与仪器
浓硝酸(65%~68%),优级纯;氢氧化钠,分析纯;废旧粉尘滤袋样品(表1)均为上海博格工业用布有限公司提供。

表1 测试样品Table 1 Test samples
iCAP电感耦合等离子体发射光谱仪(ICP-OES);Milli-Q水纯化系统;XS105电子天平;Multiwave PRO微波消解仪;SPH-310A台式通用大容量摇床。
1.2 实验方法
1.2.1 滤袋样品中重金属元素定性定量分析流程 取一定量实验样品,剪成5 mm×5 mm的碎片,称取每份(0.4±0.02)g样品,放入消解罐聚四氟乙烯内胆中,加入7 mL浓硝酸,盖好盖子,装入陶瓷套,放入微波消解仪中。消解条件为:10 min上升到100 ℃,保持5 min,15 min上升到220 ℃,保温25 min,再在30 min内快速冷却至室温,取出后赶走反应气体产物,完全转移至50 mL塑料容量瓶中,用超纯水冲洗聚四氟乙烯内胆内壁3次,并稀释至刻度定容,摇匀,过滤后移取清液于聚乙烯试管中,同时进行试剂空白实验,用ICP-OES测定重金属元素浓度。
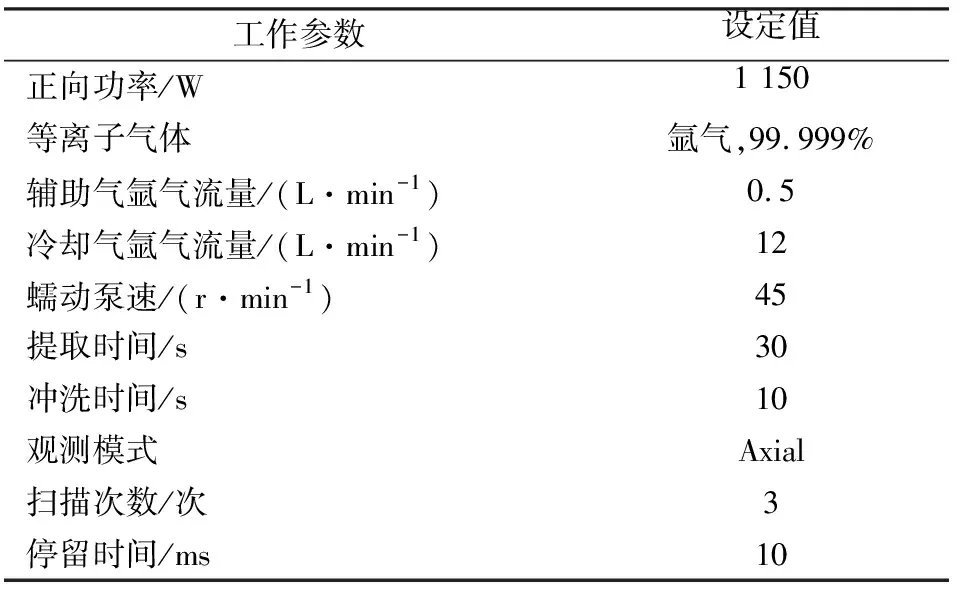
表2 ICP-OES测定条件Table 2 Test conditions for ICP-OES
1.2.2 滤袋清洗流程及清洗液中重金属元素含量分析 从滤袋样品上取10 cm2的实验样品,剪成5 mm×5 mm的碎片,放入锥形瓶中。分别将实验样品置于100 mL 2%,25%和50%硝酸溶液以及1 mol/L 和6 mol/L的NaOH溶液中,在室温下振荡清洗时间分别为1,2,4,24 h,摇床转速为120 r/min,过滤后移取清液于聚乙烯试管中,用ICP-OES测定清洗液中的重金属元素浓度。
1.3 清洗指标确定
本实验主要去除废旧滤袋样品中的重金属元素,故实验以振荡清洗后清洗液中的重金属元素含量以及清洗干燥后滤袋中残余的重金属元素含量为检测对象。定义清洗率(η,%)为清洗效果的量化指标。
其中,c1、c2分别为清洗前、后滤袋样品中所含有的重金属元素含量,mg/kg。
2 结果与讨论
2.1 废旧滤袋中重金属元素组分分析
采用ICP-OES对滤袋样品(表1)进行了重金属元素种类及含量的分析测试,结果见表3。
由表3可知,这些废旧滤袋中Hg、Cd元素含量均低于检出限,一部分原因是因为Hg、Cd相对其他重金属在飞灰中的富集程度较低,另一方面也表明各工厂污控设施运行对烟气中Hg、Cd的去除有一定的作用[8-9]。和其他样品相比,1#滤袋样品中各重金属元素含量较高,这可能是因为该废旧滤袋所处工况为燃煤电厂,且使用的原煤中Cr、Zn、Ni、Pb、Cu的含量较高,燃烧时易挥发,且非常容易被飞灰俘获,进而随飞灰被除尘滤袋拦截。此外,1#滤袋材质为普通的涤纶,过滤方式为传统的深层过滤,即粒径较小的粉尘颗粒会进入滤料深层,并且粉尘粒径越小越易吸附重金属元素,造成滤袋上重金属元素富集。而采用PTFE覆膜的2#、3#和4#滤袋能够实现表面过滤,表面覆膜起到一次粉尘层的作用,代替了传统的深层过滤,粒径较小的粉尘颗粒难以进入滤料内部。另外,PTFE覆膜滤料表面摩擦系数小,具有憎水性、不粘性,滤袋表面所黏附的粉尘也较少[10]。因此1#滤袋中各重金属元素含量远远大于2#、3#和4#滤袋中的含量。5#滤袋所处工况为水泥厂,在煅烧水泥熟料的过程中,Zn和Cu具有相当的挥发性,因此5#滤料中Zn和Cu的含量也较高。可见不同工况下废旧滤袋中所含重金属元素种类与含量差异较大,并且和所使用的滤料种类也有关系,因此对废旧滤袋进行综合处理时,首先鉴别其中的重金属元素种类以及进行定量分析是十分有必要的,使得后续步骤更有针对性。
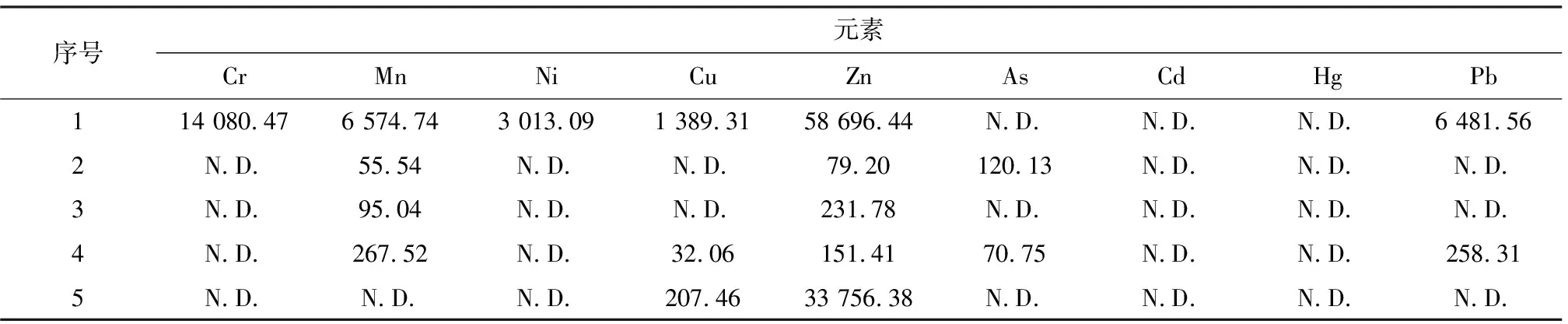
表3 实际样品分析结果Table 3 Analysis results of samples mg/kg
注:N.D.表示未检出。
2.2 废旧滤袋清洗方式检测数据分析
在室温20 ℃条件下,经不同浓度的硝酸或NaOH溶液清洗废旧滤袋试样1,2,4,24 h后清洗溶液中的重金属元素检测结果见图1(清洗溶液中As含量过低,因此没有作图)。经过各清洗剂振荡清洗24 h后的清洗效果见表4。
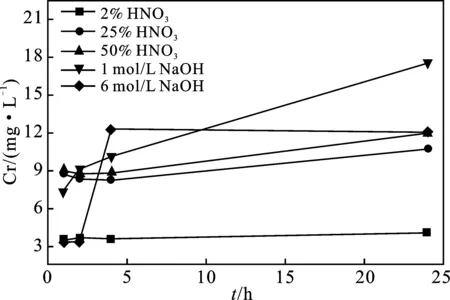




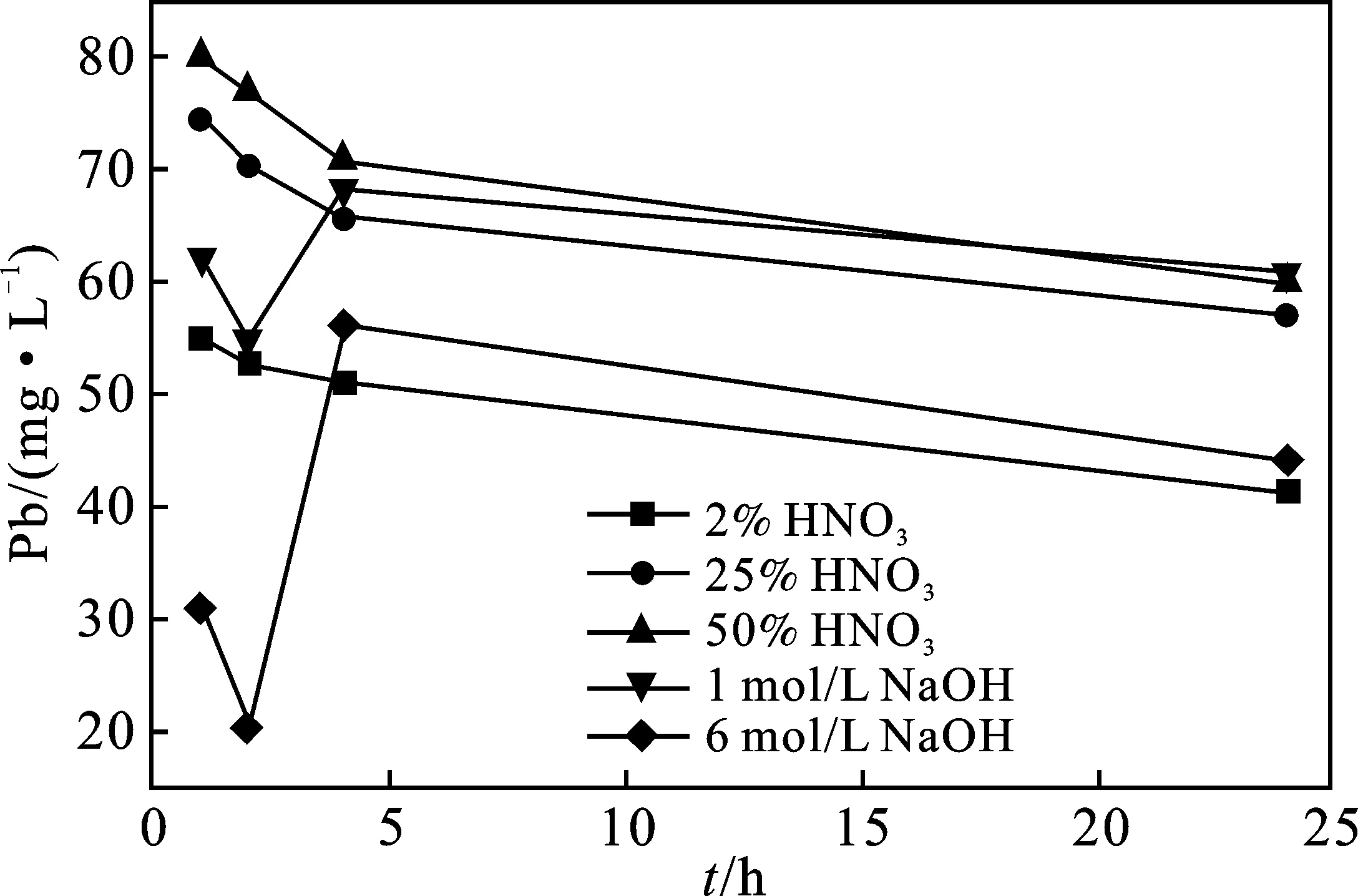
图1 清洗液种类、浓度和时间对清洗后溶液中重金属元素含量的影响Fig.1 Effects on heavy metal concentrations insolution by changing the reagents,reagentconcentrations and cleaning time
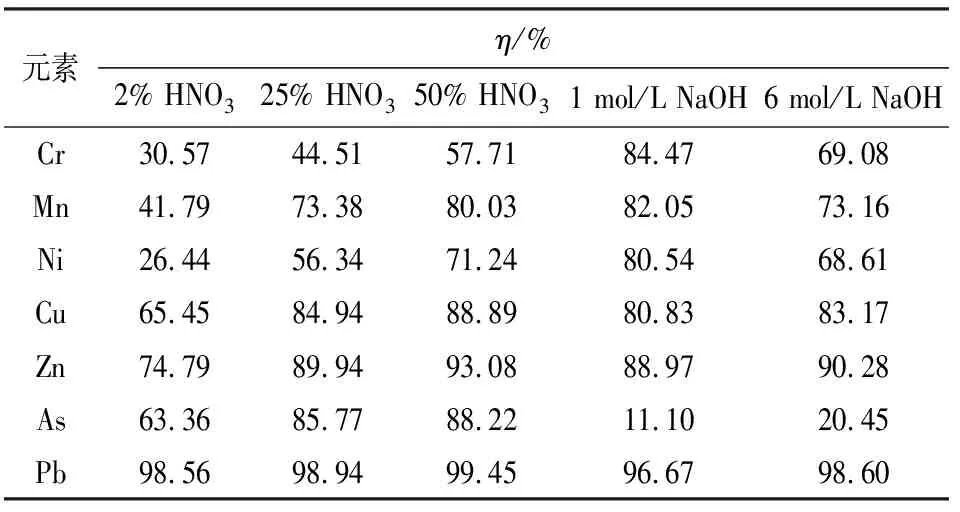
表4 不同清洗液的清洗效果Table 4 Effects of different cleaning reagents
由图1、表4可知,随着硝酸浓度的增加,滤袋样品中重金属元素溶出速率加快,相同的时间内溶出重金属元素含量增加。振荡清洗时长对大多数重金属元素的去除有着明显的促进作用。清洗液中Pb含量随清洗时间的延长而降低,原因可能是Pb离子易形成沉淀,且24 h清洗后清洗率均>96.5%,可知不管是酸性还是碱性环境下Pb的溶解度都比较高。在酸性环境下As的清洗率显著高于碱性环境,这说明As易溶解于酸性清洗剂中。当采用6 mol/L NaOH溶液为清洗剂时,振荡清洗4 h后碱洗液中重金属元素含量明显增加,再增加清洗时间至24 h,清洗液中重金属元素含量变化不明显。酸液和碱液振荡清洗对于不同重金属元素的清洗效果不同。综合来看,当As含量较少或不含有As的情况下,采用1 mol/L 的NaOH溶液为清洗剂,振荡清洗24 h后清洗率基本可以达到80%以上;当As等多种重金属元素共存时,宜采用50% HNO3作为清洗剂,可以较全面地清除所含有的重金属元素。
2.3 混合清洗效果
根据单清洗剂实验确定的结果,继续进行混合清洗实验。以硝酸浓度(A)、氢氧化钠溶液与硝酸清洗顺序(B)为影响清洗结果的2个因素进行实验,氢氧化钠溶液浓度为1 mol/L,各因素水平见表5。
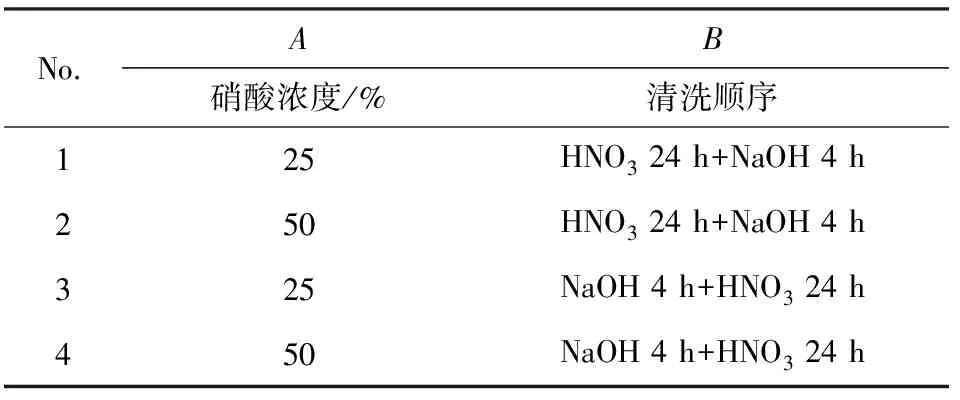
表5 各因素水平表Table 5 Factors and levels table
混合清洗后清洗效果见表6,和表4进行对比后发现,混合清洗对重金属元素清洗效果的促进作用不明显。对于不同的重金属元素,优化出的混合清洗条件也不尽相同。分析其原因可能是滤袋中的颗粒飞灰等的微观形貌不同,其中所含的重金属元素种类不同,化学性质不同,且可能以金属氧化物、可溶性盐或者不溶性沉淀等多种多样的形式存在,酸性/碱性清洗液的先后顺序及其浓度导致的作用机理会对清洗结果产生促进/抑制作用。此外,随着清洗时间的延长,重金属溶出速率降低,也可能是导致混合清洗效果不显著的原因之一。综上所述,采用混合清洗方案3,即先通过1 mol/L NaOH振荡清洗4 h,再采用25% HNO3振荡清洗24 h,综合清洗效果较好。可能由于是滤袋中存在一些难溶于水的无机盐,通过混合清洗可以先与碱性清洗液发生反应后,再采用酸性清洗液进一步清除[11]。

表6 混合清洗的清洗效果Table 6 Effects of cleaning in alternative order
3 结论
(1)采用ICP-OES对不同工况下滤袋中所含有的重金属元素含量和种类进行了分析,不同工况下废旧滤袋中所含重金属元素种类与含量差异较大,其所使用的滤料种类也千差万别,进行综合处理时,正确鉴别其中的重金属元素成分和含量,对后续更有针对性地制定清洗步骤是十分必要的。
(2)对于As含量不多的滤袋,采用1 mol/L NaOH进行清洗24 h,清洗率可达80%以上;当滤袋中含有较多As且重金属元素种类比较繁杂时,采用50% HNO3进行清洗24 h,或者先采用1 mol/L NaOH进行振荡清洗4 h,再通过25% HNO3进一步清洗24 h,综合清洗效果较好,清洗率达到59%以上。在实际工作操作中,可以根据情况进一步调整清洗剂、时间等参数,提高清洗效率。
