小麦醇溶蛋白-阿拉伯胶复合纳米颗粒的构建及其负载百里香酚研究
2020-06-13许雪儿王天缘陈正行
许雪儿 王天缘 陈正行
(盐城工业职业技术学院1,盐城 224005) (江南大学粮食发酵工艺与技术国家工程实验室2,无锡 214000)
微生物的污染往往是造成食源性疾病的主要原因。百里香酚是一种天然的防腐抑菌物质,其具有绿色、无毒的作用。因此,常被作为绿色环保的抗菌物质得到广泛研究。但目前百里香酚所存在的水溶性差、生物利用率低[2]的问题在一定程度上限制其应用。因此,本文首次通过制备复合阿拉伯胶的小麦醇溶蛋白纳米颗粒,实现对百里香酚的负载,在改善其疏水性的同时,提高小麦醇溶蛋白的利用率,开拓阿拉伯胶在制备纳米颗粒方面的可能性。小麦醇溶蛋白占据小麦面筋蛋白总量的40%~50%。小麦醇溶蛋白是由单链的多肽以分子间二硫键相连接而形成,其水溶性较差,但能够溶解于一定浓度的乙醇溶液中[3]。同时,因小麦醇溶蛋白含有一定量的色氨酸、苯丙氨酸、亮氨酸等疏水性氨基酸,使得小麦醇溶蛋白呈现两亲性[4]。因此,为提高小麦醇溶蛋白利用率、积极开发新产品,本文考虑将小麦醇溶蛋白作为制备纳米颗粒的壁材。同时,阿拉伯胶是一类天然的阴离子多糖,其独特的蛋白质和鼠李糖分子结构,使得阿拉伯胶也具有良好的两亲性[5],因此,本研究拟通过构建并制备结合阿拉伯胶的小麦醇溶蛋白纳米颗粒运载体系,以此提高小麦醇溶蛋白纳米颗粒水溶性的同时有效改善百里香酚的疏水性。孔祥珍等[6]通过制备小麦醇溶蛋白纳米颗粒实现对营养物质的负载,尹业充等[7]通过构建百里香酚-玉米醇溶蛋白的纳米颗粒,在提高百里香酚负载率的同时,可有效达到抑菌作用。
采用反溶剂法制备小麦醇溶蛋白-阿拉伯胶的复合纳米颗粒,通过改变不同小麦醇溶蛋白储备液浓度、不同搅拌速度等以探究其对复合纳米颗粒的稳定性;通过分析不同pH、不同盐离子浓度的条件对复合纳米颗粒稳定性的影响;最后,通过测定复合纳米颗粒对百里香酚的包封率及负载百里香酚的复合纳米颗粒的稳定性进行分析,可为构建负载疏水性营养物质的小麦醇溶蛋白-多糖的复合纳米颗粒的可行性提供参考。
1 材料与方法
1.1 材料与试剂
小麦谷朊粉、阿拉伯胶、百里香酚;无水乙醇、石油醚等试剂均为分析纯。
1.2 仪器与设备
R-1001N旋转蒸发仪;磁力搅拌器;CR21G型冷冻干燥机;Zetasizer Nano 纳米粒度仪;WFZ UV-2000型紫外分光光度计;LXJ-IIB型台式离心机;DHG-9101·3SA型恒温干燥箱。
1.3 实验方法
1.3.1 小麦醇溶蛋白的提取
称取100 g谷朊粉置于1 L的体积分数为70%的乙醇水溶液中,并置于磁力搅拌器上,以1 000r/min的转速持续搅拌3 h后,设定5 000 r/min转速离心10 min除去沉淀物,并收集上清液,在55 ℃条件下,旋转蒸发除去乙醇。将旋蒸后的物质冷冻干燥72 h后即可得到小麦醇溶蛋白。
1.3.2 小麦醇溶蛋白-阿拉伯胶复合纳米颗粒制备
首先制备小麦醇溶蛋白的乙醇溶液:称量0.5 g在1.3.1中制备所得的小麦醇溶蛋白并置于10 mL 70%的乙醇水溶液中,并将小麦醇溶蛋白的乙醇溶液置于磁力搅拌器上以一定的搅拌速度搅拌10 min备用;其次,制备阿拉伯胶的水溶液:称量2 g 阿拉伯胶置于去离子水中,并以一定的搅拌速度持续搅拌1 h;随后开始制备小麦醇溶蛋白-阿拉伯胶复合纳米颗粒,具体过程如下:移取一定体积的小麦醇溶蛋白的乙醇溶液,并以一定的滴加速度滴至体积为38.9 mL的去离子水中,得到小麦醇溶蛋白纳米颗粒,然后再以小麦醇溶蛋白-阿拉伯胶(1∶2)的比例,移取不同体积的阿拉伯胶水溶液至于小麦醇溶蛋白纳米颗粒中,以一定的搅拌速度搅拌60 min后,以4 000 r/min的转速离心10 min得到其上清液[8],即为小麦醇溶蛋白-阿拉伯胶复合纳米颗粒。
1.3.3 不同小麦醇溶蛋白储备液浓度下纳米颗粒粒径、电位、多分散指数(polydispersity index,PDI)测定
分别称取0.1、0.2、0.3、0.4、0.5、0.6、0.7 g 小麦醇溶蛋白溶解于10 mL体积分数为70%乙醇中,磁力搅拌30 min作为1%、2%、3%、4%、5%、6%、7%质量分数的小麦醇溶蛋白储备液,具体步骤同1.3.2;所得纳米颗粒稀释至10倍,分散均匀后取1 mL放入样品池后进行测定。
1.3.4 不同搅拌速度下对小麦醇溶蛋白-阿拉伯胶复合纳米颗粒稳定性的影响
控制纳米颗粒制备过程中的搅拌速度(300、400、500、600、700、800、900、1 000、1 100、1 200、1 300 r/min)对纳米颗粒进行制备,具体步骤同1.3.2,稳定性探究同1.3.3。
1.3.5 pH对小麦醇溶蛋白-阿拉伯胶复合纳米颗粒稳定性的影响
用pH范围在3~9的磷酸盐缓冲溶液调节纳米颗粒的pH为3~9,制备得到不同pH值的纳米颗粒后,稳定性探究同1.3.3。
1.3.6 不同盐离子浓度对小麦醇溶蛋白-阿拉伯胶复合纳米颗粒稳定性的影响
先后移取10 mL浓度分别为(0、10、20、30、50、100 mmol/L)的盐溶液,置于6只50 mL的离心管中,随后,在每管中加入10 mL小麦醇溶蛋白-阿拉伯胶复合纳米颗粒,并将纳米颗粒与盐离子溶液充分混合均匀,室温下静置30 min后,观察盐离子对复合纳米颗粒干扰后的体系稳定状态[9]。粒径、电位、多分散指数的测定步骤同1.3.3。
1.3.7 负载百里香酚的小麦醇溶蛋白-阿拉伯胶复合纳米颗粒制备
按照一定小麦醇溶蛋白/阿拉伯胶:百里香酚(1∶1、1∶2、1∶5、1∶10、1∶20、1∶30、1∶40、1∶50)的比例制备不同比例的复合纳米颗粒,移取一定量的百里香酚置于1.3.2中制备所得小麦醇溶蛋白的乙醇溶液,得到负载百里香酚的小麦醇溶蛋白的乙醇溶液;然后将移取一定量的负载百里香酚的小麦醇溶蛋白的乙醇溶液以1.3.2中具体步骤进行制备,以得到负载百里香酚的小麦醇溶蛋白-阿拉伯胶复合纳米颗粒。
1.3.8 不同小麦醇溶蛋白-阿拉伯胶复合纳米颗粒:百里香酚比例下纳米颗粒粒径、电位、多分散指数(PDI)测定
取1 mL 新鲜制备的不同小麦醇溶蛋白-阿拉伯胶:百里香酚比例(1∶1、2∶1、10∶1、50∶1、100∶1)的纳米颗粒,粒径、电位、多分散指数的测定步骤同1.3.3。
1.3.9 百里香酚包封率的测定
负载百里香酚的小麦醇溶蛋白-阿拉伯胶复合纳米颗粒对百里香酚包封率测定方法如下:将5 mL制备所得的小麦醇溶蛋白/阿拉伯胶-百里香酚纳米颗粒移入烧杯中,随后将3 mL乙酸乙酯加入纳米颗粒中搅拌60 min,以期达到萃取百里香酚的作用,重复萃取后合并萃取液,并以乙酸乙酯作为空白样,在276 nm处对样品的吸光值进行测定。根据所得百里香酚吸光值绘制标准曲线,得到方程:y=9.820x+0.019(R2=0.993),并以此计算包封率[10]:
百里香酚包封率=
2 结果与分析
2.1 不同小麦醇溶蛋白储备液浓度对复合纳米颗粒的影响


注:不同小写字母表示差异显著(P<0.05),余同。
图1 不同小麦醇溶蛋白储备液浓度下纳米颗粒粒径、PDI、电位图
如图1a所示,随着小麦醇溶蛋白储备液浓度的升高,小麦醇溶蛋白-阿拉伯胶复合纳米颗粒的粒径、PDI变化为:从2%~6%的稳定变为6%~8%的显著上升。其中,当小麦醇溶蛋白储备液浓度在6%时,复合纳米颗粒的粒径为223.6 nm,PDI为0.35,而当超过储备液质量分数超过6%时,复合纳米颗粒的粒径显著增大,这可能是由于当浓度低于6%之时,小麦醇溶蛋白充分分散于水相之中,并形成纳米颗粒,而当蛋白浓度过高时,部分过剩的蛋白分子便不能形成稳定的纳米颗粒,并直接影响制备过程中的粒径和PDI值。从图1b中也可以看出,复合纳米颗粒在不同小麦醇溶蛋白储备液浓度下电位的变化趋势与粒径及PDI的变化趋势相同,其中当小麦醇溶蛋白储备液质量分数在6%时,复合纳米颗粒的电位为-29.8 mV。该结果与王丽娟等[11]和Fu等[12]的究玉米醇溶蛋白-果胶复合纳米颗粒时所探究得出的,若蛋白的初始储备液浓度过高时,会对纳米颗粒的形成及其粒径、电位大小有直接影响的结果一致。综上所述,制备纳米颗粒时选取6%的小麦醇溶蛋白储备液浓度,在提高纳米颗粒得率的同时,又不影响其粒径、电位等稳定性指标。
2.2 不同搅拌速度对小麦醇溶蛋白与阿拉伯胶纳米颗粒的影响
从图2中可以看出,当搅拌速度小于400 r/min时,所形成的纳米颗粒的粒径大于300 nm,且体系稳定性较差,该结果表明,较低的搅拌速度不能形成稳定的纳米颗粒;当搅拌速度提高至800 r/min时,体系粒径最低;当搅拌速度为800~1 200 r/min之间时,纳米颗粒体系的粒径趋于稳定;而当搅拌速度提高至1 200 r/min时,复合纳米颗粒体系粒径显著变大,分析该粒径变化结果,这可能是由于较大的剪切力破坏复合纳米颗粒的形成,并使得蛋白纳米颗粒与阿拉伯胶之间发生絮凝,对体系起反作用。因此,确定800 r/min的搅拌速度为纳米颗粒的最适搅拌速度。Gagliardi等[13]在研究小麦醇溶蛋白的纳米颗粒形成时表明,搅拌速度所产生的剪切力较大时,会显著破坏纳米颗粒的形成。

图2 不同搅拌速度对小麦醇溶蛋白复合纳米颗粒的 粒径的影响
2.3 pH对小麦醇溶蛋白-阿拉伯胶复合纳米颗粒的影响
从图3a可以看出,在不同的pH环境下,复合纳米颗粒的粒径和PDI没有显著变化,该结果表明,复合纳米颗粒在不同pH环境下的耐受性较强,该结果可能是由于阿拉伯胶与小麦醇溶蛋白相互作用形成稳定的纳米颗粒,在保护了小麦醇溶蛋白纳米颗粒不被胃酸环境破坏的同时,还改善了纳米颗粒体系的稳定性。同时,图3b的电位图可以看出,当pH=3时,小麦醇溶蛋白-阿拉伯胶复合纳米颗粒电位较低,表明该体系不稳定,推测是由于此时pH的环境与阿拉伯胶的pka值(2.3)相近,因此阿拉伯胶的稳定性较差,进而无法促进体系稳定性的形成;在pH=4~9的环境下,复合纳米颗粒电位值均较为稳定。由此结论可以得出,阿拉伯胶可以有效结合小麦醇溶蛋白并形成稳定的纳米颗粒体系,而当环境pH达到蛋白质等电点时,蛋白质易聚集的现象。吴炜豪等[14]在研究小麦醇溶蛋白纳米颗粒的制备时也发现相同结论。

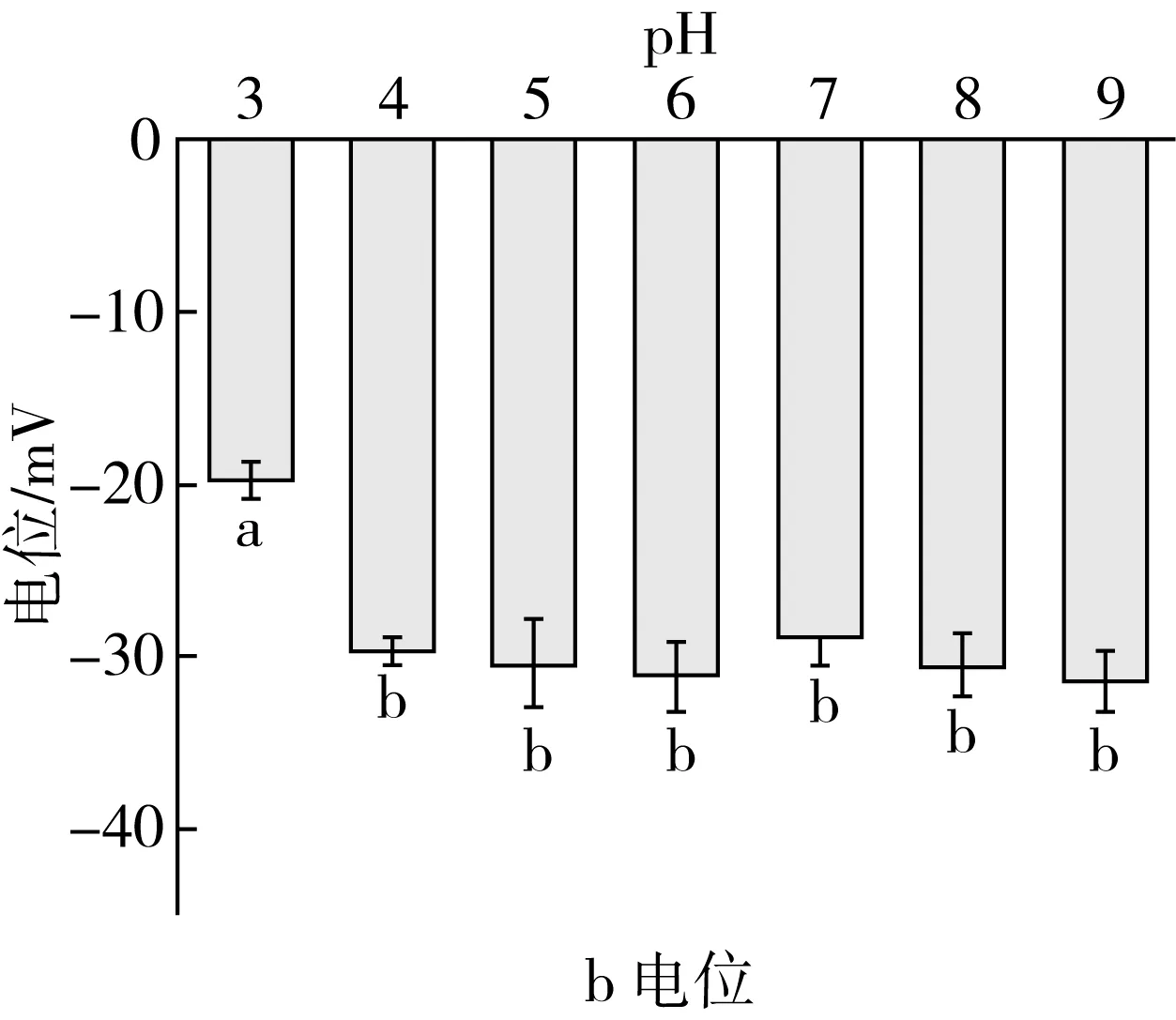
图3 pH对小麦醇溶蛋白-阿拉伯胶复合纳米颗粒粒径、 PDI、电位的影响
2.4 不同盐离子浓度对小麦醇溶蛋白-阿拉伯胶复合纳米颗粒的影响
从表1中可以看出,不同盐离子浓度对小麦醇溶蛋白-阿拉伯胶复合纳米颗粒的粒径、PDI、电位的影响,当其中,当盐离子浓度小于20 mmol/L时,纳米颗粒体系为纳米级,且PDI也较为稳定,随着盐离子浓度上升到30 mmol/L时,纳米颗粒体系的粒径增大至微米级,且PDI为1;电位也接近于0 mV;体系的不稳定性也能够表明,小麦醇溶蛋白-阿拉伯胶复合纳米颗粒的盐离子耐受浓度为20 mmol/L,推测是由于阿拉伯胶与小麦醇溶蛋白之间通过相互作用力结合生成稳定的复合物[15],20 mmol/L的盐离子浓度,不足以破坏小麦醇溶蛋白与阿拉伯胶之间的相互作用力,而当盐离子浓度大于20 mmol/L时,体系易发生电荷屏蔽效应,使得体系粒径变大、絮凝状态变严重。该结果与Dai等[16]研究盐离子对玉米醇溶蛋白纳米颗粒的干扰作用时结果相同。
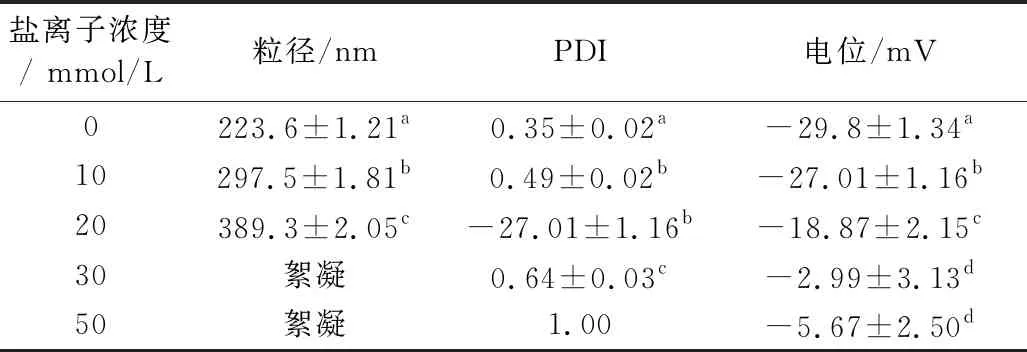
表1 不同盐离子浓度对小麦醇溶蛋白-阿拉伯胶 纳米颗粒的影响
注:不同小写字母表示差异显著(P<0.05),余同。
2.5 不同小麦醇溶蛋白-阿拉伯胶:百里香酚比例的纳米颗粒粒径、PDI、电位值
从图4a中可看出,不同小麦醇溶蛋白-阿拉伯胶∶百里香酚比例的纳米颗粒的粒径、PDI值,结果表明,当小麦醇溶蛋白负载生育酚的比例逐渐变大时,复合纳米颗粒的粒径逐渐增高,具体表现为,当小麦醇溶蛋白-阿拉伯胶∶百里香酚大于5∶1时,负载百里香酚的纳米颗粒粒径、PDI均较为稳定,即可分析为,小麦醇溶蛋白可充分包裹住百里香酚并结合成纳米颗粒;其中,小麦醇溶蛋白-阿拉伯胶∶百里香酚=5∶1时粒径为251.2 nm,PDI为0.36;而当比例小于5∶1时纳米颗粒粒径较大达到 280 nm; PDI也大于0.36。同时,如图4b所示,随着小麦醇溶蛋白-阿拉伯胶∶百里香酚比例的减小,纳米颗粒电位也逐渐下降, 小麦醇溶蛋白-阿拉伯胶∶百里香酚=5∶1时电位为-28.3 mV。该结果与 Wongsasulak等[17]和Gulfam等[18]研究结果一致。综上所述,小麦醇溶蛋白-阿拉伯胶∶百里香酚=5∶1时复合纳米颗粒的粒径、PDI、电位和包封率均达到稳定体系状态,此时,小麦醇溶蛋白复合阿拉伯胶的生物大分子纳米颗粒具备对百里香酚的负载能力。
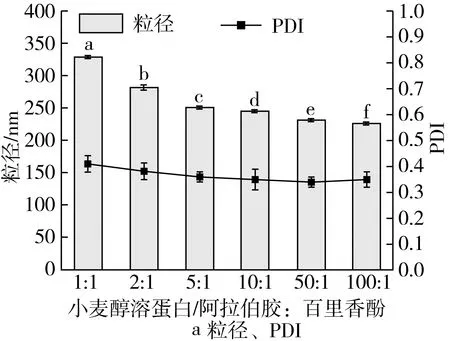

图4 不同小麦醇溶蛋白-阿拉伯胶:百里香酚比例 纳米颗粒粒径、 PDI和电位对比图
2.6 负载百里香酚的小麦醇溶蛋白-阿拉伯胶复合纳米颗粒包封率
表2是负载不同百里香酚含量的小麦醇溶蛋白-阿拉伯胶复合纳米颗粒的包封率情况,其中当小麦醇溶蛋白-阿拉伯胶复合纳米颗粒∶百里香酚的比例在100∶1、50∶1、10∶1时,包封率均达到90%以上;当比率达到5∶1,2∶1,1∶1时,百里香酚的包封率逐渐降低。该结果表明,当百里香酚负载量较低时,小麦醇溶蛋白和阿拉伯胶能够较大程度的包裹百里香酚[19],即与百里香酚能够有效结合。而当百里香酚负载量较高时,所制备得到的复合纳米颗粒不能与百里香酚充分融合,负载率较低。黄晓霞等[20]在研究负载姜黄素的玉米醇溶蛋白纳米颗粒时,表明所得的复合纳米颗粒具在比率低于1∶1时,对姜黄素都有较高的负载率。

表2 负载百里香酚小麦醇溶蛋白-阿拉伯胶复合纳米颗粒的包封率
3 结论
探讨小麦醇溶蛋白储备液浓度、搅拌速度、pH以及盐离子浓度等因素对小麦醇溶蛋白与阿拉伯胶复合纳米颗粒的稳定性影响,该复合纳米颗粒均具备耐酸碱性和一定程度的盐离子耐受性,并具备对百里香酚的负载能力;因此,阿拉伯胶对小麦醇溶蛋白的结合,可一定程度上保护小麦醇溶蛋白纳米颗粒在酸性条件及等电点环境下的分解,实现了对百里香酚的高效负载并有效拓宽小麦醇溶蛋白的应用,由此可得出,小麦醇溶蛋白与阿拉伯胶的复合纳米颗粒可被考虑作为生物运载体系,以实现对百里香酚的运载。
