PPAR-γ/FAK信号通路在C57BL/6小鼠肺成纤维细胞中的抗纤维化作用
2020-06-09龚玲刘代顺张龙举
龚玲 刘代顺 张龙举
特发性肺纤维化(idiopathic pulmonary fibrosis, IPF)是一种慢性进展性且不可逆转的纤维化间质性肺炎,目前病因不明确,其表现特征为UIP(普通型间质性肺炎)[1-2]。该病患病率不断上升,最常累计60岁以上患者,该病每年以11%的比例增长[2-4]。IPF诊断后的平均生存期仅2.8年,死亡率高于大多数肿瘤,因此被称为一种“类肿瘤疾病”[5-6]。IPF相关的主要生长因子包括TGF-β、成纤维细胞生长因子-2、血小板衍生生长因子。Kulkarni A A等[7]报道,PPAR-γ配体CDDO、15D-PGJ2及罗格列酮均有抑制肺成纤维细胞向肌纤维母细胞转化的作用,它们主要是通过抑制TGF-β诱导肺成纤维细胞向肌纤维母细胞转化的FAK下游的PI3K-AKT途径。本研究旨在应用PPAR-γ配体罗格列酮及FAK探讨PPAR-γ与PI3K-AKT途径上游的FAK通路在TGF-β诱导的小鼠成纤维细胞转化为肌纤维母细胞进程中是否存在关联性,为肺纤维化的深入研究提供新的分子机制。
资料与方法
一、细胞、药物和试剂
第3~4代C57BL/6(美国ATCC○RCRL-6013TM)细胞,罗格列酮(德国Sigma) ,TGF-β2(美国 R&D Systems),PCR试剂盒(日本TaKaRa),PCR引物合成 (中国 生工),DMEM(Hyclone USA),MTT试剂盒(中国 凯基)。
二、细胞培养
加入DMEM培养基的C57BL/6小鼠肺成纤维细胞放置于温度37℃、饱和湿度、含5%CO2的培养箱中培养。培养每2~3 d换液1次,在用于实验时,C57BL/6小鼠肺成纤维细胞处于80%左右融合状态。
三、药物处理
参照文献[8],刺激C57BL/6小鼠肺成纤维细胞的TGF-β2浓度为10 ng/mL。参照文献[9]罗格列酮用DMSO溶解,刺激C57BL/6小鼠肺成纤维细胞的浓度分别为5 μmol/L、10 μmol/L、20 μmol/L及40 μmol/L。进行MTT实验、PCR实验、细胞生长计数实验。
四、RNA提取及PCR
C57BL/6小鼠肺成纤维细胞培养24 h,以Trizol提取总RNA,判断纯度和浓度达到要求标准后,取2 μL总RNA使用反转录试剂盒(cDNA)进行反转录。PCR反应过程参考PCR试剂盒说明书。检测PPAR-γ mRNA、FAK mRNA光密度值。
五、MTT实验
取对数生长期的细胞,胰酶消化后制成单细胞悬液,每孔100 μL悬液分别接种于96孔板。24 h后设置调零孔,未处理组UNT,以TGF-β2 10 ng/mL刺激C57BL/6小鼠肺成纤维细胞转化,罗格列酮(5 μmol/L、10 μmol/L、20 μmol/L及40 μmol/L)分别加入,每组设置3个复孔,再分别培养24 h,48 h,72 h。MTT实验时吸去孔内上清液,MTS:培养基=1:5稀释后,连续加样,每孔50uL,避光孵育,酶联免疫监测仪检测各孔在490nm吸光光度,最后记录数据结果。

表1 PCR引物序列表
六、生长实验
密度相同的C57BL/6小鼠肺成纤维细胞分别接种于6孔板中,实验分为空白组、TGF-β2组(10 ng/mL)、TGF-β210 ng/mL +罗格列酮组(5 μmol/L、10 μmol/L、20 μmol/L及40 μmol/L),分别培养24 h,48 h,72 h后以血球细胞板分别进行计数。
七、统计学分析
结 果
一、PPAR-γ配体对C57BL/6小鼠肺成纤维细胞生长的影响
从图1A可以看出,随着 PPAR-γ配体(罗格列酮)培养浓度增加的增加,C57BL/6小鼠肺成纤维细胞生长受到抑制,在浓度40 μmol/L抑制72 h最明显。从图1B可以看出,在相同浓度TGF-β2 10 ng/mL刺激下,随着PPAR-γ配体(罗格列酮)培养浓度的增加,C57BL/6小鼠肺成纤维细胞生长也同样受到抑制,仍在浓度40 μmol/L抑制72 h最明显。因此,从(图1A)和(图1B)可以看出,PPAR-γ配体罗格列酮抑制肌纤维母细胞生长(见表2)。
二、PPAR-γ配体对小鼠肺成纤维细胞C57BL/6增殖的影响
从(图2)可以看出,小鼠肺成纤维细胞C57BL/6在相同浓度TGF-β2 10 ng/mL的刺激下,随着A.不同剂量罗格列酮对C57BL/6小鼠肺成纤维细胞生长影响; B.TGF-β210 ng/mL+不同剂量罗格列酮对C57BL/6小鼠肺成纤维细胞生长影响PPAR-γ配体(罗格列酮)培养浓度的增加,细胞增殖受到抑制,在浓度40 μmol/L抑制72 h最明显。因此,PPAR-γ配体罗格列酮抑制肌纤维母细胞增殖(见表3)。
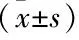
表2 罗格列酮对小鼠肺成纤维细胞C57BL/6细胞生长的影响
注: Rosi不同浓度组与空白组比较:*P<0.05;TGF-β2+ Rosi不同浓度组与空白组比较:**P<0.05,差异具有统计学意义。
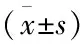
表3 罗格列酮对小鼠肺成纤维细胞C57BL/6增殖的影响
注: Rosi实验组与空白组比较:#P<0.05,差异具有统计学意义。
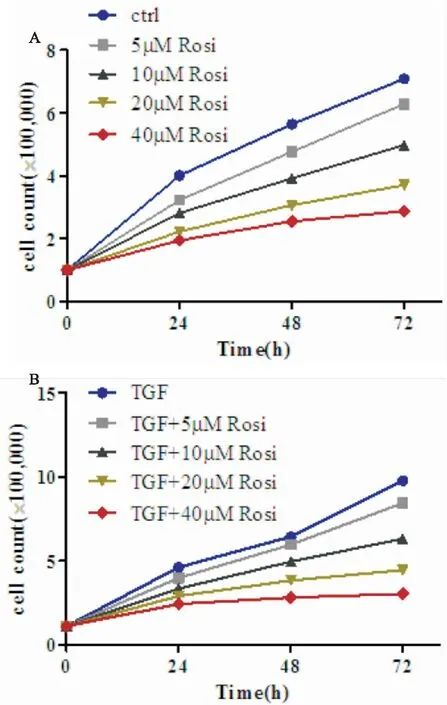
图1 罗格列酮对C57BL/6小鼠肺成纤维细胞生长的影响
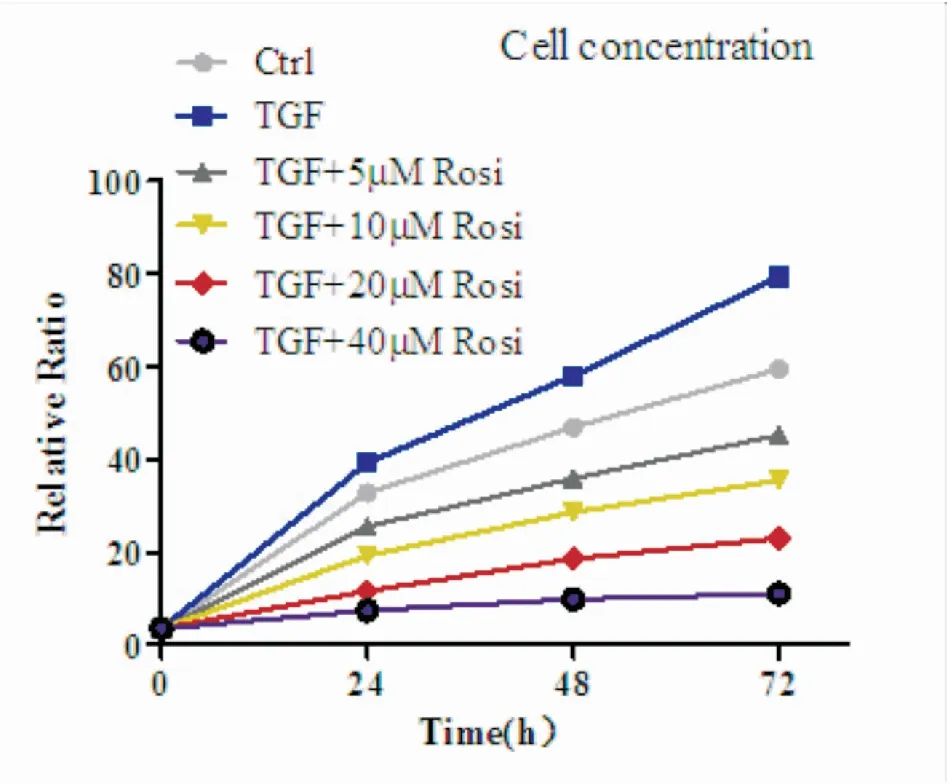
图2 罗格列酮对C57BL/6小鼠肺成纤维细胞增殖的影响
三、PCR检测不同浓度 PPAR-γ配体对PPAR-γ mRNA、FAK mRNA转录水平的影响
从图3A可以看出,PPAR-γ配体(罗格列酮)使PPAR-γ mRNA转录增加且存在明显浓度依赖,在罗格列酮40 μmol/L时PPAR-γ mRNA转录增加最明显。从图3B可以看出,罗格列酮使FAK mRNA转录减少且存在浓度依赖,在罗格列酮40 μmol/L时FAK mRNA转录减少最明显(见表4)。
讨 论
IPF的临床主要表现为以活动后明显的进行加重的呼吸困难、限制性通气功能障碍、弥散功能降低伴低氧血症、干咳及爆裂音。IPF的病因不清,但一些风险因素已经确定(如吸烟、环境暴露、慢性病毒感染及家族病史、胃酸反流异常)。IPF多为散发,
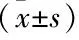
表4 罗格列酮对PPAR-γ mRNA/FAK mRNA表达影响
注:结果使用表示,PPAR-γ mRNA组*P<0.05、FAK mRNA组*P<0.05,差异具有统计学意义。

图3 A:PPAR-γ mRNA在不同浓度罗格列酮刺激下的转录水平;
B:FAK mRNA在不同浓度罗格列酮刺激下的转录水平
占所有间质性肺病的20%~30%,男女比例为1.5 ∶1~2 ∶1,IPF每年的病率约为(6.8~16.3)/10万,由于IPF病因发病机制尚不明确,影响早期诊断及治疗,确诊后的平均生存时间为3~5年[4,10-11],急性加重是IPF死亡的首要原因,加重后的中位生存期仅为3~4个月,病死率55~88%[12]。IPF预后比多数肿瘤要更差,如皮肤癌、甲状腺癌、乳腺癌等,5年生存率约20~40%,因此称其为“不是癌症的癌症”,因它的发病机制不确定、进展快、预后差,被世界卫生组织(WTO)称为肺系疑难疾病[1-2]。近年来,IPF发病机制的探讨和治疗靶点研究已成为研究热点,加大对肺纤维化发病机制、治疗方案的探讨意义深远。
近年研究发现PPAR-γ配体CDDO、15D-PGJ2及罗格列酮在细胞分化、诱导细胞凋亡、脂质代谢、抑制细胞增殖、抗炎症反应等方面发挥十分重要的作用,其中,PPAR-γ合成配体罗格列酮目前研究最多[13-14]。多项研究表明,罗格列酮、CDDO、15D-PGJ2均能阻碍TGF-β诱导的肺成纤维细胞向肌成纤维细胞转化[7,10,13]。FAK是一种非受体型酪氨酸激酶,它与细胞周期增殖、凋亡、迁移、侵袭、转移、调控等密切相关,它可以介导细胞与细胞外基质、细胞与细胞间信号的转导,而且还具有调节细胞与ECM粘附的作用。IPF存在成纤维细胞增殖及大量ECM聚集,FAK是抑制TGF-β诱导肺成纤维细胞向肌成纤维细胞转化的一个基本的要素。Kulkarni A A等[7]报道,PPAR-γ配体罗格列酮能抑制肺成纤维细胞向肌纤维母细胞转化,它们主要是通过抑制TGF-β诱导肺成纤维细胞转化的FAK下游的PI3K-AKT途径。但是,PPAR-γ与FAK上游信号通路在IPF中的关系及分子机制令人关注。
本实验通过培养小鼠肺成纤维细胞C57BL/6,以TGF-β2诱导其向肌纤维母细胞转化,使用不同浓度PPAR-γ配体罗格列酮作用于小鼠肺成纤维细胞C57BL/6,探讨PPAR-γ与FAK信号通路在IPF中的作用,细胞生长计数实验证实罗格列酮对肌纤维母细胞的生长存在抑制作用,MTT实验证实罗格列酮对肌纤维母细胞的增殖存在抑制作用,抑制肌纤维母细胞的生长及增殖存在明显的浓度依赖及时间依赖。PCR实验可以看出,PPAR-γ mRNA转录水平随罗格列酮浓度增加而增加,FAK mRNA的转录水平随罗格列酮浓度增加而减少。
综上所述,PPAR-γ配体罗格列酮抑制TGF-β诱导的小鼠肺成纤维细胞向肌成纤维细胞转化,其机制可能与抑制FAK表达,进而抑制TGF-β2诱导的小鼠肺成纤维细胞向肌纤维母细胞转化有关,该分子机制的研究对深入探讨肺纤维化发生机制及治疗靶点可能存在潜在的价值。
