利拉鲁肽提高肥胖不孕多囊卵巢综合征妇女临床妊娠率的研究
2020-06-08郝建民李春红孟宪英
郝建民,卢 涛,邱 娟,张 鑫,李春红,孟宪英
0 引言
多囊卵巢综合征(Polycystic ovary syndrome,PCOS)是无排卵不孕的最常见病因,超过20%的育龄妇女受到PCOS疾病影响[1-2]。近一半PCOS女性患者超重或肥胖。肥胖对体外受精(In vitro fertilization,IVF)结果的影响还不清楚,但大量研究表明,PCOS患者的植入率、临床妊娠和分娩率较低,流产率较高,可收集和受精的卵母细胞更少、周期更长、需要较高剂量的促性腺激素[3-8]。IVF术前减重与妊娠率(Pregnancy rates,PR)和活产率显著提高密切相关,进行减重干预可减少妊娠所需的IVF周期数,改善孕前的生活方式也可改善后代的长期健康状况。专家建议将改变生活方式作为肥胖不孕的PCOS女性的一线治疗方案,而克罗米芬柠檬酸盐(Clomiphene citrate,CC)仍然是诱导排卵的二线治疗方法[9]。与CC相比,二甲双胍在改善患者排卵率、妊娠率、活产率、流产率和多胎妊娠率方面疗效较差。而二甲双胍与CC联合用药对体重指数(Body mass index,BMI)>35 kg/m2的患者疗效更佳。长效胰高血糖素样肽-1(Glucagon-like peptide-1,GLP-1)受体激动剂(Receptor agonist,RA)利拉鲁肽对肥胖PCOS女性的减重和血糖稳态有积极的促进作用。与二甲双胍单独给药和改变生活方式相比,利拉鲁肽与二甲双胍联合用药可带来更显著的减重效果[10-12]。其减重机制既包括直接作用患者下丘脑而减少食物摄入,也可以通过自主神经系统介导的中枢作用延迟胃排空。关于利拉鲁肽对PCOS肥胖患者IVF结果影响的研究较少。利拉鲁肽是一种有效的胰岛素增敏剂,动物实验表明,GLP-1通过激素释放进行神经内分泌调节,进而起到影响患者下丘脑-垂体-卵巢轴的作用[13-14]。因此,本研究采用前瞻性、随机、对照方法,评价利拉鲁肽与二甲双胍联合给药和二甲双胍单独给药,对通过改变生活方式减重效果较差的PCOS不孕患者临床妊娠率及累计妊娠率的影响,同时比较两种用药方法对卵母细胞和胚胎质量、减重以及代谢和内分泌指数的影响。
1 资料与方法
1.1 研究对象 选取2017年6月至2018年12月在我院治疗的186例PCOS肥胖不孕患者。诊断标准:根据ESHRE/ASRM在2003年制定的鹿特丹标准对PCOS进行诊断,即下列3项标准具备2项即可诊断为PCOS:①临床或实验室指标表现高雄激素血症,包括多毛、脱发及痤疮等;②盆腔超声或阴道超声检查有卵巢多囊性改变;③闭经或月经稀发。纳入标准:①符合上述PCOS诊断标准;②BMI≥30 kg/m2;③年龄≤38岁;④患者第1次或第2次进行IVF治疗,并均经一线减重治疗失败;⑤男方无严重的不育症。排除标准:①1型或2型糖尿病患者;②有癌症病史的患者;③个人或家族有多发性内分泌腺瘤病2型病史的患者;④严重的心血管、肾脏或肝脏疾病患者;⑤研究前90 d使用除二甲双胍以外的已知或怀疑会影响生殖、代谢功能的药物或他汀类药物患者;⑥子宫内膜异位症Ⅲ级与Ⅳ级、卵巢低储备、卵巢早衰患者;⑦产生高雄激素及高泌乳素的其他内分泌疾病患者;⑧不能耐受妊娠及有严重内外科疾病不适宜接受促排卵治疗的患者。本研究经过我院伦理委员会的批准同意,患者或家属均签署了知情同意书。
1.2 治疗方法 根据随机数字表法,将186例患者分为联合用药组(联合组)与二甲双胍组,每组93例。二甲双胍组服用二甲双胍片(石家庄以岭药业股份有限公司,批准文号:国药准字H20054790)治疗,初始剂量500 mg/次,1次/d,3 d后增加至1 000 mg,2次/d。联合组在对照组治疗的基础上,加用利拉鲁肽(丹麦诺和诺德公司,注册证号:国药准字J20160037)皮下注射治疗,初始剂量为0.6 mg,1次/d,3 d后增加至1.2 mg。所有患者均治疗12周。研究开始时对所有患者进行积极生活方式干预。要求患者降低食物热量至500~800 kcal/d,食物中超过50%为低血糖指数碳水化合物,20%蛋白质和30%单不饱和脂肪和多不饱和脂肪,饱和脂肪含量低于10%。鼓励患者每天增加纤维、全谷物、谷物、水果和蔬菜摄入,并进行每天至少30 min中等强度的身体活动。在药物治疗1个月后给予患者IVF手术。
1.3 IVF治疗 以GnRH-A短方案作为患者的促排卵方案。根据患者的年龄、基础卵泡刺激素、基础卵泡数给予患者果纳芬150~225 IU/d皮下注射,当优势卵泡直径达到14 mm时,给予患者西曲瑞克(Merck Serono Europe Limited,批准文号:注册证号 H20140476)皮下注射,剂量0.25 mg/d,直至人绒毛膜促性腺激素(Human chorionic gonadotropin,HCG)注射日。通过B超监测患者卵泡直径和数量,如果直径为16~18 mm的卵泡数量>3个,则停止注射GnRH-A。给予患者HCG肌注治疗,剂量5 000~10 000 IU,34~36 h后在阴道超声引导下进行穿刺取卵,受精2~3 d后在超声引导下取出1~5个优质胚胎,并经宫颈进行胚胎移植(Embryo transfers,ET)。移植后给予患者注射黄体酮以进行黄体支持,剂量60 mg/d。移植2周后抽血HCG或验尿以确定患者是否妊娠,临床妊娠是指胚胎移植6~7周后采用B超见到患者原始胎心管搏动或孕囊。
1.4 指标检测 收集患者的临床资料,包括患者在基线期的不孕史数据,基线期与治疗后的人体测量参数、内分泌参数、体脂分布参数及治疗后的IVF结果。基线期不孕史数据包括年龄、不孕期、既往CC与芳香酶抑制剂(Aromatase inhibitors,AI)用药史、腹腔镜治疗史;人体测量参数包括体重、BMI、腰围、内脏脂肪质量、体积及面积。代谢参数包括稳态模型胰岛素抵抗指数(Homeostasis model assessment-insulin resistance,HOMA-IR)、空腹血糖、餐后2 h血糖、空腹胰岛素、餐后2 h胰岛素。内分泌参数包括游离睾酮(Free testosterone,FT)、总睾酮(Total testosterone,TT)、性激素结合球蛋白(Sex hormone-binding globulin,SHBG)及雄烯二酮。采用双能量X射线骨密度仪(Dual energy X-ray absorptiometry,DXA)测量患者脂肪含量。采用标准葡萄糖氧化酶法测定患者血糖,采用免疫放射测定法测量患者胰岛素水平。HOMA-IR=空腹血糖(mmol/L)×空腹胰岛素(mU/L)/22.5。糖耐量受损(Impaired glucose tolerance,IGT)是指口服葡萄糖耐量试验(Oral glucose tolerance test,OGTT)2 h后血浆血糖值为7.8~11.1 mmol/L。采用西门子Immulite 2000分析仪测定FT、TT、SHBG、雄烯二醇及胰岛素水平。成熟卵母细胞是指减数分裂中期Ⅱ(MⅡ)卵母细胞,主要表现为出现卵周隙,胞质均匀,可见第一极体。未成熟卵母细胞是指生殖泡卵母细胞和减数分裂数分裂中期Ⅰ(MⅠ)卵母细胞。受精率=受精数/获卵数,卵母细胞闭锁率=退化卵母细胞数/获卵数,卵母细胞未成熟率=未成熟卵母细胞数/获卵数,囊胚形成率=形成的囊胚数/转入囊胚培养的胚胎数,胚胎种植率=着床胚胎数/移植胚胎数,根据Gardner囊胚分级系统对形成的囊胚进行分级。妊娠诊断在HCG给药14 d后通过β-HCG血清测定,在ET 4周后通过经阴道超声检查来进行。临床妊娠率=临床妊娠周期数/移植周期数。累计妊娠率=所有妊娠患者数量/患者总数。治疗结束后,对患者进行12个月随访,记录患者自然妊娠情况。
2 结果
2.1 两组患者人口特征与基线结果比较 共纳入186例不孕的PCOS患者,患者年龄27~38岁,平均(30.7±4.3)岁,患者不孕期平均(54.6±22.3)个月,所有患者均经一线减重治疗失败。二甲双胍组与联合组患者基线期人体测量参数、代谢参数、内分泌参数、不孕史比较差异无统计学意义(P>0.05),具有可比性。见表1~表3。

表1 两组患者不孕史比较
2.2 两组患者人体测量参数变化比较 治疗后,联合组与二甲双胍组患者体重均较基线期显著降低,差异有统计学意义(t=2.65,P<0.01;t=4.05,P<0.01)。二甲双胍组和联合组患者体重分别下降(5.98±5.03)kg和(7.52±3.90)kg。与二甲双胍组比较,联合组患者体重较基线降低值显著提高,差异有统计学意义(t=2.33,P=0.02)。186例患者中,有117例(62.9%)患者是3个月内减重超过5%的高反应者[联合组64例(68.8%),二甲双胍组53例(57.0%),χ2=2.79,P=0.10]。没有患者体重增加。见表2。
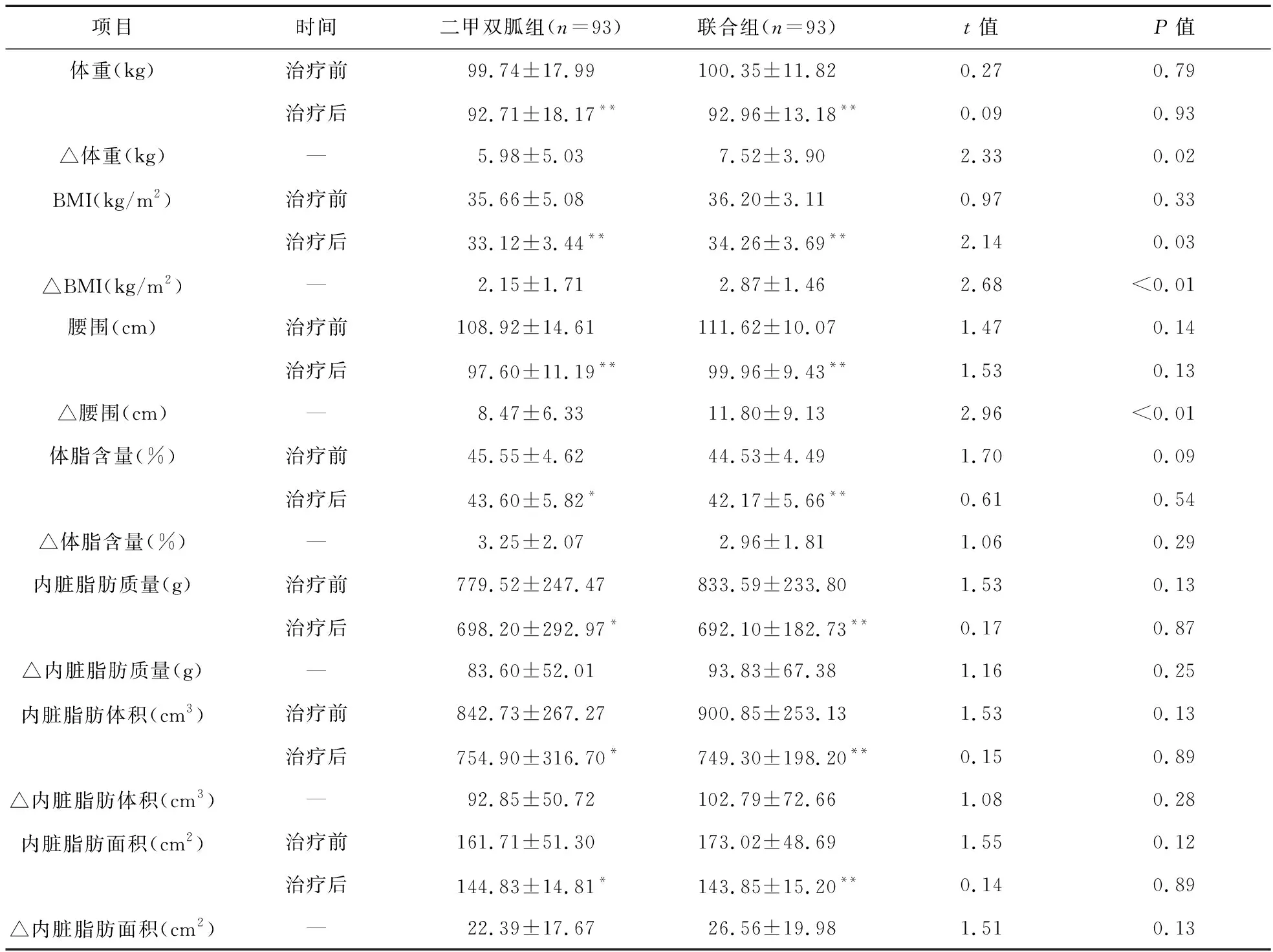
表2 两组患者基线期和治疗后的人体测量特征比较
注:与治疗前比较,*P<0.05,**P<0.01
治疗后,二甲双胍组和联合组患者BMI与腰围均较治疗前显著降低,差异有统计学意义(P<0.05)。二甲双胍组和联合组患者BMI分别降低(2.15±1.71)kg/m2和(2.87±1.46)kg/m2,联合组患者BMI降低值较二甲双胍组显著提高,差异有统计学意义(t=2.68,P<0.01)。治疗后,二甲双胍组和联合组患者腰围值分别降低(8.47±6.33)cm和(11.8±9.13)cm,联合组患者腰围降低值较联合组显著提高,差异有统计学意义(t=2.96,P<0.01)。见表2。 DXA测量结果表明,两组患者内脏脂肪含量、体积和面积均较治疗前显著降低,差异有统计学意义(P<0.05)。在3个月时,两组的平均内脏脂肪组织面积均降至160 cm2以下,二甲双胍组与治疗组内脏脂肪组织面积平均值分别为(144.83±14.81)cm2与(143.85±15.20)cm2,160 cm2是与女性心血管疾病的高风险阈值。
2.3 两组患者代谢参数变化比较 在研究开始时,35例(二甲双胍组13例,联合组22例)患者发生IGT。治疗后,联合组有21例患者对葡萄糖负荷的反应恢复正常。治疗后,联合组HOMA-IR指标较治疗前显著降低,差异有统计学意义(t=2.19,P=0.03)。与二甲双胍组比较,联合组HOMA-IR指标差值大于二甲双胍组,差异有统计学意义(t=2.47,P=0.02)。 治疗后,联合组空腹血糖和餐后2 h血糖均较治疗前显著降低,差异有统计学意义(t=3.80、2.66,P<0.01)。与二甲双胍组比较,联合组空腹血糖和餐后2 h血糖差值大于二甲双胍组,差异有统计学意义(t=9.15,t=8.63,P<0.01)。见表3。
2.4 两组患者内分泌参数变化比较 治疗后,二甲双胍组与联合组患者的SHBG均较治疗前显著提高,差异有统计学意义(t=2.30,P=0.03;t=2.72,P<0.01),但两组SHBG差值比较差异无统计学意义(t=1.85,P=0.07)。见表3。
2.5 两组患者妊娠和IVF参数 联合组中93例患者有64例(68.8%)在1年内妊娠。7例患者在治疗后立即自然妊娠,42例在IVF手术后妊娠,15例在IVF失败后自然妊娠。二甲双胍组93例患者有35例(37.6%)在1年内妊娠,6例在治疗后立即妊娠,14例在接受IVF手术后妊娠,15例在IVF失败后自然妊娠。与二甲双胍组比较,联合组的临床妊娠率(χ2=30.42,P<0.01)和累计妊娠率(χ2=18.16,P<0.01)显著提高,差异有统计学意义。但两组间总Gn剂量、获卵数、成熟、受精和退化的卵母细胞数、胚胎数、第5天胚胎数比较差异无统计学意义(P>0.05)。见表4。

表3 两组患者基线期和治疗后的内分泌参数比较
注:与治疗前比较,*P<0.05,**P<0.01

表4 两组患者IVF治疗结果比较
2.6 两组患者药物不良反应发生情况比较 二甲双胍组患者发生恶心6例、腹泻7例,联合组患者发生恶心11例、腹泻10例。两组患者恶心与腹泻发生率比较差异无统计学意义(χ2=1.56,P=0.21;t=0.58,P=0.45),利拉鲁肽的低剂量和逐渐滴定降低了胃肠不良反应发生率。
3 讨论
本研究结果表明,低剂量利拉鲁肽联合二甲双胍对肥胖不孕的PCOS患者进行短期干预,可以显著提高患者的临床妊娠率和累计妊娠率,并显著降低患者的体重、内脏脂肪、代谢和内分泌参数,但没有显著提高患者的药物不良反应发生率。目前的国际指南推荐肥胖女性自然妊娠前或IVF手术前减轻体重,但缺乏减重最佳幅度和时间的数据。一些前瞻性随机对照研究评价了肥胖育龄妇女接受IVF前进行短期减重的情况,而关于IVF妊娠结果的研究较少。Sim等[15]的研究评价了减重干预对肥胖妇女妊娠率的影响,结果显示,减重组在饮食、运动和行为支持下的临床妊娠率和活产率更高(48%vs.14%,P<0.01;44%vs.14%,P=0.02)。Espinós等[16]的研究表明,减重后的PCOS患者累计活产率显著提高(61.9%vs.30%)。在一项对澳大利亚的非PCOS肥胖患者研究中,患者通过科学饮食和运动在5~9周内减重(3.8±3.0)kg,干预组和对照组的临床妊娠率和活产率差异无统计学意义,妊娠率增加与腰围降低有关[17]。但Mutsaerts等[18]的一项有290例肥胖女性参与的多中心研究显示,IVF之前减重未能改善生殖结果。
本研究中,联合组中68.8%的女性和二甲双胍组中57.0%的女性在通过12周的药物干预和生活方式改变减重超过5%。二甲双胍组患者平均减少(6.98±6.03)kg,而联合组患者减少(7.52±3.90)kg。联合组的减重幅度与之前的研究结果一致,二甲双胍组的减重幅度超出预期,因为使用二甲双胍的PCOS肥胖女性有记录的最大绝对减重约为2.7 kg,小于体重的5%。本研究中二甲双胍组患者减重幅度更大,其原因可能是本研究中内分泌学医生和妇科医生等多学科团队通过教育,让患者认识到与母亲肥胖相关的妊娠和胎儿风险,极大地提高了患者改变生活方式的积极性。
目前关于胰高血糖素样肽-1受体激动剂(Glucagon-like peptide-1,GLP-1)类似物对不孕患者生殖影响的研究较少。利拉鲁肽可能通过几种不同的机制影响患者生殖系统,减重是其中最重要的机制之一。Liu等[19]进行了一项为期24周的前瞻性随机临床研究,比较了176例接受短效GLP-1RA艾塞那肽(Exenatide,Exe)和二甲双胍的PCOS超重/肥胖女性的妊娠情况,结果表明,短期Exe治疗与体重显著减轻[(4.29±1.29)kg vs.(2.28±0.55)kg,P<0.001]、总脂肪减少百分比、IR改善和月经频率提高有关,Exe治疗患者12周内的自然妊娠率显著高于二甲双胍治疗患者(43.60%vs.18.70%)。其研究提示减重改善了月经周期和排卵的机制,并主要通过减少内脏脂肪和改善胰岛素敏感性实现。
利拉鲁肽的第2种作用机制是通过减重改善患者IR来提高患者临床妊娠率。相关研究深入评价了IR和高胰岛素血症在PCOS疾病中的作用,结果表明,IR和高胰岛素血症在PCOS和无排卵的病理生理学中发挥重要作用[20]。胰岛素可通过增加卵巢雄激素分泌来增强黄体生成素(Luteinizing hormone,LH)的作用。胰岛素还能够抑制肝脏分泌SHBG,促进睾酮水平提高。胰岛素敏感性的改善在卵巢功能恢复过程中起着关键作用[1,21]。在本研究中,联合组HOMA-IR指标显著降低,二甲双胍组和联合组中SHBG的增加降低了雄激素的生物利用度。两组患者大多数雄激素均有所下降,不过降低值比较差异无统计学意义。
尽管两组患者内脏脂肪组织和雄激素生物利用度的降低程度相似,但联合组对临床妊娠率的影响更显著。这一结果提示,利拉鲁肽对生殖潜力的影响超过了减重和IR改善。动物实验表明,GLP-1通过下丘脑-垂体系统参于生殖系统的调节,侧脑室注射GLP-1可提高大鼠血浆LH水平[22]。近期的一项大鼠研究发现,在发情周期中大鼠GLP受体在下丘脑、垂体和卵巢的表达发生变化。在发情前用天然GLP-1紧急治疗,可使大鼠LH变化幅度加倍并导致黄体期黄体酮增加。这些变化增加了成熟格雷夫氏卵泡数量,提高了大鼠生殖能力。但应用EXE治疗具有与GLP-1相反的作用,可使LH波动降低50%。下丘脑-垂体轴调节系统可使月经周期更加规律,促进排卵,并调节饥饿感和饮食习惯。研究假设GLP-1参与了下丘脑-垂体系统中这两种活动的耦合,并作为生殖系统的代谢信号。在空腹48 h后,垂体LH迅速减少时,大鼠的下丘脑GLP-1水平显著降低。重新喂食后,GLP-1有恢复正常的趋势,可能有助于恢复LH分泌[23]。
动物研究表明,由于在子宫内膜上皮和基质层中被诱导的细胞毒性,糖尿病与子宫内膜的结构和功能的变化相关[21]。被诱导的子宫内膜改变可能导致植入失败、妊娠失败和胎盘缺陷,这在PCOS患者中较为常见。子宫内膜基质纤维化和变性增加在糖尿病大鼠中得到证实,短效GLP-1类似物Exe改善了动物模型中的子宫内膜功能。其所观察到的Exe效应可能主要是由于拮抗氧化应激和转化生长因子β水平降低减少了子宫内膜的纤维化。
研究表明,GLP-1 RA在2型糖尿病患者和无糖尿病的肥胖患者中有着良好的8年风险-效益平衡。有关人类在妊娠期间应用GLP-1 RA的研究较少,这些研究均为单一的病例报告,例如Artunc-Ulkumen等[24]的研究显示,妊娠13周的患有2型糖尿病患者应用利拉鲁肽后妊娠结果正常。Yang等[25]的病例报告报道了1例患有PCOS和IR的超重女性应用GLP-1 RA Exe进行短期的孕前干预,患者成功自然妊娠,治疗过程中Exe没有引起患者的药物不良反应。Liu等[19]的临床研究评价使用Exe进行妊娠前干预对超重/肥胖PCOS患者的生殖和代谢功能的影响,结果表明,Exe没有发生重大的安全性问题。利拉鲁肽在2型糖尿病和肥胖受试者中具有良好的短期安全性,因此用其对PCOS受试者进行短期孕前治疗是可行的。
二甲双胍是肥胖糖尿病患者临床治疗的一线药物,其既有降糖作用,也有显著的降低体重的作用,但是关于二甲双胍减重的机制目前还不清楚,其中可能的机制包括:①实验室研究表明,二甲双胍加入到含有脂肪前体细胞培养基后,苏氨酸上的AMP蛋白激酶被磷酸化,进而破坏了细胞内脂质的聚集,抑制了脂肪的合成;②二甲双胍可以激活棕色脂肪的P44/P41MAPK,进而减少了瘦素分泌,并最终达到对食欲的抑制作用。这一效应有剂量依赖性,与PI3K完全不相关[26]。本研究显示,以二甲双胍为基础用药,同时联合利拉鲁肽患者的减重效果更好。利拉鲁肽是一种GLP-1受体激动剂,最初是作为降糖药物上市的。利拉鲁肽能够特异性地结合胰岛B细胞上的GLP-1受体,并激活G蛋白信号通路,进一步活化环磷酸腺苷(Cyclic adenosine monophosphate,cAMP),激活依赖cAMP的蛋白激酶A(Protein kinase A,PKA),PKA可以使蛋白质磷酸化,进而促进机体分泌胰岛素,这些蛋白质在葡萄糖转导途径中起到关键作用。同时,利拉鲁肽可以磷酸化和活化CREB核转录因子,使CREB结合胰岛素原基因启动子区的关键DNA序列,提高了胰岛素原基因的转录效率,促进胰岛素基因转录到胰岛素的生物合成作用。另外,利拉鲁肽具有较长的半衰期,每天仅需要注射1次,能够最大限度地降低患者的痛苦[27]。 综上所述,低剂量利拉鲁肽联合二甲双胍对超重不孕的PCOS患者进行短期干预,可以显著提高患者的临床妊娠率和累计妊娠率,并显著降低了PCOS患者的体重、内脏脂肪组织,没有显著增加患者的药物不良反应。
