新型镉(Ⅱ)配位聚合物的合成与性能
2020-06-05顾祥伟仇立亚李育杰
顾祥伟, 仇立亚, 李育杰, 黄 薇
(常州大学 石油化工学院,江苏 常州 213164)
金属有机框架(metal-organic frameworks, MOFs)材料是一种以无机金属离子与有机配体通过自组装过程形成的具有周期性网络结构的晶体材料,因此它兼备了有机高分子和无机化合物的优点,其后的功能化修饰是制造可调MOF和衍生高性能功能材料的一种有效策略。其后功能化修饰已被证明可促进MOF主体和客体分子之间的可逆解离/缔合,这是开发具有电子应用潜力的功能性分子固体的理想特征[1-6]。在过去的几十年中,通过后合成方法制备了多种具有改进性能的、结构可调的MOF和MOF衍生材料[7-11]。在这些材料中,后功能化荧光MOF吸引了研究人员的广泛关注[12-14]。荧光单个发射源通常不覆盖整个可见光谱[15-17],因此为了获得发白光(WLE)材料,需要不止一种发光物质。镧系元素共掺杂是制备WLE镧系元素MOF的重要方法。然而,通过直接合成精确控制材料中不同镧系元素离子的化学计量是很困难的。因此,后功能化掺杂策略可以在直接合成方面,特别是在WLE材料的设计中具有一些优点,例如制造工艺更简单,成本降低,准确性增强和改进的结构可预测性。从应用的角度来看,后功能化混合材料的发光可以通过MOF内可弯曲的镧系元素的可逆封装来定制,以覆盖整个可见光区域,从而能够设计多色温度计[18-19]。为了构筑具有特殊拓扑结构的多维MOFs 材料,人们常使用含氮、氧等多齿有机配体和含羧基芳香类配体混合调控其结构。1,3,5-三(咪唑基)苯(tib)作为一种刚性较强的有机配体,可用于多维配位聚合物的设计和构筑[20];4,4-二苯醚二甲酸(H2L)由于其配位方式灵活多样,配位点丰富[21],也被广泛用于MOFs材料的合成。
本文以tib,H2L和Cd(NO3)2·6H2O 为原料,用水热法合成了一种新的三维Cd (Ⅱ)配位聚合物[Cd2(L)4(tib)2DMF]n·DMF (Cd-2 MOF)(1),其结构和固体荧光性能经IR,元素分析和XRD表征。
1 实验部分
1.1 仪器与试剂
FT-IR-960型红外光谱仪(KBr 压片);EAI CE-44型元素分析仪;PHOTON 100 CMOS detector型X-射线单晶衍射仪;FS5型荧光仪。
H2L和Cd(NO3)2·6H2O,分析纯,安耐吉试剂公司;tib按文献[22]方法合成;其余所用试剂均为分析纯或化学纯。
1.2 配合物1的合成
在25 mL内衬聚四氟乙烯的不锈钢反应釜中依次加入H2L 24.0 mg(0.1 mmol), tib 27.6 mg(0.1 mmol), Cd(NO3)2·6H2O 29.7 mg(0.1 mmol)和N,N-二甲基甲酰胺10 mL,于150 ℃反应4 d。经24 h冷却至室温,过滤得无色棒状晶体,产率89%(以Cd计);FT-IRν: 475(w), 662(m), 754(w), 887(m), 942(w), 1015(w), 1115(s), 1198(w), 1224(w), 1370(w), 1467(w), 1597(w), 3224(s), 3424(w) cm-1; Anal. calcd for C52H34N9O15Cd2: C 51.36, H 2.72, N 10.37, found C 50.79, H 2.69, N 10.47。
1.3 晶体结构测定
在显微镜下挑选一颗形态较为完整、光泽较均匀的配合物1的单晶,采用经过石墨单色器单色化的MoKα(λ=0.71073 Å)作为入射光源,以φ-ω扫描方式收集173(2) K条件下的单晶衍射数据,强度经经验吸收校正和Lp校正。采用直接法解析晶体结构,对全部非氢原子坐标及其各项异性热参数进行了全矩阵最小二乘法修正,氢原子的位置由理论加氢得到。所有计算用SHELXS-2013[23]和SHELXL-2014/7[24]程序包完成。配合物1(CCDC: 1901161)的晶体学数据见表1,主要键长和键角数据见表2。

表1 1的晶体学数据
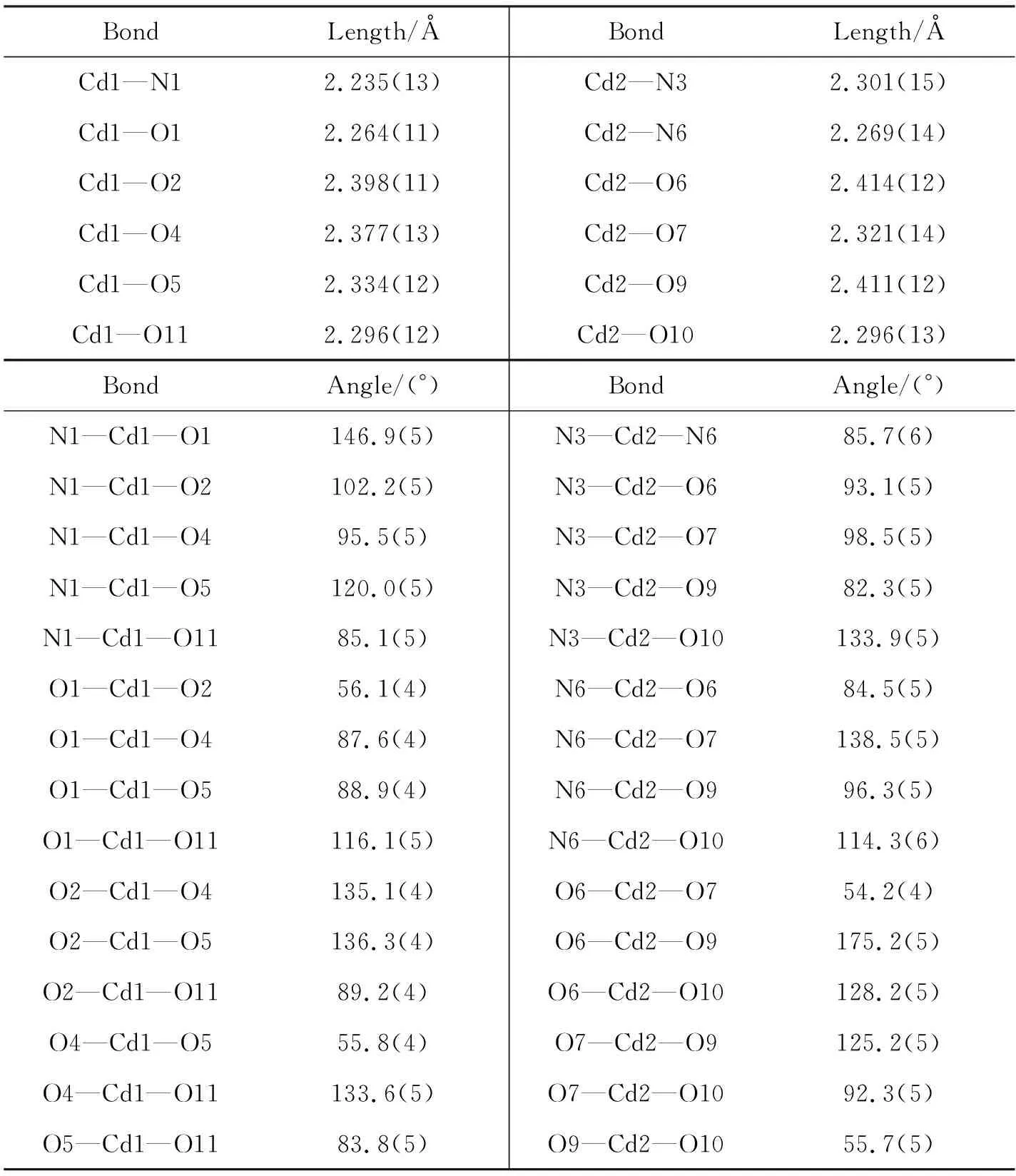
表2 配合物1的部分键长和键角
2 结果与讨论
2.1 表征
配合物1的FT-IR分析表明:3424 cm-1处吸收峰为酰胺中的N—H的伸缩振动峰;3224 cm-1处吸收峰归属于羧基的伸缩振动;1597 cm-1处吸收峰为苯环中的C—C骨架振动峰;1467和1370 cm-1处吸收峰归属于甲基中C—H的弯曲振动;942 cm-1处吸收峰归属于醚基的弯曲振动;1224、 1198、 1115、 1015、 887、 754、 665和475 cm-1处吸收峰为苯环的C—H面外弯曲振动峰。
2.2 晶体结构
配合物1的晶体结构见图1。从图1可以看出,配合物1的最小不对称单元里包含了两个Cd(Ⅱ)、 4个柔性H2L、两个刚性tib以及一个DMF(N,N-二甲基甲酰胺),两个Cd(Ⅱ)均采用两种不同的六配位模式(图1a):六配位的Cd1分别和两个H2L中两个羧酸酯的双齿O(O1, O2, O4, O5)及溶剂DMF中的一个O(O11)和配体tib中的一个N(N1)进行配位,呈高度扭曲的八面体构型;另一个六配位的Cd2则和两个H2L中羧酸酯基的双齿O (O6, O7, O9, O10)及两个tib的N(N3, N6)同时进行配位,形成扭曲的八面体构型。Cd—N键的键长范围2.269(14)~2.301(15) Å, 4个柔性的H2L配体参与配位并提供配位氧原子,Cd—O键的键长范围1.917(16)~-2.377(13) Å(表2)。晶体结构分析结果表明,两个羧酸基团均充当双齿配体,通过金属中心与tib连接在一起。相邻Cd1中心通过tib和H2L2交叉连接,从而形成复杂的3D金属有机框架,如图1(b)所示。

(a)
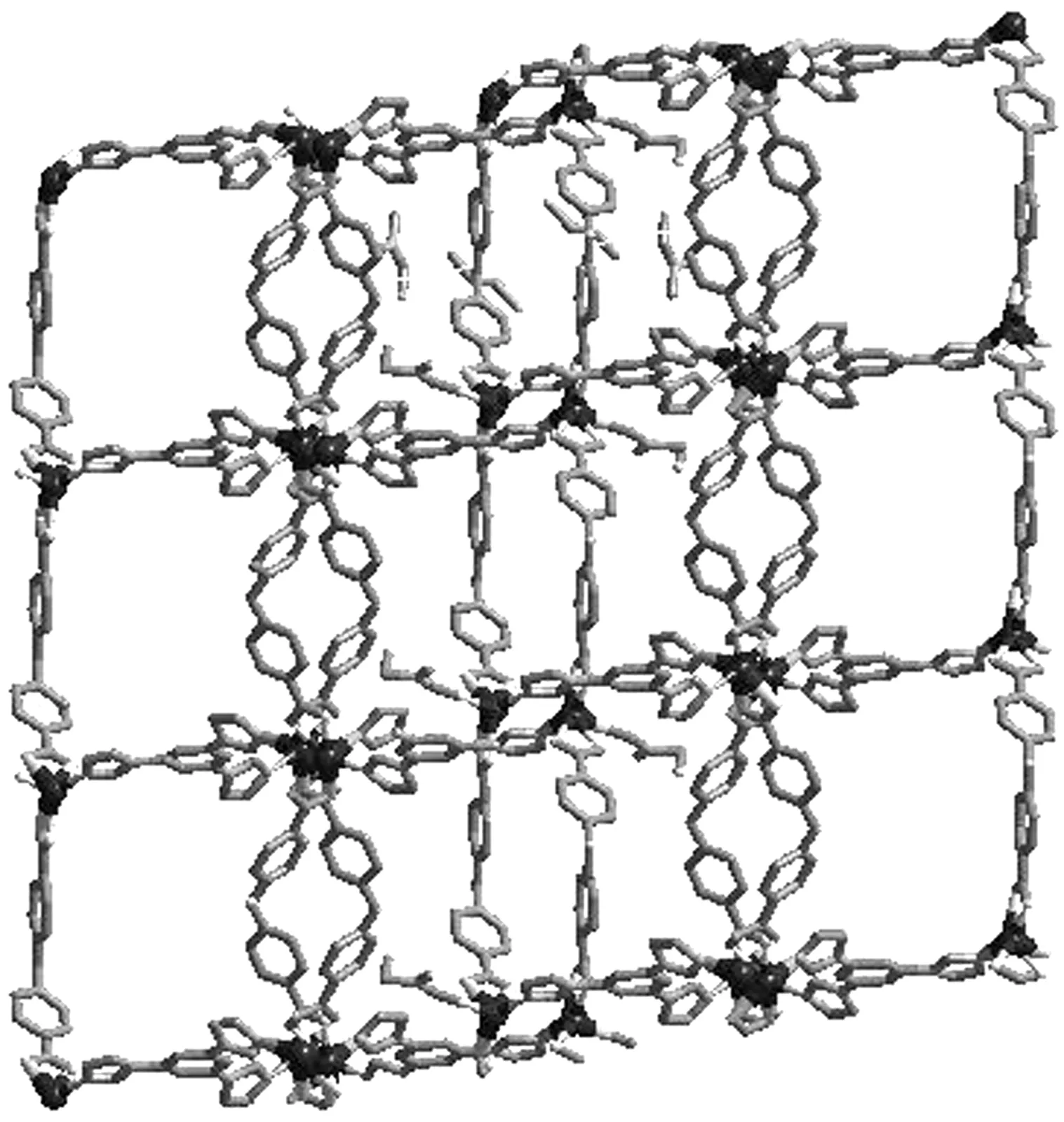
(b)
2θ/(°)
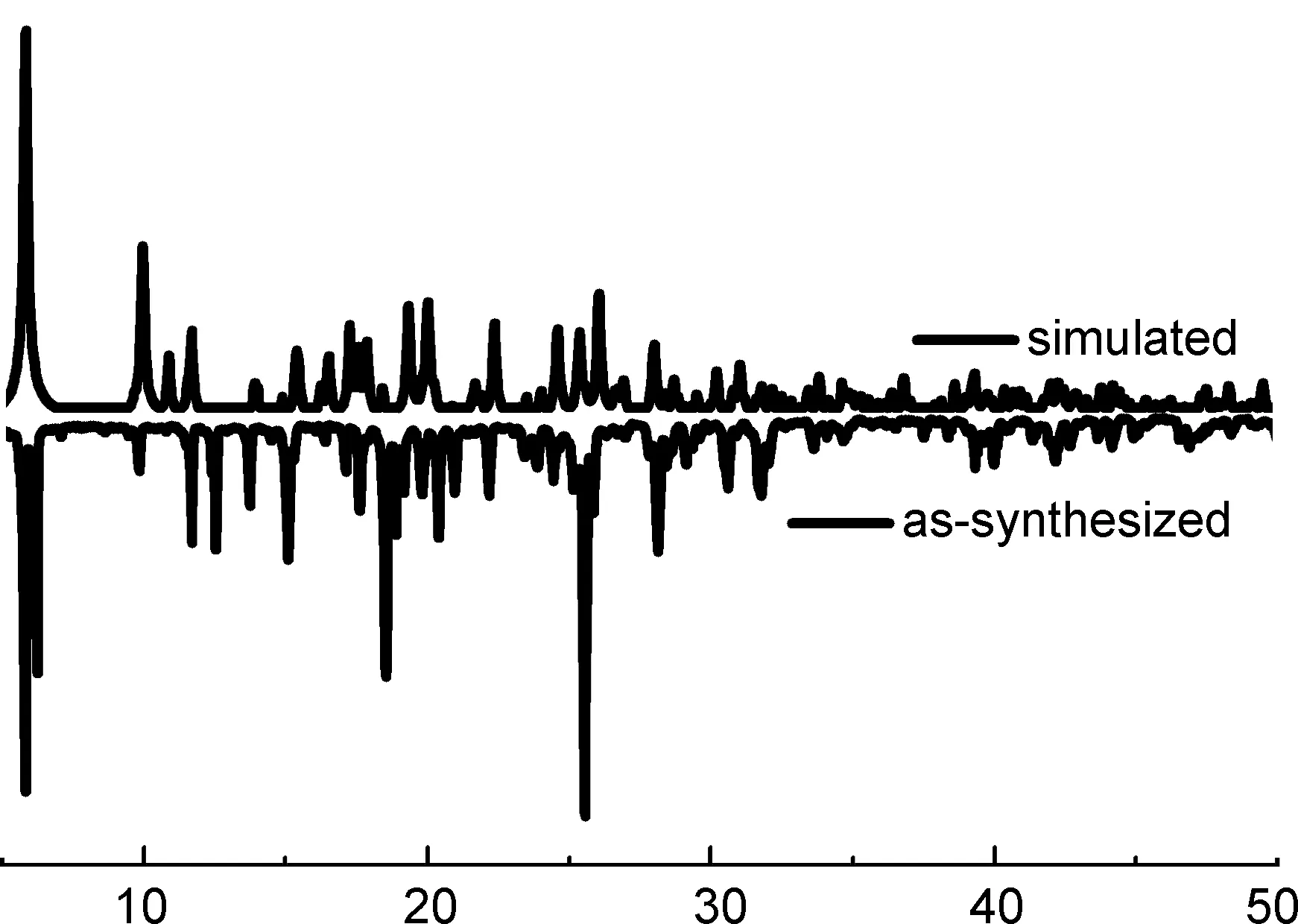
2.3 X-射线粉末衍射分析
图2为配合物1X-射线粉末衍射谱图。由图2可见,晶体样品的粉末衍射与模拟谱衍射峰的位置和强度基本一致。

λ/nm

λ/nm

Temperature/K图3(a)配体tib和配合物1在室温下归一化的固体发射光谱;(b) 配合物1对温度响应的荧光光谱;(c) 配合物1在377 nm、 466 nm处的温度依赖变化趋势
λ/nm

n(Tb3+)/n(Eu3+)
2.4 荧光性质
配合物1在室温下的固态荧光发射光谱见图3。H2L在270 nm波长下激发时,在315 nm处具有最强的荧光发射峰。在425 nm波长下激发时,配合物1具有宽且强的荧光发射峰,在490 nm处具有最强的发射峰,与配体tib在相同激发波长下的最强发射峰(471 nm)比较,配合物的发射光谱发生了明显的红移,其原因是配体到金属离子(LMCT)间的电荷转移[25](图3a)。配合物1具有温度响应的荧光现象,有利于其在温度传感中的使用。配合物在一定的温度下具有双发射。随着温度的升高,长波长处发射峰的强度逐渐下降,当温度达到350 K时,发射峰几乎完全消失,配合物的非辐射跃迁的增强是荧光强度减弱的原因[26]。在80~160 K, 466 nm处的发光强于377 nm处的发光强度,并随温度的升高荧光强度减弱。值得注意的是,在170~350 K, 377 nm处发光强于466 nm处的荧光强度,这主要是由于配体与配体间的能量转移引起的(图3c)。
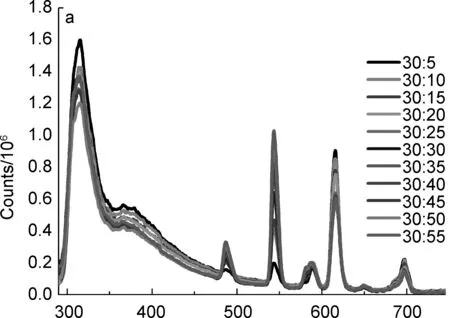
文献[27]研究了单层MOF和双层金属有机框架镧系元素的包封,我们将Ln3+阳离子结合到Cd-2 MOF的三维平台。通过向Cd-2 MOF在甲醇中的悬浮液中逐渐添加Eu3+、 Tb3+来探究Eu3+、 Tb3+共掺杂复合材料(EuTb@Cd-2 MOFs)的荧光性质。通过调节Eu3+与Tb3+物质的量比来调节其荧光的发射,当n(Eu3+)/n(Tb3+)从30变化到30/55时实现由红光→白光的荧光转变[CIE坐标(0.30, 0.32)]。主要策略是控制Eu3+的含量不变,增加Tb3+的浓度,在此过程中发现Eu3+在617 nm处特征峰的荧光强度逐渐减弱,而Tb3+在545 nm处特征峰的荧光强度逐渐增强,这是由于发生了从Tb3+到Eu3+的能量转移,如图4(a)所示,且Cd-2 MOFs中稀土离子n(Tb3+)/n(Eu3+)的发射强度比呈线性相关,如图4(b)所示。
采用水热法合成了一个新型的Cd(Ⅱ)配位聚合物[Cd2(L)4(tib)2DMF]n·DMF,并研究了配合物的晶体结构和发光性质。室温固态荧光测试结果表明,配合物具有宽且较强的荧光发射。
