含硼替佐米化疗的两种方案治疗初治多发性骨髓瘤疗效及对患者总生存期和毒副反应的影响
2020-06-03张天琰吴秋慧陈春平
张天琰,阳 梅,吴秋慧,陈春平
(四川大学华西医院血液内科,四川 成都 610041)
多发性骨髓瘤是一种起源于骨髓浆细胞的恶性肿瘤,其病理特征为骨髓浆细胞异常增生伴有单克隆免疫球蛋白或轻链过度生成,且常伴有多发性溶骨损害、高钙血症、肾脏损伤等[1,2]。随着对多发性骨髓瘤发病机制研究的深入,新型靶向药物蛋白酶体抑制剂硼替佐米被广泛应用于临床,并取得较好疗效[3,4]。本研究比较含硼替佐米化疗的两种方案疗效及对患者生存期和毒副反应的影响,现报道如下。
1 资料与方法
1.1 一般资料2014年1月至2016年1月我院收治的初治多发性骨髓瘤患者107例,纳入标准:参照《中国多发性骨髓瘤诊治指南(2013年修订)》[5]中多发性骨髓瘤的诊断标准;均为初发未治患者;同意使用含硼替佐米的化疗方案;年龄18~80岁;依从性好;临床资料完整。排除标准:肾功能不全者;本研究化疗药物禁忌者;重要器官功能障碍;合并其他恶性肿瘤;既往相关化疗治疗史;严重感染;先天性免疫疾病;妊娠、哺乳期女性。其中75例行BCD方案化疗(BCD组,硼替佐米+环磷酰胺+地塞米松),32例行BAD化疗方案(BAD组,硼替佐米+阿霉素+地塞米松)。BCD组年龄35~78岁[(55.73±14.26)岁];男46例,女29例;免疫球蛋白(Ig)分型:IgG型35例,IgA型18例,IgD型 7例,轻链型15例;Durie-Salmon(D-S)分期:1A期5例,2A期7例,3A期52例,3B期11例。BAD组年龄33~80岁[(57.43±14.81)岁];男21例,女11例;Ig分型:IgG型19例,IgA型7例,IgD型 2例,轻链型4例;D-S分期:1A期2例,2A期4例,3A期22例,3B期4例。两组年龄、性别、Ig分型及D-S分期资料比较,差异无统计学意义(P> 0.05)。
1.2 治疗方法BCD组:于治疗第1、4、8、11 d给予硼替佐米(西安杨森制药有限公司,国药准字J20120055,规格3.5 mg)静脉推注,剂量1~1.3 mg/(m2·d);于治疗第1、2、3、4 d给予环磷酰胺(江苏盛迪医药有限公司,国药准字号H32020857,规格0.2 g)静脉滴注,剂量200 mg/(m2·d);于治疗第1~2、4~5、8~9、11~12 d给予地塞米松磷酸钠(天津金耀集团湖北天药药业股份有限公司,国药准字号H42020019)静脉滴注,20 mg/d。BAD组:于治疗第1、4、8、11 d给予硼替佐米静脉推注,剂量1~1.3 mg/(m2·d);于治疗第1、2、3、4 d给予盐酸表阿霉素(浙江海正药业股份有限公司,国药准字H19990280)静脉滴注,剂量10 mg/(m2·d);于治疗第1~2、4~5、8~9、11~12 d给予地塞米松静脉滴注,20 mg/d。所有患者均完成2~4个疗程,且均口服沙利度胺(常州制药厂有限公司,国药准字H32026129)100 mg/d,作为维持治疗;若患者在化疗过程中出现难以耐受的不良反应时,应暂停推迟甚至终止化疗。
1.3 观察指标①疗效评价:参照《中国多发性骨髓瘤诊治指南(2013年修订)》中临床效果评估标准[5],分为完全缓解、非常好的部分缓解、部分缓解、疾病稳定和疾病进展,治疗有效率=(完全缓解例数+非常好的部分缓解例数+部分缓解例数)/总例数×100%。②不良反应:参照美国国立癌症肿瘤研究所制定常见毒性反应标准[6](NCI-CTCAE),详细记录患者出现的相关不良反应,如头晕、乏力、恶心、呕吐、四肢麻木及水肿等,计算不良反应发生率。③Karnofsky(KPS)评分:于患者开始化疗前1 d及治疗结束时,采用KPS评分[7]评价患者生存质量,分值0~100分,分值越高表明健康状况越好,越能忍受治疗给身体带来的副作用,从而接受彻底治疗。④随访至2019年1月31日,以复查、电话形式,观察患者无进展生存期(PFS)和总生存期(OS);PFS是指患者从开始治疗到疾病出现进展、复发、死亡、随访结束或失访的时间,OS是指患者从开始治疗到死亡、随访结束或失访的时间[8]。
1.4 统计学方法采用SPSS 21.0统计学软件分析数据。计量资料以均数±标准差表示,两两比较采用独立t检验;计数资料以率(%)表示,采用卡方检验;釆用Kaplan-Meier生存函数描述患者生存数据,采用Log-rankχ2进行组间比较。P< 0.05为差异有统计学意义。
2 结果
2.1 两组治疗效果比较BAD组治疗总有效率显著高于BCD组(χ2=3.982,P< 0.05),见表1。

表1 两组治疗效果比较
2.2 两组不良反应比较两组各不良反应发生率比较,差异无统计学意义(P> 0.05),见表2。

表2 两组不良反应比较 [n(%)]
2.3 两组KPS评分比较治疗前,两组KPS评分比较,差异无统计学意义(P> 0.05);治疗后,BAD组KPS评分显著高于BCD组(P< 0.05),见表3。

表3 两组KPS评分比较 (分)
2.4 两组生存情况比较随访至2019年1月31日,BCD组3年无进展生存率为21.33%(16/75),中位PFS为12.6个月;3年总生存率为77.33%(58/75)。BAD组3年无进展生存率为37.50%(12/32),中位PFS为19.2个月;3年总生存率为81.25%(26/32)。两组3年无进展生存率和总生存率比较,差异无统计学意义(Log-rankχ2=2.051,P= 0.152;Log-rankχ2=0.212,P= 0.646)。见图1。
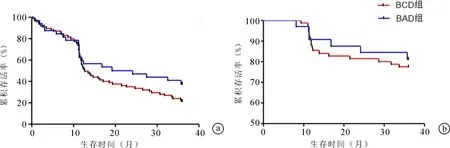
图1 两组生存情况比较 a:PFS;b:OS
3 讨论
近几年,临床研究发现,硼替佐米在初发未治多发性骨髓瘤中有良好的疗效,且其不良反应较传统化疗方式少[9]。硼替佐米具体作用途径主要有:①调控细胞凋亡信号通路,引起肿瘤细胞凋亡;②抑制肿瘤细胞生存相关信号通路,如NF-κB途径;③阻碍血管新生相关蛋白因子的表达,从而抑制肿瘤细胞的浸润和侵袭[10]。沙利度胺是一种免疫调节剂,可通过抑制成纤维细胞和血管内皮生长因子的分泌,最终抑制肿瘤新生血管的形成[11]。据报道,沙利度胺联合地塞米松用于多发性骨髓瘤的治疗有较好效果[12]。环磷酰胺和阿霉素是治疗多发性骨髓瘤的传统化疗药物,均属于周期非特异性药物。环磷酰胺是目前广泛应用的抗癌药物,多用于恶性淋巴瘤、多发性骨髓瘤、急性或慢性淋巴细胞白血病等;主要通过抑制细胞周期中DNA的合成而起到抗癌作用。阿霉素主要作用于细胞核,抗癌机制可能是通过与DNA结合,抑制核酸物质的合成和细胞有丝分裂过程。
本研究在硼替佐米联合地塞米松及沙利度胺的基础上,分别加入环磷酰胺和阿霉素,分别组成化疗方案BCD(硼替佐米+环磷酰胺+地塞米松),BAD化疗方案(硼替佐米+阿霉素+地塞米松),107例患者中75例患者接受BCD方案,32例接受BAD方案。BAD组患者治疗总有效率为96.88%,显著高于BCD组,提示BAD治疗初治多发性骨髓瘤疗效优于BCD。同时,BAD组患者治疗后KPS评分显著高于BCD组,表明BAD化疗方案能更有效提高患者生活质量。
Chen等[13]研究显示,硼替佐米治疗的不良反应主要有周围神经病变、血液系统损伤、感染及消化系统损伤等。本研究发现,经2~4个疗程治疗,两组患者均出现不同程度的不良反应,且对症治疗后均好转。不良反应可分为血液系统和非血液不良反应,前者临床表现为粒细胞减少、血小板减少及贫血,非血液不良反应主要有乏力、感染、便秘、腹泻、胸腹积水、带状疱疹及周围神经病变,与Peng等[14]报道一致。但两组患者各种不良反应发生率和3年生存情况无显著差异,但本研究纳入病例数较少,远期影响观察不足,后期需多中心扩大样本量、延长随访时间,深入分析BCD和BAD对于初发未治多发性骨髓瘤患者的毒副作用。值得注意的是,两组患者周围神经病变发生率较高,提示硼替佐米治疗过程中,应密切监测患者神经学表现,需要根据患者疾病情况,及时调整化疗方案。
综上所述,BAD方案治疗初治多发性骨髓瘤疗效较好,可有效改善患者生存质量,效果优于BCD方案;但两种方案不良反应发生率和对患者生存期的影响相差无几,还需要收集远期观察数据作进一步比较。另外,含硼替佐米化疗方案的神经毒性作用较大,治疗过程中需密切关注患者病情的变化,适度调整用药方案。
