治疗新型冠状病毒肺炎潜在药物:Remdesivir
2020-06-03杨兴祥周巧灵杨仁国
庹 琳,杨兴祥,周巧灵,杨仁国
(四川省医学科学院·四川省人民医院感染科,四川 成都 610072)
2019年12月,我国湖北省武汉市出现了一系列不明原因的肺炎病例。经研究发现感染源为一类新型的冠状病毒(CoVs),后被命名为2019新型冠状病毒(2019 novel coronavirus,2019-nCoV)(图1)[1]。截止2020年3月1日,全世界已有86461人受到病毒侵害,死亡2978人。目前尚无循证医学证据支持现有抗病毒药物对 2019-nCoV 有效[2],因此寻找到合适的抗病毒药物对于控制疫情蔓延十分危急且重要。
Remdesivir(GS-5734)是一类抑制RdRp(RNA-dependent RNA polymerase)的腺苷核苷酸类似物,见图2。疫情爆发初期,复旦大学卢洪洲教授提出广谱抗病毒药物Remdesivir[3~5]是治疗2019-nCoV的潜在药物之一[6]。2020年2月1日发表的有关美国首例新冠肺炎患者的个案报道中,患者使用Remdesivir后低氧血症、肺部感染等得到了很好的恢复[7]。上述报道均提示Remdesivir极有可能成为新型冠状病毒肺炎潜在的治疗药物,本文主要对该化合物的历史、作用机制、临床研究等方面进行综述。
1 历史
2013~2016年西非爆发的埃博拉病毒感染是有史以来最大规模的埃博拉相关疫情,累计超过28000例患者受到感染,并导致超过500名医护人员在内的11000重症感染者死亡[8]。针对埃博拉病原,研究者在早期临床试验中开发了包括单克隆抗体(ZMapp),7种干扰RNA,和小分子核苷抗病毒药(favipiravir/brincidofovir)等[9~11],但是这些潜在的疗法均未建立起用于治疗病毒急性感染或持续后遗症的临床功效。
图1 新型冠状病毒武汉株01(国家微生物科学数据中心.首株环境样本中分离的新型冠状病毒毒种信息[EB/OL].2020-01-27.http://nmdc.cn/#/nCoV)
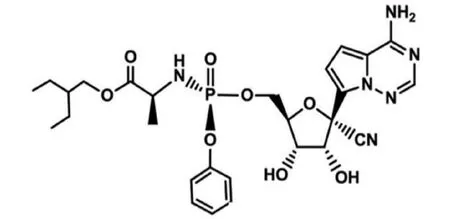
图2 Remdesivir的分子结构[4](Agostini M L.mBio,2018,9(2))
Remdesivir是疾病预防控制中心(CDC)和美国陆军传染病医学研究所(USAMRIID)合作,从1000个不同的核苷和核苷膦酸酯类似物的文库中筛选出了针对埃博拉病毒(Ebola virus,EBOV)的化合物之一。在巨噬细胞中,以埃博拉病毒EC50=86 nm作为临床候选指标之一,重点筛选和前导优化鉴定出GS-5734,其包含的1′-CN基团和C连接的核碱基对于抗EBOV效能和针对宿主聚合酶的选择性至关重要。在非人类灵长类EBOV感染模型中,感染后3~14天,每天一次静脉注射10 mg/kg Remdesivir,对病毒血症和死亡率有显着影响,导致被感染动物的存活率为100%,从而实现了临床前疗效[12]。目前,该药物已经在乌干达完成了治疗埃博拉病毒的II期临床试验,大型临床试验验证了其安全性[13]。III期临床试验已于2020年2月3日在中国武汉中日友好医院的270例样本中进行,不同的是此次临床实验针对的病原体是2019-nCov。
2 抗冠状病毒的药物
CoVs是一种有包膜的正单链RNA病毒,包括α、β、γ、δ四类基因组,可感染鸟类和多种哺乳动物[14]。大多数CoVs菌株的寄主范围较窄,迄今为止已知仅α、β亚科可以感染人类,但是随着人类和野生动物生态学的重叠越来越多,人畜共患的CoV更倾向于出现在人类群体。严重的急性呼吸综合症冠状病毒(SARS-CoV)和中东呼吸综合症冠状病毒(MERS-CoV)及本次的2019-nCoV均属于人畜共患的β属冠状病毒,其自然宿主主要为蝙蝠[15]。这些新颖的冠状病毒能够有效利用人类血管紧张素转化酶2(Angiotensin Converting Enzyme 2,ACE2)受体,在人类气道粘膜细胞等中复制至高滴度,并且对现有的药物及疫苗具有抵抗性[16]。因此,急需研究出一类广谱的抑制冠状病毒的药物或疫苗,应对当前或将来出现的新型冠状病毒感染疫情。
冠状病毒是病毒中种类最多,变异最快的组之一,而新型的冠状病毒会在无法预测的时间内反复出现,因此专门针对现有的冠状病毒复制的药物可能对新型冠状病毒无效,包括特异性的病毒酶抑制剂[17],靶向受体细胞的试剂[18]以及单克隆抗体[19]等。因此,广谱的抗冠状病毒药物是急需深入研究并进行进一步临床实验的。靶向病毒核苷酸的药物通常具有针对多种CoV和其他病毒的广谱活性,如霉酚酸酯[20];针对长病毒双链RNA(dsRNA)的抗病毒药物选择性地诱导在包含病毒dsRNA的细胞凋亡,如DRACO[21];抑制CoV蛋白酶能够抑制冠状病毒的复制、裂解以及释放,如洛匹那韦/利托那韦[22];增强宿主固有的干扰素反应能够控制感染后的冠状病毒的复制,如干扰素α/干扰素β[23,24]。
3 Remdesivir抗冠状病毒的作用
2016年,Warren等[12]报道了腺苷类似物Remdesivir在非人类灵长类动物中对埃博拉病毒的体内抗病毒功效。其发挥作用主要靶向于CoV RNA依赖的RNA聚合酶(RdRp),而鉴于CoV复制酶固有的遗传保守性,Remdesivir有极大的希望能够作为一类广谱的抗冠状病毒药物对抗过去、现在和将来的CoV。
2017年Baric等[3]在细胞层面验证了Remdesivir能够抑制多种冠状病毒(如SARS-CoV、MERS-CoV以及人畜共患的蝙蝠-CoV)的复制,并且能够在小鼠模型中减少SARS-CoV引起的肺部疾病,包括裸露的细支气管炎,炎性浸润的血管周围蓄积(即“套囊”)以及与弥漫性肺泡损害相关的肺泡内水肿,提示其具有一定的预防作用。类似的,Denison等[4]于2018年也证实了Remdesivir能够以最小的细胞毒型抑制小鼠肝炎病毒、SARS-CoV、MERS-CoV等多种冠状病毒,提示了其在临床应用的可行性及安全性。而今年最新的研究比较了Remdesivir与经典的LPV/RTV-IFNβ抗病毒联用药物,结果在体内、体外实验中均体现出了Remdesivir具有更好的抗病毒活性,并且其是唯一可显著降低肺部病理的治疗方法[25]。上述文章均体现了Remdesivir抗冠状病毒的作用,并且其可能成为此次2019-nCoV潜在的有效药物。
4 Remdesivir的药效学研究
4.1 动物实验在恒河猴模型上已证实,静脉注射Remdesivir有强大的抑制埃博拉病毒的作用。在感染埃博拉病毒的恒河猴模型中,每天一次静脉给予10 mg/kg或是3 mg/kg GS-5734连续12天,均可导致EBOV复制受到严重抑制。而10 mg/kg剂量的治疗组能够保护100%EBOV感染的动物免于致死性疾病,并且改善其临床疾病征象和病理生理指标。即使在病毒暴露三天后开始治疗,在六只经治疗的动物仅有两只检测到全身病毒RNA,提示为该小分子抗病毒化合物在非人灵长类动物中提供了第一个实质性的接触后保护[12]。在另一研究中,给非洲绿猴接种致死剂量的尼帕病毒,24小时后开始每日一次的静脉内Remdesivir治疗持续12天,与对照组动物均出现严重的呼吸道症状并死于感染相反,治疗组中仅有两只出现轻度的呼吸道症状[26]。
4.2 临床试验2018年11月20日至2019年8月9日,研究人员在刚果民主共和国进行了四种EVD疗法的临床试验,共招募到681例埃博拉病毒RNA阳性患者参与研究,随机接受三联单克隆抗体ZMapp (对照组)、抗病毒药物Remdesivir、单抗单克隆抗体MAb114或三联单克隆抗体REGN-EB3。研究的主要终点是28天死亡。Remdesivir组的患者在第1天接受负荷剂量(成人200 mg,儿科患者根据体重进行剂量调整),然后在第2天开始接受每日维持剂量(成人100 mg),持续9到13天[13]。
在研究过程中,研究人员针对四种疗法报告了29例严重不良事件,可能与实验性治疗有关,且并非所有事件都在治疗期间发生。Remdesivir的安全性概况与其先前发表的I期实验结果相符,提示其临床应用具有一定的安全性。但令人遗憾的是,Remdesivir治疗组中患者28天死亡率高达53.1%,显著高于另外3个治疗组;由于增高的死亡率,估计病毒清除的中位时间超过28天,治疗效果并不理想。
4.3 对婴幼儿埃博拉病毒感染病例的治疗作用埃博拉病毒感染后患者死亡率在在胎儿和新生儿中最高,几乎所有受EBOV感染的孕妇都以流产或死胎而告终。2017年,Antierens等报道了首个先天性获得性埃博拉病毒感染的幸存的新生儿[27]。在救治过程中,患儿出现发热及阵挛性肌肉活动,考虑到可能的中枢神经系统病毒感染,医生考虑加用能够穿过血脑屏障的小分子抗病毒药物Remdesivir,静脉输注10 mg/day药物并持续12天。整个治疗过程中及疗程结束后患儿耐受良好,无肝肾功能受损的表现,且没有任何与药物相关的毒性证据。虽然没有足够的脑脊液相关证据证明Remdesivir能够清除神经系统内复制的病毒,但在没有特异性治疗措施的前提下可以考虑使用广谱的小分子抗病毒药物在内的多种药物联合治疗。
5 Remdesivir的耐药性问题
冠状病毒具有独特的核糖核酸外切酶(Exoribonuclease,ExoN),并且由于其校对活性,使多种抗病毒核苷的药物(如5-氟尿嘧啶和利巴韦林)产生耐药性[28]。在β冠状病毒鼠肝炎病毒(Mouse Hepatitis Virus,MHV)模型中,Remdesivir在缺少校对的ExoN(-)突变株显示出药物易感性增加;而在野生型(WT)病毒中,Remdesivir仍会干扰nsp12聚合酶,并通过增加浓度来克服耐药性,从而显着抑制病毒复制和病毒RNA合成[4]。上述结果进一步支持了Remdesivir作为一类广谱的抗病毒药物,可抵御现有和未来新发的CoV疫情。
6 结语
Remdesivir(GS-5734)是一种潜在的广谱抗病毒药物,其能够在体内三磷酸化,作为底物加入到合成病毒RNA过程中,从而中断病毒基因组的复制。在前期针对埃博拉病毒治疗的II期临床试验中Remdesivir展现了良好的安全性。在针对多种冠状病毒的体外实验中,Remdesivir能够强效且安全地抑制病毒复制。而正在开展的Remdesivir的III期临床试验,为人类控制2019-nCov疫情提供了一个新的潜在有效选择。
