基于谱-效关系探究黄芩抑制白色念珠菌的质量标志物
2020-06-02商利娜王亚静鑫赵海宁周梦楠张怡高迪王雁雯叶相印
商利娜 王亚静 ∗赵 鑫赵海宁周梦楠张 怡高 迪王雁雯叶相印
(1.天津中医药大学中医药研究院,天津301617; 2.天津中医药大学,现代中药发现与制剂技术教育部工程研究中心,天津301617)
黄芩为唇形科植物黄芩Scutellaria baicalensisGeorgi 的干燥根,其性寒,味苦,归肺、胆、脾、大肠、小肠经[1],最早记载于《神农本草经》,具有清热祛湿、泻火解毒等功效;现代药理学表明,黄芩提取物具有抗肿瘤、抗病毒、抗微生物、抗炎、抗氧化等作用[2-3],对多种致病菌的抑制作用是其重要药效物质基础之一。黄芩苷是黄芩中含有量最高的成分,也是2015 年版《中国药典》 规定的质量控制成分。
目前,黄芩提取工艺及质量控制大多是根据《中国药典》 或文献,以黄芩苷或总黄酮为指标[4-6],但也有对黄芩谱-效关系进行研究的报道,发现其抑制金黄色葡萄球菌关联性最强的成分是白杨素-6-C-阿拉伯糖-8-C-葡萄糖苷,而不是黄芩苷[7]。因此,应制定适宜的方法进行相关分析,以提高黄芩质量控制的科学性。
另有研究表明,黄芩对白色念珠菌具有一定抑制作用。白色念珠菌是一种常见的条件性真菌病原体,当机体抵抗力低下或菌群失调时它会大量繁殖并形成芽生菌丝,侵犯皮肤、黏膜或内脏,引起鹅口疮、外科伤口感染、真菌血症等疾病[8-9],但目前黄芩抑制白色念珠菌的质量标志物仍不清晰,因此有必要对相关质量标志物进行考察。
中药质量标志物是在中药材和中成药中固有的或加工过程中形成的、与中药功能属性密切相关的化学物质,是反映中药质量和药效的存在[10];中药指纹图谱是反映中药所含所有化学成分种类和数量的一种形式,在一定程度上可揭示其化学特征,目前已成为中药质量评价的有效方法,但它仅能反映化学信息,并不能体现与药效学相关的具体成分[11],故若要科学评价中药质量,就应开展指纹图谱与药效的相关性研究,即谱-效关系。
灰色关联分析是一种用于中药质量评估的相关性分析方法,可定量描述事物或因素之间关联性的大小,也能反映各指标性成分对药效的贡献程度[12-13]。因此,本实验采用该方法对黄芩进行谱-效关系研究,根据各成分贡献程度来确定该药材抑制白色念珠菌的质量标志物。
1 材料
1.1 仪器 Agilent 1260 高效液相色谱仪,配置Agilent 20RBAX Eclipse Plus 色谱柱(250 mm×4.6 mm,5 μm);LS-B50 L 立式压力蒸汽灭菌锅(上海医用核子仪器厂);SW-CJ-JF 垂直层流超净工作台 (苏州净化厂);HPX-9052MBE 电热恒温培养箱(上海博讯实业有限公司医疗设备厂);Infinite 200 PRO 多功能酶标仪(瑞士Tecan 公司);FA124 电子天平(天津亿诺科学仪器有限公司);YP1001电子天平(上海箐海仪器有限公司);AX205 电子天平(十万分之一,瑞士Mettler-Toledo 公司);默克纯水机(天津信睿生物科技有限公司);N-1210B 旋转蒸发仪(上海爱朗仪器有限公司)。
1.2 试剂与药物 黄芩饮片 (批号190102,产地山西) 购自河北安国市誉林药业有限公司,经专家鉴定为正品。黄芩苷 (批号P20A9F59353)、黄芩素 (批号C20MBY31962)、汉黄芩 素 (批 号W30M10284622)、橙皮苷(P06D9F77001) 对照品均购于上海源叶生物科技有限公司;汉黄芩苷对照品(批号823B022) 购于北京索莱宝科技有限公司。乙腈、磷酸为色谱纯;水为超纯水。
1.3 菌种与培养基 白色念珠菌 [编号BNCC337321(=ATCC1231)] 购自北纳创联生物技术有限公司。改良马丁琼脂培养基购自北京索莱宝生物科技有限公司;改良马丁培养基购自山东拓普生物工程有限公司。
2 方法与结果
2.1 溶液制备
2.1.1 供试品溶液 精密称取4 份药材粗粉,每份10 g,加入水或60%乙醇200 mL,以回流水提取、回流60%乙醇提取、温浸水提取、温浸60% 乙醇提取4 种方式各提取2 h,提取液放凉后,对应溶剂补足减失的质量,离心弃去药渣,0.45 μm 微孔滤膜过滤,即得,4 ℃下备用。
2.1.2 内标溶液 精密称取橙皮苷对照品1.47 mg,甲醇定容至25 mL,即得(质量浓度为58.8 μg/mL),4 ℃下备用。
2.1.3 对照品溶液 精密称取黄芩苷、汉黄芩苷、黄芩素、汉黄芩素对照品适量,甲醇溶解,制成质量浓度分别为0.516、1.000、0.506、0.515 g/L 的贮备液,各吸取1 mL 置于10 mL 量瓶中,甲醇定容至刻度,超声混匀,0.45 μm 微孔滤膜过滤,取续滤液,即得。
2.1.4 抑菌用供试品溶液 取“2.1.1” 项下药液适量,旋蒸至生药量1 g/mL,即得。
2.1.5 试验用菌液 将白色念珠菌冻干粉进行复苏、活化、传代至第3 代,取10 μL 加到10 mL 改良马丁液体培养基中,于30 ℃恒温培养箱中静置培养24 h,即得(菌浓度为1×107CFU/mL)。
2.2 HPLC 指纹图谱建立
2.2.1 色谱条件 Agilent ZORBAX Eclipse Plus 色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈(A) -0.1% 磷酸(B),梯度洗脱(0~25 min,85%~75% B;25~40 min,75%~70% B;40~45 min,70%~60% B;45~60 min,60%~57% B;60~65 min,57%~30% B;65~70 min,30%~85%B;70~75 min,85% B);体积流量1 mL/min;检测波长202 nm;柱温30 ℃;进样量10 μL。
2.2.2 图谱分析 对照品溶液用0.45 μm 微孔滤膜过滤后,在“2.2.1” 项色谱条件下进样测定,结果见图1A;取“2.1.1” 项下供试品溶液1 mL 于5 mL 量瓶中,对应溶剂定容至5 mL,取1 mL,与1 mL “2.1.2” 项下内标溶液混合,0.45 μm 微孔滤膜过滤,在“2.2.1” 项色谱条件下进样测定,结果见图1B。
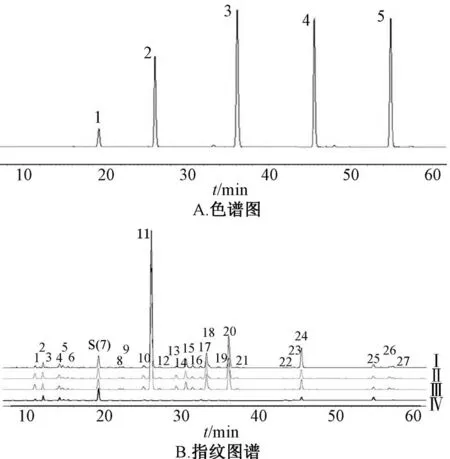
图1 对照品HPLC 色谱图及供试品HPLC 指纹图谱
2.3 体外抑菌实验 根据美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI) 操作规范,采用微量肉汤稀释法[3,14]进行测定,设置实验组、阴性对照组、阳性对照组、空白对照组。取无菌96 孔板,在A1~A11 孔中分别加入1 000、500、250、125、62.5、31.25、15.63、7.81、3.91、1.95、0.98 g/L 药材提取液100 μL,再分别加入100 μL 稀释至1×104倍的白色念珠菌菌液,使每孔终质量浓度分别为500、250、125、62.5、31.25、15.63、7.81、3.91、1.95、0.98、0.49 g/L,作为实验组;B1~B11孔中依次加入质量浓度为1 000、500、250、125、62.5、31.25、15.63、7.81、3.91、1.95、0.98 g/L 药材提取液100 μL,再分别加入100 μL 改良马丁液体培养基,作为阴性对照组;A12 孔中加入灭菌水、稀释至1×104倍的菌液各100 μL,作为阳性对照组;B12 孔中加入灭菌水、改良马丁液体培养基各100 μL,作为空白对照,每组平行3 次,将96 孔板置于酶标仪中测定600 nm 波长下的吸光度(A),计算抑菌率,公式为抑菌率=[1-(A实验组-A阴性对照组) /(A阳性对照组-A空白对照组)] ×100%。
2.4 药材指纹图谱数据及抑菌效果 药材指纹图谱数据以各标志峰峰面积与内标物峰面积的比值表达,抑菌效果以供试品溶液质量浓度为7.81 g/L 时的抑菌率来表达(7.81 g/L为药材抑制白色念珠菌的最低抑菌浓度,此时4 种提取方式下的抑菌率具有显著差异),结果见表1。
2.5 灰色关联分析 参考文献[7,15-16] 报道的方法。
2.5.1 参考序列、比较序列确定 本实验考察不同提取工艺下药材提取液中各成分(即各组分峰面积) 对白色念珠菌抑菌率的影响程度,以抑菌率为参考序列(母序列),记作X0(k),k=1、2、3、4;以27 种成分峰比值为比较序列(子序列),记作Xi(k),i=1、2、3、…、27,k=1、2、3、4。
2.5.2 无量纲化处理 为了确保实验结果准确性,便于各指标比较,在计算灰色关联度之前需要对数据进行无量纲化处理。本实验研究采用均值化法,即用各序列元素分别除以相应序列平均值,计算公式为i=0、1、2、3、…、27,k=1、2、3、4。其中为序列i的样本数据平均值,Xi(k) 为原数据,Xi′ (k) 为无纲量化处理后的数据,从而得到均值化的序列{Xi′ (k) }。

表1 药材指纹图谱数据及抑菌效果
2.5.3 求差数列建立 计算参比序列与比较序列的绝对差值ΔXi(k),计算公式为
2.5.4 关联系数确定 灰色关联系数ζi(k) 表示参考序列X0和比较序列Xi在k(k=1、2、3、4) 时的关联程度,计算公式为ξi(k)=(i=0、1、2、3、…、27,k=1、2、3、4),式中|X0(k) -Xi(k) | 为序列X0与序列Xi在k点差值的绝对值;为差值绝对值的二级最小值,即在各序列差值最小值的基础上,进一步得出所有序列的差值最小值;为差值绝对值的二级最大值,即在各序列差值最大值的基础上,进一步得出所有序列的差值最大值;ρ为分辨系数,取值区间为(0,1),本实验取ρ=0.5。
2.5.5 灰色关联度计算 灰色关联度γ0i计算公式为,式中n为任一序列i下的样本数,本实验取n=4。
2.5.6 关联极性分析 序列Xi′ (k) 与X0′ (k) 之间的关联极性 σi计算公式为(i=1、2、3、…、27,k=1、2、3、4,n=4)。若sgn (σi) =sgn (σ0),则Yi与Y0正关联,即前者对后者起到增强作用;若sgn (σi) =-sgn (σ0),则Yi与Y0负关联,即前者对后者起到削弱作用,sgn (X)为符号函数,即
2.6 分析结果 按“2.5” 项下方法对谱-效关系进行分析,结果见表2,可知除了成分1、3、8、10、12、14、21、22、26 对抑菌起到削弱作用外,其他成分都起到促进作用,各成分对抑菌率的影响程度见图2~3。在促进抑菌活性的成分中,关联度最强的是峰24 (黄芩素),其关联度为0.768 9;对削弱抑菌活性的成分中,关联度最强的是峰22,其关联度为0.624 7,即峰24 (黄芩素)、峰22 分
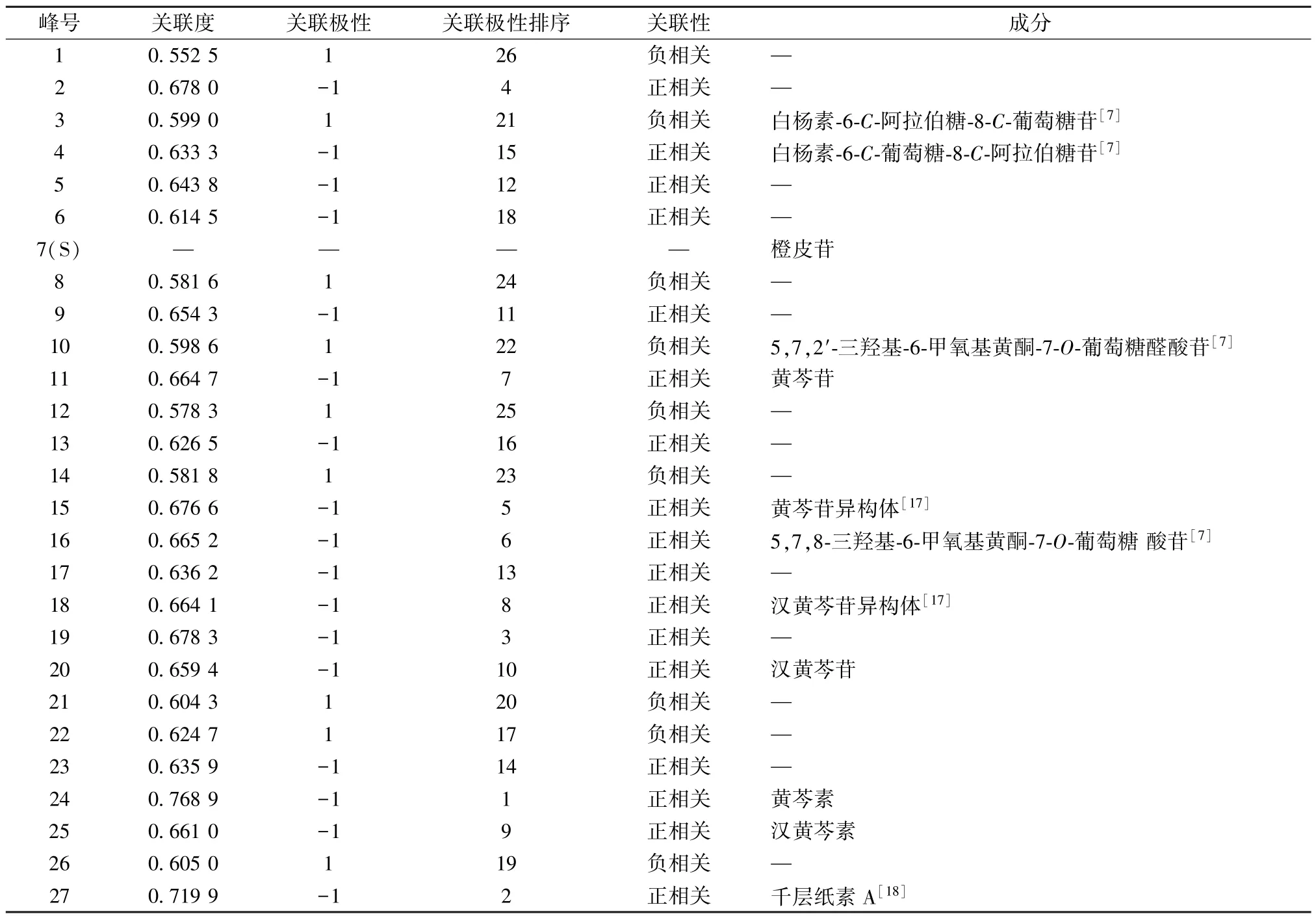
表2 抑菌质量标志峰与抑菌率之间的关联度
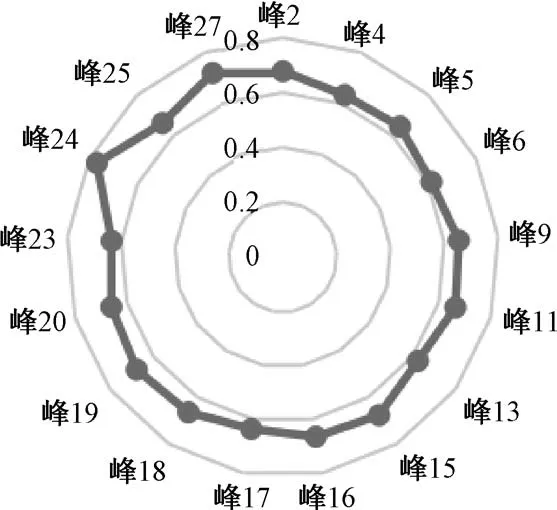
图2 对抑制白色念珠菌起促进作用的成分及其贡献程度

图3 对抑制白色念珠菌起削弱作用的成分及其贡献程度
3 讨论
白色念珠菌是一种条件致病性真菌,是真菌感染的最常见原因之一,并且具有显著的死亡率。黄芩具有显著抑制白色念珠菌的活性,而且它属于天然中药产物,不易产生耐药性,故本实验旨在考察该药材相关质量标志物。
中药质量标志物(Q-marker) 是中药质量控制的一个新概念,其核心内容包括有效、特有、传递与溯源、可测、处方配伍[17],其中有效最为重要。目前,已有文献表明黄芩苷、黄芩素等单体成分对白色念珠菌具有抑制作用[19-20],本实验印证了这一点,但更着重对黄芩提取物中各成分对抑菌效果的强弱进行研究,并将贡献程度最大的黄芩素作为质量标志物。中药是否有效与其化学成分、提取工艺等因素密不可分,故本实验设置4 种提取方式使其化学成分及药效(抑菌率) 具有显著差异,以便通过谱-效关系确定该药材抑制白色念珠菌的质量标志物。
中药化学成分十分复杂,并非所有成分在疾病治疗中都起着同样重要的作用,故需应用一种合适的方法对谱-效关系进行研究,以便得到在药效学中发挥作用的贡献者。中药谱-效关系的研究方法很多,如灰色关联分析、相关分析、聚类分析、偏最小二乘法分析等,其中灰色关联分析具有样本量小、计算量小、结果与定量结果一致等优点[12]。因此,本实验采用灰色关联分析法对黄芩的“谱-效” 关系进行研究,发现其中抑制白色念珠菌关联性最强的成分是黄芩素,而不是含有量最高的黄芩苷。因此,针对中药中每种特定成分的药效,均需要制定合适的方法对其谱-效关系进行分析,以便确定其质量标志物。
本实验首次采用谱-效结合模式,从抑菌差异性特点的角度出发,对黄芩进行质量综合评价体系研究,并通过灰色关联分析对不同提取工艺所得黄芩HPLC 指纹图谱与药液对白色念珠菌的抑制作用进行关联,明确了该药材抑菌物质基础的关联程度。结果,初步确定了黄芩抑制白色念珠菌的主要质量标志物是黄芩素,其药效发挥是多种成分共同作用的结果,可为该药材提取工艺优化、质量控制建立等方面的研究提供可行性参考。但本实验结果与目前黄芩质量控制指标(黄芩苷) 不完全符合,具体原因仍需进一步探讨。
