影响重度新生儿缺氧缺血性脑病预后的LOGISTIC因素分析
2020-05-29翁海美林明静周丽霞
翁海美,林明静,周丽霞
(海南省人民医院新生儿科,海南 海口 570311)
新生儿缺氧缺血性脑病(hypoxic-ischemic encephalopathy,HIE)是指在围产期出现新生儿窒息造成的脑缺氧缺血性损害,发病率在活产足月儿中占比1%~2%。其不仅是新生儿窒息的严重并发症,而且可导致神经发育障碍,重则出现脑瘫或死亡,已引起临床医师及家属的高度关注[1]。由于重度新生儿HIE病情相对严重,病死率高,且存活儿致残率(脑瘫、遗留神经发育障碍等)较高,据文献报道可高达55%~73%,预后相对差[2]。虽然目前临床通过早期评估与治疗干预能够一定程度促进该类患儿预后改善,但有关研究[3]指出:影响重度新生儿HIE的预后因素较多,临床治疗干预仍缺乏针对性。当前已有研究报道新生儿HIE预后的危险因素,但针对重度新生儿HIE预后的影响因素研究尚少。基于此,本研究主要分析影响重度新生儿HIE预后的临床相关因素,以期为制定针对性治疗干预措施、改善患儿预后提供依据。现将结果报告如下。
1 资料与方法
1.1 一般资料:选取2016年1月至2019年4月本院诊治的重度HIE患儿134例为研究对象。纳入标准:①HIE符合中华医学会儿科学分会新生儿学组制定的新生儿HIE诊断标准,经颅脑CT检查确诊,临床分度为重度:昏迷、肌张力松软或间歇性伸肌张力增高、反射消失、生后12h内出现惊厥且可呈持续状态、瞳孔不对称或扩大并对光反射迟钝;②母孕期体健;③无家族遗传病史;④临床资料完整。排除标准:①早产儿(胎龄<37周);②先天性心肺疾病;③代谢性疾病;④随访6个月内失访病例。
1.2 治疗方法:严格按照“三支持、二对症”原则进行治疗:维持血糖、血气、血压稳定,控制惊厥、降颅压。根据患儿具体情况及症状给予亚低温治疗或高压氧治疗。新生儿期后定期随访,必要时给予早期干预与康复治疗:听觉、视觉、爬行等刺激,语言听力、智力等训练,药物干预为胞二磷胆碱、脑活素等。
1.3 研究方法:回顾性收集患儿临床资料:性别、胎龄、出生体重、分娩方式、Apgar评分、脏器损伤情况、开始治疗日龄、血清tau蛋白水平等。患儿均随访6个月,无失访病例,统计预后情况。预后判断标准:①生命体征平稳;②神经系统症状及体征均消失;③肌张力正常;④原始反射正常;⑤可正常进食母乳;⑥瞳孔对光反射正常。上述6项均符合的存活患儿视为预后良好,不符合、运动神经发育异常、死亡患儿视为预后不良。根据预后情况将134例患儿分为预后良好组、预后不良组,进一步结合临床资料分析影响重度HIE患儿预后的相关因素。
2 结 果
2.1 重度HIE患儿一般资料及预后情况:本研究134例重度HIE患儿中,男73例,女61例;胎龄37~41周,平均(39.25±5.84)周;出生体重2.54~4.21kg,平均(3.46±0.45)kg;分娩方式:剖宫产45例,阴道分娩89例。随访结果统计显示,预后良好103例(76.87%),预后不良31例(23.13%)。预后不良组中包括4例死亡,占比2.99%。
2.2 影响重度HIE患儿预后的单因素分析:单因素分析显示,重度HIE预后良好组与预后不良组患儿的性别、胎龄、出生体重、分娩方式、1min Apgar评分比较差异无统计学意义(P>0.05);而5min Apgar评分、脏器损伤、开始治疗日龄、血清tau蛋白水平比较中,预后不良组5min Apgar评分低于预后良好组,脏器损伤≥2个者占比高于预后良好组,开始治疗日龄<48h占比低于预后良好组,血清tau蛋白≥8ng/L者占比高于预后良好组,差异均有统计学意义(P<0.05)。见表1。
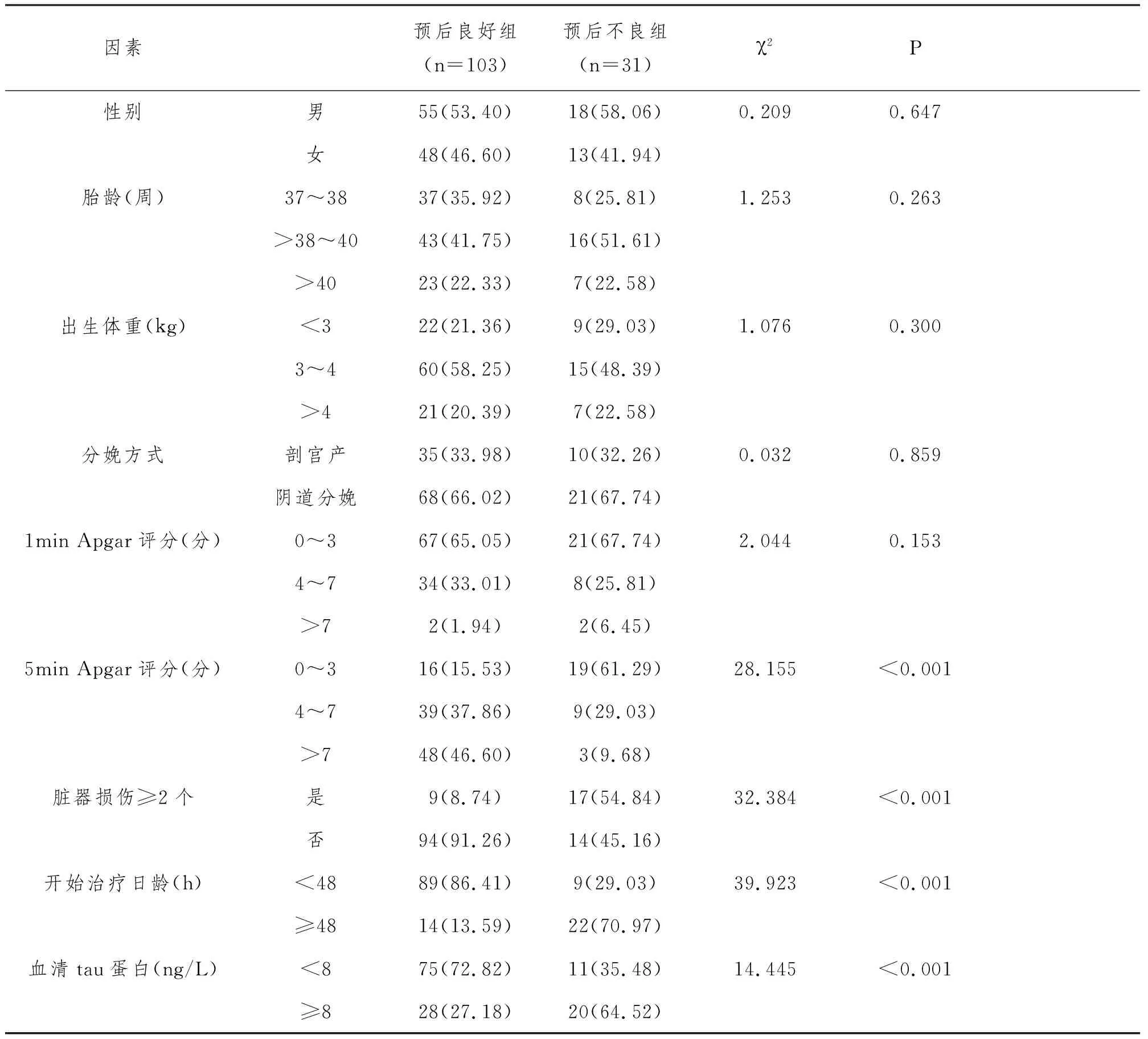
表1 影响重度HIE患儿预后的单因素分析n(%)

表2 各因素行Logistic回归分析的分类变量编码
2.3 影响重度HIE患儿预后的多因素Logistic回归分析:以重度HIE患儿“预后”为因变量(赋值:0=预后良好,1=预后不良),以“5min Apgar评分、脏器损伤≥2个、开始治疗日龄、血清tau蛋白水平”为自变量,纳入多因素Logistic回归分析。结果显示,5 min Apgar评分≤3分(OR=58.658,95% CI=6.984~492.682)、脏器损伤≥2个(OR=31.145,95% CI=3.522~275.415)、开始治疗日龄≥48h(OR=33.747,95% CI=5.992~190.066)、血清tau蛋白≥8ng/L(OR=5.846,95% CI=1.372~24.918)是影响重度HIE患儿预后的危险因素(P<0.05)。见表2、3。
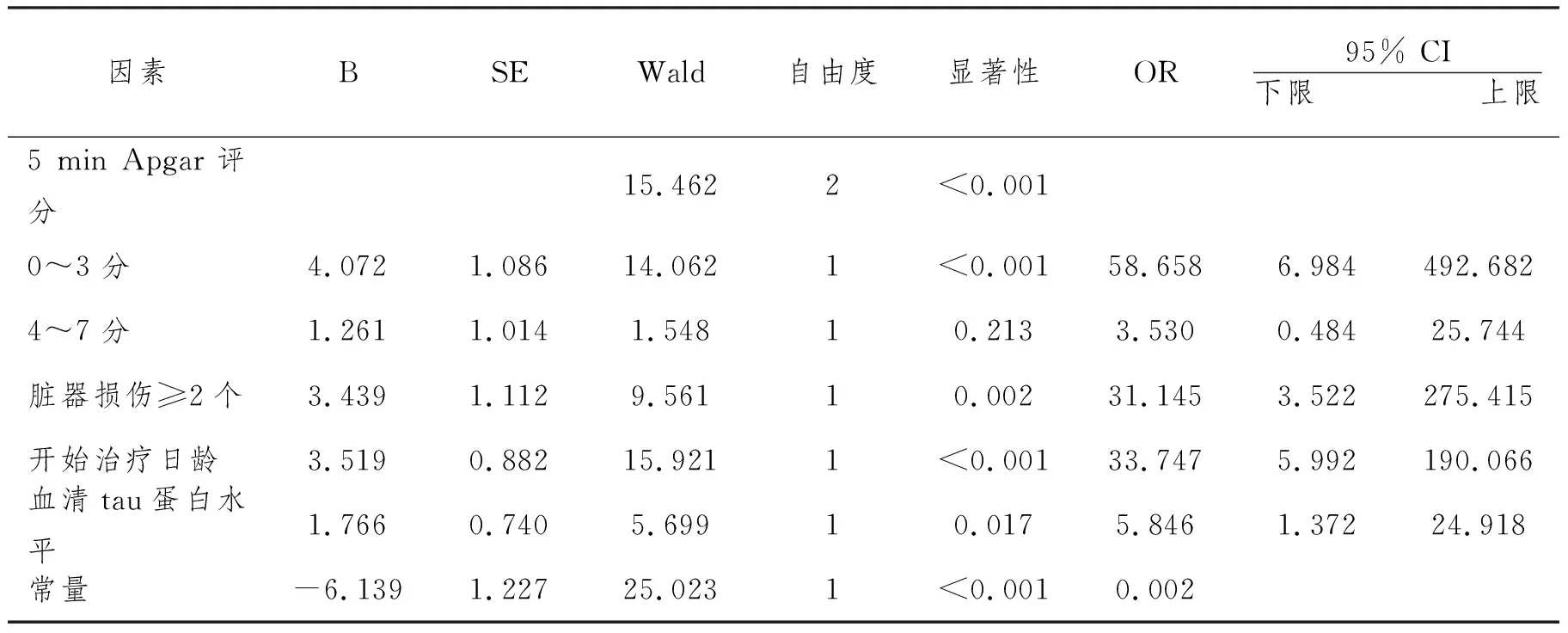
表3 影响重度HIE患儿预后的多因素Logistic回归分析结果
3 讨 论
新生儿HIE临床表现为肢体张力改变、反射异常等,是新生儿期危害较大的疾病,尤其重度HIE多导致患儿运动神经发育异常、死亡,存活儿可留有视听障碍、脑瘫、癫痫、共济失调等严重后遗症,加重社会和家庭负担,影响我国整体人口素质的提升。HIE发病机制复杂,影响因素众多。据Abdelaziz等[4]研究报道,宫内窘迫、产程异常、羊水污染等均是新生儿HIE发病的危险因素。且资料显示,重度HIE的核心发病机制与宫内窘迫、新生儿缺氧等有关,而多种分子信号通路参与该机制的调节,进而影响患儿预后[5]。本研究随访6个月结果统计显示,预后良好103例(76.87%),预后不良31例(23.13%),预后不良组中包括4例死亡,占比2.99%。提示重度HIE有较多患儿出现近期不良预后。因此,探寻影响重度HIE患儿预后的具体影响因素,为重度HIE患儿的早期针对性治疗和及时干预提供依据,对临床工作及该类患儿预后改善具有重要意义。
本研究单因素分析显示,5min Apgar评分、脏器损伤、开始治疗日龄、血tau蛋白水平与重度HIE患儿不良预后有关;而与性别、胎龄、出生体重、分娩方式、1 min Apgar评分无关。进一步多因素Logistic回归分析结果显示,5 min Apgar评分≤3分(OR=58.658,95% CI=6.984~492.682)、脏器损伤≥2个(OR=31.145,95% CI=3.522~275.415)、开始治疗日龄≥48h(OR=33.747,95% CI=5.992~190.066)、血tau蛋白≥8ng/L(OR=5.846,95% CI=1.372~24.918)是影响重度HIE患儿预后的危险因素。①Apgar评分:Apgar评分主要通过评估皮肤颜色、心搏速率、呼吸、肌张力及运动、反射情况判断新生儿窒息状况,普遍应用于临床。相关研究表明,5min Apgar评分≤3分预示患儿重度窒息且存在并发神经系统后遗症、病死的风险。Apgar评分持续较低,提示窒息程度无明显减轻,可引起低氧血症、酸中毒,使得血液重新分布,重度患儿剩余碱、血糖等明显异常,脑能量代谢衰竭,进而造成脑水肿、细胞损伤,重则死亡。该阶段应及时进行复苏治疗,改善预后。②脏器损伤:相关资料显示,重度HIE并发脏器功能损伤的几率更高,脑、肺、心损伤发生率均可高于60%。另有研究表明,伴多脏器损伤的HIE患儿预后不良风险性更高[6]。而重度HIE病情、窒息程度相对重,可导致肝、肾、心、脑等不同程度损害,同时伴电解质紊乱,易加重患儿机体负担,造成不良预后。③开始治疗日龄:Alsina等[7]研究报道,早期进行亚低温等治疗,可显著降低重度HIE患儿病死率、致残率,改善预后效果。新生儿大脑可塑性、代偿功能较强,信号传导快,若发病早期给予良性刺激能够正向引导神经系统发育,促进脑功能代偿适应,降低后遗症发生率。且资料显示,神经系统症状在婴儿出生后12h内可出现,重度HIE患儿呈进行性加重,48h内进行干预是关键,反之可能对预后不利[8]。这为本研究提供了依据。④血清tau蛋白:tau蛋白是微管相关蛋白,广泛表达于神经系统。重度HIE时可出现神经元损伤,使得tau蛋白自神经轴突大量释放,引起血清tau蛋白水平异常增高。动物模型实验表明,缺氧缺血性脑损伤大鼠皮质、脑室周围白质神经细胞凋亡和血清tau蛋白水平呈同向增加,tau蛋白可反映脑损伤、神经系统损害程度[9]。另有资料显示,血清tau蛋白水平高的HIE患儿不良预后率高,神经系统后遗症发生率大;而重度HIE患儿血清tau蛋白表达显著高于轻度、中度HIE患儿[10]。因此,密切监测tau蛋白水平有助于提示重度HIE患儿预后,而关于如何调节tau蛋白水平以减轻其对重度HIE患儿预后的不利影响还有待进一步实验明确。
综上所述,5min Apgar评分≤3分、脏器损伤≥2个、开始治疗日龄≥48h、血清tau蛋白≥8ng/L的重度HIE患儿发生预后不良的危险性更高,临床应加强针对性监护与及时干预。鉴于本研究样本量不大,为单中心研究,可能影响结果普遍性,故今后有待进一步结合长期随访情况实施大样本、多中心的研究检验。