豆渣一锅法均相制备羧甲基纤维素的研究
2020-05-25廉梦云李兴江吴学凤姜绍通李传运
廉梦云 郑 志 李兴江 吴学凤 姜绍通 李传运
(合肥工业大学食品与生物工程学院;安徽省农产品精深加工重点实验室,合肥 230601)
豆渣是豆制品生产中产生的副产物,我国豆渣年产量大约在300万t[1]。豆渣中含有40%~45%的纤维素及少量半纤维素和木质素[2,3],结构复杂,溶解性差,多作为饲料或肥料,甚至被丢弃,造成资源的浪费和环境污染。
羧甲基纤维素是一种阴离子型纤维素衍生物,具有良好的水溶性、增稠性、乳化性等,广泛应用在医药、食品、化妆品等行业[4]。传统的羧甲基纤维素多采用微晶纤维素在有机试剂中异相合成[5,6],原料需要经过提纯精制,成本高、制备工艺复杂,同时异相合成还存在取代基分布不均匀,取代度>0.4时才能溶于水,需多次加入碱液,有机试剂的利用率低、回收困难等问题。NaOH/尿素水体系是一类新型纤维素绿色水溶液,它能在低温5~30 min将纤维素完全溶解,是一种经济、环保的试剂[7,8]。该体系用于合成纤维素衍生物时具备反应试剂和催化剂的功能,制备的产品包括羟丙基纤维素[9]、苄基纤维素[10]、O-(2-羟乙基)纤维素[11]。
目前豆渣制备CMC的研究主要从纤维素提纯出发,异相体系中碱化、醚化分步反应。本研究利用NaOH/尿素水反应体系直接溶解、碱化豆渣中的纤维素得到碱纤维素后醚化处理,一锅法均相制备CMC,实现分步反应一次在相同反应容器和相同反应条件下完成[12,13],简化工艺流程,减少不必要的分离、纯化步骤,避免在反应过程中多次加碱和醚化剂的问题,且反应条件温和,取代基分布均匀,在取代度>0.2时即能溶于水。
本研究直接以豆渣为原料,NaOH/尿素为反应体系,采用一锅法均相合成CMC,并通过红外光谱、核磁共振分析、热重分析和扫描电镜对样品结构、性质进行表征。研究结果对实现豆渣的综合应用、降低CMC的生产成本、拓展制备CMC的来源有重要意义。
1 材料和方法
1.1 材料与试剂
豆渣(具体成分见表1)、氯乙酸钠、氢氧化钠、尿素、盐酸、乙醇酸、硝酸、硫酸等均为国产分析纯。
1.2 主要仪器
FD-1B-50冷冻干燥机;G1-20G-Ⅱ离心机;Nicolet 67傅里叶红外光谱仪;VNMRS600超导核磁共振波谱仪;STA449F3同步热分析仪;JSM-6490LV电子显微镜。

表1 豆渣组成成分
1.3 实验方法
1.3.1 一锅法均相制备羧甲基纤维素
将6.8 g豆渣缓慢加入到200 g的6%NaOH/4%尿素水溶液中,搅拌反应20 min后放于-20 ℃冰箱中静置过夜约15 h,取出后4 ℃、7 000 r/min离心机中离心15 min,得到含有碱纤维素的上清液,倒入烧杯中放于35 ℃水浴锅中搅拌,缓慢加入冰水浴中配制的氯乙酸钠/NaOH共混物(与豆渣纤维素摩尔比4:1的氯乙酸钠溶于5 mL 1.5%的NaOH溶液),55 ℃水浴锅中搅拌3 h,68 ℃保温1 h,将所得醚化产物用3倍体积的95%乙醇沉淀后用少量50%乙酸中和,抽滤,用75%乙醇洗涤2~3次,无水乙醇洗涤固体2次,移入烘箱 60 ℃干燥,得到豆渣CMC。
经过前期单因素实验,确定以豆渣添加量、氯乙酸钠与豆渣的摩尔比、NaOH浓度和反应时间为影响因素,以取代度为评价指标,设计正交实验(表2)。

表2 正交实验因素水平表
1.3.2 羧甲基纤维素取代度的测定
采用GB 1886.232—2016中灰分法测定羧甲基纤维素的取代度[14]。
1.3.3 溶解度测定
精确称取1 g制备的CMC在25 ℃溶解于100 mL蒸馏水中配成1%的溶液,搅拌24 h。经过反复抽滤、洗涤后105 ℃烘箱中烘干至恒重,计算溶解度。
1.3.4 红外光谱分析
利用溴化钾压片法分析豆渣、制备CMC的红外光谱特性。取1 mg样品与200 mg KBr在干燥环境下研磨均匀,压成透明薄片在傅里叶红外光谱仪测试,选择波长范围400~4 000 cm-1,扫描32次,记录样品的结构变化。
1.3.5 核磁共振分析
取0.2 g制备CMC在60 ℃下溶解在2 mL D2O中,取出冷却至室温冷冻干燥,重复操作3次。取8 mg处理后的样品加入到0.6 mL D2O/D2O(体积比=4∶1)的溶液中,在90 ℃下放置2 h,间歇震荡,避免凝胶化,最终形成浅黄色的均相溶液。采用超导核磁共振波谱仪在500.13 MHz下扫描2 h得到CMC的1H核磁光谱。
1.3.6 热重分析
取豆渣和制备CMC 5~10 mg在同步热分析仪上进行热重分析,温度范围为25~600 ℃,升温速率为10 ℃/min,氮气流速为30 mL/min。通过相应热重曲线的变化,我们可以得到样品热稳定性的变化
1.3.7 扫描电镜分析
将切成薄片的豆渣和制备CMC冷冻干燥后进行喷金处理,喷金时间为120 s,在20 kV 的电压和不同放大倍率下进行钨灯丝扫描电子显微镜观察,并记录样品的微观结构。
1.3.8 数据分析处理
利用Origin 8.5对实验所得数据进行分析处理。实验结果3次平行测量取其平均值。
2 结果与讨论
2.1 正交实验结果分析
在正交实验表中,可以用极差R的大小代表影响因子对结果的影响程度,R值越大,影响程度越高。本研究中对取代度影响最大的是豆渣添加量,其次是氯乙酸钠和纤维素的摩尔比、醚化时间,NaOH的浓度影响最小。根据以上分析,制备高取代度CMC的优化反应条件为:55 ℃下醚化3 h,68 ℃保温1 h,豆渣添加量6.8 g,摩尔比为4∶1,NaOH的浓度为1.5%,制备的CMC的取代度为0.51、溶解度为83.88%的淡黄色粉末,得率约为30.21%。经测定改性样品中含有0.12%左右的N元素,以及极少量的S元素,可能与蛋白质未完全除去有关,表明尿素未参与取代反应[15]。
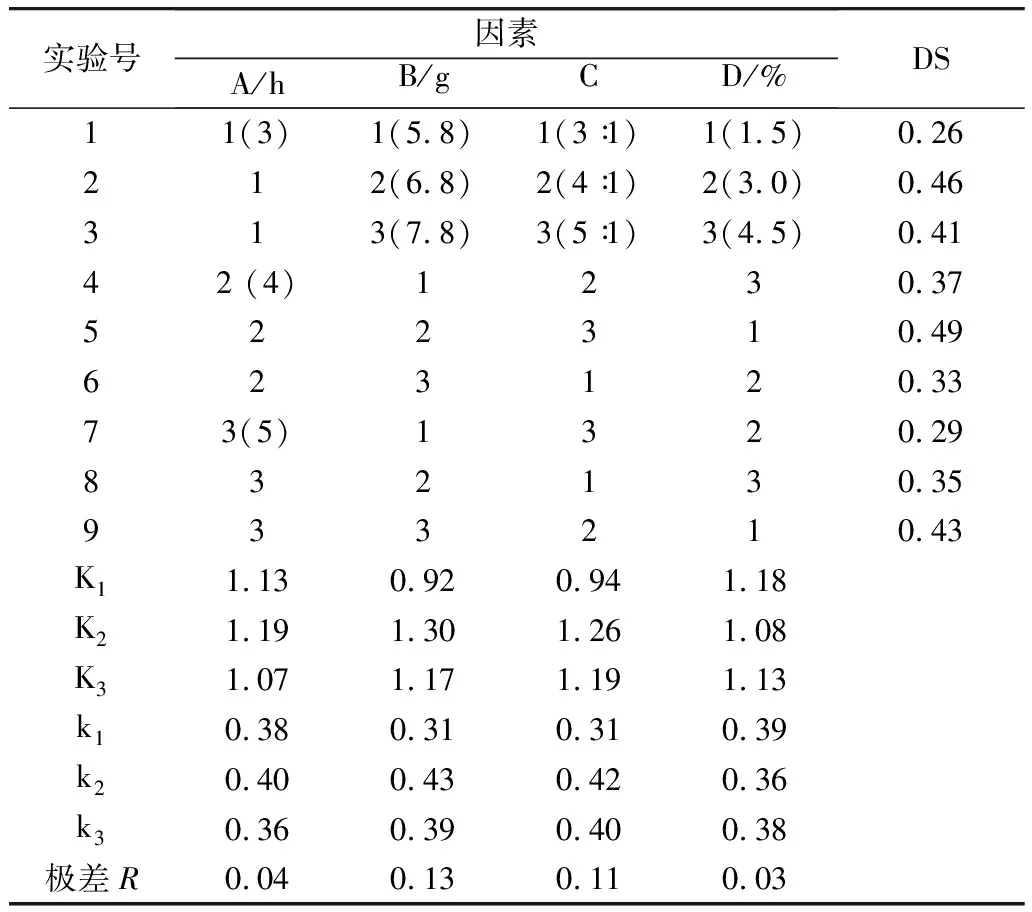
表3 利用豆渣制备CMC工艺优化正交实验结果
注:A代表醚化时间,B代表豆渣添加量,C代表氯乙酸钠和纤维素的摩尔比,D代表NaOH的浓度。
2.2 红外光谱分析
与豆渣相比,经过羧甲基化处理的样品在1 608.12 cm-1出现非常明显的羧羰基非对称伸缩振动吸收峰(图1),证明豆渣分子上的部分羟基被羧甲基成功取代[16,17]。
图1中样品在3 423 cm-1处显示出强烈的宽吸收带,这归因于—OH基团的伸缩振动[18],表明样品的含水量较高。1 700 cm-1附近的特征峰属于CMC产物的取代基团中的C—O或副产物羟乙酸钠的C—O基团[19],产物(b、c)的光谱中此特征峰不明显,说明产物中基本不存在副产物。1 729.82 cm-1处的吸收峰对应于半纤维素的羧基伸缩振动,木质素的特征峰波长是1 270.41 cm-1[20],豆渣(a)明显观察到这两个吸收峰,经过改性后样品(b)的吸收峰基本消失,说明经过改性处理后半纤维素和木质素大部分被除去。在1 374.52 cm-1和1 162.91 cm-1处观察到纤维素II的振动吸收峰。在1 031.12 cm-1处检测到的峰是指CMC中的醚(C—O—C)和葡萄糖单元中的醇的C—O键。随着羧甲基取代更多的羟基时,1 031.12 cm-1处的吸收峰增强,可能与未反应的纤维素和羧甲基纤维素水解产生的葡萄糖残基有关。700~500 cm-1区域是参与形成氢键的O—H基团的振动,可视为纤维素结晶区的吸收峰。可以推测CMC中羟基的取代越多,无定形区增大,结晶度降低。然而,在图中没有观察到该区域的变化,可能是因为该区域对其他振动比较敏感[21]。

注:a SD;b 制备CMC(DS=0.51)。图1 豆渣与制备CMC红外光谱图
2.3 核磁共振分析
制备CMC经过多次置换反应和酸解后,利用核磁共振波谱仪扫描得到1H NMR光谱图(图2)。1H NMR光谱图主要通过化学位移的改变判断纤维素上具有反应活性的三个反应位点是否有羧甲基取代。通过查阅资料发现,2.50~3.00 ppm之间的光谱区域是羧甲基基团吸收峰,充分说明了成功引入了羧甲基。由于糖苷键的断裂,可以观察到H2质子处出现α和β异头物,α-异头物(在较高的场)和β-异头物(在较低的场)特定的化学位移在2.92和2.96之间。被羧甲基基团取代H3、H6位置羟基后产生的化学位移分别是2.99、2.35。未经醚化的脱水葡萄糖单元H4和H5的质子在2.83~2.87的范围内有一个重叠信号峰[22-24]。在CMC的1H NMR光谱中已经证实,6号位的伯羟基的空间位阻小更容易被取代,并且仲羟基显示出较低的反应性。然而,在均相体系中,仲羟基的取代相对增加,可能与反应体系有关。Ramos等[25]使用新溶剂DMSO / TBAF制备CMC得到O6>O2≥O3。

图2 CMC在D2SO4/D2O中酸解的1H NMR 光谱图
2.4 热重分析
图3是豆渣和制备CMC的热失重曲线图。样品在100 ℃左右出现的重量损失,主要是纤维素上物理吸附的水分子损失造成的,CMC的水分吸附能力要高于SD,主要是因为CMC分子链上的羧甲基是强亲水性基团,使CMC的亲水性增强。SD的失重区域在210~400 ℃,通过作图可以看出SD的最大降解温度在341 ℃,改性后CMC的失重区域在190~370 ℃之间,分解温度大约是264 ℃。对比SD与CMC的热重曲线可以发现:CMC的热分解温度要低于SD,主要是因为经过碱化、醚化处理后,豆渣分子的整体结构被破坏,羧甲基取代纤维素分子上的羟基,使分子间氢键减少,分子结构更容易被破坏,从而使得CMC的热稳定性降低。总体上看,制备的CMC热分解温度较高,表现出良好的耐热性。当温度继续升高,CMC样品的残余物的重量质量分数约为25%,略高于SD,这是由于羧甲基反应过程中Na+的引入,在高温处理后生成了盐,从而使残余物含量较高。

图3 豆渣与制备CMC的TG图
2.5 SEM分析
SEM反映了所观察物体的形貌结构。图4a和图4b显示未改性的豆渣表面比较光滑,有断裂层出现,木质素和半纤维素的存在使纤维素束的表现不明显,整体以大颗粒状存在。图4c、图4d是经过羧甲基化处理后样品的形貌,可以明显观察到改性后的样品结构发生了改变。样品经过碱化处理使大部分木质素和半纤维素除去,以及醚化处理后羧甲基的取代使表面结构发生变化,断裂层消失,空隙率增多,凹凸性明显,呈现蜂窝状结构,分子以短棒状存在。这与FT-IR的结果相似,不同物质的羧甲基化改性也有类似的形貌变化[26]。

注:图a和图b是SD;图c和图d是制备CMC(DS=0.51)。图4 豆渣、制备CMC的SEM图
3 结论
豆渣溶解在6%NaOH/4%尿素水溶液中得到富含纤维素的上清液,以氯乙酸钠为醚化剂,经正交优化后制备了溶解性较高、耐热性良好、取代度达到0.51的羧甲基纤维素。红外光谱和核磁共振图谱验证确有羧甲基取代纤维素上的羟基,分子结构发生改变,实现了以豆渣为原料在NaOH/尿素水溶液中一锅法制备CMC,为CMC的合成提供了一条新的路径。
