HPLC法同时测定地西泮直肠凝胶中地西泮、苯甲酸、苯甲醇含量
2020-05-23徐佳雯张彦卓胡雅君
徐佳雯,李 尚,张彦卓,胡雅君,张 斐*
1 徐州医科大学 新药研究与临床药学重点实验室,徐州221000 2 江苏恩华药业股份有限公司,徐州 221000
小儿癫痫持续状态(status epilepticus,SE)属于常见急性病的一种,临床上常使用地西泮、咪达唑仑、丙戊酸钠静脉注射方式治疗[1],起效快,但作用持续时间短,且需要医务人员操作。而直肠用凝胶可用于急性发作时的病情控制,操作方便起效快,适合家庭使用。
地西泮直肠凝胶由瓦利安特(Valeant)制药国际公司研发并于2005年上市,作为治疗癫痫的一种新剂型,它是美国FDA迄今唯一批准可居家安全使用的癫痫急性发作的治疗药。国内未有同品种上市。
地西泮直肠凝胶在制备和存储过程中会受到微生物的污染,为保证产品的稳定性和安全性,处方中添加了辅料苯甲酸钠、苯甲酸和苯甲醇作为防腐剂。由于苯甲酸及其盐类摄入过量会影响人体对钙的吸收、刺激胃肠道系统,并有一定致癌性和细胞毒性[2],需控制其含量;而苯甲醇易被氧化,毒性强,在儿童用药方面受到限制[3]。ICH Q6a中明确规定制剂标准中应制定防腐剂含量的可接受标准[4]。因此,防腐剂含量的测定是药品质量控制中的一项重要指标。
《中国药典》2015版、欧洲药典、英国药典、日本药典等[5-9]对地西泮注射液和地西泮片中的地西泮含量测定采用高效液相色谱法,方法重现性差,峰形不佳,且无法同时测定苯甲酸和苯甲醇含量。目前尚无同时测定这3个组分的相关文献报道。本文采用高效液相色谱法(HPLC),同时测定地西泮直肠凝胶中地西泮、苯甲酸、苯甲醇的含量,方法简便、高效、灵敏度高,为该制剂中主药及防腐剂含量的控制提供依据。
1 仪器与药品、试剂
1.1 仪器
Agilent 1260 infinityⅡ高效液相色谱仪(安捷伦科技有限公司);ME55型、ME204E型电子天平,FE28型pH计(均梅特勒-托利多仪器上海有限公司)。
1.2 药品与试剂
地西泮原药(批号:161101,山东信宜制药有限公司);苯甲酸(批号:20180802-202007,四川乐康药用辅料有限公司);苯甲酸钠(批号:20180425-20200424,湖北华日制药有限公司);苯甲醇(批号:20181001-2020.09,成都华邑药用辅料制造有限责任公司);无水乙醇(药用级,批号:P1464903,南京化学试剂股份有限公司);丙二醇(批 号100420181101,湖南尔康制药股份有限公司);羟丙基纤维素E5(批号:PD229197,上海卡乐康包衣技术有限公司);乙酸铵(色谱纯);冰醋酸(分析纯);甲醇(色谱纯);水为纯净水。
2 方 法
2.1 地西泮直肠凝胶的制备
精密称定地西泮原药50 mg,置于100 mL烧杯内,依次加入苯甲酸钠4.0 g、苯甲酸0.2 g、苯甲醇1.5 g、乙醇10.0 g、丙二醇40.0 g和羧甲基纤维素E5 100 g,搅拌均匀,加水至100.0 g,再次混合均匀后,即得地西泮直肠凝胶样品,密封静置备用。
按本方法共制备3批,批号分别为:N19040201、N19040202、N19040203。
2.2 测定方法
2.2.1 色谱条件 色谱柱:Agilent Eclipse Plus C18(4.6 mm×150 mm,3.5 μm);流动相A:0.05 mol·L-1乙酸铵缓冲溶液(称取乙酸铵3.8 g,加水溶解并稀释至1000 mL,用冰醋酸调节pH值至4.0),流动相B:甲醇,按表1进行梯度洗脱;流速:1 mL·min-1;检测波长:254 nm;柱温:35 ℃;进样量:10 μL。
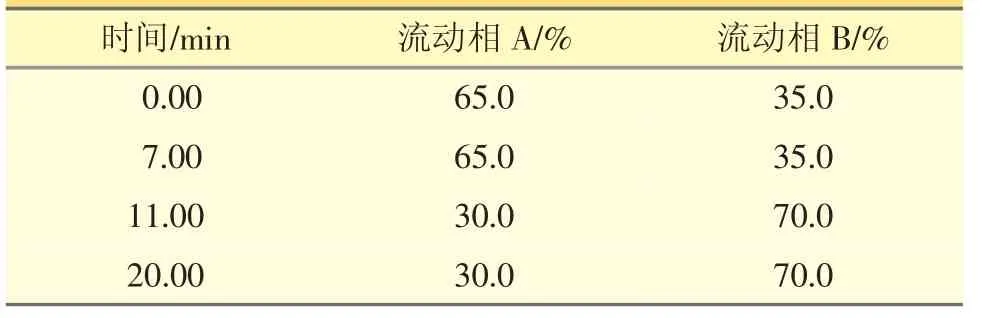
表1 梯度洗脱程序
2.2.2 地西泮对照品溶液配制 精密称定地西泮原药50 mg,置于25 mL量瓶中,加稀释剂(乙酸铵缓冲溶液/甲醇=65∶35)溶解稀释至刻度,摇匀,作为地西泮对照品储备液;精密吸取该储备液2.5 mL至50 mL量瓶中,加稀释剂稀释至刻度,摇匀,制成含地西泮0.1 mg·mL-1的对照品溶液。
2.2.3 苯甲酸对照品溶液配制 精密称定苯甲酸359 mg,置于25 mL量瓶中,加稀释剂溶解并定容至刻度,摇匀,作为苯甲酸对照品储备液;精密吸取该储备液2.5 mL至50 mL量瓶中,加稀释剂稀释至刻度,摇匀,制成含苯甲酸718 μg·mL-1的对照品溶液。
2.2.4 苯甲醇对照品溶液配制 精密称定苯甲醇对照品300 mg,置于50 mL量瓶中,加稀释剂溶解并定容至刻度,摇匀,作为苯甲醇对照品储备液;精密吸取该储备液2.5 mL至50 mL量瓶中,加稀释剂稀释至刻度,摇匀,制成含苯甲醇0.3 mg·mL-1的对照品溶液。
2.2.5 混合对照品溶液配制 分别精密吸取地西泮对照品储备液、苯甲醇对照品储备液、苯甲酸对照品储备液各1.0 mL,置于20 mL量瓶中,加稀释剂稀释至刻度,摇匀,即为混合对照品溶液。
2.2.6 供试品溶液配制 精密称定地西泮直肠凝胶样品(批号为19040201)1.0 g至50 mL量瓶中,加稀释剂溶解并定容至刻度,摇匀,即为供试品溶液。
3 结果
3.1 系统适用性及专属性考察
分别精密量取地西泮对照品溶液、苯甲酸对照品溶液、苯甲醇对照品溶液、混合对照品溶液、稀释剂各10 μL,按“2.2.1”项下色谱条件分别进样。
结果表明,地西泮、苯甲酸和苯甲醇的分离度均大于1.5,达到基线分离。理论塔板数均大于15 000。见图1。
3.2 线性关系考察
精密量取地西泮对照品溶液、苯甲酸对照品溶液、苯甲醇对照品溶液各0.1、0.2、0.5、0.8、1.0、1.5、2.0 mL,分别置于50 mL量瓶中,加稀释剂稀释成一系列不同浓度的对照品溶液,按“2.2.1”项下色谱条件分别进样10 μL。以峰面积(Y),浓度(X,μg·mL-1)进行线性回归,得地西泮、苯甲酸和苯甲醇回归方程与线性范围,见表2。结果表明,地西泮、苯甲酸和苯甲醇线性关系均良好,r2均≥0.999 8。
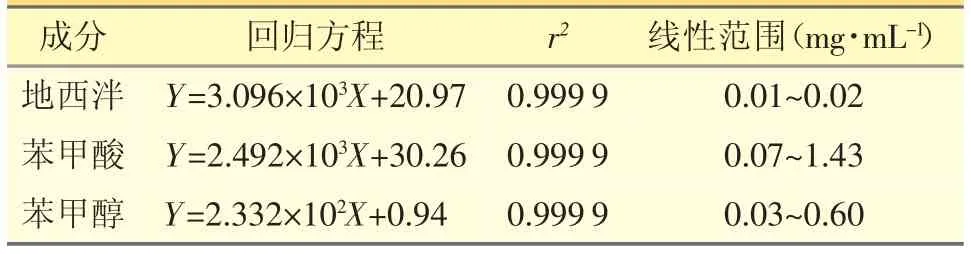
表2 线性关系考察结果
3.3 定量限设定
取“2.2.5”项下混合对照品溶液,逐级稀释后进样测定,按峰高为噪音10倍测得量为定量限。结果表明地西泮、苯甲酸、苯甲醇的定量限分别为0.10、0.18、1.00 μg·mL-1。
3.4 进样精密度试验
精密吸取同一混合对照品溶液10μL,按“2.2.1”项下色谱条件重复进样6次,记录峰面积,测得地西泮、苯甲酸、苯甲醇峰面积的RSD分别为0.02%、0.03%、0.04%(n=6)。表明精密度均良好。
3.5 稳定性试验
精密吸取“2.2.6”项下的供试品溶液10 μL,按“2.2.1”项下色谱条件,分别在0、1、2、4、6、12、24 h进样测定,记录峰面积,测得地西泮、苯甲酸、苯甲醇峰面积的RSD分别为0.11%、0.32%、0.19%,表明供试品溶液在24 h内稳定。
3.6 重复性试验
称取同一批地西泮直肠凝胶样品(批号N19040201),按“2.2.6”项下制备方法平行制备供试品溶液6份,按“2.2.1”项下色谱条件,进样测定,分别记录每份供试品溶液中地西泮、苯甲酸、苯甲醇的峰面积,地西泮、苯甲酸、苯甲醇的平均含量的RSD分别为1.92%、1.50%、1.37%。表明该方法重复性良好。
3.7 加样回收率试验
称取同一批已知含量的地西泮直肠凝胶(批号N19040201)9份,每份1.0 g,分别置于25 mL量瓶中,精密量取地西泮、苯甲酸、苯甲醇对照品溶液3.5、2.5、1.5 mL各3份,加入上述量瓶内(加入水平依次为80%、100%、120%),加稀释剂溶解并稀释至刻度,摇匀;精密量取上述溶液5 mL,分别置于20 mL量瓶中,加稀释剂溶解并定容至刻度,摇匀,按“2.2.1”项下色谱条件分别进样10 μL,记录峰面积,以外标法计算3种成分的含量及回收率,结果见表3。地西泮、苯甲酸和苯甲醇的平均回收率均在98%~101%,RSD均小于2.0%(n=9)。表明该方法回收率符合要求。
3.8 耐用性检测
取同一批供试品溶液(批号N19040201),分别在pH值3.8、4.0、4.2,流速0.8、1.0、1.2 mL·min-1,柱温30 ℃、35 ℃、40 ℃条件下进样,记录峰面积,并考察各成分峰之间的分离情况,结果见表4。地西泮、苯甲酸、苯甲醇的分离度均大于1.5,理论塔板数均大于15 000,各成分含量测定值的RSD值均在限定范围内(≤2.00%),本方法耐用性良好。
3.9 样品测定
精密称定不同批号样品2.0 g,各2份,按“2.2.6”项下方法制备供试品溶液,依照“2.2.1”项下色谱条件进样测定,记录峰面积,以外标一点法分别计算地西泮、苯甲酸、苯甲醇的含量,结果见表5。
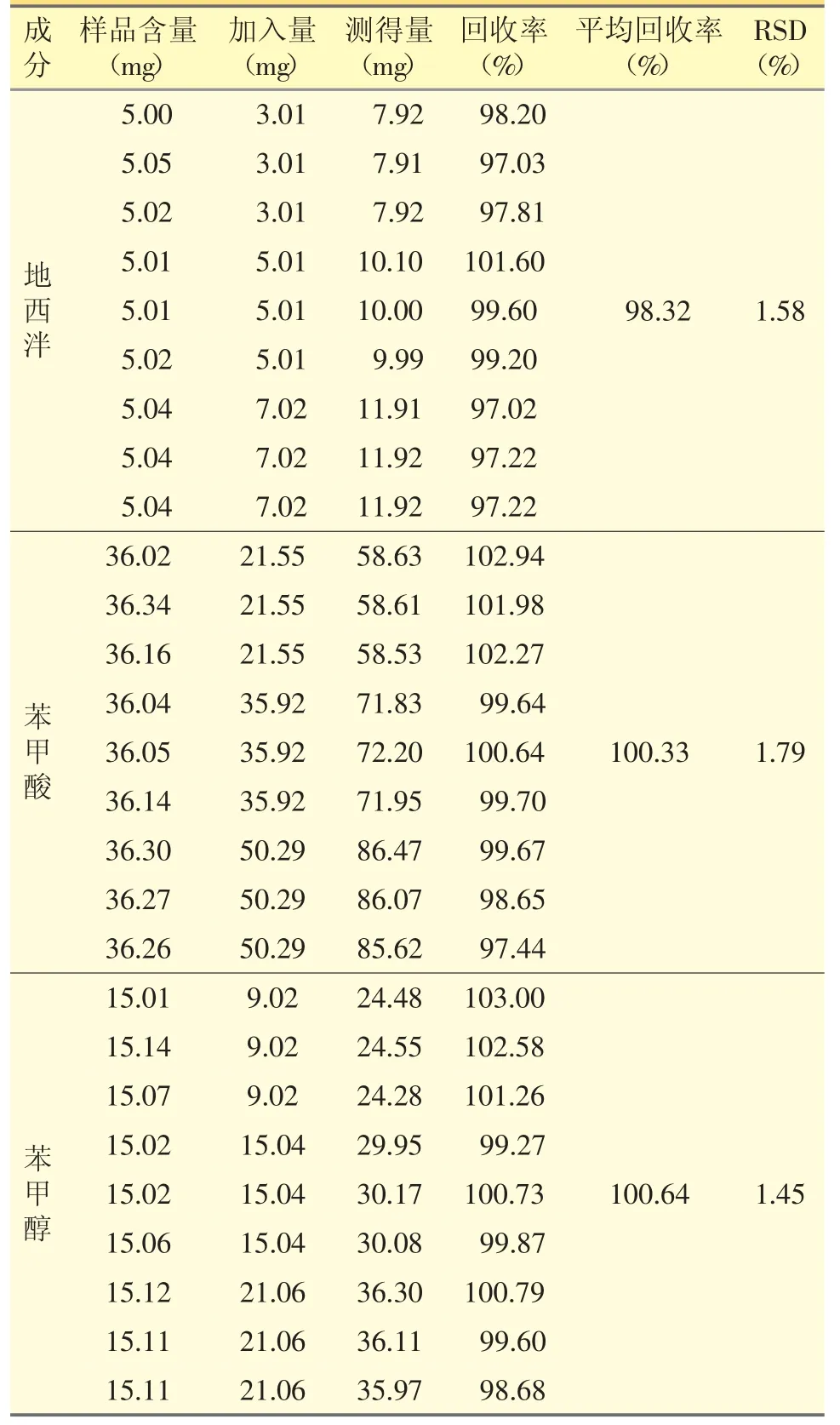
表3 加样回收率试验结果(n=9)

表4 耐用性考察因素及实验结果(n=2)
4 讨论
4.1 流动相pH值的选择
本实验选择乙酸盐缓冲液作为流动相和稀释剂,其pH值是4.0,苯甲酸钠在此条件下可完全转化成苯甲酸。

表5 3批地西泮直肠凝胶中地西泮、苯甲酸、苯甲醇含量检测结果(n=2)
4.2 流动相比例的选择
苯甲酸和苯甲醇需要在高比例水相下出峰,地西泮需要在高比例有机相下出峰,本方法结合3种成分的出峰位置和峰形,选用梯度洗脱程序。本法选用的梯度洗脱程序可同时用于地西泮直肠凝胶有关物质的检测,在地西泮峰和苯甲酸峰相隔时间内可检测到其他杂质峰。如果只用于含量检测,可通过进一步优化,缩短检测时间。
本实验可在同一色谱条件下,同时测定地西泮直肠凝胶中地西泮、苯甲酸、苯甲醇的含量,方法简便准确,为有效控制地西泮等成分的含量提供了科学依据。
