手性柱液质联用法同时测定人体尿液中泮托拉唑对映体浓度*
2020-05-23张学会鲍丽琴
张学会,柏 蓉,费 姚,赵 萍,鲍丽琴
南京医科大学附属江苏盛泽医院 药学部,苏州 215228
泮托拉唑是一种质子泵抑制剂,主要用于胃溃疡、十二指肠溃疡、反流性食管炎、卓-艾综合征(胃泌素瘤)等[1]消化性疾病的治疗。其结构中含有一手性中心硫原子,存在(S)-和(R)-型对映异构体,左旋泮托拉唑具有比泮托拉唑更高的疗效[2]。为了研究左旋泮托拉唑在人体的尿药排泄特征,有必要建立一种简单而具有选择性的检测方法,测定人尿液中泮托拉唑对映异构体的含量。
国内外对泮托拉唑对映异构体的测定方法有高效液相色谱法、超高效液相色谱法(UPLC)、液质联用法等[3,4]。已报道的测定泮托拉唑对映异构体的手性HPLC-UV法,存在分析时间较长、灵敏度较低和样本前处理复杂等问题[5]。已报道[6]的测定泮托拉唑钠对映异构体的手性HPLC法,虽然手性柱的立体选择性强,但是结构选择性却很差,生物样品中的内源性物质通常会干扰目标物的测定,液相检测分析时间长,检测效率低,且生物样品前处理较复杂。本文建立了手性柱-液质联用法(Chiral-LCMS)同时测定人体尿液中左旋泮托拉唑和右旋泮托拉唑的药物浓度,该方法具有分析时间短、高灵敏度和线性范围宽等优点。
1 材 料
1.1 药品和试剂
对照品为左旋泮托拉唑钠(手性HPLC纯度99.6%,批号:20150301)、右旋泮托拉唑(手性HPLC纯度:99.6%,批号:1653-022A4)和内标(R)-Pantoprazoled6(手性HPLC纯度:99.3%,批号:1653-018A3),均由TLC Pharmachem Inc.提供。
乙腈、乙酸(色谱纯);甲酸、乙酸铵、氨水(分析纯);去离子纯化水通过Millipore纯水机制备。
1.2 仪器与设备
液质联用仪:1290 Infinity高效液相色谱仪,包括:柱温箱(G1316C)、多孔板自动进样器(G4226A)和二元高压泵(G4220A),安捷伦科技有限公司;API 4000,美国应用生物公司;色谱工作站:Analyst®软件:1.6.2版本,美国应用生物公司;BP 211D型电子天平,Sartorius公司;AL-204型分析天平,Mettler Toledo公司;STRATOS高速冷冻离心机,Thermo公司。
2 方 法
2.1 检测条件
色谱条件:色谱柱:ChiralPAK IE(4.6mm×150mm,5 μm);柱温:30℃;流动相:乙腈∶10 mmol·L-1乙酸铵(含0.1%乙酸)=72∶28(v/v);流速:0.5 mL·min-1;进样量:1.0 μL;分析时间:10 min。
质谱条件:离子检测方式为多重反应监测(MRM);离子化方式为电喷雾离子化(ESI);离子极性为正离子;离子化电压(IS)为5500V;温度为600℃;雾化气(Gas 1)为379 kPa;涡轮气(Gas 2)为79 kPa;气帘气(Curtain Gas)为276 kPa;碰撞气(Collision Gas)为69 kPa。检测离子对:左旋泮托拉唑和右旋泮托拉唑均为m/z 384.1→200.1;内标为390.1→206.0。
2.2 溶液的配制
左旋泮托拉唑溶液的配制:精密称取左旋泮托拉唑钠10.62 mg,用乙腈溶解并稀释配制成浓度约为1.000mg·mL-1的储备液;用乙腈稀释储备液,制成不同浓度的左旋泮托拉唑溶液,于-40℃冰箱保存备用。
右旋泮托拉唑溶液的配制:精密称取右旋泮托拉唑钠10.04 mg,用乙腈溶解并稀释配制成浓度约为1.000 mg·mL-1的储备液;用乙腈稀释储备液,制成不同浓度的右旋泮托拉唑溶液,于-40 ℃冰箱保存备用。
内标((R)-Pantoprazole-d6)溶液的配制:用乙腈将对照物瓶中的1 mg内标充分溶解(经纯度校正相当于内标0.993 mg),配制成浓度为99.3 μg·mL-1的内标储备液;用乙腈稀释储备液,制成99.3 ng·mL-1的内标溶液,于-40 ℃冰箱保存备用。
2.3 尿液样本的前处理
取1.5mL塑料离心管数支,加入100μL尿液样本和5μL乙腈,涡旋10 s,混匀,再加入200 μL含内标99.3ng·mL-1的乙腈,涡旋10 min,于4 ℃、16 000 r·min-1离心15min。取上清液50μL于另一1.5mL塑料离心管中,加入0.1%氨水150 μL,涡旋混匀,取上清液转移至样品瓶中,进行Chiral-LC-MS分析。
2.4 标准曲线样本及质控样本的配制和处理
取1.5 mL塑料离心管数支,分别加入空白尿液100 μL,再加入5 μL相应浓度的标准曲线用工作液或质控用工作液,涡旋10 s,混匀,制成含左旋泮托拉唑和右旋泮托拉唑浓度分别为2.50、5.00、15.00、50.0、150、500、1500、2500、4500、5000 ng·mL-1的标准曲线用标准含药尿液样本,以及左旋泮托拉唑和右旋泮托拉唑浓度分别为6.00、200、4000 ng·mL-1的质控用标准含药尿液样本。于上述制备好的各标准含药尿液样本中,加入200 μL含内标99.3 ng·mL-1的乙腈,以下操作同“2.3”项。
2.5 测定
研究2名健康受试者静脉输注20 mg注射用左旋泮托拉唑钠后的尿药排泄预特征。经检查合格的2名健康受试者在试验日前入住Ⅰ期临床试验病房,晚上进统一清淡饮食,然后禁食10 h,不禁水过夜。早上恒速泵单次静脉输注给药20 mg(60 min内滴完)。于给药前(0 h)及静脉开始输注后收集血浆样品,同时收集给药0 h及开始给药后0~3 h、3~6 h、6~12 h、12~24 h各时间段的所有尿液。
3 结果
3.1 特异性考察
按“2.1检测条件”项下进样分析,左旋泮托拉唑、右旋泮托拉唑和内标的保留时间分别约为7.5 min、6.0 min和5.9 min,典型的色谱图见图1。结果表明,左旋泮托拉唑、右旋泮托拉唑和内标峰形良好,无杂峰干扰测定。
3.2 标准曲线制备
取“2.4”项下的左旋泮托拉唑和右旋泮托拉唑,浓度均为2.50、5.00、15.0、50.0、150、500、1500、2500、4500、5000 ng·mL-1的标准样本,制备标准曲线,进样分析,记录色谱图,计算左旋泮托拉唑和右旋泮托拉唑各自峰面积As和内标峰面积Ai的比值f(f=As/Ai),以峰面积比值f对血药浓度C作权重回归计算,根据最小二乘法得出直线回归方程并作出标准曲线(f=a×C+b),权重系数为1/C2。计算各样本实测浓度及准确度(Accuracy,%),DB(空白样品,不含分析物和内标的基质)、BK(零浓度样品,只含内标的基质)不参与标准曲线的回归分析。结果显示,左旋泮托拉唑和右旋泮托拉唑的线性范围均为2.50~5000 ng·mL-1,线性关系良好。典型的回归方程为:
左旋泮托拉唑:f=4.62×10-3C+7.75,r=0.9973,w=1/C2
右旋泮托拉唑:f=4.35×10-3C+0.00125,r=0.9958,w=1/C2
该方法的左旋泮托拉唑和右旋泮托拉唑的定量下限均为2.50 ng·mL-1,且信噪比均大于10。
3.3 准确度和精密度试验
按“2.4”项下方法制备含左旋泮托拉唑和右旋泮托拉唑浓度均为2.50、6.00、200、4000 ng·mL-1的样本,每个浓度各配制5份,共测定3个分析批。按“2.3”项下方法处理。左旋泮托拉唑和右旋泮托拉唑的批内、批间精密度和准确度结果见表1。表明高、中、低及定量下限4种浓度的批内、批间精密度和准确度均小于15%,符合生物样本分析测试的要求。
3.4 基质效应和提取回收率
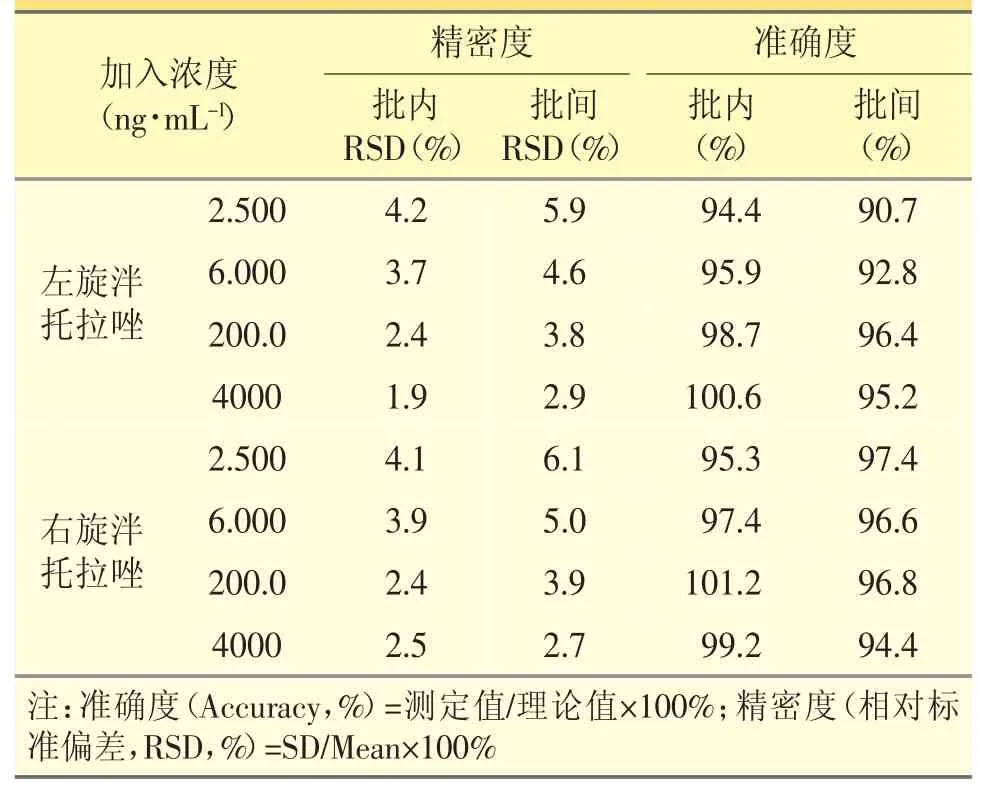
表1 Chiral-LC-MS法测定人尿液中左旋泮托拉唑和右旋泮托拉唑的批内、批间准确度和精密度(n=5)
3.4.1 基质效应 配制空白尿液样本,按配制低、高2种浓度的标准含药尿液的量,分别加入对照品溶液和内标溶液,涡旋混匀,稀释后进行LC-MS/MS分析,以67%的乙腈水代替的同法处理样本进样峰面积,比较尿液样本中左旋泮托拉唑、右旋泮托拉唑及内标的基质效应。浓度为12.0、8000 ng·mL-1的左旋泮托拉唑的基质效应分别是(110.7±3.2)%和(104.4±2.4)%;浓度为12.0、8000 ng·mL-1的右旋泮托拉唑的基质效应分别是(108.9±2.9)%和(105.2±2.4)%;浓度为100 ng·mL-1内标的基质效应是(106.0±2.8)%。实验结果表明,尿液样本中左旋泮托拉唑、右旋泮托拉唑及内标均无基质效应。
3.4.2 提取回收率 按“2.4”项下方法,分别制备含低、中、高3种浓度的标准含药尿液;同时配制空白尿液样本,按配制低、中、高3种浓度标准含药尿液的量,分别加入对照品溶液和内标溶液,涡旋混匀,稀释后进行LC-MS/MS分析,分别计算低、中、高3种浓度的提取回收率。浓度为12.0、400、8000 ng·mL-1的左旋泮托拉唑的提取回收率分别是(92.4±5.4)%、(96.2±4.2)%和(91.6±1.9)%;浓度为12.0、400、8000 ng·mL-1的右旋泮托拉唑的提取回收率分别是(94.0±1.9)%、(95.9±3.9)%和(90.5±2.5)%;浓度为100.00 ng·mL-1内标的提取回收率是(97.4±4.6)%。泮托拉唑对映异构体的提取回收率良好。
3.5 稳定性试验
分别考察在不同实验条件下,左旋泮托拉唑(无右旋泮托拉唑)、右旋泮托拉唑(无左旋泮托拉唑)以及左旋泮托拉唑-右旋泮托拉唑(含量比为1∶1)在尿液及待测样品溶液中左旋泮托拉唑和/或右旋泮托拉唑的稳定性。按“2.4”项下方法配制含左旋泮托拉唑和右旋泮托拉唑浓度均为6.00、200、4000 ng·mL-1的混合样本,同时配制仅含左旋泮托拉唑或仅含右旋泮托拉唑的浓度分别为6.00、200、4000 ng·mL-1的样本,每种浓度配制数份。按“2.3”项下方法处理上述泮托拉唑对映异构体的样本,于4 ℃进样器中放置24 h;于室温24 ℃放置8 h;于-70 ℃反复冻融3次;于-70 ℃冰箱中冷冻保存30天、待测前取出化冻后等,作稳定性参考。结果表明,左旋泮托拉唑及右旋泮托拉唑尿液样本在上述不同实验条件下稳定性均良好;符合生物样本分析测试的要求。
3.6 残留效应
按“2.4”项下方法配制并处理1份含左旋泮托拉唑和右旋泮托拉唑浓度均为10 000 ng·mL-1的标准含药尿液样本,同时按“2.3”项下方法处理5份空白尿液样本,将标准含药尿液样本和空白尿液样本交替进样,进行Chiral-LC-MS分析。结果表明,左旋泮托拉唑和右旋泮托拉唑标准曲线最高浓度点进样分析后,无残留,不影响后续样本的测定。
3.7 应用结果
2例受试者单次静脉输注注射用左旋泮托拉唑钠后,尿液样本中该品浓度小于25 ng·mL-1,左旋泮托拉唑在尿液中未发生手性转化,未测得右旋泮托拉唑,经计算受试者的累积尿排泄率均小于0.03%。
4 讨论
在试验方法建立前,对色谱柱类型、流动相比例、内标浓度及离子对的选择等条件进行了摸索,而后选择了最佳的分析方法,并对该方法进行了验证。建立了同时测定人尿液中左旋泮托拉唑和右旋泮托拉唑浓度的Chiral-LC-MS法,尿液中杂质不干扰样品的测定,标准曲线线性范围为2.50~5000 ng·mL-1,线性关系均良好;高、中、低3种浓度的质控样本准确度在±15%;样品和内标均无基质效应。在泮托拉唑对映体的储存、处理和分析过程中未发现两者间的手性转化,测定过程中各化合物稳定性符合要求。试验证明,采用本法测定人体尿液中药物浓度,定量准确、精密度高、稳定性好,易于操作,可用于泮托拉唑钠左旋体与右旋体的立体选择性药代动力学研究,具有一定的实用性。
