不同内膜准备方案对PCOS患者冻融胚胎移植妊娠结局影响的网状Meta分析
2020-05-22张蕾孔鑫靓张建伟
张蕾,孔鑫靓,张建伟
(1. 山东中医药大学,济南 250014;2. 山东中医药大学附属医院,济南 250011)
多囊卵巢综合征(PCOS)是临床常见的不孕症之一,也是辅助生殖技术(ART)助孕的指征之一[1]。冻融胚胎移植(FET)是PCOS患者常用的治疗方案,可以改善其妊娠结局,预防卵巢过度刺激综合征(OHSS)的发生[2]。FET常用的内膜准备方案包括:自然周期方案、激素替代方案、降调节后激素替代方案以及药物诱导排卵方案等,不同的内膜准备方案对PCOS患者妊娠结局的影响目前尚无定论[3]。本研究从循证医学的角度,探讨不同的内膜准备方案对PCOS患者FET妊娠结局的影响,以期为临床应用提供可靠的依据。
资料与方法
一、检索策略
检索中国知网(CNKI)、维普、万方及PubMed、Embase、Cochrane Library等数据库;检索日期自建库截至2019年4月30日。中文数据库以CNKI为例,检索式如下:(“多囊卵巢综合征”)和(“冻融胚胎移植”或“冻胚移植”)和(“内膜准备”或“自然周期”或“促排卵周期”或“诱导排卵周期”或“人工周期”或“替代周期”或“降调节”)。英文数据库检索以“主题词”+“自由词”检索。
纳入标准:(1)研究人群为PCOS患者,符合2003年鹿特丹诊断标准[4];(2)干预为FET内膜准备方案;(3)限制语种为中文或英文;(4)研究中含有必要的评价指标及结果,如临床妊娠率、早期流产率、胚胎种植率等。
排除标准:(1)未提及PCOS患者的诊断标准;(2)综述;(3)个案报道、经验总结等;(4)数据资料不完整且无法联系获取数据的研究。
二、文献筛选与信息提取
将检索到的文献导入NoteExpress文献管理软件,通过软件查重和人工查重,阅读摘要和关键词,剔除明显不符合的文献,其余文献下载原文后再次进行判断,最终由2名评价员独立对文献资料进行提取,建立Excel数据库,主要包括:标题、作者、发表时间、患者数目、患者基本特征、内膜准备方案、观察指标及结果等。遇到意见分歧时邀请第3位研究员进行讨论解决。
三、文献质量评价
回顾性研究的文献质量由2名评价员采用纽卡斯尔-渥太华量表(Newcastle Ottawa Scale,NOS)[5]进行评价,NOS评分5~9分为高质量文献。随机对照研究(RCT)研究的文献质量采用Cochrane手册Jadad’s量表(随机序列产生、分配隐藏、盲法、结果数据的完整性)进行评价,评分大于3分为高质量文献。
四、统计分析
首先,通过Stata 15.0软件进行网络证据图的绘制、不一致性检验,然后,通过RevMan 5.3软件进行直接比较的传统Meta分析,ADDIS 1.16.8软件进行网状Meta分析,以P<0.05和95%CI作为有统计学差异的标准。计数资料应用比值比(OR)及其95%CI表示效应量,并绘制各干预措施的排序表。ADDIS软件主要采用潜在的标尺缩减参数(potential scale reduction factor,PSRF)来评价结果收敛性,当PSRF接近或等于1时,表明结果有很好的收敛效能,分析可信度高。
结 果
一、文献检索
通过检索初步得到的研究文献有262篇,其中中文文献149篇,英文文献113篇。采用NoteExpress删除重复文献81篇,阅读文章的题目和摘要,根据纳入标准剔除文献146篇,对剩余35篇文献进行全文阅读,最终筛选出17篇文献[2,6-21],检索及筛选流程见图1。
二、纳入研究基本特征
纳入的17篇研究,其中16篇[6-21]为回顾性队列研究,1篇[2]为随机对照研究,FET总周期数3 663个,分别来自17家医院的生殖中心。所有研究均给出了研究对象的平均年龄,仅有5项研究[14,17,20,21,2]未给出研究对象的不孕年限,2项研究[13,17]未给出研究对象的体重指数(BMI)。在妊娠早期不良事件的报道中,异位妊娠共16例。详细见表1。
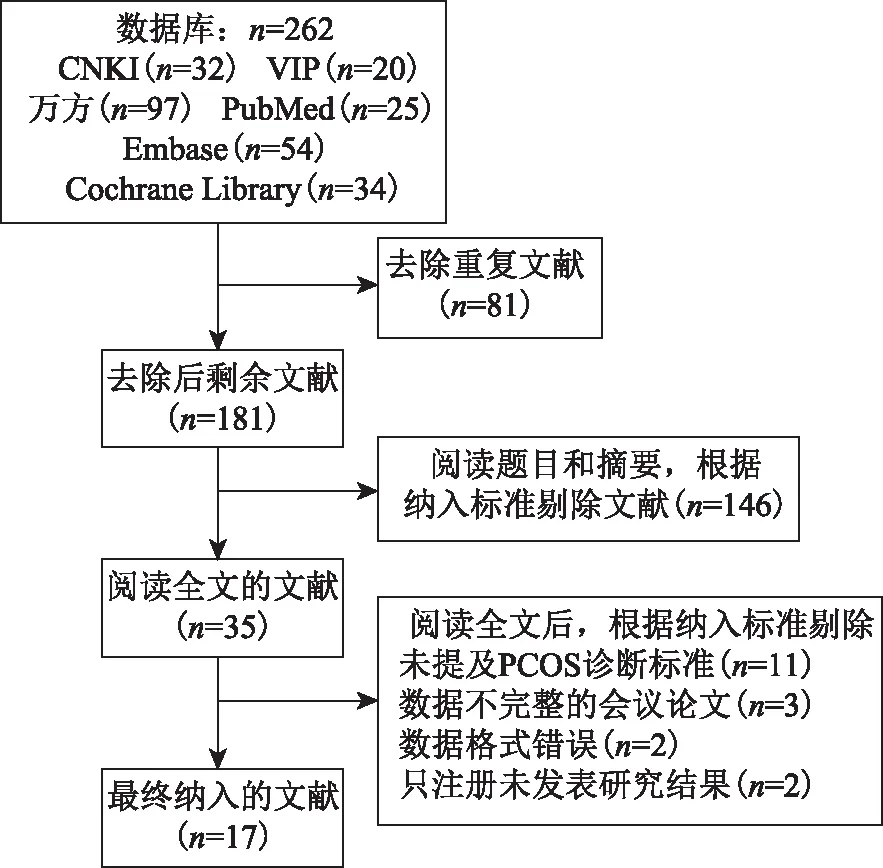
图1 文献筛选流程及结果
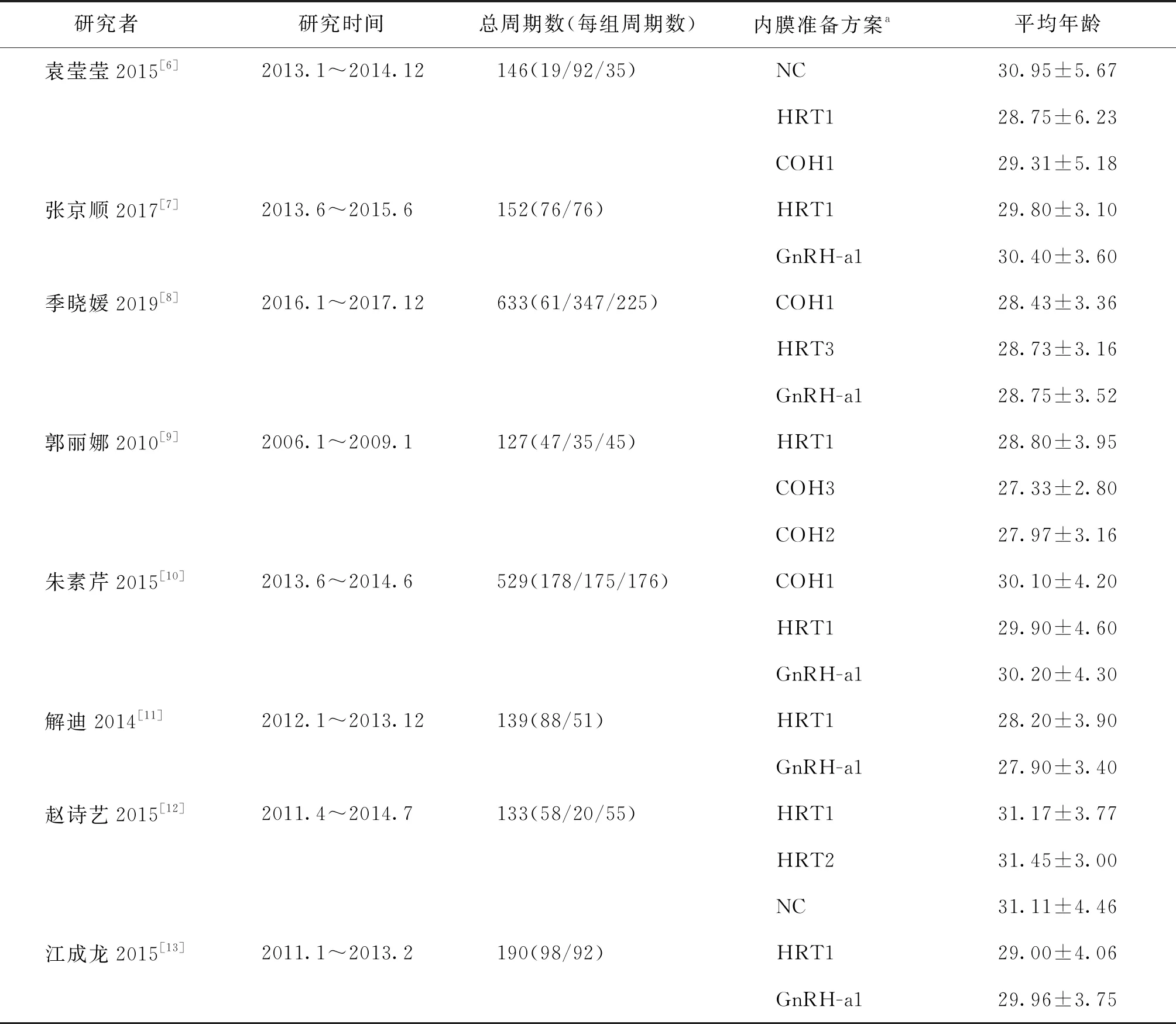
表1 纳入文献的基本特征
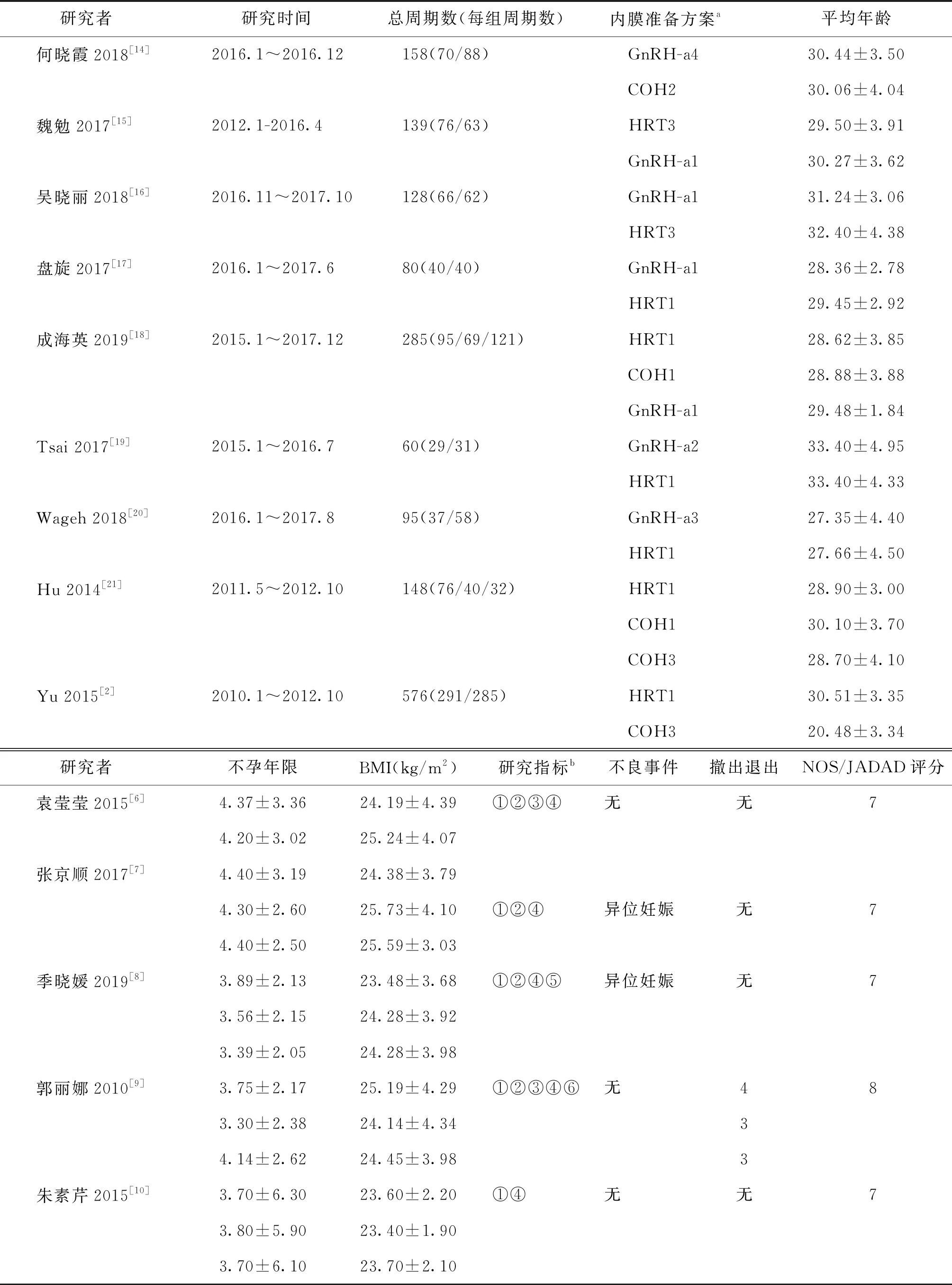
续表
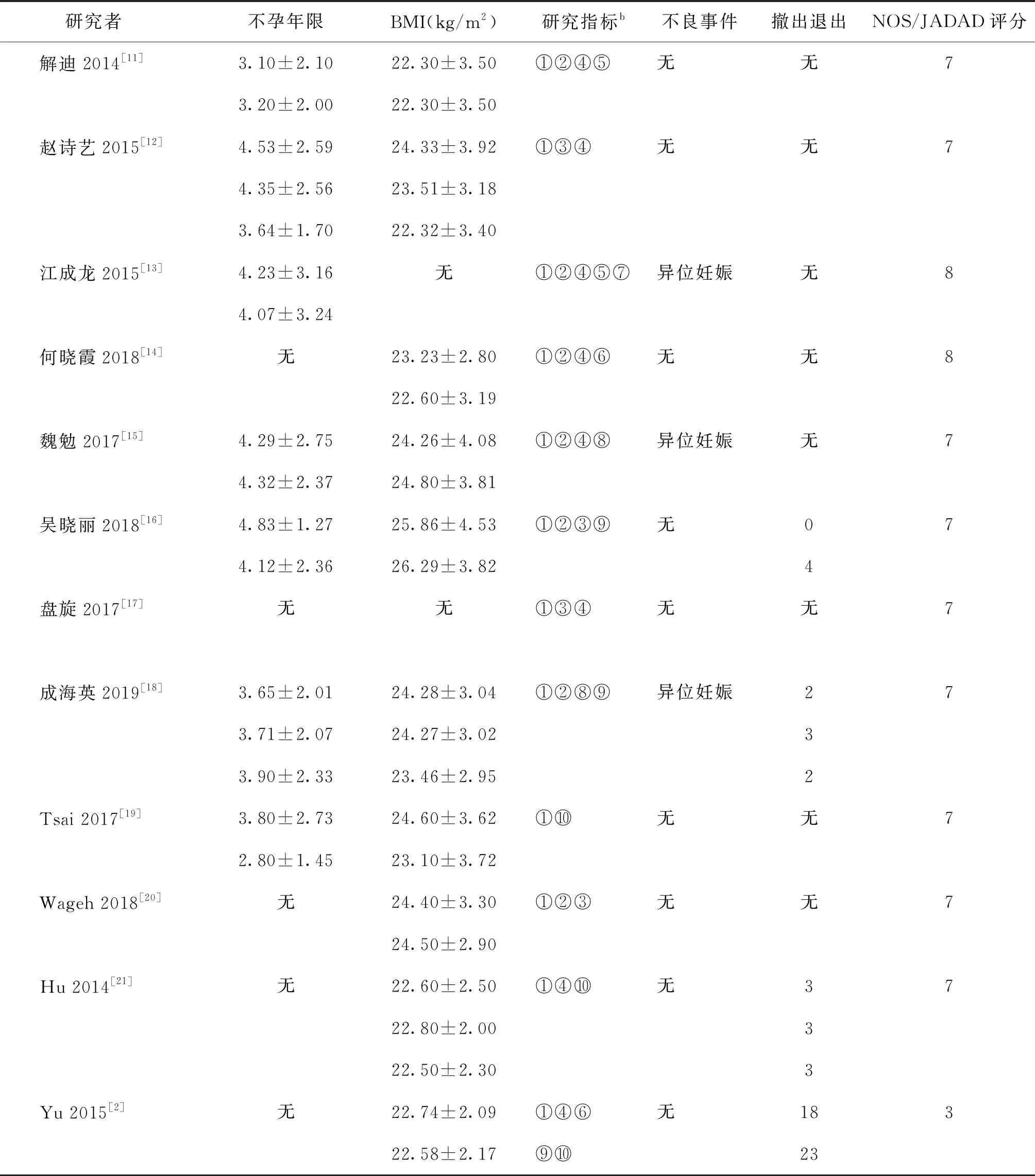
续表
注:a内膜准备方案中:NC为自然周期;HRT1为激素替代周期1(补佳乐+黄体酮);HRT2为激素替代周期2(芬吗通+黄体酮);HRT3为激素替代周期3(补佳乐/芬吗通+黄体酮);COH1为诱导排卵周期1(LE/HMG+HCG);COH2为诱导排卵周期2(LE+HCG);COH3为诱导排卵周期3(HMG+HCG);GnRH-a1为降调节后激素替代组1(卵泡期长效降调节);GnRH-a2为降调节后激素替代组2(提前降调节2个周期);GnRH-a3 为降调节后激素替代组3(黄体期短效降调节);GnRH-a4为降调节后激素替代组4(黄体期长效降调节)。b研究指标:①临床妊娠率;②早期流产率;③生化妊娠率;④种植率;⑤多胎妊娠率;⑥活产率;⑦分娩率;⑧优质胚胎率;⑨周期取消率;⑩持续妊娠率。
三、纳入文献质量评价
回顾性研究的质量评价,应用NOS评分;队列研究评分项“选择、可比、结局”依次进行评分;RCT研究应用Jadad’s量表进行质量评价,具体见表1。
四、网状meta分析
1.网状证据图:纳入的17篇文献研究结局均涉及临床妊娠率,11种方案构成15对直接比较,连线表明2种干预措施存在直接比较,无连线则表明无直接比较,可通过间接比较获得结果,见图2。
2.不一致性检验:11种内膜方案形成了5个三角形闭环,作Z检验,结果提示各闭环的95%CI下限值均为0,P值均>0.05,说明各闭环一致性良好,满足一致性假设,说明直接结果与间接结果一致,见表2(组别缩写同图2注)。
五、临床妊娠率网状Meta分析结果
1.临床妊娠率的比较-校正漏斗图:对纳入的17个研究涉及11种干预措施制作比较-校正漏斗图,结果显示漏斗图大致对称,提示研究存在发表偏倚的可能性较小,见图3(图示同图2)。
2.临床妊娠率网状Meta分析结果:采用ADDIS1.16.8软件的贝叶斯方法对11种方案的临床妊娠率进行排序。首先进行直接Meta分析和网状Meta分析,结果见表3(组别缩写同图2注)。图4为临床妊娠率概率排序图,Rank值越小则代表妊娠率越高。结果表明采用GnRH-a1方案PCOS患者FET的妊娠率最高,概率排序依次为GnRH-a1>GnRH-a4>GnRH-a2>COH1>HRT3>COH2>GnRH-a3>HRT1>COH3>HRT2>NC。

注:N为自然周期;H1为激素替代周期1(补佳乐+黄体酮);H2为激素替代周期2(芬吗通+黄体酮);H3为激素替代周期3(补佳乐/芬吗通+黄体酮);C1为诱导排卵周期1(LE/HMG+HCG);C2为诱导排卵周期2(LE+HCG);C3为诱导排卵周期3(HMG+HCG);G1为降调节后激素替代组1(卵泡期长效降调节);G2为降调节后激素替代组2(提前降调节2个周期);G3为降调节后激素替代组3(黄体期短效降调节);G4为降调节后激素替代组4(黄体期长效降调节)。图2 网状证据图
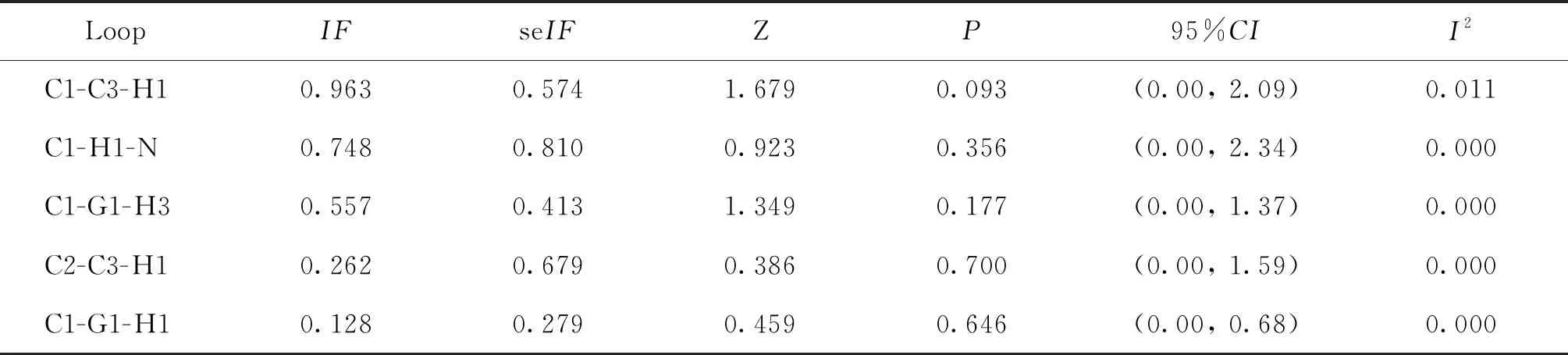
表2 纳入研究不一致性检测结果
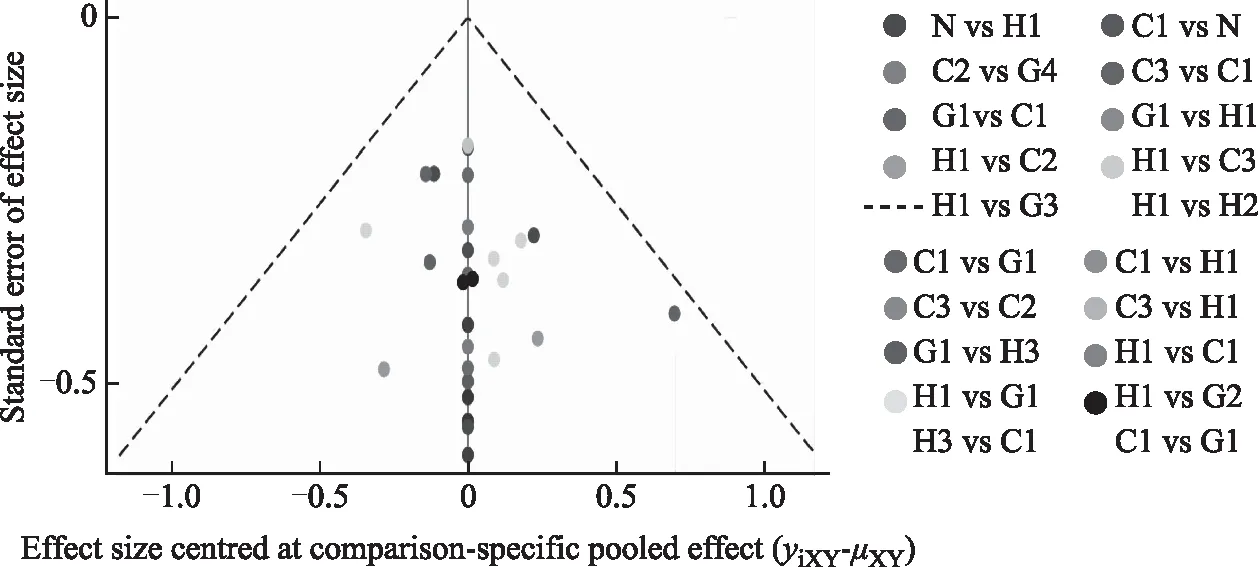
图3 临床妊娠率的比较-校正漏斗图
表3 不同内膜准备方案对PCOS患者FET妊娠率影响的直接与网状Meta分析结果
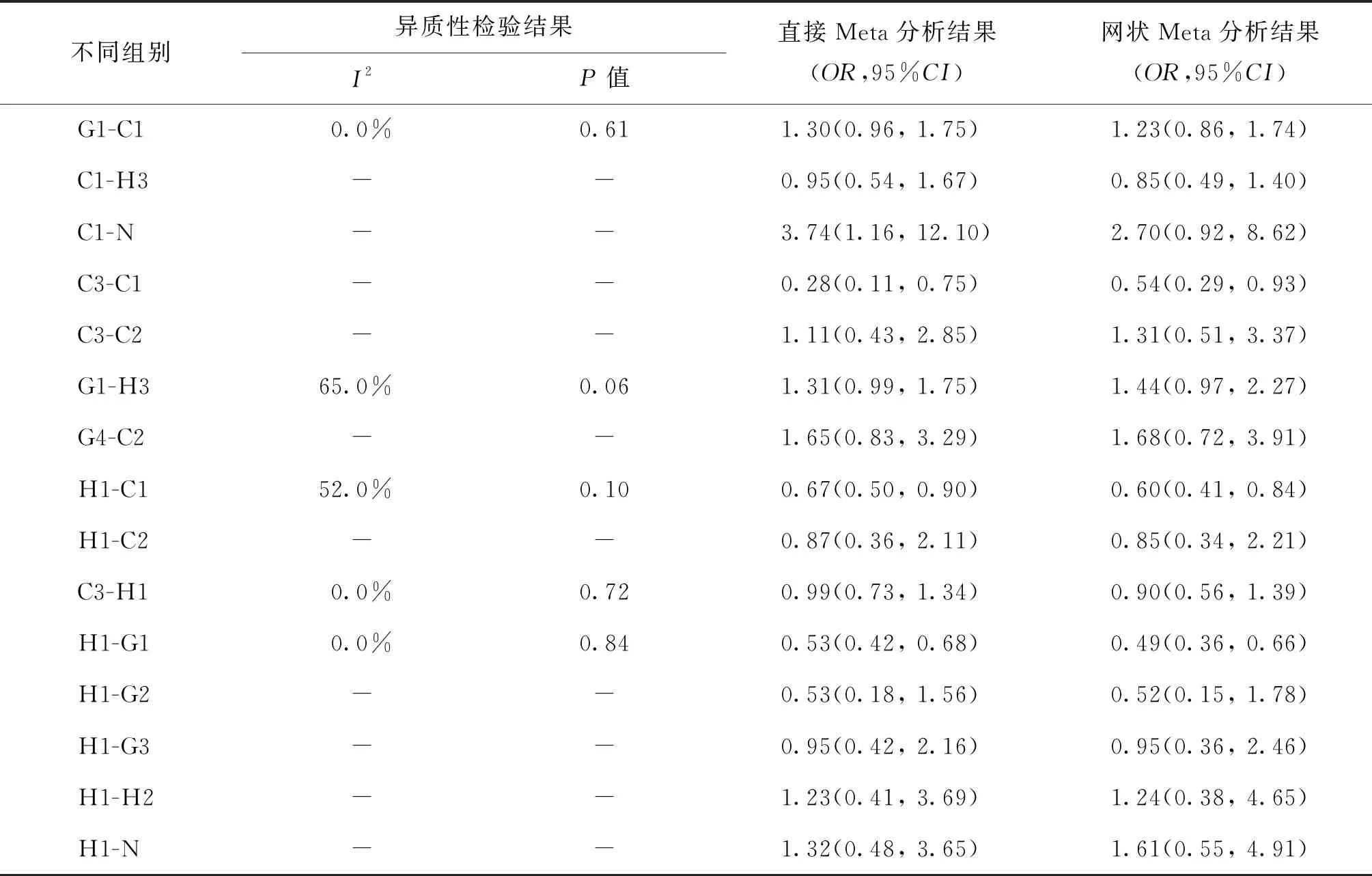
不同组别异质性检验结果I2P值直接Meta分析结果(OR,95%CI)网状Meta分析结果(OR,95%CI)G1-C10.0%0.611.30(0.96, 1.75)1.23(0.86, 1.74)C1-H3--0.95(0.54, 1.67)0.85(0.49, 1.40)C1-N--3.74(1.16, 12.10)2.70(0.92, 8.62)C3-C1--0.28(0.11, 0.75)0.54(0.29, 0.93)C3-C2--1.11(0.43, 2.85)1.31(0.51, 3.37)G1-H365.0%0.061.31(0.99, 1.75)1.44(0.97, 2.27)G4-C2--1.65(0.83, 3.29)1.68(0.72, 3.91)H1-C152.0%0.100.67(0.50, 0.90)0.60(0.41, 0.84)H1-C2--0.87(0.36, 2.11)0.85(0.34, 2.21)C3-H10.0%0.720.99(0.73, 1.34)0.90(0.56, 1.39)H1-G10.0%0.840.53(0.42, 0.68)0.49(0.36, 0.66)H1-G2--0.53(0.18, 1.56)0.52(0.15, 1.78)H1-G3--0.95(0.42, 2.16)0.95(0.36, 2.46)H1-H2--1.23(0.41, 3.69)1.24(0.38, 4.65)H1-N--1.32(0.48, 3.65)1.61(0.55, 4.91)
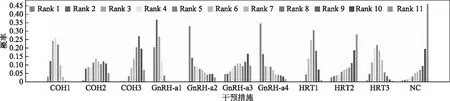
图4 不同内膜准备方案PCOS患者FET临床妊娠率的概率排序图
讨 论
本网状Meta分析结果显示,PCOS患者FET前不同内膜准备方案的临床妊娠率比较中,降调节后激素替代组>诱导排卵组>激素替代周期组>自然周期组,具体排序如下:GnRH-a1>GnRH-a4>GnRH-a2>COH1>HRT3>COH2>GnRH-a3>HRT1>COH3>HRT2>NC,4种降调节后激素替代方案,最优是在卵泡期长效降调节;3种诱导排卵方案,最优是使用来曲唑/HMG+HCG;3种激素替代周期方案,最优是补佳乐/芬吗通+黄体酮;妊娠率相对较差的是自然周期进行移植前内膜准备。并且在临床妊娠率的概率排序中,排名前3位的均是降调节后激素替代组内膜准备方案。本研究结果与Xie等[22]的一项回顾性队列研究结果一致,在FET前加用GnRH-a评估最适宜的不孕症类型,结果表明从活产率、胚胎种植率、临床妊娠率方面看,GnRH-a降调节联合激素替代周期,更适宜PCOS患者。
PCOS作为常见的内分泌代谢紊乱疾病,其病理变化相对复杂。一方面,PCOS患者体内过高的LH水平可使子宫内膜上孕激素受体提前表达,使内膜转化为分泌期,种植窗缩短,影响胚胎着床;另一方面,PCOS患者子宫内膜白血病抑制因子、血管内皮生长因子、基质金属蛋白酶、整合素αvβ3等相关因子均呈低水平表达[23],可能影响子宫内膜容受性,继而导致妊娠率的下降。1988年,Salat-Baroux等[24]通过研究供卵FET周期受卵者的内膜准备方案,得出垂体降调节后应用雌激素可以促进子宫内膜与胚胎的同步发育。此后,降调节激素替代周期FET的可行性逐渐得到认可,并认为其可从促进胚胎发育和提高子宫内膜容受性方面提高IVF-ET患者的妊娠率。有动物实验表明,围种植期胚胎表面存在GnRH-a受体,且围种植期胚胎发育与GnRH-a的增加呈正相关,提示GnRH-a可能对胚胎发育起到促进作用[25];还有研究证实,GnRH-a可以通过增加子宫内膜胞饮突的数量,提升整合素αvβ3的表达,增加子宫内膜容受性[26]。此外,GnRH-a可降低白细胞介素-1和肿瘤坏死因子等细胞因子的浓度,有利于胚胎着床[27]。因PCOS患者稀发排卵或无排卵的特点,临床上在FET中多采用激素替代周期或诱导排卵周期进行内膜准备。动物实验证实,分泌期高浓度雌激素环境可使子宫内膜种植窗缩短[28];激素替代方案可能出现优势卵泡发育,出现早发LH峰,干扰胚胎着床[29];而促排卵周期无法避免内膜生长不同步、高卵巢过度刺激综合征(OHSS)风险等问题。GnRH-a降调节后,可完全去除内源性雌激素的影响,使子宫内膜处于低雌激素环境,有利于胚胎着床,同时也不存在多个卵泡生长发育等问题。综合多方面因素考虑,对PCOS患者而言,使用降调节激素替代周期进行内膜准备具有一定的优势,同时本研究结果可作为佐证。但由于临床应用降调节激素替代周期方案费用较高,增加了患者的经济负担,因此本方案临床应用仍较少。
最近的一篇Meta分析对FET前不同的内膜准备方案进行两两之间比较,结果显示,不同内膜准备方案的临床妊娠率、活产率没有显著性差异[30]。本研究是第一个对PCOS患者FET不同内膜准备方案采用直接和间接证据进行分析排序的网状Meta分析。针对PCOS患者FET前的不同内膜准备方案,纳入的17家生殖中心共有11种内膜准备方案,这种综合了直接和间接比较的证据使得我们对不同内膜准备方案的比较更精准,能获得一个较全面、较客观的评价,以指导临床更加合理地应用。且本研究质量评价结果显示,本篇Meta分析虽纳入的非随机对照研究居多,但仍属较高质量文献。
但本研究亦存在一些局限性:(1)本篇网状Meta分析纳入的研究以回顾性研究居多,随机对照研究仅1篇,对研究结果潜在的偏倚可能更大,降低了本次网状Meta分析所提供的证据强度。(2)所纳入的研究分别在不同的生殖中心进行,因患者的身体素质、医生的水平不同,可能对结果产生偏倚。(3)提前降调节2个周期的内膜方案仅1篇研究[19],黄体期短效降调节方案仅1篇研究[20],黄体期长效降调节方案仅1篇研究[14],所纳入研究数量不足,增加了结果的偶然性,可能会降低最终结果的可靠性。
基于目前的证据,对PCOS患者FET前的不同内膜准备方案比较,认为相对最优的是降调节后激素替代组,其次是诱导排卵组和激素替代组,相对较差的是自然周期方案。未来需要开展更加严谨、多中心的随机对照试验,以便为相关研究提供更有科学依据的数据参考。
