共沉淀法制备Co9S8/C材料以及性能研究
2020-05-22李志学杨占旭
李志学,杨占旭
(辽宁石油化工大学化学化工与环境学部,辽宁抚顺113001)
目前,环境污染、新能源短缺问题日益加剧,寻找污染小、储量丰富、高效的新能源成为非常紧迫的问题[1]。将能源经济从以化石燃料为主导转变成以可再生能源为主导的经济载体上,势必会成为一种新的发展理念。其中,重大挑战是将可再生的新能源更充分地转化为电能以及储藏电能或合成燃料[2-4]。
在众多新型能源中,氢能由于具有较高的能量密度、燃烧产物为水、对环境无污染等特点而受到了重点关注[5]。为了缓解能源危机,人们开发了许多具有潜在应用价值的制备氢能源手段,包括光催化方法制氢、电解水方法制氢、电解水方法制氧等[6]。在这些技术中,电解水制氧受到人类的广泛关注[7]。电催化制氧反应(OER,H2O→O2+4H++4e-)是电解水析氧的决速步骤,反应采用4e-转移过程,反应过程相对复杂,在热力学和动力学上限制了电解水制氧的转换效率。同时,在碱性电解水制氧过程中,由于受到O2的过电位、电解液的电阻以及其他因素的影响,实际电压远高于理论电压。因此,设计合成高效的析氧催化剂,加速反应过程至关重要。众所周知,贵金属催化剂(如RuO2、IrO2)是标准的析氧反应催化剂,并且已经应用于商业化生产。但是,贵金属催化剂的低产量、重污染、高费用阻碍了它的大规模应用。因此,开发储量丰富、价格低廉、污染小的电催化材料至关重要。在非贵金属电催化剂中,由于钴硫化合物在碱性电解液中具有较低析氧过电位、价格低廉、良好的操作稳定性等特点而受关注[8-9],并且有望取代RuO2、IrO2贵金属催化剂[10]。但是,纯相Co9S8材料作为电催化剂用于电解水的主要缺点是在碱性电解液中很容易被氧化,从而导致其电导率和长期稳定性降低[11-13]。碳材料复合Co9S8可以有效提高电化学产氧性能,一般认为材料性能提升的原因是:在电催化反应过程中,提高中间体在材料表面的吸附,并且增强催化剂表面和反应中间体之间的电子转移[14];碳材料复合可以有效地保护粒子,避免团聚现象的发生,从而显著提高电催化反应中材料的稳定性能;碳材料复合Co9S8后,增加材料表面的氧空位[15],改变原子与晶格氧键能[16],提高材料的催化活性[17]。
本文采用共沉淀方法合成了Co9S8/C复合材料,通过X-射线粉末衍射(XRD)、扫描电子显微镜(SEM)、透射电子显微镜(TEM)等手段对材料的结构和形貌进行表征,优化了材料的催化性能,材料在1.58 V(相对于标准氢电极RHE,下同)下电流密度可以达到10 mA/cm2。
1 实验部分
1.1 试剂与仪器
六水合硝酸钴(Co(NO3)2·6H2O)、六水合硝酸锌(Zn(NO3)2·6H2O)、葡萄糖(C6H12O6·H2O),分析纯,国药集团化学试剂有限公司;2,2-硫代二乙酸(C4H6O4S),分析纯,上海阿拉丁试剂公司;氯化钾(KCl),分析纯,天津市博迪化工有限公司;氧化铝粉,分析纯,上海楚兮实业有限公司;萘酚,分析纯,上海河森电气有限公司;无水乙醇(C2H5OH),分析纯,天津市大茂化学试剂厂;盐酸,分析纯,天津市富宇精细化工有限公司;硝酸,分析纯,沈阳市派尔精细化工制品厂;高纯氮气,抚顺气体厂;去离子水,实验室自制。
VSP-300多通道电化学工作站,法国Biologic公司;D8 Advance X射线衍射仪(Cu靶,Kα射线,工作电压40 kV,工作电流40 mA),德国Bruker公司;SU8010型扫描电子显微镜,日本日立公司;JEM-2100F型透射电子显微镜,日本电子株式会社;超声波清洗器,德国Wiggens公司。
1.2 工作电极的打磨
首先分别配置体积比为1∶1的HNO3和H2O、C2H5OH和H2O溶液待用,其次先用0.30 μm氧化铝粉以画圆的方式打磨10 min,再用0.05 μm氧化铝粉打磨10 min。用去离子水冲去电极表面的氧化铝粉,然后分别用去离子水超声1 min,C2H5OH和H2O混合液超声1 min,HNO3和H2O混合液超声1 min,最后再用去离子水超声至电极表面清洁干净为止。配制2.0 mmol/L铁氰化钾和0.1 mol/L KCl溶液,测试玻碳电极是否打磨干净。
1.3 实验方案
称取一定量的 Co(NO3)2·6H2O、Zn(NO3)2·6H2O加入30 mL的无水乙醇中,搅拌至完全溶解,即为溶液1;称取一定量的C4H6O4S加入20 mL无水乙醇中,搅拌至完全溶解,即为溶液2。将溶液2缓慢倒入溶液1中,同时将这两种混合液搅拌3 h,直至产生粉色的沉淀物。称取0.6 g C6H12O6·H2O溶解在20 mL水中,把C6H12O6·H2O溶液加入上述混合液中,搅拌24 h,在室温下把沉淀物用无水乙醇和去离子水各洗涤3次,离心分离沉淀物放入60℃烘箱中烘干、研磨,最后在800℃管式炉中煅烧2 h,即制备出纯相的Co9S8/C材料,采用同样的方法制备纯相的Co9S8。
1.4 析氧电化学性能测试
通过电化学工作站测试了Co9S8/C以及Co9S8材料的电化学产氧性能,测试采用标准的三电极体系,其中旋转盘电极(RDE)(直径为3 mm)作为工作电极,铂丝作为对电极,饱和甘汞电极(SCE)作为参比电极。工作电极的制备:将2 mg的电催化剂分散在1 mL的乙醇和30 μL的萘酚溶液中,配置成质量浓度为2 mg/mL的催化材料,超声60 min,移取7 μL的电催化材料涂在RDE表面(催化剂的负载量为0.2 mg/cm2),自然条件下烘干。
2 结果与讨论
图1为Co9S8/C和Co9S8的XRD图谱。从图1可以看出,Co9S8/C的衍射峰与标准的立方晶型Co9S8的标准图谱JCPDS(No.19-0364)相吻合,且衍射峰尖锐,即样品的结晶度好。2θ为 29.8°、39.5°、47.6°、51.9°处的衍射峰分别对应(311)、(331)、(511)和(440)晶面,结构完整而无杂相,表明产物的纯度很高。另外,Co9S8/C催化材料的衍射峰最强,说明Co9S8/C产生较高的结晶度,晶粒尺寸也逐渐增加,尤其(311)晶面对应的特征峰强度明显增加,说明(311)晶面可能存在择优生长。因此,Co9S8/C材料能够促进晶体的结晶以及在特定晶面上择优生长,从而使Co9S8/C颗粒的晶面取向发生变化。
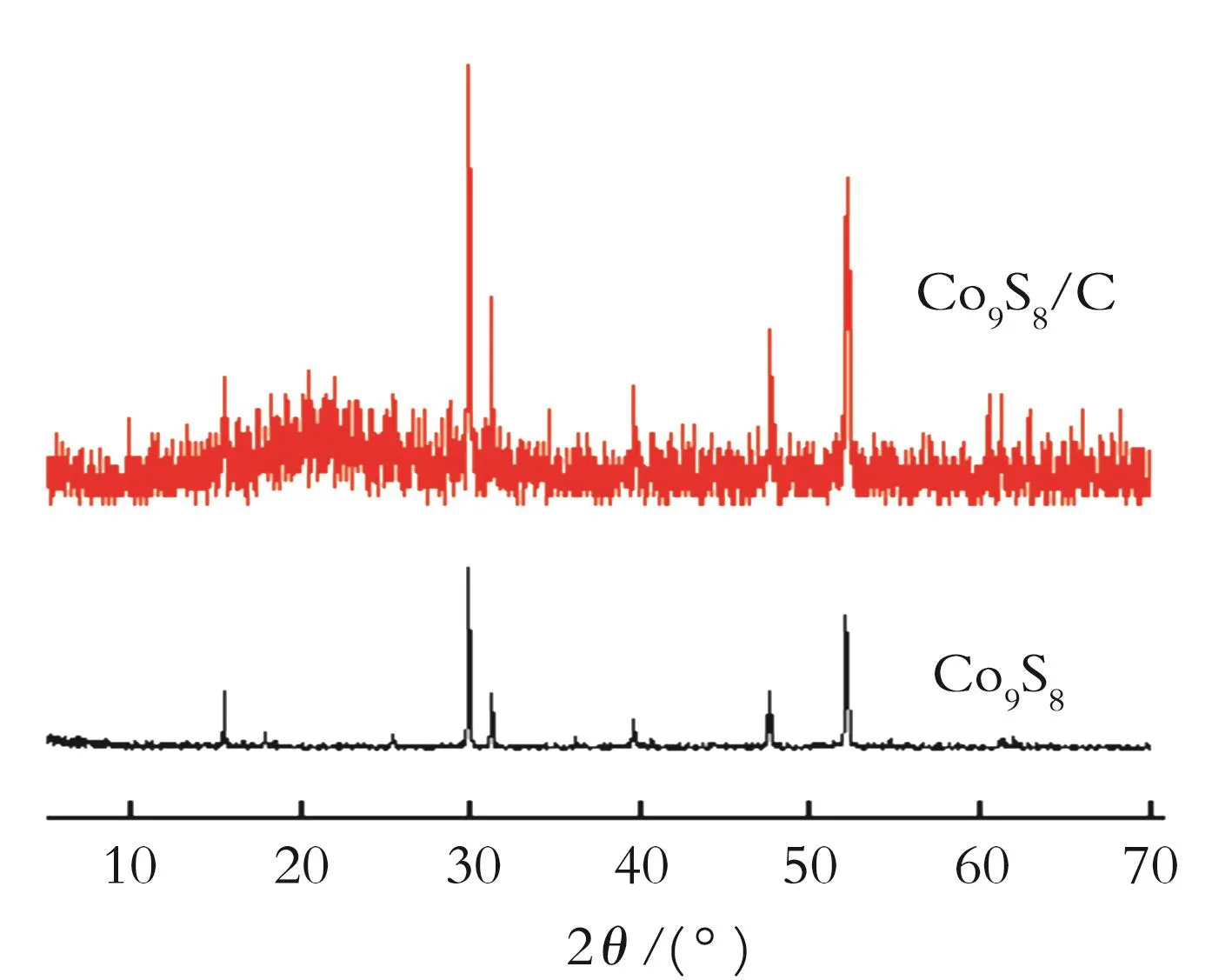
图1 Co9S8/C和Co9S8的XRD图谱
图2为Co9S8/C和Co9S8的SEM照片。从图2(a)可以看出,材料出现片状结构,其形成机理可能是:立方晶型的 Co9S8材料在(311)晶面和(440)晶面的化学势能高于其他晶面,晶核形成后为了降低势能,其优先沿着这两个晶面增长,从而形成片状结构[18],这说明与碳材料复合可以明显提高Co9S8材料的导电性能[19]。对比图2(b)可以看出,Co9S8/C材料的表面粗糙,从而使催化材料的活性位点增加,提高电解水析氧性能。

图2 Co9S8/C和Co9S8的SEM图
图3(a)为Co9S8/C的TEM图。从图3(a)可以看出,Co9S8/C催化材料呈现片状结构,这与图2(a)观察结果一致。图3(b)为Co9S8的高分辨率透射电镜(HRTEM)图。从图3(b)可以看出,晶面间距为0.3 nm,对应着Co9S8的(311)晶面,说明合成了Co9S8/C材料。

图3 Co9S8/C的TEM图和Co9S8的HRTEM图
在扫描速率为10 mV/s条件下,1 mol/L KOH电解液中测试Co9S8和Co9S8/C的稳态极化(LSV)曲线,结果见图4。从图4可以看出,纯相Co9S8的析氧(OER)起始电位(1.70 V)较大,电流密度相对较小,说明纯相Co9S8对析氧的活性较低。Co9S8/C和纯相Co9S8两个催化材料中,Co9S8/C起始电位(1.35 V)较高,电流密度相对较大,表明Co9S8/C具有更好的电催化析氧性能。同时,在电流密度为10 mA/cm2时,Co9S8/C过电势(350 mV)远小于纯相Co9S8过电势(550 mV),表明碳材料复合后可以明显提升Co9S8/C对OER的催化能力。然而,Co9S8/C的OER性能优于贵金属RuO2(380 mV)以及贵金属IrO2(380 mV)催化剂[20]。根据碱性条件下OER催化机理[21],这是碳材料复合后材料表面氧空位增多、原子与晶格氧键能改变作用的结果。值得注意的是,与大多数报道的硫化钴催化剂相比,Co9S8/C催化剂过电势相对较低,如Co-S/Ti mesh(361 mV)[22]和 CoS2(400)/N,S-GO(380 mV)[23],同时与活性高的非贵金属电催化剂相比有较高的优势。因此,Co9S8/C催化剂有望取代贵金属催化剂。
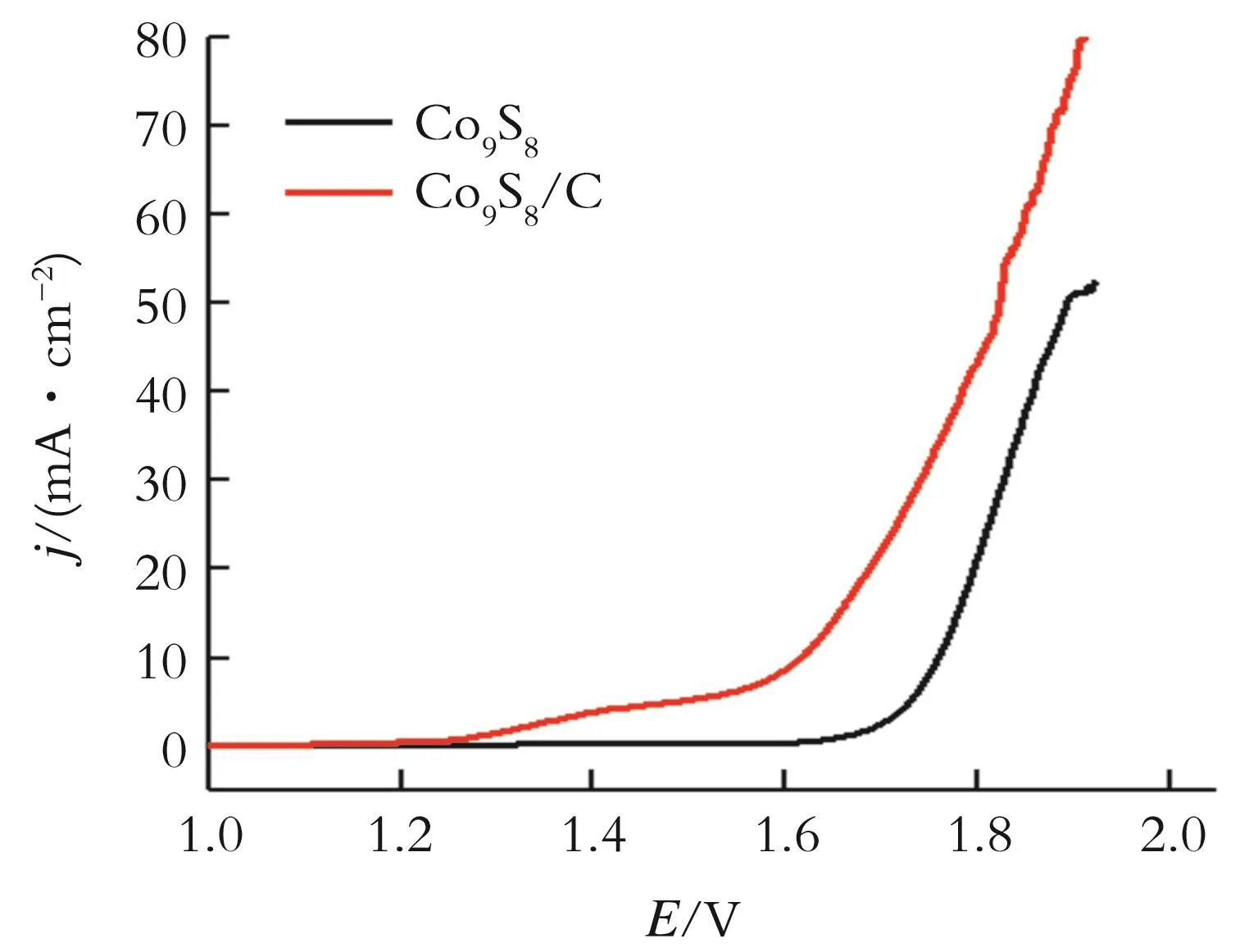
图4 Co9S8/C和Co9S8的稳态极化(LSV)曲线
为了能够更好地了解Co9S8/C和Co9S8材料的快速析氧动力学,采用电化学阻抗光谱(PEIS)技术检测催化剂中电子传输过程,得到Co9S8/C和Co9S8催化材料的电化学阻抗图,如图5所示。在极化曲线中,高频区半圆对应的半径越小,催化剂的电荷转移阻抗数越小[24-26]。从图5可以看出,Co9S8/C催化材料在高频区的半径明显小于Co9S8催化材料,说明Co9S8/C具有更小的阻抗和更快的电子传输速度。

图5 Co9S8/C和Co9S8的电化学阻抗图
为了研究析氧反应的动力学过程,根据析氧极化曲线进行了塔菲尔斜率的拟合分析。塔菲尔斜率是评价电催化性能好坏的指标之一,塔菲尔斜率越大,电极极化现象越严重,越不利于析氧反应的发生。利用线性扫描拟合得出不同催化剂对应的塔菲尔斜率,如图6所示。塔菲尔斜率的计算公式为η=a+blgj。式中,a为塔菲尔线与电势轴的截距;b为塔菲尔斜率,即图像中的直线斜率;j为电流密度,mA/cm2;η为超电势,mV[27]。从图 6 可以看出,Co9S8和Co9S8/C催化材料的塔菲尔斜率分别为192 mV/dec和102 mV/dec。在两种催化材料中,Co9S8/C的塔菲尔斜率要低于Co9S8的塔菲尔斜率,说明Co9S8/C催化材料具有更好的导电性能,从而更有利于电解水析氧反应。

图6 Co9S8/C和Co9S8的塔菲尔斜率图
对于电解水析氧过程,催化剂的稳定性也是评价电催化产氧性能的重要指标。在碱性电解液中,对Co9S8/C和Co9S8催化材料进行稳定性测试,结果见图7。从图7可以看出,在电流密度为10 mA/cm2条件下,经过200 min循环测试后,可发现Co9S8/C催化材料稳定性没有明显的降低。与Co9S8相比,Co9S8/C这种复合材料有更好的稳定性。
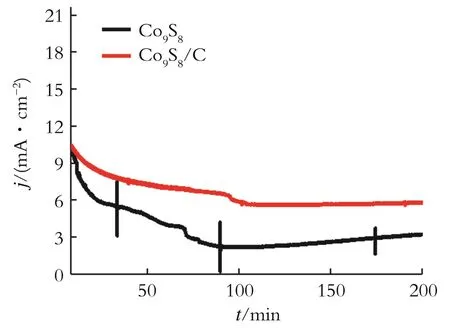
图7 Co9S8/C和Co9S8催化材料循环稳定性测试曲线
3 结 论
采用共沉淀的方法制备了碳材料复合Co9S8电催化剂(Co9S8/C),与纯相 Co9S8相比,Co9S8/C催化材料表现出良好的电化学析氧性能,其在电流密度10 mA/cm2下过电势为350 mV,塔菲尔斜率为102 mV/dec,并且显示出良好的析氧催化稳定性。这是因为纯相Co9S8导电性及在碱性电解液中稳定性较差,而与碳材料复合之后,Co9S8活性组分与碳材料之间的协同作用提高了催化材料的导电性,同时碳材料作为催化剂的载体也提升了催化材料的稳定性。因此,Co9S8/C催化材料具有更高的电催化产氧性能。如何实现多种催化成分的有效复合,极大地发挥催化材料与碳材料的协同效应,这是开发出具有更高析氧性能的催化剂仍然需要努力的方向。
