螺旋链状结构的亚磷酸钬的无溶剂合成及表征
2020-05-22修志佳李虹陆马怡轲黄亮亮
修志佳,李虹陆,刘 陆,马怡轲,陈 立,黄亮亮
(1.辽宁石油化工大学化学化工与环境学部,辽宁抚顺113001;2.远东页岩炼化有限责任公司,辽宁抚顺113015)
由于金属磷酸盐晶体在离子交换、催化和分离领域的广泛应用,金属磷酸盐微孔材料新结构的合成成为研究人员的一个重点研究课题[1]。20世纪80年代初,第一例磷酸铝微孔化合物问世[2],为后来越来越多的磷酸盐(Ga、In、Fe、Co、Ni、Mn等)的制备开辟了新篇章[3-8]。近年来,人们开始用假四面体[HPO3]2-结构单元取代四面体[PO4]3-结构单元来构建开放骨架。假四面体的[HPO3]2-单元通过P-O-M(M=金属)与3个相邻的阳离子相连,降低了连接点的个数,有望产生更加空旷的有趣结构[9]。1995年,G.Bonavia等[10]报道了首例亚磷酸钒,拓宽了微孔化合物的合成路径。随后又有大量的亚磷酸盐化合物被报道,其金属元素已经涉及到大部分过渡金属、主族金属,例如 Zn、V、Mn、Fe、Co、Ni、Al、Ga、In 等[11]。然而,关于稀土亚磷酸盐化合物的报道却相对较少。稀土金属有“点铁成金”的功效,犹如一个“魔术师”,只要在一些传统产品中加入适量的稀土,就会产生许多神奇的效果。例如,冶炼钢时加入适量稀土就能显著提高钢的耐磨性、耐磨蚀性和韧性[12];钬元素又可用作金属卤素灯添加剂[13]、钬激光碎石技术等[14]。同时,稀土金属具有多样性的配位数,容易形成有趣的结构。例如,六配位的Dy(H2PO2)3、八配位的[Pr(H2PO2)(HPO3)(H2O)]·H2O[15]、九配位的Er2(C2O4)3(H2O)6·12H2O[16]。 因此,稀土化合物的研究极其重要。
传统的分子筛合成方法主要以水热及溶剂热合成为主,不可避免地产生大量的废弃溶剂,对环境造成影响。此外,合成中需要较长的时间和较高的温度,以及伴随高温产生的高自生压力,这些都和“绿色化学”的理念背道而驰。因此,基于绿色化学的理念,离子热合成、无模板及无溶剂合成成为近几年分子筛材料合成的热点[17]。无溶剂合成与传统的水热及溶剂热合成相比,具有高效性、高选择性、较低的成本、简单的合成步骤以及较低的环境污染等优点[17-18]。然而,该合成方法在获得完美晶体方面却有一定的局限性,因此采用该方法合成的磷酸盐以及亚磷酸盐化合物的报道较少。例如,四川大学林之恩课题组通过无溶剂法成功合成了具有20-元环超大孔道的磷酸-草酸镓(H2dab)2·Ga4(HPO4)5(H2PO4)2(ox)2(H2O)2,具有金刚石拓扑的亚磷酸-草酸钴CN3H6·Co(H2PO3)(C2O4)[19-20]。
本课题组一直从事金属亚磷酸盐化合物的合成、结构及性质研究,并且报道了一系列具有新颖结构的亚磷酸盐化合物,例如,具有相反手性螺旋链的2D层状结构亚磷酸镓Ga(HPO3)F3·(trans-C6N2H16)[21],具有经典6*1 SBU的新型三维开放骨架亚磷酸镓 Ga8(H2O)6(HPO3)14·(C3N2H6)3·H3O[22],具有极低骨架密度的亚磷酸镓Ga(HPO3)F2(H2A)0.5(A=C5N2H12或C6N2H14)[23]。近年来,本课题组开展了通过绿色合成方法合成金属磷酸盐、亚磷酸盐方面的工作。例如,通过离子热的合成方法合成了具有二维层状结构的磷酸镓Ga3(PO4)4(C2N2H8)·(H2C2N2H8)2·Cl,该化合物表现出一定的荧光性质[24];通过无溶剂合成的方法合成了具有二维层状结构的亚磷酸钴Co2(H2PO3)2(C2O4)2(C6N2H16),该化合物表现出一定的质子传导性质[25]。本文采用无溶剂的合成方法,以稀土金属钬作为金属源,以N,N′-二甲基哌嗪(Me2ppz)为结构导向剂,合成了一个由亚磷酸单元修饰的一维链状结构的新型亚磷酸钬化合物Ho(H2PO3)4(C6N2H16)0.5(1),对其合成、晶体结构进行了细致的描述和表征,并对稀土磷基化合物中稀土元素的配位数以及构型进行了总结。值得注意的是,在结构中存在一对左右手螺旋链。
1 实验部分
1.1 试剂与仪器
试剂:草酸,分析纯,国药集团化学试剂有限公司;Ho(Ac)3·6H2O,质量分数 99%,济南恒化科技有限公司;亚磷酸,分析纯,美国阿拉丁工业公司;N,N′-二甲基哌嗪(Me2ppz),质量分数 98%,梯希爱(上海)化成工业发展有限公司。
仪器:101-1A电热鼓风干燥箱,上海一恒科学仪器有限公司;Perkin-Elmer 3300DV ICP分析仪、Perkin-Elmer 2400元素分析仪、Perkin-Elmer TG-7热重分析仪(N2气氛,温度为300~1 073 K,升温速率为10 K/min),珀金埃尔默公司;D8 Advance粉末X-射线衍射分析(XRD),Cu-Kα(λ=0.154 18 nm),管电压40 kV,管电流40 mA,德国布鲁克公司;Nicolet Impact 410 FTIR红外仪,KBr压片,波长为400~4 000 cm-1,美国 NICOLET 公司;Bruker D8 QUEST 单晶衍射仪,Mo-Kɑ (λ=0.071 073 nm),德国布鲁克公司。
1.2 实验过程
化合物1采用无溶剂法合成。首先依次将H3PO3(0.80 g)、H2C2O4·2H2O(0.20 g) 和 Me2ppz(0.20 mL)加入25 mL聚四氟乙烯反应釜内衬中,然后加入Ho(Ac)3·6H2O(0.10 g)。将聚四氟乙烯内衬装入不锈钢外套拧紧,放入130℃烘箱中,在自发压力下反应3 d。反应结束后,取出反应釜自然降至室温。冷却后,反应釜中得到无色透明块状晶体。用蒸馏水洗涤,干燥、称重,计算收率约为56%(基于Ho的质量)。
1.3 晶体结构测定
在光学显微镜下仔细挑选尺寸为0.20 mm×0.15 mm×0.15 mm化合物1的合适单晶,在环境温度为296 K下,通过单晶衍射仪,以ω扫描方式收集,数据还原在SAINT程序上进行。通过SHELX TL-2014软件,采用直接法解析化合物1的晶体衍射数据[26]。首先将Ho和P原子确定,其次从差Fourier图中找出C、N、O原子。[HPO3]2-基团上的H原子从差Fourier图中找到。非H原子坐标和各向异性参数通过全矩阵最小二乘法进行精修(CCDC No.1896106)。化合物1晶体学数据见表1。

表1 化合物1的晶体学数据
2 结果与讨论
2.1 晶体结构
化合物1的不对称结构单元图如图1所示。由图1可知,化合物1的不对称单元含有1个晶体学上独立的Ho原子和4个P原子。Ho原子采用六配位的模式和周围来自亚磷酸单元[H2PO3]-的6个氧配位。Ho-O键长平均值为0.223 7 nm。这与Dy(H2PO2)3中的Dy-O键长相似[15]。

图1 化合物1的不对称结构单元图
该化合物中所有P均符合P(III)的常见配位模式,即伪金字塔的配位模式:3个O原子和1个H原子配位,然而其配位环境不同。P(1)和P(2)周围的3个O原子分别为桥连O原子[O(3)和O(11)]、端基O原子[O(2)和O(10)]以及羟基O原子[O(1)和O(12)]。P(3)和P(4)周围的2个O原子为桥连O原子[O(4)、O(5)和O(7)、O(8)],另一个O原子为羟基O原子[O(6)和O(9)]。P-O键长平均值为0.150 67(37)nm,键角平均值为111.7(7)o,这与文献[27]金属亚磷酸盐的P-O键长和O-P-O键角一致。P-H平均键长为0.132 0 nm。通过IR的表征(νH-P=2 415 cm-1)可进一步确定P-H。质子化的Me2ppz位于孔道内,平衡主体骨架结构中的电荷。
化合物1具有一维链状结构,该结构由HoO6八面体和[H2PO3]-假四面体通过共顶点的O原子相互连接组成。化合物1的结构示意图如图2所示。
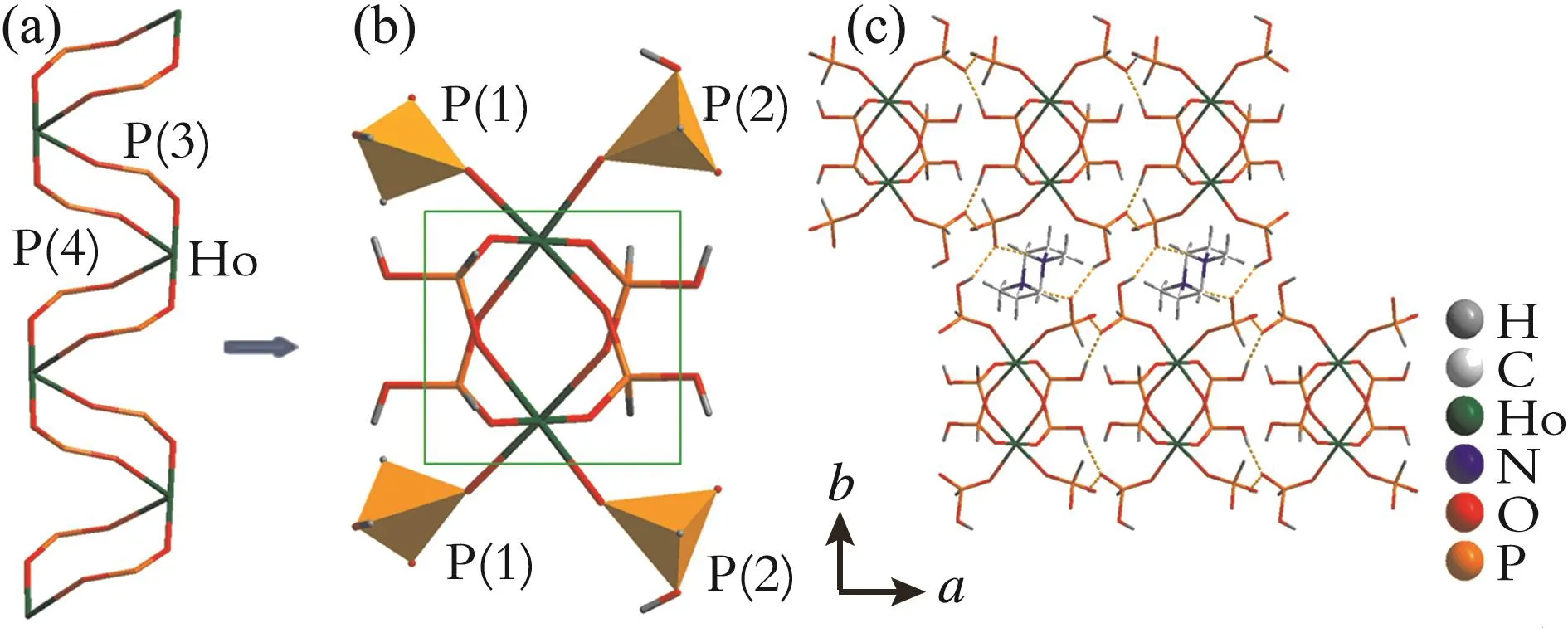
图2 化合物1的结构示意图
由图2可知,HoO6八面体、[H2P(3)O3]-和[H2P(4)O3]-假四面体通过共顶点的O原子连接组成一个具有四元环的链状结构(见图2(a)),[H2P(1)O3]-和[H2P(2)O3]-假四面体镶嵌在该一维链的两侧,对该一维链起修饰作用(见图2(b))。相似的被修饰四元环链状结构在金属磷酸盐Zn(HPO4)(DLC3H7NO2)被报道[28]。其相同点在于两种化合物中一维链都是四元环通过共顶点的O原子交替连接形成的,链的两侧镶嵌着其他单元。其不同点为:在Zn(HPO4)(DL-C3H7NO2)中,每个Zn原子连接3个HPO4单元,从而形成的四元环共处于同一平面,并且模板剂分子参与骨架的组成;而在化合物1中每个Ho原子连接4个[H2PO3]-单元,形成了褶皱状的四元环链状结构,[H2PO3]-假四面体修饰了该一维链。值得注意的是,该四元环一维链是由两种左右螺旋链通过共用Ho原子作为铰链连接构成。如图2(c)所示,相邻的[H2PO3]-假四面体修饰的一维链沿着a轴通过O-H···O[dO···O=2.538(5)~2.692(6)]之间的氢键作用相互连接组成二维层,质子化的Me2ppz离子填充在层与层之间的空间,并通过强烈的 N-H···O[dN···O=2.684(5)]氢键作用与相邻的层相互连接,从而组成三维超分子结构。
由左右手螺旋链组成的四元环链如图3所示。由图3可知,HoO6八面体通过共顶点的O原子与[H2PO3]-假四面体连接组成具有相反手性的两种螺旋链,沿着21螺旋轴的螺距为0.781 8 nm。
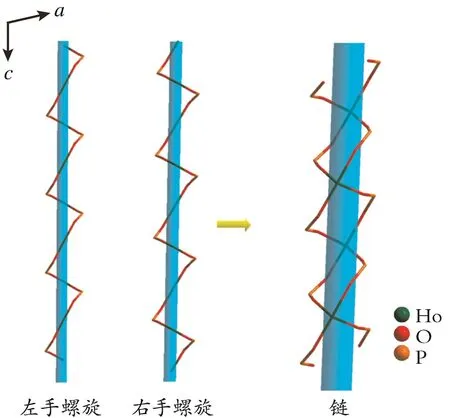
图3 由左右手螺旋链组成的四元环链
值得注意的是,在该化合物中稀土元素Ho的配位数为6。众所周知,稀土金属具有多种配位模式,例如,十二配位、十一配位、十配位、九配位、八配位、七配位、六配位、五配位、四配位、三配位。通过总结稀土膦酸盐、磷酸盐、亚磷酸盐的配位模式及几何构型可以看出,八配位和九配位的稀土金属在膦酸盐、磷酸盐和亚磷酸盐化合物中比较常见[29-66]。在7种化合物中,稀土金属表现出六配位的模式[29-35]。Y.Q.Guo等[29]报道了一系列具有Ln(H2L)(H3L)分子式的稀土化合物,包括 La、Pr、Nd、Sm、Eu、Gd、Tb,其中在 La-Eu的稀土化合物中,稀土金属的配位数均为8,其结构为一维链状结构,随着原子序数的增加,当金属变成Gd和Tb后,金属的配位数以及结构均发生了变化,配位数由8降至6。将Ln(H2L)(H3L)中六配位模式的出现归结为“镧系收缩”效应[29]。在化合物1中,实验选用稀土金属为Ho,其原子序数更高,属于重稀土,因此有利于形成六配位的稀土化合物。
2.2 粉末X-射线衍射分析
图4为化合物1的粉末X-射线衍射谱图。从图4可以看出,两个谱图中衍射峰的位置相同,这说明产物为纯相。

图4 化合物1的粉末X-射线衍射谱图
2.3 元素分析
化合物1的ICP和CHN元素分析实验值(%,质量分数):Ho,30.61;P,22.59;C,6.44;H,2.43;N,2.41;理论值(%,质量分数):Ho,30.15;P,22.65;C,6.59;H,2.95;N,2.56。这表明元素分析的结果与单晶结构分析结果基本一致。
2.4 红外光谱分析
图5为化合物1的红外光谱图。从图5可以看出,3 424 cm-1处的振动峰归属于结构中的O-H基团;2 969、3 020、3 037、3 190 cm-1处的峰归属于N,N′-二甲基哌嗪中N-H和C-H的伸缩振动;1 272、1 455、1 486、1 511、1 643 cm-1处的峰归属于N-H和C-H的弯曲振动;2 415 cm-1和1 004~1 144 cm-1处的峰归属于P-H和P=O的伸缩振动;600~800 cm-1处的峰归属于P-O的弯曲振动。通过红外吸收峰可以判断骨架中含有[H2PO3]-基团和N,N′-二甲基哌嗪分子。
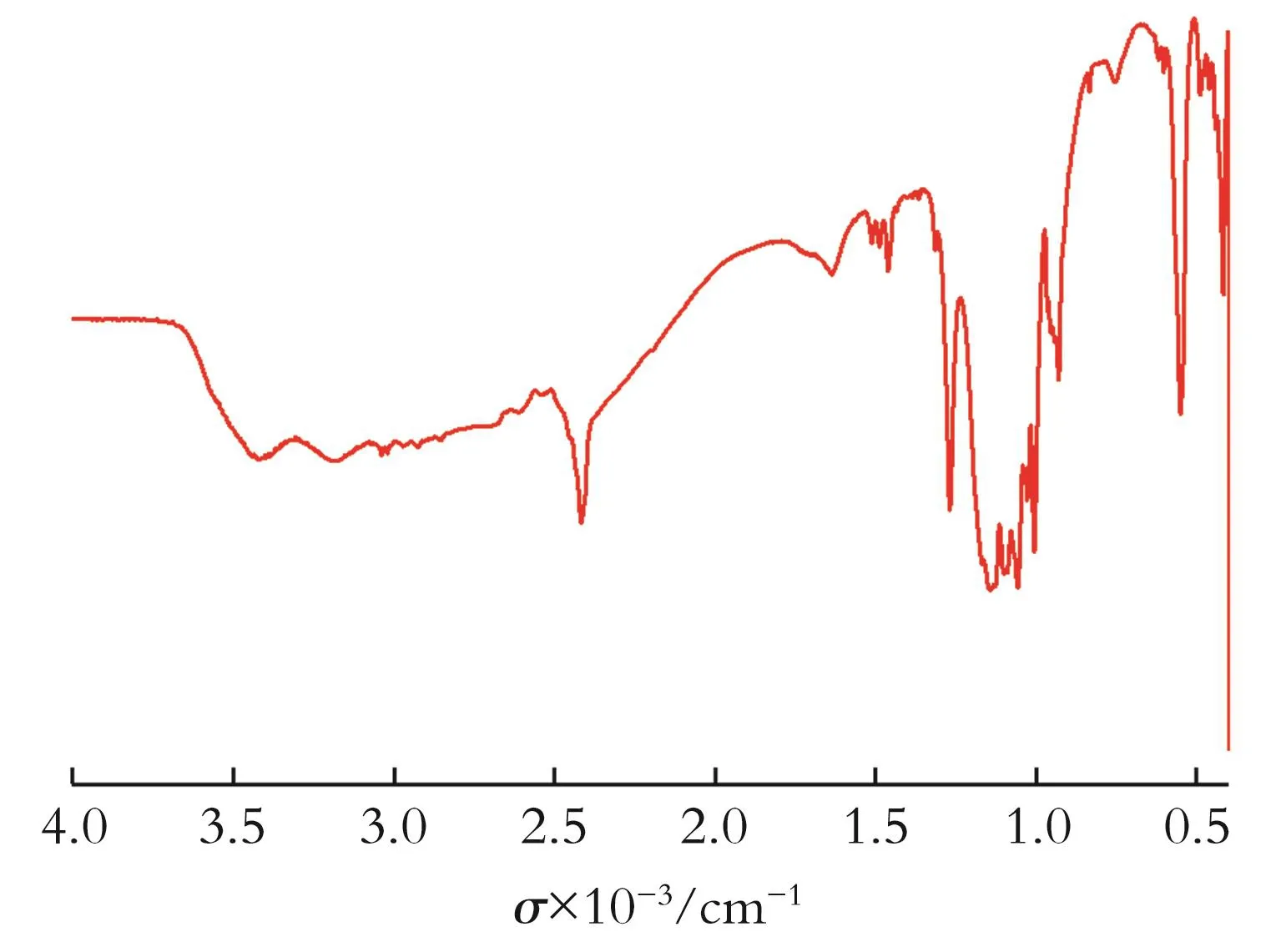
图5 化合物1的红外光谱图
2.5 热重分析
图6为化合物1的热重分析曲线。
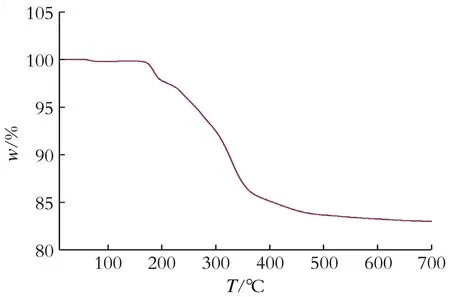
图6 化合物1的热重分析曲线
从图6可以看出,温度为60℃左右时,样品有轻微的失重(0.18%),这主要是样品失去吸附的水。温度为165~600℃时,样品有一步明显失重,失重为16.55%,该步失重可以归结为样品中有机胺单元的失去(10.56%)以及亚磷酸[H2PO3]-单元中水分子的脱除(13.17%)。理论值大于实际值,其差异是由于模板剂不完全燃烧而产生的碳单质引起(样品为黑色)。粉末X-射线衍射分析表明,样品在两步失重之后变成了无定型。
3 结 论
以Me2ppz为模板剂,采用无溶剂法合成了一个亚磷酸钬化合物。单晶测试结果表明,该化合物具有亚磷酸基团修饰的一维链状新型结构,值得注意的是,该四元环一维链是由两种左右螺旋链通过共用Ho原子作为铰链连接构成。该化合物是第一个采用无溶剂合成法得到的稀土亚磷酸盐化合物。该化合物的合成丰富了金属亚磷酸盐家族,为无溶剂法合成亚磷酸盐积累了实验数据,有利于无溶剂合成法在金属磷酸盐、亚磷酸盐化合物合成中的进一步应用。
