宫颈环形电切除术和冷刀锥切术对宫颈上皮内瘤变伴高危型人乳头瘤病毒感染的疗效观察
2020-05-17程美萍吴翊群
程美萍 吴翊群 冷 英
(1.泰州市第三人民医院,江苏泰州 225321;2.泰州市人民医院,江苏泰州 225300)
女性生殖系统疾病中,宫颈癌属于常见恶性肿瘤,发病率达到2%~3%,且呈年轻化趋势[1]。最新中国癌症统计数据显示,中国宫颈癌的发病率仍在逐年增加。宫颈上皮内瘤变(CIN)属于宫颈癌癌前病变,与宫颈癌的发病密切相关,早期发现早期治疗CIN,对于降低宫颈癌的发病率有着至关重要的意义。虽然CIN一般无特殊症状,但随着医学技术的发展,CIN早期检出率不断提高。在诱发宫颈癌或CIN的病毒中,高危型人类乳头瘤病毒(HR-HPV)感染属于常见诱发因素,且CIN合并HR-HPV感染的患者中,宫颈癌发病率高出正常人群7倍以上[2]。所以,为了预防宫颈癌的发生,对CIN伴HR-HPV感染需及时进行有效的治疗,以去除病灶、清除HPV,阻断该病的进展转化。目前针对宫颈上皮内瘤变的治疗措施有冷冻、激光及子宫颈锥切术,对于年龄较大、无生育要求、合并其他有手术指征的妇科良性疾病的高级别上皮内瘤变也可以行全子宫切除术[3]。其中子宫颈锥切术又有子宫颈环形电切术(LEEP)和冷刀锥切术(CKC)之分,二者并存多年,临床上对二者的疗效差异有着不同的观点。本研究对86例CIN伴HR-HPV感染患者采用子宫颈环形电切除术与冷刀锥切术治疗的效果进行比对,结果如下。
1 资料与方法
1.1 一般资料
选取泰州市第三人民医院2016年6月至2019年6月收治的86例患者作为研究对象,采用随机数字表法分为观察组(n=44)与对照组(n=42)。观察组年龄21~ 56 岁,平均年龄(34.2±2.7)岁,其中CIN II级26例、CIN III级18例;对照组年龄22~57岁,平均年龄(34.6±2.5)岁,其中CIN II级24例、CIN III级18例。两组患者一般资料相比,差异无统计学意义(P>0.05),具有可比性。所有入选患者均经宫颈细胞学筛查、阴道镜检查、组织病理学检查等确诊为CIN伴HR-HPV感染,均已婚,有性生活史;排除阴道分泌物检查III~IV度者、急性生殖道感染者、宫颈萎缩者、宫颈治疗史者、妊娠及哺乳期患者、盆腔放射史者等。本研究经泰州市第三人民医院医学伦理委员会审查通过。
1.2 方法
所有患者均选择在月经结束后3~7 d内进行手术。术前3 d禁止性生活并进行白带化验,排除阴道炎症。观察组进行宫颈环形电切除术治疗,对照组进行冷刀锥切术治疗。手术前排空膀胱,宫颈环形电切除术无需麻醉,冷刀锥切术采用腰硬联合麻醉或全身麻醉,取膀胱截石位。给予常规消毒铺巾,对子宫颈采用窥阴器进行暴露后再次消毒,在整个宫颈及穹窿部涂抹碘酊液,明确病变范围。冷刀锥切术:用鼠齿钳牵拉宫颈,将垂体后叶素稀释液注射到宫颈间质内,在碘未着色区域外0.5 cm处做环形切口,然后垂直进刀环切,以宫颈管为轴线,呈30 °角向内逐渐切入宫颈深部,对宫颈病变组织进行切除,锥高2~3 cm;采用电凝方法对创面进行止血,然后采用可吸收线进行缝合,对宫颈口形态进行再造,检查宫颈是否畅通,无异常后用一卷碘伏纱布进行填塞压迫止血,留置导尿管,术毕。宫颈环形电切除术:根据病变大小,对电切环型号进行选择,从9点处开始做环形病变组织切除,以顺时针方向进行切除,深度15 mm,如果患者病灶范围比较大,分次进行病灶切除,采用球形电极电凝对创面进行止血,术毕。术后两组均给予常规抗生素预防感染。
1.3 观察指标
对两组手术时间、术中出血量进行对比。
术后对两组病灶残留率(各组切缘阳性患者例数/各组总例数×100%)进行对比;术后3个月,对两组愈合率(各组创面已愈合例数/各组总例数×100%)进行对比;术后6个月,对两组复发率(各组复查细胞学检查阳性例数/各组总例数×100%)及HPV转阴率(各组HPV转阴患者例数/各组总例数×100%)进行对比。
1.4 统计学分析
2 结果
2.1 两组患者手术相关指标比较
在手术时间、术中出血量方面对比,观察组均少于对照组,差异有统计学意义(P<0.05),见表1。
2.2 两组患者治疗效果比较
在病灶残留率、愈合率、复发率及HPV感染转阴率方面对比,两组差异均无统计学意义(P>0.05),见表2。
表1 两组患者手术指标比较(±s)

表1 两组患者手术指标比较(±s)
组别 手术时间(min) 术中出血量(mL)观察组(n=44) 15.27±5.44 12.04±6.28对照组(n=42) 24.93±7.91 27.84±9.46 t 4.527 7.436 P<0.05 <0.05
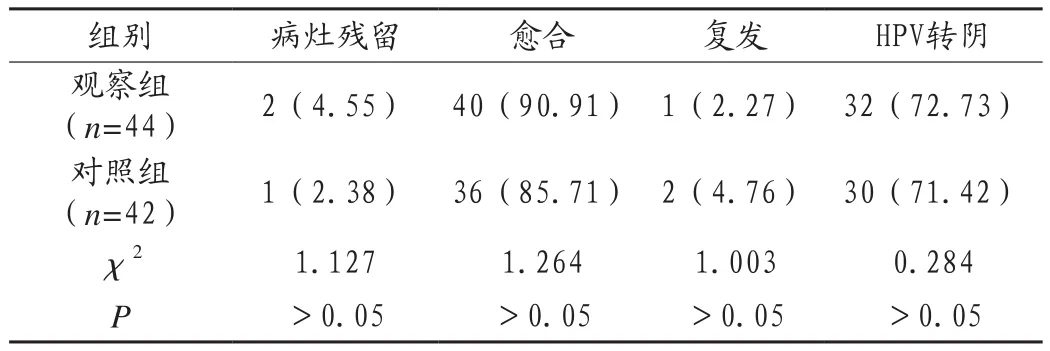
表2 两组患者治疗效果比较[例(%)]
3 讨论
宫颈上皮内瘤变属于宫颈癌的癌前病变,根据病变程度可分为CIN I、CIN II、CIN III,有研究显示,我国宫颈癌癌前病变发生率方面,CIN I、CIN II、CIN III发病率分别为3.1%、1.5%及1.2%,很多时候CIN I、CIN II可不经过CIN III而直接发展为浸润癌[4]。CIN发展为宫颈浸润癌的病因目前未完全明确,但诸多研究显示,机体免疫力低下、吸烟、过早性生活、多个性伴侣、口服避孕药及HR-HPV感染等为CIN发展为宫颈浸润癌的高危因素[5-6]。其中HRHPV的持续感染被普遍认为是宫颈发生病变的必要条件[7-8]。HR-HPV的及时清除可有效预防宫颈癌的发生。随着医学及科技的发展,CIN及HR-HPV的早期检出率有了大幅提升,及早进行干预治疗,为宫颈癌的消灭提供了可能。因此,创伤小、安全性高的治疗方法受到广泛关注。
如前所述,CIN有多种治疗手段,其中冷冻、激光等消融治疗病灶清除不彻底,不宜用于高级别上皮内瘤变、阴道镜检查不充分或者颈管搔刮阳性者。而全子宫切除术,创伤大,患者再无月经及生育能力,为大多患者所不能接受,故而目前针对宫颈上皮内瘤变应用最广泛的治疗措施是宫颈锥切。其既是避免CIN发展为浸润癌的主要术式,也是排除宫颈浸润癌的一种诊断措施。根据手术术式的差异,目前临床中主要包含宫颈环形电切除术(LEEP)及冷刀锥切术(CKC)等术式。其中宫颈环形电切除术因在临床中应用具有操作简单、手术时间短、创伤小、安全性高等优势,应用范围比较广[9];但有研究显示,部分患者采用宫颈环形电切除术治疗后,会出现所切组织切缘阳性情况,可存在CIN病灶残留[10]。但是本次研究显示,在CIN伴HR-HPV感染患者的治疗中,分别采用宫颈环形电切除术与冷刀锥切术,二者在病灶残留率、愈合率、复发率及HPV感染转阴率方面差异均无统计学意义(P>0.05),表明在CIN伴HR-HPV感染患者的治疗中,两种术式均能达到较好的病灶清除及HPV转阴作用,宫颈上皮内瘤变锥切术后复发的高风险因素常有高危型HPV持续感染,细胞学异常和宫颈组织切缘阳性[11],而上述两种术式病灶清除及HPV转阴率均无明显差异,愈合率、复发率近似,均有较好的疗效。然而在手术时间、术中出血量上对比,观察组均低于对照组(P<0.05),表明宫颈环形电切除术对CIN伴HR-HPV感染患者进行治疗,相比冷刀锥切术,创伤较小,手术时间较短。
综上所述,在对CIN伴HR-HPV感染患者的治疗中,宫颈环形电切除术与冷刀锥切术均能达到较好的治疗效果,但宫颈环形电切除术切除宫颈过程中可同时电凝止血,出血量少,手术时间短,患者所受痛苦少,而且LEEP刀有多种不同的刀头和切割手法,有利于更完全的切除病变组织,以减少病灶残留,且对宫颈形态破坏小,可多次重复手术,更有利于患者术后恢复,值得推广应用。
