异性官能团修饰石墨烯吸附GIS特征气体能力的DFT研究
2020-05-15王成江梅侣松李亚莎刘玉斌赵一帆
王成江,梅侣松,李亚莎,刘玉斌,赵一帆,谢 烨
(三峡大学 电气与新能源学院,宜昌 443002)
1 引 言
GIS设备以其可靠性高,体积小,维护简单,不受外界环境影响等优点,在电力系统的使用不断增加.而六氟化硫气体因其良好的绝缘性能和灭弧性能在GIS中被广泛应用[1].以往运行经验表明,电气设备在长期运行中不可避免的存在绝缘缺陷,这些潜在缺陷往往会引起不同程度的局部放电(partial discharge,PD).在PD作用下,GIS内部SF6出现分解并与设备内部的微水微氧反应生成SO2、SO2F2、SOF2、CF4等GIS特征气体[2].这些产物会腐蚀金属表面进一步加速设备绝缘老化,最终可能导致绝缘设备的损坏甚至使整个供电系统瘫痪.因此,通过准确检测GIS特征气体,判断局部放电的总体状况,能够尽早发现绝缘设备内部缺陷,避免GIS潜在故障的发生[3].
石墨烯具有优异的结构特性和电子特性,基于石墨烯的传感器有着高灵敏度、响应快、尺寸小且工作温度低等优点被广泛应用.石墨烯基气体传感器依赖于石墨烯表面吸附物作为电子供体或受体,局部电荷载流子密度的变化引起石墨烯电导率改变,从而实现对待测气体的检测[4].本征石墨烯只对少数气体如NO2、NH3吸附效果较好[5],这使得石墨烯基气体检测传感器试用范围小,灵敏度低,而通过掺杂和功能化修饰来提高本征石墨烯对特定气体的响应特性是一种有效方法.例如,过度金属(Cr和Mn)掺杂石墨烯,能够有效提高对H2CO3分子的敏感性[6].金属原子Ga掺杂石墨烯能够提升对NO2的吸附能力[7].总结近年来在石墨烯基气体检测传感器领域的研究成果,掺杂常见过渡金属元素以及吸附一些气体如SO2、CO、CH4已取得较好的研究进展,而鲜有对官能团修饰石墨烯及检测GIS特征气体的研究报道.
本文基于密度泛函理论(DFT)对本征石墨烯(graphene)、羟基石墨烯(gra-OH) 、羧基石墨烯(gra-COOH)与4种GIS特征气体间的吸附过程进行模拟研究,通过吸附能、态密度、分子前线轨道、能隙探讨了异性官能团修饰对石墨烯吸附性能的影响,研究结果旨在得出强吸附修饰吸附材料及其规律性特征,为针对GIS特征气体的高性能气体检测传感器的研制工作提供科学的理论指导.
2 建模与仿真
本文吸附材料石墨烯模型采用4×4×1超晶胞盒子,共32个碳原子.层与层之间建立15 Å真空层以避免层间相互作用,所得晶胞晶格参数为9.84 Å×9.84 Å×21.8 Å,同时建立了4种气体分子(SO2,CF4,SO2F2,SOF2)模型.在graphene模型基础上,分别在同一位置碳原子上接入羟基、羧基得到上述官能团修饰石墨烯模型.将单个气体分子依次放入晶胞并位于官能团正上方2 Å处,使吸附过程仅发生在石墨烯与气体分子之间.
所有计算均由分子模拟软件MS完成,DFT计算采用广义梯度近似(GGA)下的Perdew-Burke-Enzerhof (PBE)[8]修正模式处理研究对象的电子间交换交联作用,该方法考虑了电荷密度梯度对电子密度的影响,使计算结果接近于实验值[9].原子轨道由双数值极化基组(DNP)指定.迭代过程加入DFT-D色散校正算法来减小吸附过程中范德华相互作用的影响.几何优化自洽场SCF(self-consistent field)收敛阈值为1.0*10-5Ha,原子最大偏移收敛标准为0.005 Å,设置布里深渊K点为6×6×1,能量收敛标准设为2.0*10-5Ha.几何优化完成后的稳定石墨烯模型如图1所示.
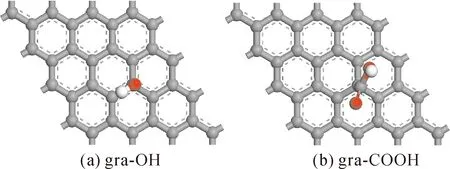
图1 石墨烯模型结构Fig.1 structure models of graphene
3 结果与讨论
3.1 吸附GIS特征气体能力的表征
为分析GIS特征气体在gra-OH与gra-COOH表面吸附的稳定性,计算了气体分子吸附能ΔEad,它反映了吸附过程中系统能量变化,公式如下:
ΔEad=Egraphene&gas-(Egraphene+Egas)
(1)
其中Egraphene&gas为石墨烯表面吸附气体分子的稳定结构能量,Egraphene为吸附材料能量,Egas为气体分子能量.ΔEad<0表明吸附过程自发进行且伴随能量释放,|ΔEad|越大,表明石墨烯表面与气体分子间相互作用越强,吸附结构更为稳定.
为反映吸附材料与被吸附气体分子间电荷转移情况,引入电荷转移量Qt,其计算公式为[10]:
Qt=Qabsorbed gas-Qisolated gas
(2)
其中Qabsorbed gas为吸附稳定后气体分子携带的电荷量,Qisolated gas为吸附前携带电荷量,恒定为0.Qt为负值表示电荷从吸附材料转移到气体分子,Qt为正值电荷转移路径则与其相反,且|Qt|越大,表面电荷转移越多,相互作用越激烈,吸附能力越强.
为进一步了解4种气体分子在gra-COOH与gra-OH表面化学吸附机制,计算并分析了各吸附体系的态密度(density of states,DOS)和局部态密度(partial density of states,PDOS).相邻原子态密度发生“共振” (轨道杂化)是化学键形成的一个明显标志.轨道杂化区域越大,表面电子转移越多,相互作用越激烈,对气体分子吸附能力越强.
3.2 吸附GIS特征气体能力的计算
对GIS特征气体在gra-OH与gra-COOH表面的吸附过程进行结构优化,得到稳定吸附构象如图2所示,最后通过计算得出稳定吸附模型的各项参数.表1给出了结构优化完成后,各气体分子与graphene、gra-OH、gra-COOH之间的吸附能ΔEad、作用距离D以及电荷转移量Qt,吸附材料与气体分子相邻原子的PDOS计算结果如图3-6所示.

图2 气体分子稳定吸附模型结构Fig.2 Stable adsorption model structures of gas molecules

图3 SO2吸附体系H与O原子PDOSFig.3 The PDOSs of H and O atoms in SO2 adsorption system
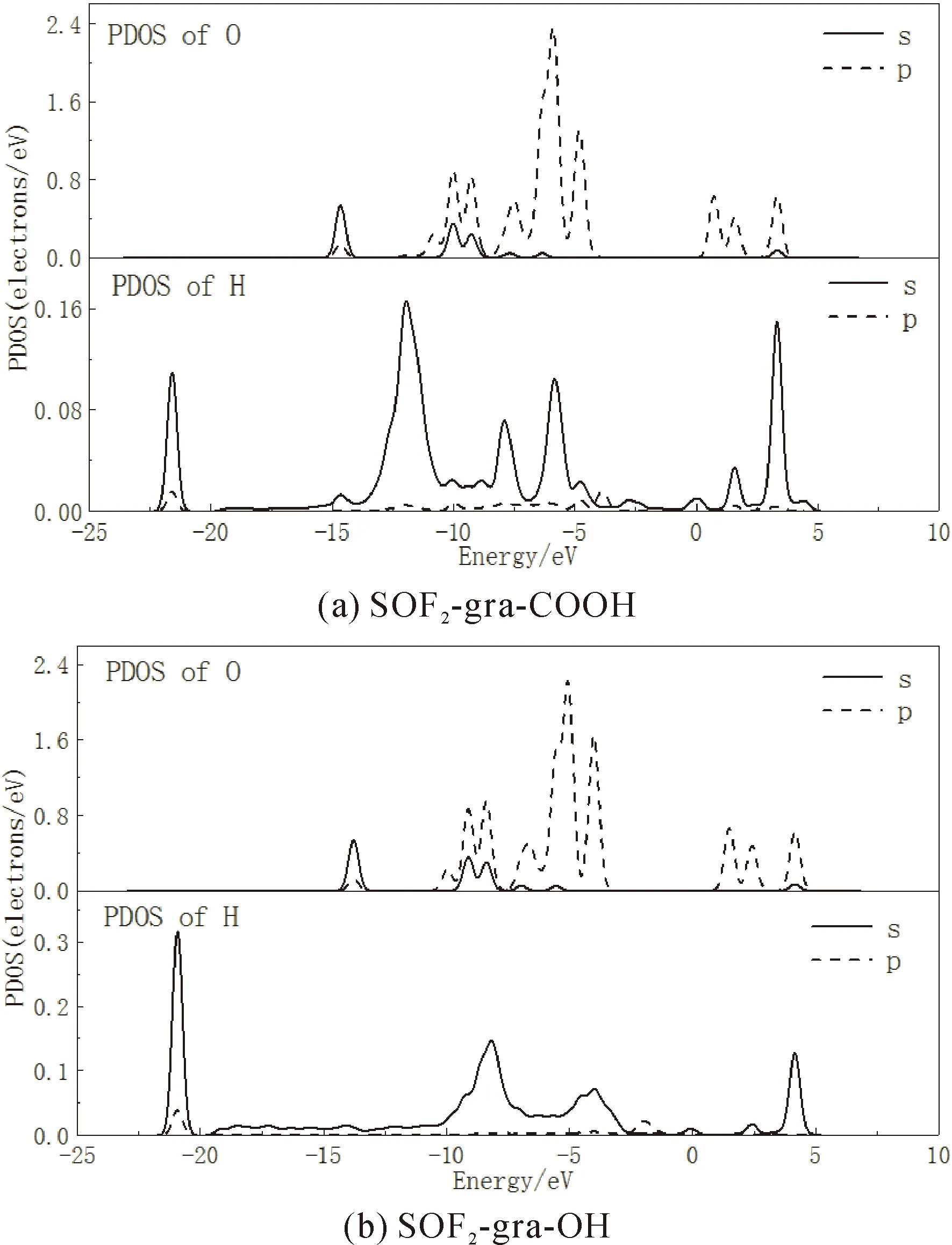
图4 SOF2吸附体系H与O原子PDOSFig.4 The PDOSs of H and O atoms in SOF2 adsorption system
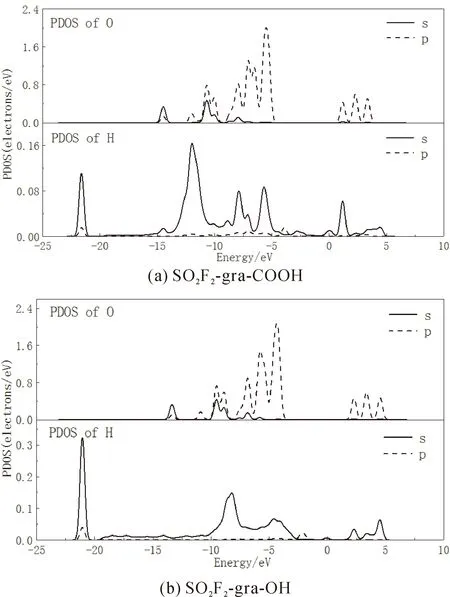
图5 SO2F2吸附体系H与O原子PDOSFig.5 The PDOSs of H and O atoms in SO2F2 adsorption system
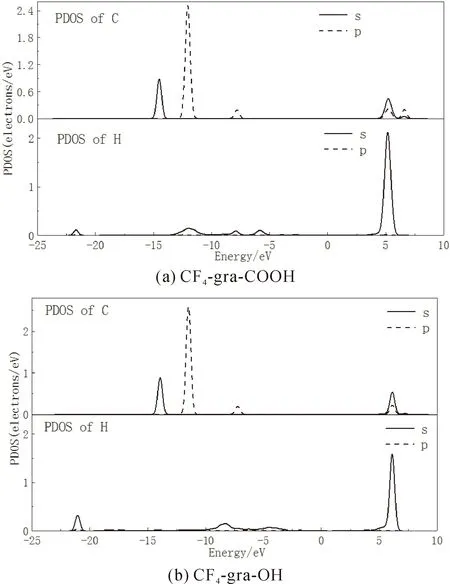
图6 CF4吸附体系H与C原子PDOSFig.6 The PDOSs of H and C atoms in CF4 adsorption system
3.3 吸附GIS特征气体能力的比较
3.3.1吸附能及电荷转移量比较
由表1可知,对比于graphene,gra-COOH与gra-OH对SO2,SOF2与SO2F2的吸附能力均有明显的增强.吸附能ΔEad与电荷转移量Qt增大,作用距离D减小,表明活性官能团羟基、羧基的修饰对吸附过程起着重要作用.各吸附体系的ΔEad均小于零,吸附过程均为可自发进行的放热反应.
gra-OH对SO2、SO2F2、SOF2的ΔEad相差不大,但SO2F2与SOF2的Qt约为SO2的1/6,表明SO2与gra-OH吸附过程中电荷转移较多,宏观上表现为吸附体系的电导率较大,表面载流子增加,gra-OH对SO2的气敏性能最好.CF4吸附能最小且与另外3种气体分子相差接近1个数量级,说明gra-OH对CF4的吸附能力最差.SOF2与SO2F2吸附体系的电荷转移量与作用距离较为接近,ΔEad(SOF2)略高于ΔEad(SO2F2),故gra-OH与SOF2的相互作用稍强于SO2F2.
gra-COOH对CF4分子吸附能最小仅为SO2、SO2F2、SOF2的1/18、1/14和1/16,且Qt也相差较大,表明gra-COOH对CF4分子最不敏感.在吸附能与电荷转移量方面,另外3种气体分子中SO2的ΔEad与Qt均最高,且SO2在吸附过程中Qt为SO2F2与SOF2的8.2倍和5.5倍,表明SO2分子吸附于gra-COOH表面后,体系电导率发生较大变化,吸附过程电荷转移较为激烈,gra-COOH对SO2最敏感.SOF2吸附体系的ΔEad与Qt均高于SO2F2,故gra-OH与SOF2的相互作用强于SO2F2.
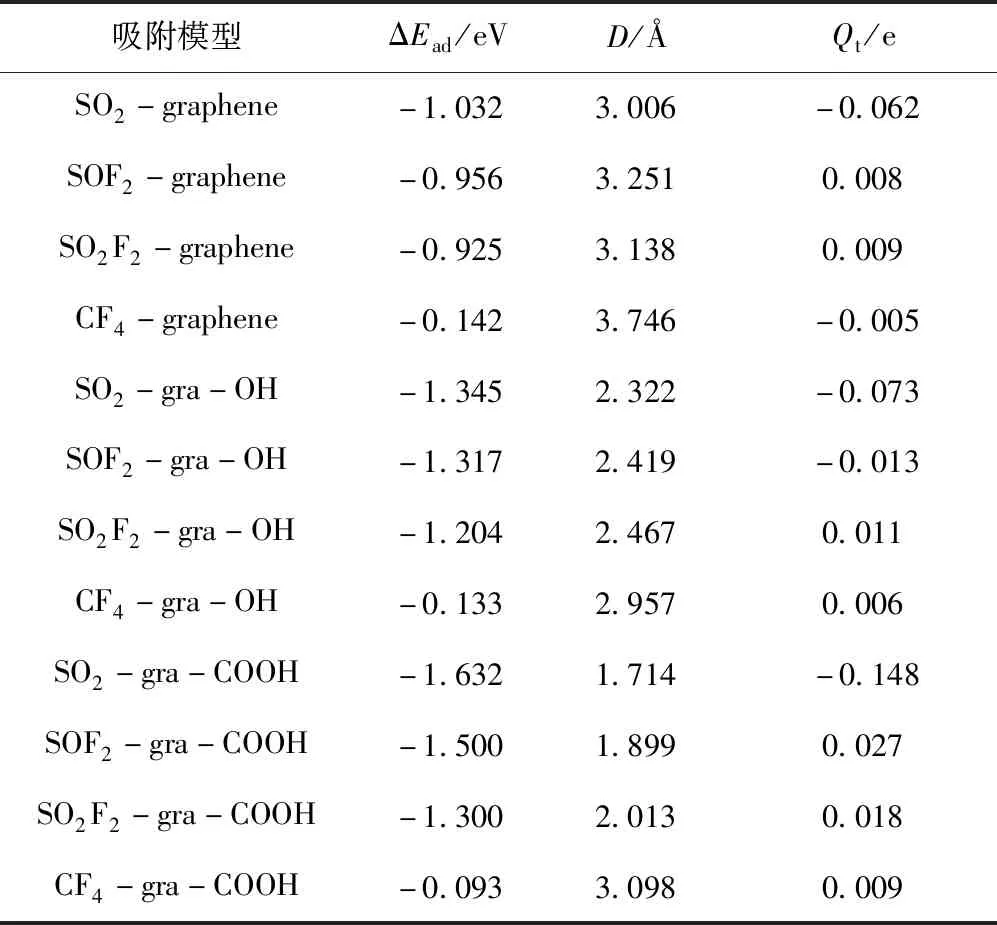
表1 吸附能力计算结果Table 1 Calculation results ofadsorption ability
综上所述,gra-COOH对GIS特征气体的吸附能力在吸附能、作用距离和电荷转移方面比gra-OH更强,因此,可将gra-COOH作为检测GIS特征气体的气敏材料.
3.3.2 态密度比较
图4为SO2吸附体系中吸附材料与SO2相邻H与O的PDOS.可以看出SO2-gra-COOH体系主要在导带4.5 eV、0.5 eV与价带-7 eV处H1s轨道与O2p轨道出现一定程度杂化重叠,而SO2-gra-OH体系主要出现在导带4.5 eV与价带-4 eV处,前者重叠程度高于后者,表明两者吸附SO2过程中H原子与O原子发生了较为激烈的相互作用,轨道杂化重叠有利于电子在原子间的运输,故两者对SO2表现出较高的灵敏度,且gra-COOH作用更为强烈.
gra-OH与gra-COOH吸附SOF2、SO2F2、CF4的PDOS如图5-7所示.从gra-OH与SOF2、SO2F2吸附体系PDOS可以看出,H与O均在-8 eV、-6 eV处存在峰值重叠,而gra-COOH中则在-6 eV、-3 eV存在轨道杂化,且SOF2、SO2F2吸附体系重叠程度小于SO2吸附体系,表明SOF2、SO2F2同gra-COOH与gra-OH间存在一定的相互作用与电子运输,但要小于SO2.CF4-gra-COOH的5 eV与CF4-gra-OH的6 eV处H1s轨道态密度峰值较前者有所增加,但此处离费米能级较远,对体系性质影响相对较小,而在靠近费米能级区域内不存在峰值杂化,表明CF4与gra-OH、gra-COOH间的相互作用与电荷转移均非常小,故对CF4不敏感.
4 吸附GIS特征气体能力差异的原因分析
为进一步探究GIS特征气体在异性官能团修饰石墨烯表面吸附能力存在强弱差异的内因,计算分析了各吸附体系的分子前线轨道和能隙.
4.1 分子前线轨道
吸附能力分析结果表明gra-COOH对GIS特征气体的吸附能力要强于gra-OH,且两者均与SO2相互作用较强,表现出较高灵敏度,与CF4作用微弱,几乎不敏感.gra-OH与gra-COOH对气体分子的选择性吸附可通过分子前线轨道理论[11]解释.前线轨道能量及差值计算结果在表2中给出,其中EH-L为吸附材料的最高已占轨道(HOMO)与气体分子最低空轨道(LUMO)能量差值,EL-H为气体分子的HOMO与吸附材料的LUMO轨道能量差值.

表2 分子前线轨道能量差Table 2 Molecular frontier orbital energy differences
分子相互作用期间,电子从HOMO能级转移至LUMO能级.EH-L越小,吸附材料电子从自身HOMO跃迁到气体分子LUMO所需能量越少,气体分子越容易得到电子,同理EL-H越小,吸附材料越容易从气体分子中得到电子.从表2可以看出,gra-COOH与gra-OH对SO2的分子前线轨道能量差在4种气体分子中均最小,表明SO2与两种吸附材料间的电子转移最容易发生,故两者均对SO2最敏感,吸附效果最好.同理另外3种气体分子EH-L和EL-H从大到小依次为SOF2、SO2F2、CF4,故gra-COOH与gra-OH对4种气体分子的吸附能力排序为SO2>SOF2>SO2F2>CF4.
4.2 能隙
能隙大小反映了吸附体系自身电子从HOMO激发到LUMO轨道的难易程度,宏观上可体现为电流变化大小[12].若修饰材料吸附气体分子后Egap变小,电子在吸附体系上的转移越容易,电流变化大,对气体响应灵敏.Egap可用吸附体系自身HOMO与LUMO能量差绝对值表示,能隙计算结果如表3所示.

表3 能隙计算结果Table 3 Calculation results of energy gap
上表数据可以看出,羟基、羧基石墨烯吸附体系中,SO2吸附于gra-COOH与gra-OH表面后能隙减小较为明显,SOF2与SO2F2吸附体系能隙较小略微,而gra-COOH吸附CF4后能隙增大,gra-OH吸附CF4后能隙保持不变,这表明gra-COOH与gra-OH在吸附SO2后,自身电子转移能力增强,电流变化大,响应灵敏;吸附CF4后,两种吸附材料电子转移能力均减弱,响应不灵敏;而吸附SOF2与SO2F2后,电子转移能力有微弱提升,响应灵敏度略高于CF4.
5 异性官能团修饰石墨烯吸附GIS特征气体的规律
5.1 异性官能团修饰石墨烯的强吸附规律
通过对上述吸附能力差异的原因分析,电子在气体分子与吸附材料间以及吸附体系内部转移难易程度与吸附效果有着必然联系.一方面电子转移有利于化学键的形成,使气体分子与吸附材料间的作用更为稳固,另一方面,电子在吸附体系内部的运输难易宏观上决定了吸附材料检测气体分子的灵敏性.电子在修饰材料与气体分子间以及修饰材料内部转移的难易分别可通过分子前线轨道与修饰材料能隙反映.
将表1中各吸附体系吸附能与表2中分子前线轨道计算结果对比分析可知,修饰材料与气体分子间的EH-L、EL-H越小,对气体分子的吸附作用越强;通过对表3中两种修饰材料能隙大小与其对气体分子吸附能力的分析,可以看出能隙较小的gra-COOH对气体分子的吸附能力更强.综上所述,异性官能团修饰石墨烯后,分子前线轨道能级差与能隙越小,将此官能团修饰石墨烯作为检测GIS特征气体的气敏材料效果越好,反之,异性官能团修饰石墨烯后的分子前线轨道能量差与能隙增大,则不利于对GIS特征气体的吸附.
5.2 实例测试
为测试上述规律性结论正确与否,引入氨基官能团修饰石墨烯,计算出氨基石墨烯(gra-NH2)分子前线轨道能量差与能隙大小如表4所示.对GIS特征气体在gra-NH2的吸附行为进行模拟计算,得出吸附能计算结果如表5所示.由表4可知,gra-NH2与GIS特征气体分子前线轨道能量差EH-L与EL-H均有SO2>SOF2>SO2F2>CF4,而gra-NH2能隙Egap为0.436 eV,略大于羟基、羧基石墨烯能隙.根据上述规律性结论,gra-NH2应对GIS特征气体分子吸附能力应满足SO2>SOF2>SO2F2>CF4,且整体吸附能力弱于gra-COOH与gra-OH.

表4 分子前线轨道能量差Table 4 Molecular frontier orbital energy differences
Egap=0.436 eV

表5 吸附能计算结果Table 5 Calculation results of adsorption energy
表5可以看出,gra-NH2对4种分子吸附能存在SO2>SOF2>SO2F2>CF4,而对比于羟基、羧基石墨烯,gra-NH2对SO2的吸附能介于两者之间,小于gra-COOH,略高于gra-OH;对SOF2、SO2F2的吸附能均明显小于gra-COOH与gra-OH,3种吸附材料均对CF4不敏感.综上所述,羟基、羧基、氨基官能团修饰石墨烯对GIS特征气体整体吸附能力为-COOH>-OH>-NH2,满足上述规律性特征,即在异性官能团修饰石墨烯后,分子前线轨道能级差与能隙越小,对GIS特征气体吸附能力越强.因此,寻找能够有效减小石墨烯能隙及其与气体分子前线轨道能量差的修饰材料,对高性能GIS特征气体检测传感器的研制具有重要指导意义.
6 结 论
本文采用基于密度泛函理论方法,对GIS特征气体在异性官能团修饰石墨烯表面上的吸附能力及强弱机理进行了理论研究,得出如下结论:
1)羟基与羧基的修饰有效提高了石墨烯对SO2、SO2F2、SOF2的吸附能力,吸附过程SO2中O2p轨道与修饰材料H1s轨道杂化重叠程度最高,吸附作用最强烈,SO2F2与SOF2其次,对CF4不敏感,且羧基石墨烯整体吸附能力最强.因此,可将羧基石墨烯作为检测GIS特征气体传感器的气敏材料.
2)分子前线轨道计算结果显示羟基、羧基石墨烯吸附SO2后EH-L和EL-H均为最小,吸附过程中最容易发生电荷转移;能隙计算结果表明,gra-COOH吸附SO2后能隙明显减小,gra-COOH的电子转移能力有所提升,电流变化大,响应最灵敏.
3)气体分子与吸附材料间以及吸附体系内部的电子转移难易与吸附效果存在必然联系.异性官能团修饰石墨烯后的能隙及其与气体分子前线轨道能量差越小,对GIS特征气体吸附能力就越强.异性官能团修饰石墨烯的能隙与前线轨道能量差可以作为选择特征气体敏感材料的依据.
